米氏方程与双倒数作图法(Lineweaver-Burk plot)
米氏方程(Michaelis-Menten Equation)或米曼氏动力学(Michaelis-Menten kinetics)是由Leonor Michaelis和Maud Menten在1913年提出,是酶学中极为重要的可以描述多种非变异构酶动力学现象、表示一个酶促反应的起始速度V(有些资料中也称为Vo)与底物浓度[S]关系的速度方的方程,米氏方程形式如下:
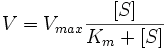
其中,Vmax表示酶被底物饱和时的反应速度,Km值称为米氏常数,是酶促反应速度V为最大酶促反应速度值一半时的底物浓度。在酶促反应中,底物情况在低浓度下,反应相对于底物是一级反应(first order reaction);而当底物浓度处于中间范围时,反应(相对于底物)是混合级反应(mixed order reaction);当底物浓度增加时,反应由一级反应向零级反应(zero order reaction)过渡;当底物浓度[S]逐渐增大时,速度V相对于[S]的曲线为一双曲线。下图为米氏方程的模拟作图:
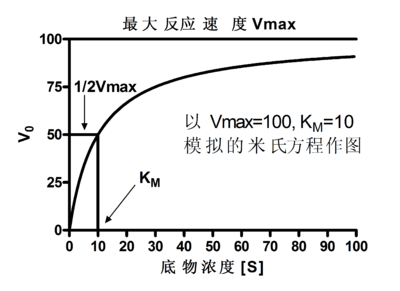
酶促反应中的米氏常数的测定和Vmax的测定有多种方法。比如固定反应中的酶浓度,然后测试几种不同底物浓度下的起始速度,即可获得Km和Vmax值。但直接从起始速度对底物浓度的图中确定Km或Vmax值是很困难的,因为曲线接近Vmax时是个渐进过程。因此,通常情况下,我们都是通过米氏方程的双倒数形式来测定,即Lineweaver-Burk plot,也可称为双倒数方程(double-reciprocal plot):
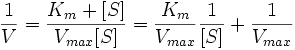
将1/V 对1/[S]作图,即可得到一条直线,该直线在Y轴的截距即为1/Vmax,在X轴上的截距即为1/Km的绝对值。示意图如下:







 本文介绍了米氏方程及其在酶学中的应用,详细解释了如何使用双倒数作图法(Lineweaver-Burkplot)来确定酶促反应中的米氏常数Km和最大反应速度Vmax。通过改变底物浓度并绘制1/V与1/[S]的关系图,可以直观地获取这些关键参数。
本文介绍了米氏方程及其在酶学中的应用,详细解释了如何使用双倒数作图法(Lineweaver-Burkplot)来确定酶促反应中的米氏常数Km和最大反应速度Vmax。通过改变底物浓度并绘制1/V与1/[S]的关系图,可以直观地获取这些关键参数。

















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








