敏感性分析
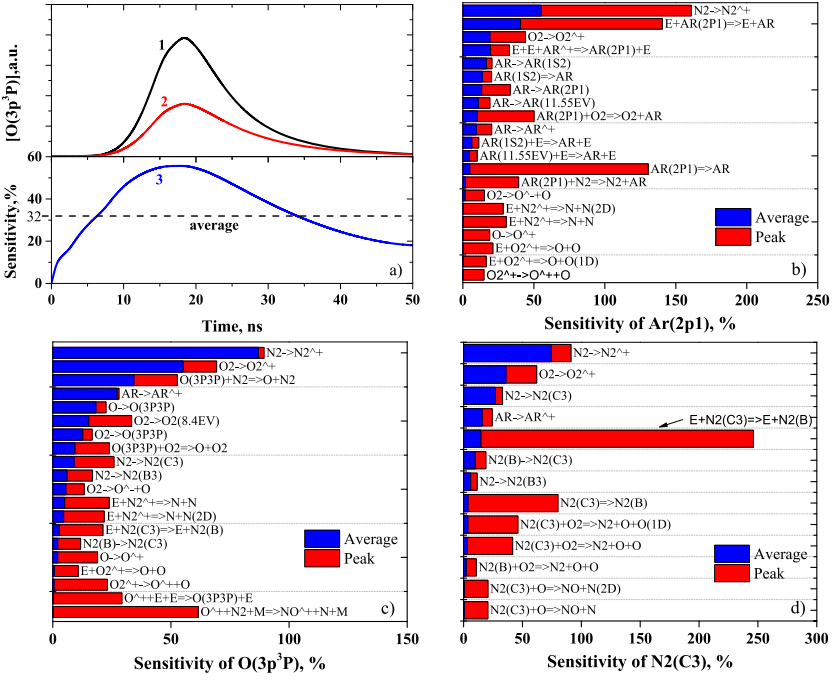
敏感性分析作为化学反应机理简化的核心方法,其重要性主要体现在能够定量评估各基元反应对系统关键组分的影响程度。在复杂反应体系中,通过这种方法可以有效地筛选出对目标物种具有显著影响的基元反应,从而实现机理的合理简化。本文采用了一种基础但有效的敏感性分析方法,其本质是通过人为扰动反应速率来考察特定组分浓度对该扰动的响应程度。
具体而言,我们以N2/O2混合气体体系中O2浓度对N + O2 → O + NO反应的敏感性分析为例,详细说明该方法的应用流程。首先,在标准条件下(即保持所有反应速率常数为原始值),通过数值求解计算得到O2浓度随时间变化的基准曲线,记为[O2]k。然后,选择性地将目标反应N + O2 → O + NO的速率常数k增大至原始值的2倍(即2k),同时保持其他所有反应条件不变,再次进行数值求解得到扰动后的O2浓度曲线[O2]2k。
为量化该反应对O2浓度的影响程度,采用归一化的敏感性系数计算公式:
S = ([O2]2k - [O2]k)/[O2]k
该系数具有明确的物理意义:当S为正值时,表明增大该反应速率会促进O2的生成;反之,若S为负值,则说明该反应速率的增加会抑制O2的生成。敏感性系数的绝对值大小直接反映了该反应对O2浓度影响的强弱程度。
反应路径分析
化学反应路径分析是研究特定组分在给定时间范围内的生成和消耗途径的重要方法。与敏感性分析不同,路径分析关注的是组分在反应网络中的具体来源与去向,而非仅考察其对速率变化的响应。因此,二者在机理简化过程中相辅相成,共同确保简化机理的完整性和准确性。
1.路径分析与敏感性分析的互补性
敏感性分析能够筛选出对目标组分浓度影响较大的反应,但该方法存在一定局限性:
可能遗漏关键消耗路径:敏感性分析通常侧重于考察某组分的生成或消耗趋势,但单独使用可能无法完整识别所有重要反应。例如,在N/O反应体系中,敏感性分析可能识别出促进O₂生成的关键反应,但如果某些消耗O₂的反应敏感性较低(如O₂ + N → NO + O),这些反应可能被忽略,导致O₂在模拟过程中出现不合理累积。
可能忽略低敏感性但关键的反应:某些反应虽然对目标组分的净浓度变化影响较小(敏感性系数低),但在特定时间或条件下可能主导该组分的生成或消耗。例如,在低温燃烧阶段,某些链传递反应可能对自由基(如H、O、OH)的平衡起关键作用,但由于其对主要组分(如CO₂、H₂O)的敏感性不高,可能被错误剔除。
路径分析能够弥补这些不足,通过追踪组分的来源与去向,确保机理简化时既保留重要的生成路径,也保留关键的消耗路径,避免因片面依赖敏感性分析而导致机理失真。
2.路径分析的具体应用示例
以NOx生成机理为例,假设我们关注NO的生成与消耗:
敏感性分析筛选出的关键反应可能包括:
N + O₂ → NO + O(主要NO生成路径)
N₂ + O → NO + N(高温下重要)
NH + O → NO + H(含氮燃料燃烧中的关键路径)
路径分析补充的消耗反应可能包括:
NO + H → N + OH(NO的还原路径)
NO + O → N + O₂(在贫燃条件下可能影响NO浓度)
NO + CH₃ → HCN + H₂O(在碳氢燃烧中可能发生)
若仅依赖敏感性分析,可能会忽略NO的某些消耗路径,导致模拟时NO浓度被高估。而通过路径分析,可以明确NO的生成与消耗平衡,确保简化机理的合理性。

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








