前 言
iPSC具有分化成几乎所有类型细胞的多能性,广泛用于细胞免疫治疗、再生医学、疾病建模、药物筛选和个性化诊疗。同时iPSC不受限于来源,具有可以无限扩增的能力,为提升药物可及性提供了可能。iPSC的分化需要相应的细胞因子,不同细胞因子可以使iPSC生成不同类型的细胞,用于不同的研究。
01 iPSC概述
iPSC全称诱导多功能干细胞(Induced pluripotent stem cells),是一种通过成熟体细胞重新编程获得的多能干细胞,由日本科学家Shinya Yamanaka于2006年建立,并获得2012年的诺贝尔奖。他们利用4种转录因子(Oct4、Sox2、Klf4和c-Myc)的过表达将小鼠胚胎成纤维细胞诱导成为类似胚胎干细胞(ESC)的状态。iPSC在形态、基因和蛋白表达、表观遗传修饰状态、细胞倍增能力、类胚体和畸形瘤生成能力、分化能力等方面都与ESC极为相似,具备和ESC一样的应用潜能,几乎可以分化成为所有类型的细胞。
目前用于细胞治疗的主要有成体干细胞、胚胎干细胞以及诱导多功能干细胞。成体干细胞来源困难、体外扩增较难且有分化局限性;胚胎干细胞的分化潜能最大,但却一直受限于伦理及个体化差异、免疫排异等问题,因此发展和转化应用也受到一定局限。诱导多功能干细胞的发现彻底打破了ESC临床应用中的细胞来源和伦理问题,为个体化治疗提供了有力的支持,极大地克服了干细胞治疗中的免疫排斥问题,开辟了再生医学的全新领域。
| 来源 | 优势 | 局限 |
| 成体干细胞 | ·没有伦理学问题 ·自体来源的没有组织相容性问题 ·安全性好,理论上没有致瘤性 | ·含量低,难分离纯化 ·体外扩增难 ·尚未从人体全部组织中分离出成体干细胞 ·一些具有遗传缺陷的疾病中,自体来源的干细胞可能也有缺陷,不适合用于移植 |
| 胚胎干细胞 | ·增殖能力强 ·分化能力强,可形成内、中、外三胚层及各类细胞 | ·伦理问题 ·异体来源会有排异反应 ·有致瘤风险 |
| 诱导多能干细胞 | ·增殖能力强 ·分化能力强 ·避免了伦理问题 ·自体来源的免疫原性较低 | ·操作复杂且重编程效率低 ·有诱导突变的可能 ·长期安全性尚未证实 |
02 iPSC主要应用
目前,iPSC通过基因工程改造后可用于自体或异体 T细胞或NK细胞疗法,也可分化成其它功能性细胞,如心肌细胞、胰岛细胞、上皮细胞、间质干细胞或神经元等,因此iPSC衍生的细胞疗法主要为免疫细胞疗法与干细胞再生疗法。基于iPSC的药物筛选也被广泛应用。
1)iPSC衍生的免疫细胞疗法
细胞疗法近年来热度“狂飙”,并在血液类肿瘤治疗领域取得佳绩。但是无论是CAR-T,还是在实体瘤领域具有更大潜力的CAR-NK或NK,都面临着细胞来源不足或质量不均一的问题,因此iPSC衍生的细胞成为很好的选择。
iPSC可以在体外无限培养,分化为淋巴细胞并生成主细胞系,为T细胞、NK细胞等细胞疗法提供了可再生的、稳定的细胞来源,与此同时,iPSC在体外易于接受基因工程改造,有潜力接受多轮的基因工程优化步骤,改造潜力更高,可以实现控制细胞分化过程,增强细胞疗法的持久性。
目前大多iPSC衍生的免疫细胞疗法处于临床前或者更早的药物发现阶段,只有Fate公司的iNK及iT产品成功进入了临床试验阶段。其他的如Cytovia的CAR-iNK用于实体瘤治疗,Century的CAR-iNK和CAR-iT处于临床前,用于治疗B细胞淋巴瘤、复发性胶质母细胞瘤、急性髓系白血病等。在国内,启函生物、赛元生物、爱凯生物、昕传生物、济元基因等公司正在进行iNK、CAR-iNK、CAR-iT、CAR-iMAC相关临床前或药物发现研究。
2)iPSC衍生的再生疗法
iPSC衍生的功能细胞种类更多、涉及的适应症也更广泛,包括心衰、糖尿病、神经退行性疾病甚至是脱发等领域。第一项临床试验在2014年启动,使用人iPSC分化的视网膜色素上皮细胞(Retina pigment epithelium, RPE)治疗黄斑变性。帕金森是目前iPSC衍生再生疗法最主要的适应症之一,有多家公司在这一领域布局。在2021年,iPSC诱导的多巴胺能神经元疗法DA01成功进入1期临床试验。Heartseed公司的HS-001是心衰领域唯一迈入临床阶段的iPSC衍生细胞疗法,这是一种异体iPSC衍生的心室心肌细胞,适应症为缺血性心脏病伴有重症心力衰竭。
3)基于iPSC的药物筛选
不同于细胞治疗临床应用上的各种限制,iPSC在构建疾病模型上的应用则发展更快速。将患者的体细胞重编程为特异性iPSC,再将其诱导分化为疾病相关的细胞类型,构建体外疾病模型,更好的模拟人类疾病,指导精准治疗。在有效化合物的筛选上,由于iPSC所构建的疾病模型能够更精准地反映出疾病相关细胞的状态及表型,提供更加接近临床的药物数据,因而在高通量筛选及药物优化上发挥着重要作用。在药物毒性检测上,利用iPSC建立的患者特异性细胞有利于评价药物对不同患者的治疗效果及副作用。
迄今为止,已有多个使用iPSC开发成功的疾病模型,如阿尔茨海默病和帕金森病已使用源自iPSC的神经元进行建模,使用星形胶质细胞与神经元的共培养来模拟肌萎缩侧索硬化症的病理学。尤其是近年来3D类器官的火爆,更是加速iPSC相关疾病模型的构建,如脑、肠、肝脏、胰腺、肾及肺等相关的多种类器官疾病模型。
03 iPSC分化相关细胞因子
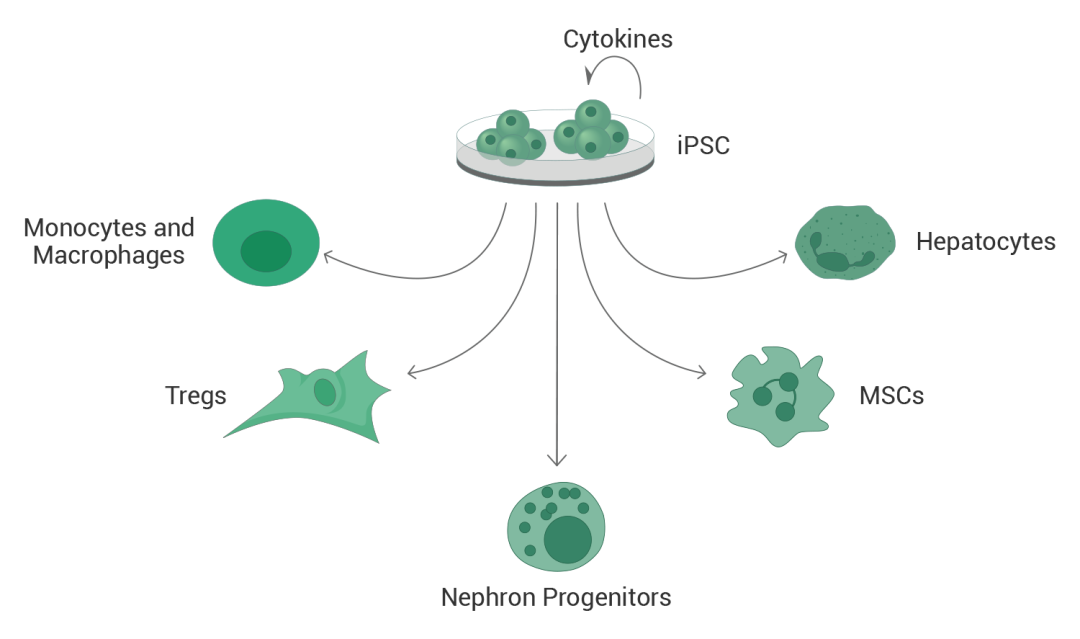
iPSC的广泛应用是基于分化能力。通过不同的细胞因子,iPSC能够分化成不同类型的细胞。将人类iPSCs分化为各种细胞系常见的因子有GM-CSF、Activin A、DLL4、NOG、TNF-α、IL-2、VEGF、FGF、IL1β、EGF等。
| 分化的细胞类型 | 主要相关细胞因子 |
| 单核细胞、巨噬细胞 | GM-CSF、IL-3、M-CSF |
| 调节性T细胞(Treg) | DLL-4、IL-2、BMP4、TGF-β、IL-33、IL-10 |
| 肾祖细胞 | Activin A、BMP4、MRAP、FGF2 |
| 间充质干细胞 | NOG、TNF-α、BMP2、TGF-β、FGF2 |
| 肺上皮细胞谱系 | FGF10、BMP4、TGF-β、FGF2 |
| 内皮细胞 | VEGF121、FGF2、Ang-1、TNF-α |
| 肝细胞 | EGF、OSM、HGF |
| 巨核细胞 | IL-1β、TPO、SCF |
iPSC这一革命性技术的出现为再生医学开辟了全新的道路,基于iPSC的临床试验和疾病模型研究较多。iPSC与细胞免疫治疗、类器官等新技术相结合,在潜在治疗方面取得了巨大进展。
✦义翘神州iPSC细胞因子相关产品
义翘神州提供一系列与干细胞相关的精品细胞因子产品,以支持干细胞研究。这些产品经过严格的质量控制,活性已经得到验证,并且多次被客户引用于顶级期刊。
Human DLL4 Protein,Cat: 10171-H02H
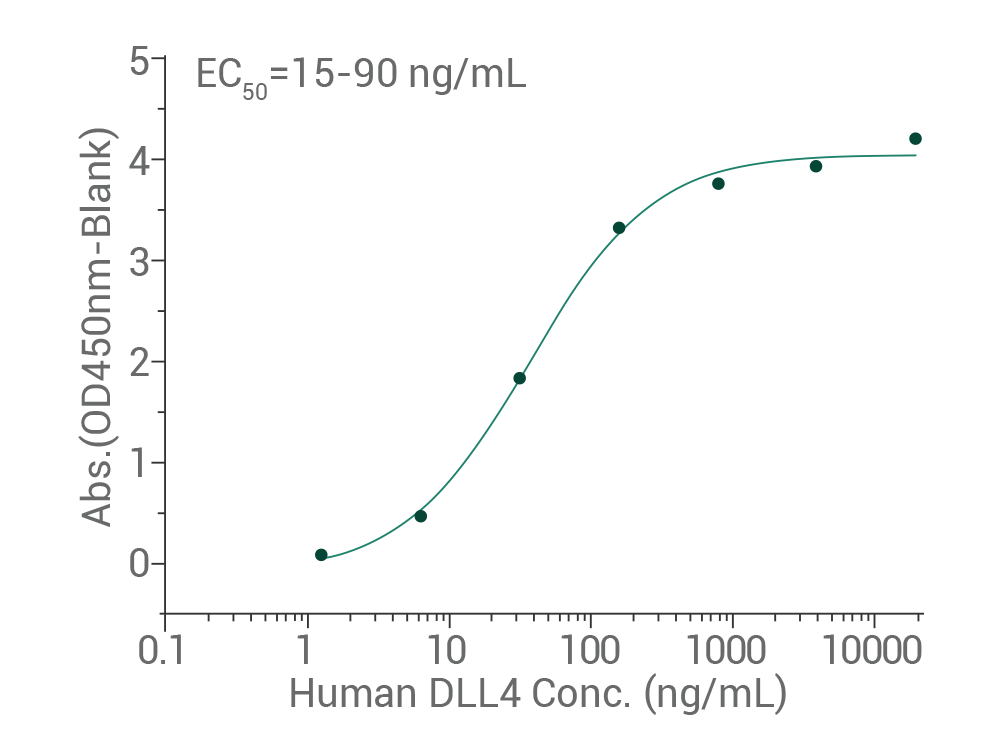
Immobilized mouse NOTCH1 (Cat: 50654-M08B) can bind human DLL4
Human GM-CSF Protein,Cat: 10015-HNAH
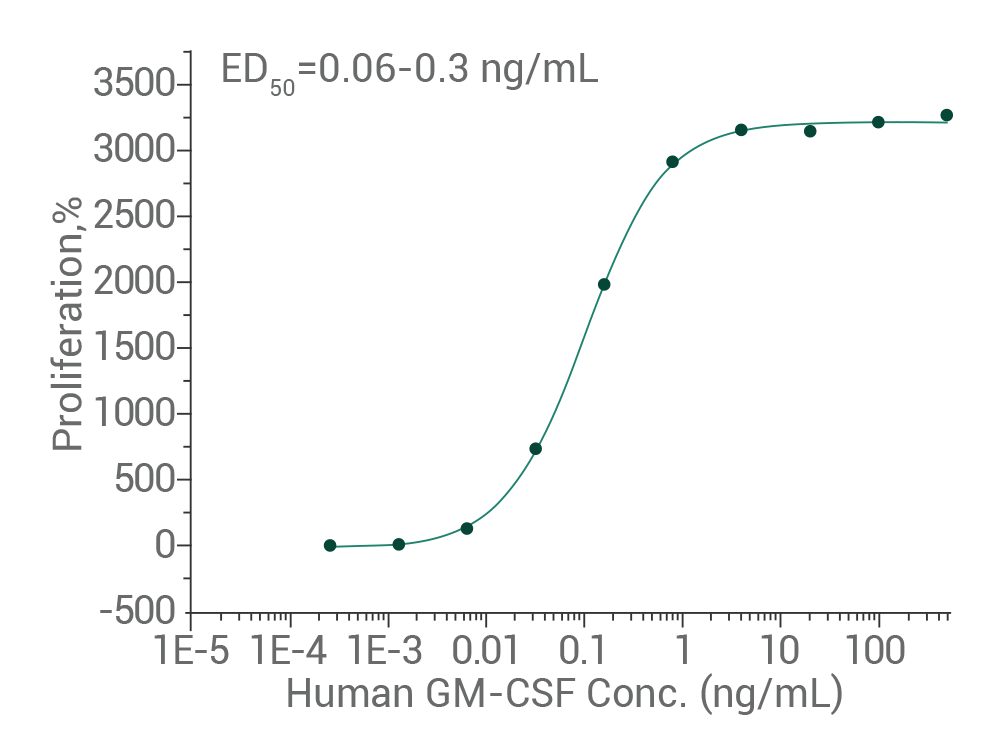
Cell proliferation assay using TF-1 human erythroleukemic cells
Human Activin A Protein,Cat: 10429-HNAH
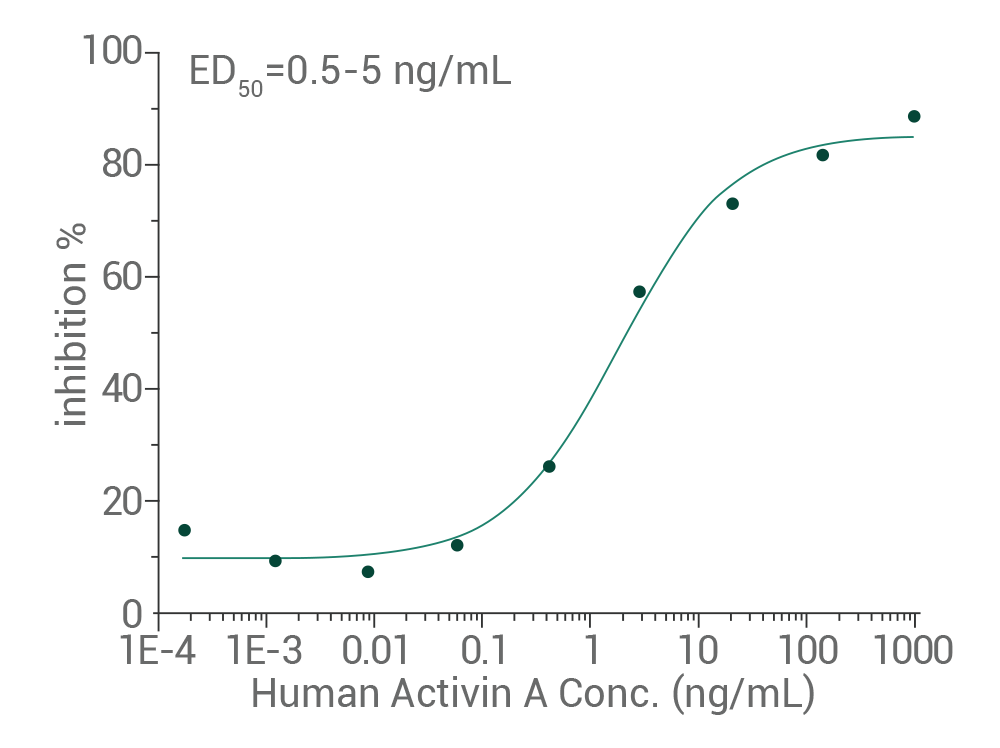
Ability to inhibit proliferation of MPC-11 cells
| GMP级iPSC相关细胞因子 | |||
| 货号 | 靶点 | 内毒素 | 纯度及活性 |
| GMP-10015-HNAH | GM-CSF | < 5 EU/mg | ≥95%,Active |
| GMP-10452-HNAH | OSM | < 5 EU/mg | ≥95%,Active |
| GMP-10605-HNAE | EGF | < 0.01 EU/mg | ≥95%,Active |
| GMP-10602-HNAE | TNFA | < 5 EU/mg | ≥95%,Active |
| GMP-11848-HNAE | IL2 | < 5 EU/mg | ≥95%,Active |
【参考文献】
[1] Guidelines and Techniques for the Generation of Induced Pluripotent Stem Cells
[2] Induced pluripotency: history, mechanisms, and applications
[3]INDUCED PLURIPOTENT STEM CELLS AND THEIR USE IN HUMAN MODELS OF DISEASE AND DEVELOPMENT
[4] Induced pluripotent stem cells: applications in regenerative medicine, disease modeling, and drug discovery
[5] The promise of induced pluripotent stem cells in research and therapy
























 1138
1138

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










