
文章标题:配体-受体相互作用结合组织病理学改善 HPV 阴性头颈部鳞状细胞癌的预后模型
期刊:npj precision oncology
影响因子:6.80
JCR分区:Q1
中科院分区(2025):医学1区 Top
发表时间:2025年2月
研究关键词:公共数据库挖掘,单细胞,空间组,病理组学
基于配体-受体特征的HPV阴性HNSC预后风险模型
研究者们使用了TCGA-HNSC(头颈部鳞状细胞癌)队列的bulk RNA-seq数据(395个样本)。利用BulkSignalR工具,识别了667个在HPV阴性肿瘤中存在的配受体对。通过最佳截断算法(best-cutoff algorithm),筛选出150个与总生存期(OS)和无进展间隔(PFI)显著相关的配受体对。其中,52个被归类为不利(高风险)配对,98个被归类为有利(低风险)配对。随机森林生存模型及Lasso-Cox回归模型进一步对这些显著性配体-受体对进行优化,最终筛选出与14个与患者预后最为相关的配体-受体对。根据该模型评估的风险等级,患者的总体生存被划分为高风险组和低风险组。生存分析结果显示两组之间存在显著差异。PPI网络和Kmeans聚类方法解释了不同配受体对之间的交互关系,并将其划分为三簇。
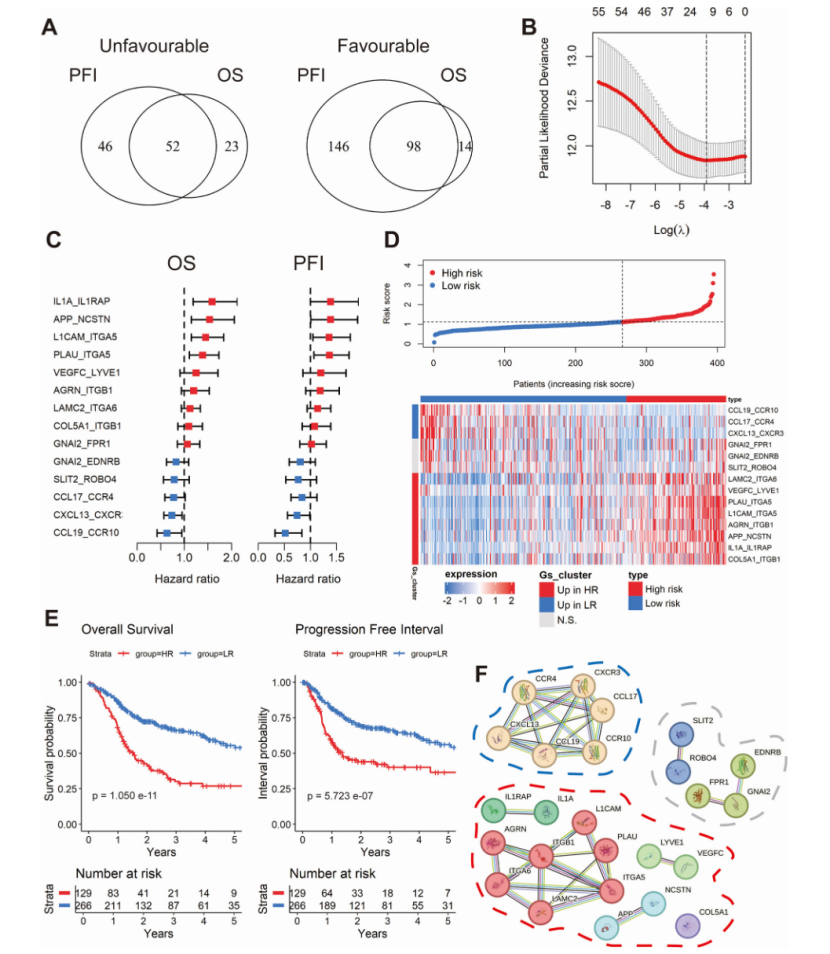
预后风险模型模型的机制解释
预后风险组的分子动力学
为了解析不同预后风险群体患者的分子动力学,研究者比较了低风险患者与高风险患者之间的全基因组变化情况。与低风险肿瘤相比,高风险肿瘤中具有更多的全基因组改变数量。拷贝数变异分析(CNV)显示,高风险群体存在显著的8p和12p缺失及11p扩增现象,而肿瘤突变负荷(TMB)在不同风险组之间未表现出显著差异。此外,高风险患者的TP53突变频率相对更高,低风险患者中RELN、NSD1、CASP8等体细胞突变频率相对更高。差异基因分析结果表明多个配体-受体对同时存在在对应的差异基因列表中(|Log2FC|≥1;FDR≤0.05)。基因集富集(GSEA)结果显示高风险群体显著富集在细胞外基质重塑、TGF-beta等信号通路中。基于oncoPredict 的药物敏感性分析发现六种对高风险患者有潜在益处的药物,包括络氨酸酶抑制剂、TGF-beta抑制剂等。
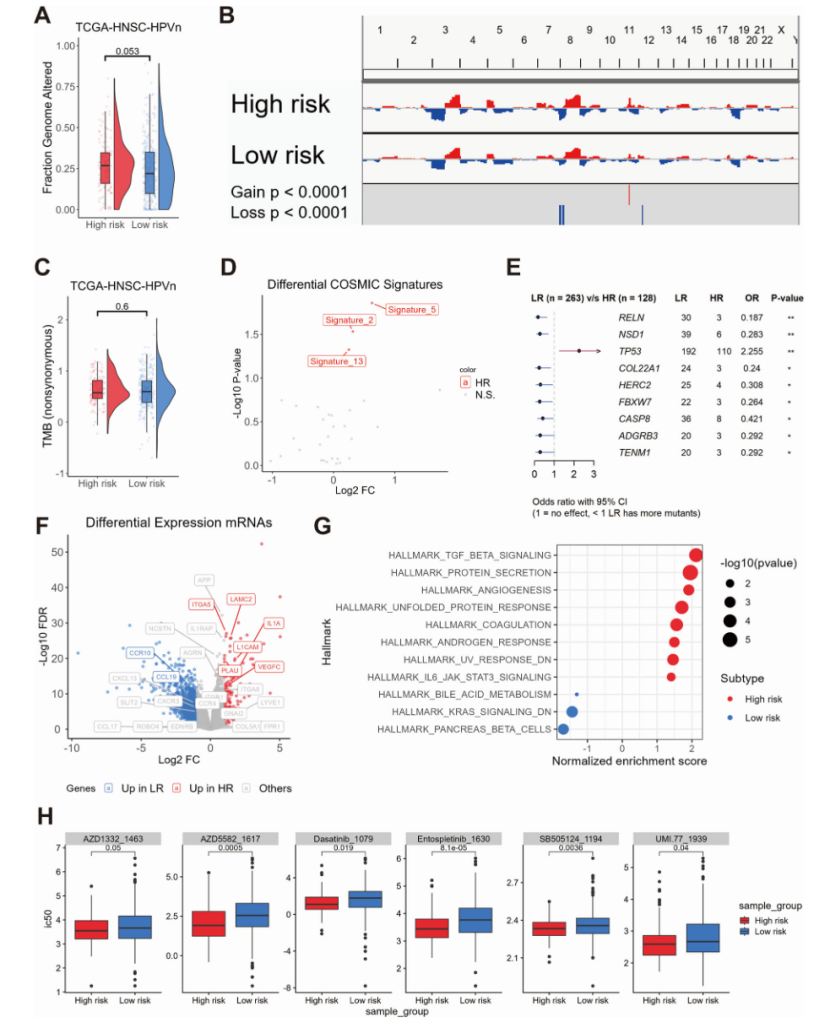
预后模型相关配体-受体对的细胞和空间分布
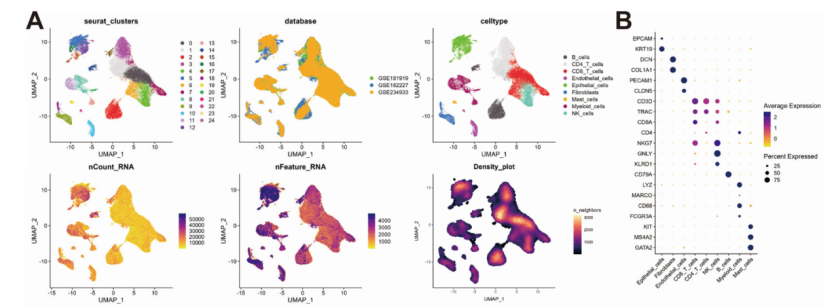
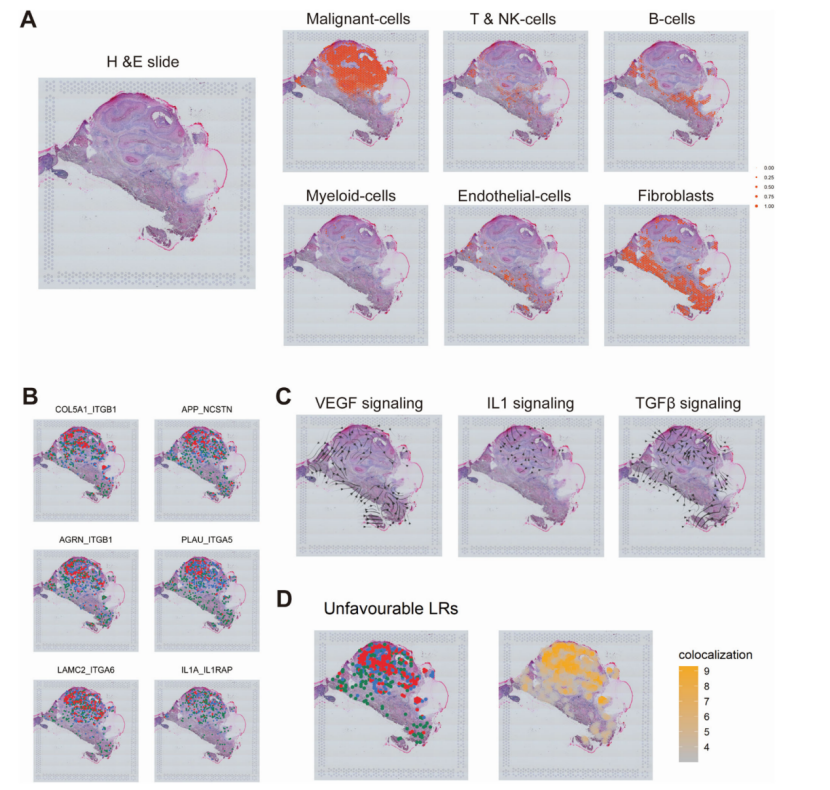
为了进一步研究预后配体-受体对的细胞分布,研究者分析了来自三个数据集(GSE181919、GSE182227、GSE234933)的 34 个 HPV 阴性 HNSC 样本的单细胞 RNA 测序数据。数据集包含10万个HNSC细胞,共鉴定出8种主要的细胞类型。在低风险群体中,配体-受体对之间的相互作用主要在髓系细胞与T,B细胞之间(图C),而在高风险群体中则主要富集在上皮细胞、成纤维细胞和内皮细胞之间(图D)。
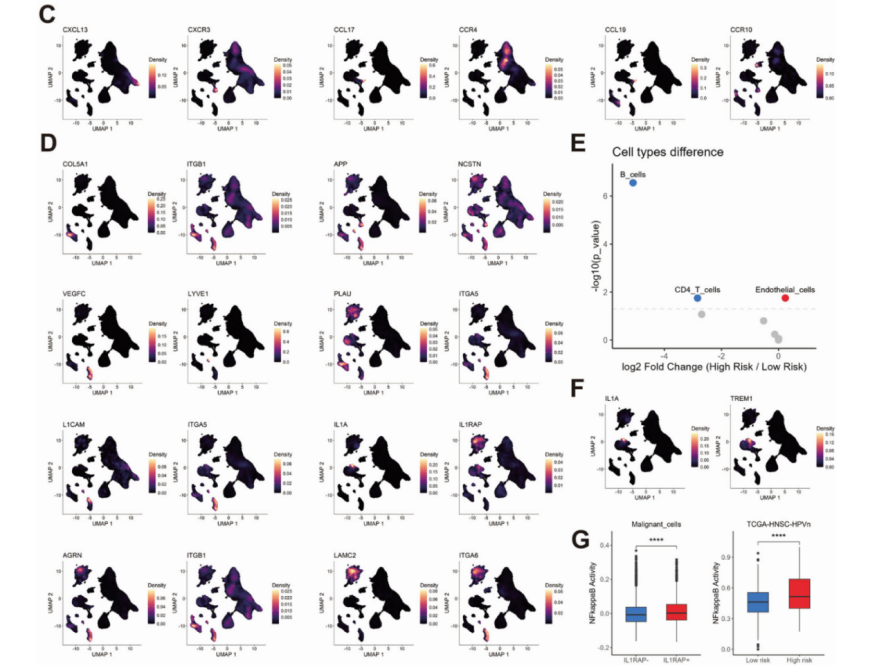
预后模型相关配体-受体对的空间分布
研究者进一步将单细胞 RNA 测序识别的细胞类型进行了空间映射,从而揭示了肿瘤内的空间排列(图 4A)。与高风险肿瘤相关的配体-受体对,包括 IL1A_IL1RAP、COL5A1_ITGB1等在肿瘤区域显著富集(图 4B)。 风暴图映射了关键信号通路, TGF-β和 VEGF 信号表明了肿瘤与间质相互作用,而IL1 的相互作用主要发生在肿瘤内部,可能与髓系细胞相关(图 4C)。
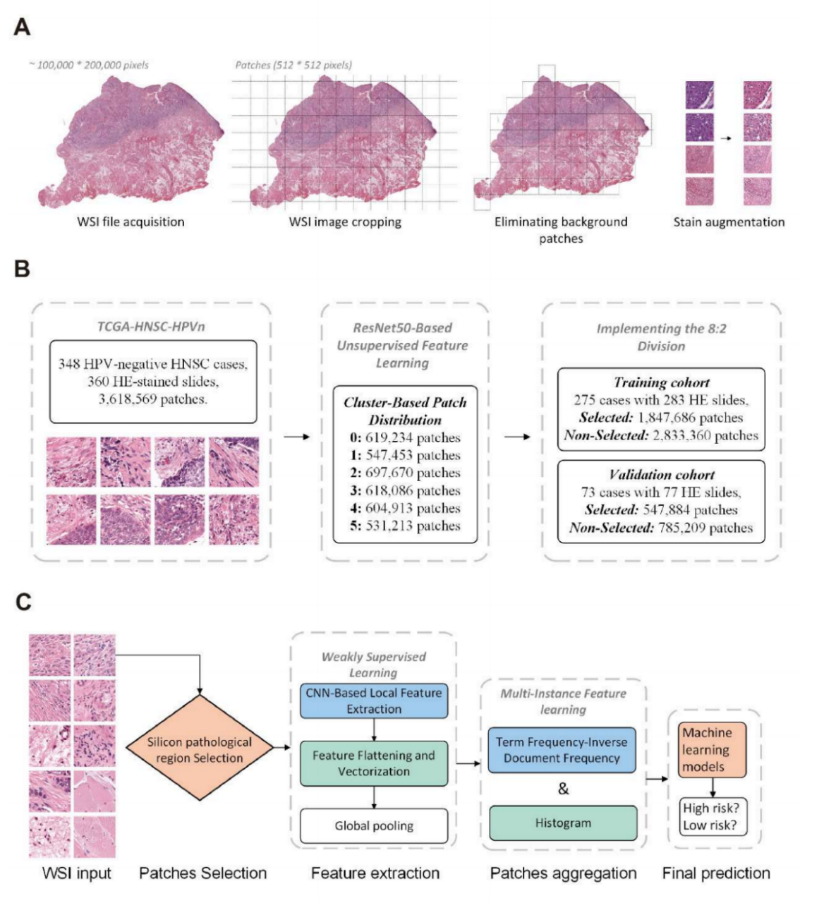
病理预测模型的建立与验证
本研究期望用病理切片预测上述基于配受体对得到的高低风险组,采用病理区域注释策略比较不同病理区域对模型的效能。最后根据注释的结果对预测结果进行生物学解释。
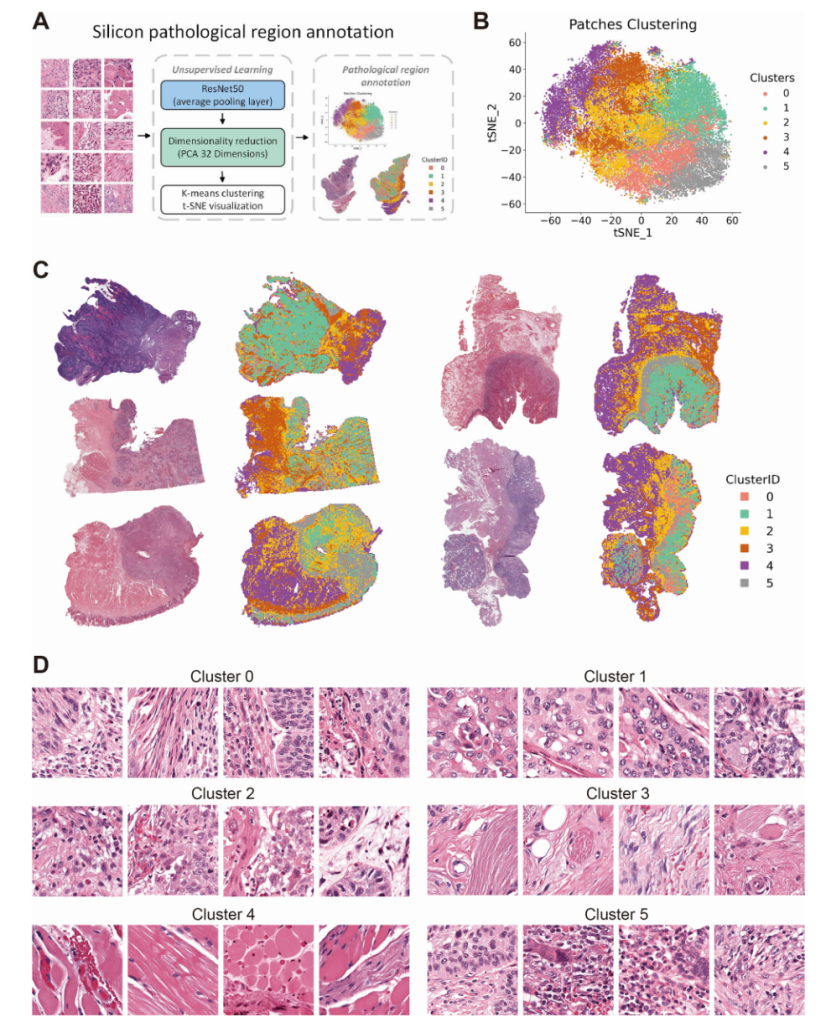
病理区域注释策略及对模型的改进
所有WSI被切割成3,618,569 个单独的补丁,并进行图片颜色归一化。采用预训练模型ResNet50对每个patch提取了2024维特征,PCA将特征降维至32维,进一步采用K-means对patch进行无监督聚类将patch聚类为6个类别。将patch类别mapping至原始WSI图像上,以确认不同组织区域的patch聚类分布。结果表明,簇0和簇2代表靠近肿瘤组织的间质区域;簇1为肿瘤组织;簇3和簇4被归类为基质和肌肉组织;簇5则被分类为肿瘤侵袭的边缘区域。
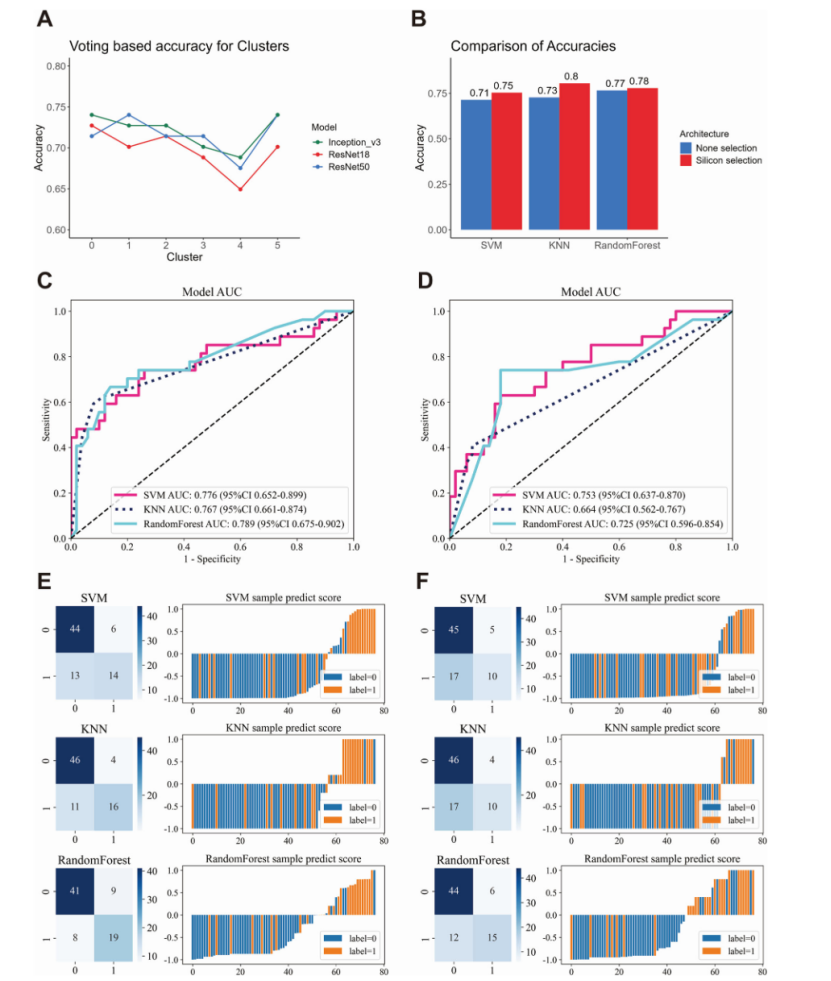
模型建立与评估
该分析的目的是确定与没有选择的弱监督深度学习相比,硅病理区域选择策略是否增强了风险预测的有效性。共有 348 例和 360 张 HE 染色载玻片以 8:2 的比例随机分为训练组和测试组。具体来说,275 例 (283 个 WSI) 被分配给训练队列,73 例 (77 个 WSI) 被分配给测试队列。多实例学习 (MIL) 架构显示,采用硅病理区域选择策略的模型在不同机器学习模型中表现出明显更高的准确性(图 6B),同时增强 AUC 和预测性能(图 6C-F)。
病理预测模型的生物学解释
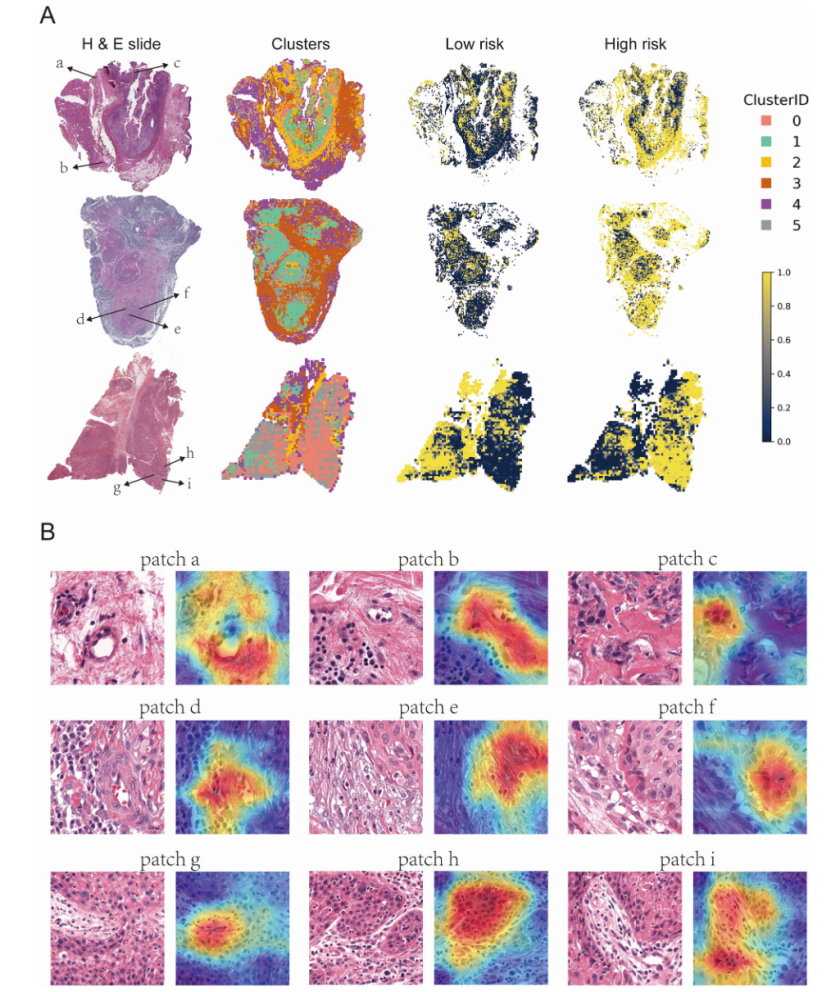
下图为正确预测的高危肿瘤的可解释性分析。在这些样本中,预测为高风险的斑块表现出肿瘤和内皮细胞相互作用以及肿瘤-基质相互作用等特征。 Grad-CAM 热图突出显示了集中在血管浸润和基质浸润部位的高风险斑块—侵袭性肿瘤表型的标志通常与不良临床结果相关。这种可视化为驱动高风险分类的关键形态学特征提供了可解释的见解。
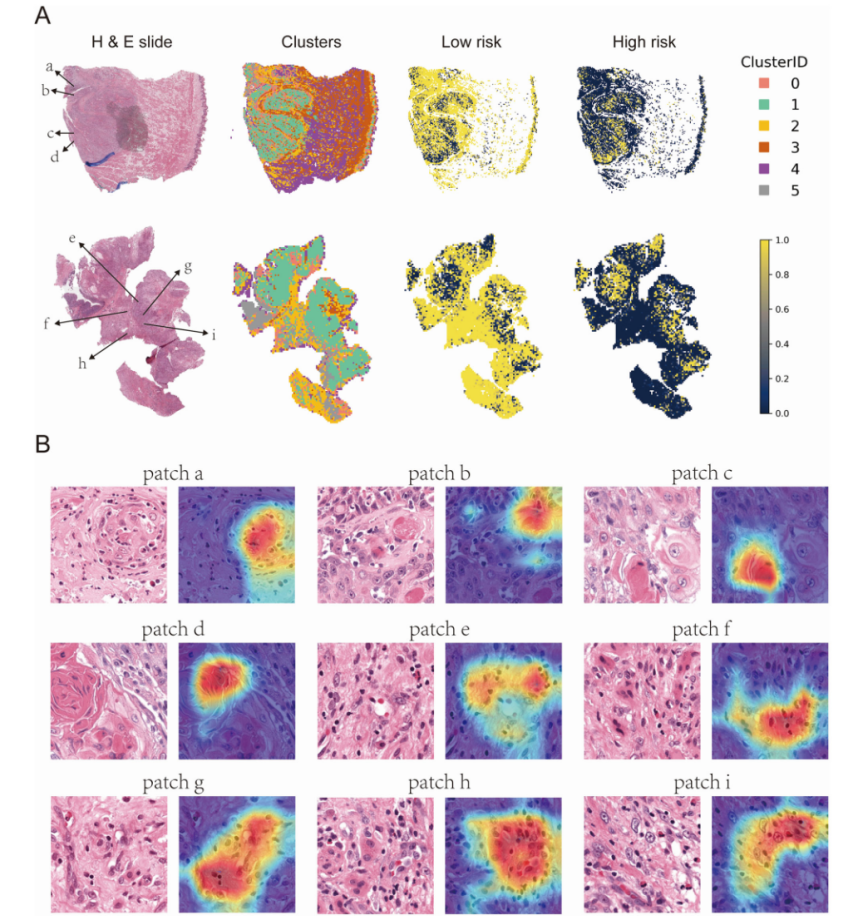
下图为正确预测的低风险肿瘤的可解释性分析,揭示了表明侵袭性行为较弱的形态特征,特别是角化(分化良好肿瘤的标志)和强大的免疫细胞浸润,反映了积极的抗肿瘤反应。Grad-CAM 热图突出了这些特征,这两者都与更有利的临床结果有关。
FENG B, ZHAO D, ZHANG Z, et al. Ligand-receptor interactions combined with histopathology for improved prognostic modeling in HPV-negative head and neck squamous cell carcinoma [J]. NPJ Precis Oncol, 2025, 9(1): 57.


























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










