热敷贴(袋)是一种外用物理治疗器械,通过铁粉氧化反应产生热量,以热传导方式作用于人体局部,促进血液循环,辅助消炎、消肿和止痛。其核心发热材料不含药物成分,符合Ⅱ类医疗器械管理要求。为确保产品性能稳定,需结合YY0060-2018等标准,通过专用测试设备(如热敷贴温度特性测试仪)进行严格质量控制。
一、产品组成
热敷贴(袋)通常由以下几部分组成:
1、外袋:具有密封性能,隔绝空气,防止发热包中水分蒸发。
2、无纺布层:覆盖在透气膜上,防止透气膜磨损,增加使用时的舒适度。
3、透气层:控制放热时间和温度,防止温度过高或过低。
4、发热料层:由铁粉、水、活性炭、食盐等原料混合而成,是热敷贴的核心组成部分。
5、粘贴层:使热敷贴可以直接固定于皮肤或衣物上。
6、防粘隔离层:在使用前保持粘性,方便使用。
二、工作原理
主要材料(铁粉、水、活性炭、食盐等,且不含任何药物成分),按一定比例放入内袋密封,铁粉接触空气中的氧气,在盐和水作用下发生化学反应产生热量,产生的热量通过热传导作用传递到人体局部,使局部温度升高,扩张血管,促进血液循环,从而达到辅助治疗的效果。
三、风险管理分类
在我国的医疗器械注册管理分类目录09物理治疗器械下,热敷贴(袋)的风险等级管理类别为Ⅱ类。

四、注册单元划分原则和实例
热敷贴(袋)的注册单元原则上以功能、性能指标和预期用途为划分依据。
1.产品的功能不同应作为不同注册单元进行注册。
如:多功能敷贴类产品和单一功能敷贴类产品,由于功能、性能指标和预期用途均不相同,应作为不同注册单元。
2.产品温度特性的最高温度和持续时间不同应作为不同注册单元进行注册。
如:直接与人体皮肤接触和不直接接触产品最高温度不同,材料的生物学评价要求不同,应作为不同注册单元。
五、产品常见标准
国内注册-检测方案
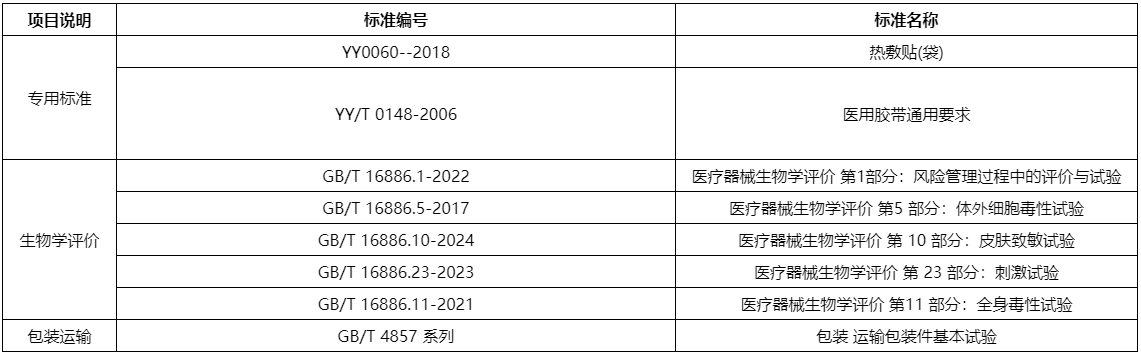
国外注册-检测方案
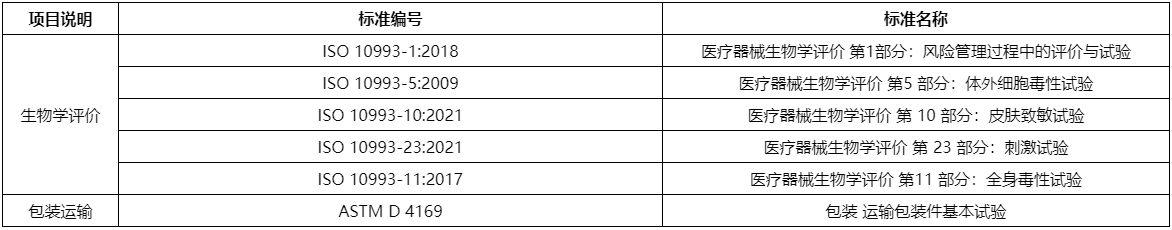
备注:上述标准包括了产品技术要求中经常涉及到的标准;企业需要根据产品的特点引用其他适用的标准。
六、热敷贴温度特性测试仪的应用
Delta德尔塔仪器热敷贴温度特性测试仪完全满足 YY0060-2018《热敷贴》标准设计研发制作而成,用于模拟人体恒温反应环境,自动检测自动检测热敷灵、热敷眼贴、暖宝宝产品从发热开始至40℃以上经过最高温度又回落到40℃的时间。可同时测试1-10个样品,内部温度恒定,不受外界温度影响,温度可以进行自动调节;自动巡检1-10个样品的反应温度变化并对每一个样品形成温度特性曲线。

主要技术参数:
水浴容积:120L
控温范围:常温~ 90℃(温度任意可调)
控温精度:35±0.1℃
控温方式:液晶数显 PID控制
工作通道: 10通道检验(10个传感器)
加热方式:进口电热管加热
工作板面尺寸:长度:600mm高度:300mm
温度采集系统:进口PT100温度传感器(专业定制)( 10组带导线温度采集器已安装在主机中)
量程:-50~150℃
精度:±0.01℃
采集速度:>1点/s(可选)
工作环境:温度 : 95~-40℃/相对湿度:《 80%
工作电源:电压:220V±10%
整机功率:1500W
组成如下:
1、恒温试验装置1台
2、高精度温度传感器10根
3、温度采集系统1套
4、热敷灵分析软件1套
测试意义
- 验证发热均匀性、最高温度及持续时间,规避烫伤风险。
- 确保产品符合生物学评价要求(如无皮肤刺激或过敏反应)。
热敷贴(袋)类产品常见不合规原因包括:
材料老化或变质、发热效果不达标、发热不均匀、皮肤刺激或过敏反应、烫伤风险、包装密封性不足、标签信息不准确等。企业应着重注意产品上述项目或功能完善。
七、总结
热敷贴(袋)的注册需严格遵循国内外标准,结合专用测试设备(如热敷贴温度特性测试仪)确保性能可靠。Delta德尔塔仪器的热敷贴温度特性测试仪以精准控温与智能分析为核心,严格遵循行业标准,为热敷贴研发与质检提供高效保障。凭借可靠性能与技术创新,助力企业优化产品安全及用户体验,推动热疗领域高质量发展。企业应重点关注温度特性、生物学评价及包装密封性,通过科学的检测流程规避合规风险,提升产品市场竞争力。























 1156
1156

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








