构建类器官模型通常涉及在3D环境中培养多能干细胞或成体干细胞。虽然传统的3D培养技术是一种简单且有效的方法,用于在实验室环境中生产类器官,但它们往往缺乏精确控制。
嗨,大家好,这里是知识泥土汲取知识营养,本期内容我们了解“类器官的微环境控制”。
一 生化微环境的控制
类器官的发育依赖于适时激活形态发生信号转导通路,以引导细胞命运的规范化和不同细胞类型的物理分离,这些过程共同促进自组织。

图片来源:Kretzschmar K, Clevers H. Organoids: Modeling Development and the Stem Cell Niche in a Dish. Dev Cell. 2016 Sep 26;38(6):590-600. doi: 10.1016/j.devcel.2016.08.014.
传统类器官培养中,通过在特定时间点添加外源性形态原来实现这一过程。形态原和细胞分泌的可溶性因子在干细胞局部微环境中形成生化梯度,但这些梯度难以控制,并且通常无法精确模拟体内器官发生过程中关键的形态原渐变分布。
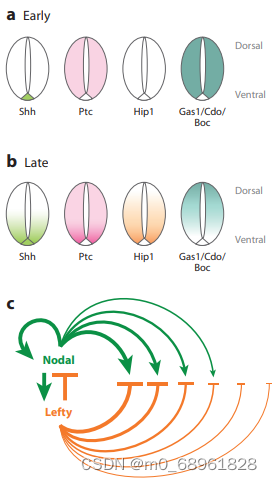
图片来源:Rogers KW, Schier AF. Morphogen gradients: from generation to interpretation. Annu Rev Cell Dev Biol. 2011;27:377-407. doi: 10.1146/annurev-cellbio-092910-154148.
研究人员利用微工程技术解决类器官培养中形态原梯度控制的问题。例如,为模拟神经管发育,开发了包含微通道的微流控系统,通过这些通道在富含胚胎干细胞的水凝胶中产生稳定的形态原梯度。这种微工程平台能够模拟神经管背腹轴上的关键信号分子梯度,诱导脊髓发育中的神经管模式化。类似的方法也应用于人脑类器官芯片的开发,以研究尼古丁对大脑皮质发育的影响。
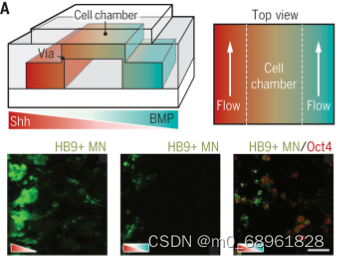
图片来源:Park SE, Georgescu A, Huh D. Organoids-on-a-chip. Science. 2019 Jun 7;364(6444):960-965. doi: 10.1126/science.aaw7894.
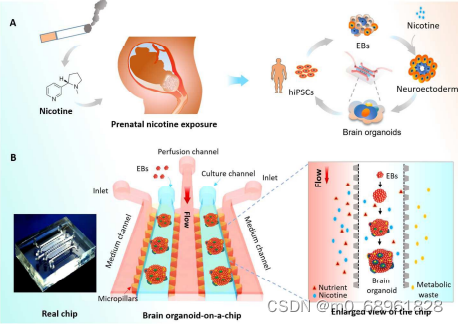
图片来源:Wang Y, Wang L, Zhu Y, Qin J. Human brain organoid-on-a-chip to model prenatal nicotine exposure. Lab Chip. 2018 Mar 13;18(6):851-860. doi: 10.1039/c7lc01084b.
最近的研究表明,结合源汇方法和微图案培养支架可以在干细胞和类器官培养中产生生理生化梯度。例如,肠道芯片系统通过在模仿肠绒毛和隐窝的改良Transwell插入物上的微加工阵列中培养自我更新的上皮细胞,用于模拟肠上皮中的Wnt和BMP信号转导的天然相反梯度。
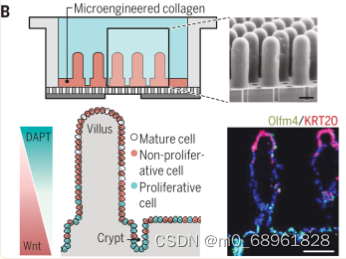
图片来源:Park SE, Georgescu A, Huh D. Organoids-on-a-chip. Science. 2019 Jun 7;364(6444):960-965. doi: 10.1126/science.aaw7894.
二 营养供应的控制
在3D培养中,类器官通过被动扩散获取营养和氧气以及清除废物,但随着体积增大,这种方法无法满足其代谢需求,限制了生长和成熟。
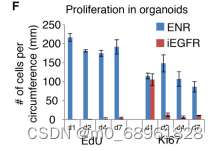
图片来源:Basak O, Beumer J, Wiebrands K, et.al.. Induced Quiescence of Lgr5+ Stem Cells in Intestinal Organoids Enables Differentiation of Hormone-Producing Enteroendocrine Cells. Cell Stem Cell. 2017 Feb 2;20(2):177-190.e4. doi: 10.1016/j.stem.2016.11.001.
发育生物学研究指出,胚胎发育与血管发育紧密相关,功能性脉管系统对器官发生的后期阶段至关重要。因此,使类器官血管化是一种有前景的策略,可以解决营养供应问题并延长其寿命。
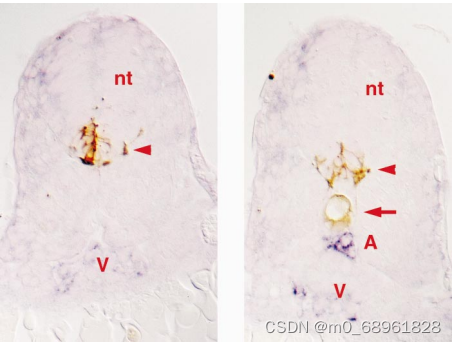
图片来源:Weinstein BM. What guides early embryonic blood vessel formation? Dev Dyn. 1999 May;215(1):2-11. doi: 10.1002/(SICI)1097-0177(199905)215:1<2::AID-DVDY2>3.0.CO;2-U.
Shirure等人开发的肿瘤类器官芯片可模拟可灌注血管,由三个相互连接的腔室支持内皮细胞形成3D血管网络并向乳腺癌类器官结构进行血管生成。这一平台不仅允许类肿瘤的血管化,还能在生理流动条件下进行灌注,从而模拟体内肿瘤微环境的运输特征。该模型能够长期培养血管化肿瘤,并且还可用于评估患者对化疗药物如紫杉醇的特异性反应,为临床前药物筛选提供了有价值的研究工具。
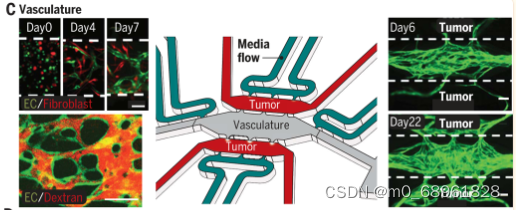
图片来源:Park SE, Georgescu A, Huh D. Organoids-on-a-chip. Science. 2019 Jun 7;364(6444):960-965. doi: 10.1126/science.aaw7894.
尽管在微流控器件中实现了3D多细胞构建体的血管化和灌注,但这一方法尚未在多能干细胞衍生类器官的培养中得到验证,因为特殊的培养基可能干扰血管自组装和重塑。作为替代,可以使用小型化生物反应器,利用强制对流和介质混合来改善类器官的营养供应,延长其维护时间。这种方法已在脑和胰腺类器官模型中得到了应用。
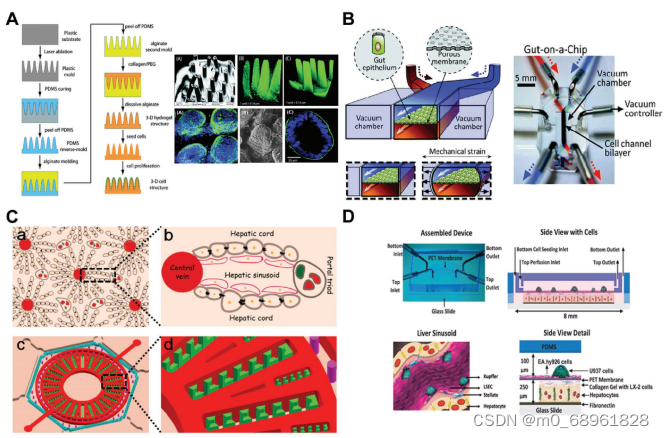
图片来源:Lee SH, Sung JH. Organ-on-a-Chip Technology for Reproducing Multiorgan Physiology. Adv Healthc Mater. 2018 Jan;7(2). doi: 10.1002/adhm.201700419.
三 生物物理微环境的控制
发育中的胚胎受到多种机械力的作用,包括由单细胞和大细胞群体(如心脏和胎儿呼吸运动)产生的牵引力、流体剪切应力和固体机械力。这些作用力与形态原和细胞外基质信号共同作用,调节器官的发育和成熟。在培养物中缺乏这种生物力学控制是开发成熟和生理相关类器官模型的一个关键限制。
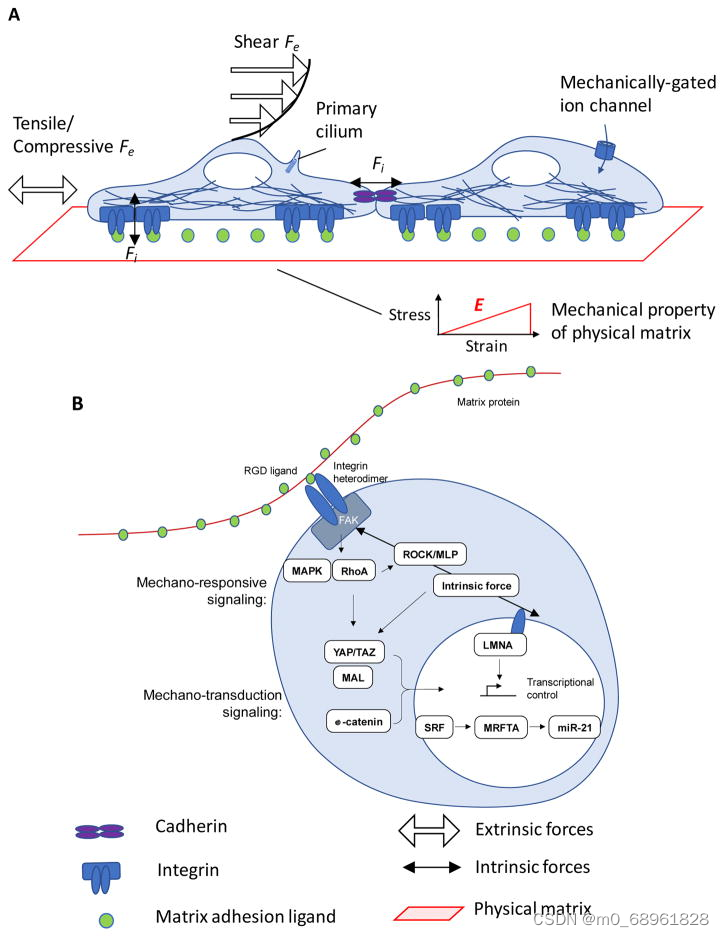
图片来源:Vining KH, Mooney DJ. Mechanical forces direct stem cell behaviour in development and regeneration. Nat Rev Mol Cell Biol. 2017 Dec;18(12):728-742. doi: 10.1038/nrm.2017.108.
为了模拟体内环境中的机械力,最近的研究已经开发了机械可驱动的微工程平台,应用于类器官培养。例如,Lee等人创建了一种胃芯片模型,其中包含从人多能干细胞生成的胃类器官,这些器官在Matrigel中培养,并通过一对微量移液器插管使流体进入内室。利用连接到移液器的蠕动泵,这个平台能够通过类器官产生流体流动,模拟体内胃的管腔流动和节律性收缩。
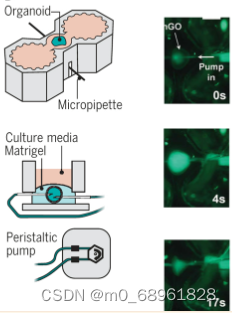
图片来源:Park SE, Georgescu A, Huh D. Organoids-on-a-chip. Science. 2019 Jun 7;364(6444):960-965. doi: 10.1126/science.aaw7894.
机械活性培养系统可以提供生理生物力学线索,促进类器官的结构和功能成熟。在人类肾脏类器官芯片的研究中,3D打印的毫米级腔室用于研究流体流动对肾脏类器官的血管化和成熟的影响。连续流动促进了内皮祖细胞的扩张和可灌注血管的形成,伴随着更成熟的管状结构的产生。此外,流体剪切应力还诱导了肾小球室的血管化和足细胞足突的成熟。类似地,胰腺和肠道类器官模型中也观察到了生理流动对成熟的积极影响。这些研究表明,类器官和器官芯片的结合能够实现更高水平的细胞成熟。
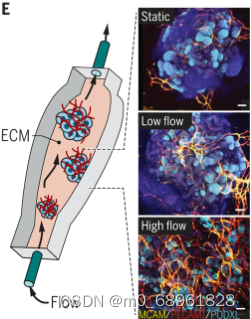
图片来源:Park SE, Georgescu A, Huh D. Organoids-on-a-chip. Science. 2019 Jun 7;364(6444):960-965. doi: 10.1126/science.aaw7894.






















 955
955

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










