1. 自发成瘤,成瘤率低,个体差异大,一般不用该方法。
2. 诱发性成瘤
化学诱导的 HCC 模型通常涉及作为引发剂的遗传毒性致癌物和作为肿瘤促进剂的非遗传毒性致癌物。遗传毒性致癌物作为肿瘤起始剂,通过直接 DNA 损伤诱导肝癌发生。它们可以直接与 DNA 相互作用并形成 DNA 加合物,从而破坏 DNA 结构并产生促癌突变。与遗传毒性致癌物不同,非遗传毒性致癌物不与 DNA 相互作用。它们通过破坏细胞结构、刺激恶性细胞转化和促进癌前细胞的克隆扩增来增强肿瘤形成。
最常用的遗传毒性致癌物是二乙基亚硝胺(DEN),其次是2-乙酰氨基芴(2-AAF)和黄曲霉毒素(AFB1)。常用的非遗传毒性致癌物包括四氯化碳 (CCl4)、硫代乙酰胺(TAA)和苯巴比妥(PB)。
二乙基亚硝胺 (DEN) 和四氯化碳 (CCl4) 诱导的 HCC 小鼠模型几乎概括了 HCC 纤维化和炎症的特点,最常用来建模。
(1)DEN 诱导
DEN 主要靶向肝脏,肝脏中它被肝细胞中的细胞色素 P450 酶代谢激活,形成烷化剂。活化的 DEN 充当烷化剂, 通过在 DNA 分子的两个鸟嘌呤碱基之间添加烷基来连接它们,导致 DNA 链断裂和诱变 DNA 加合物形成。其次,激活的 DEN 诱导活性氧 (ROS) 的产生,这对 DNA 稳定性构成威胁 [17,65]。随后的肝细胞坏死和再生促进突变、肿瘤转化,并最终促进肝癌发生。
DEN 的代谢激活发生在给药后 4 小时内。单独由 DEN 诱导的小鼠肿瘤通常携带 Hras 或 Braf 原癌基因的起始激活突变。
(2)CCL4 诱导
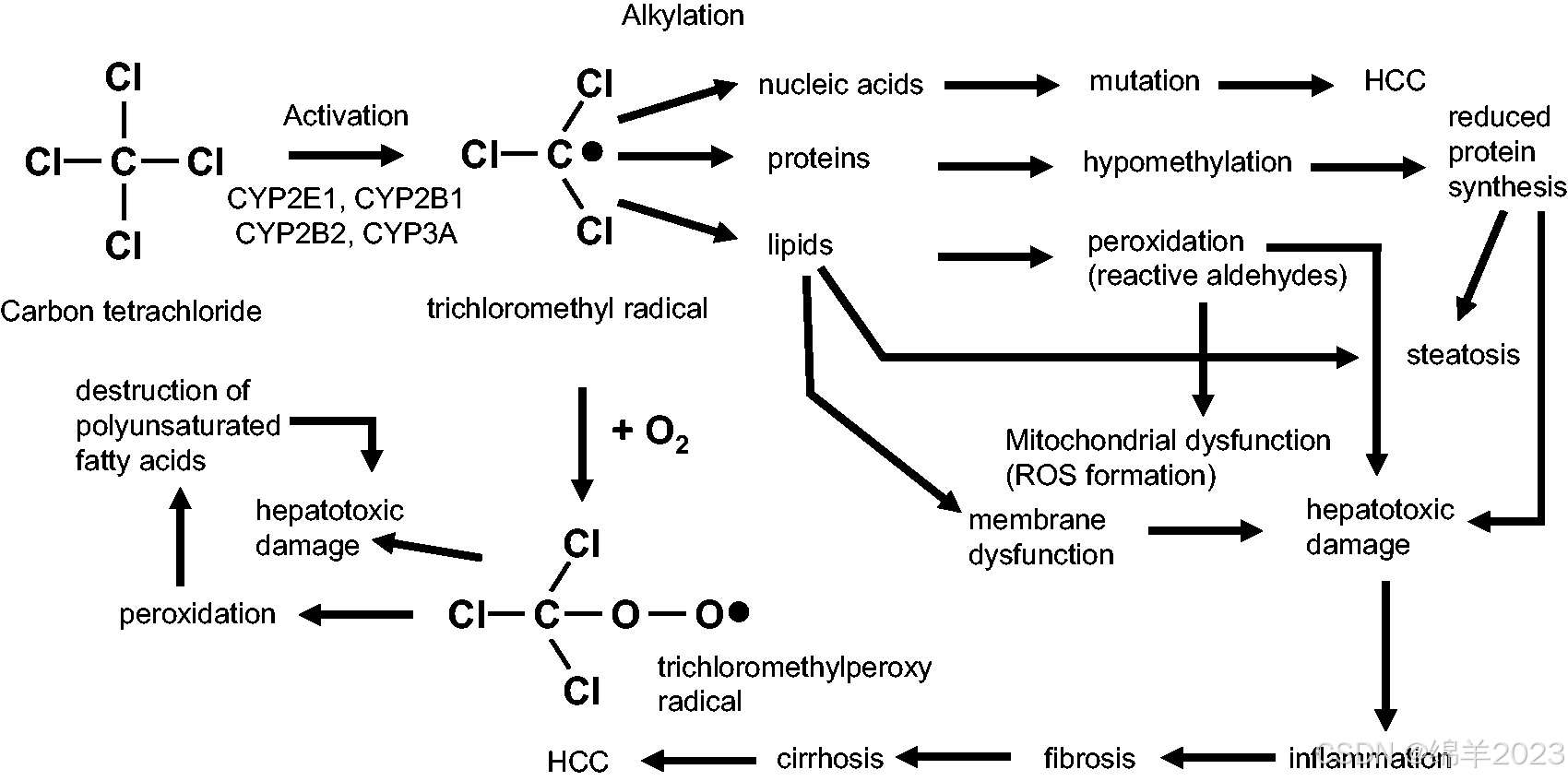
图 1.四氯化碳 (CCl4) 诱导的肝损伤。在肝脏中,CCl4被细胞色素 P450 (CYP) 酶代谢为三氯甲基自由基,该自由基可进一步氧合为三氯甲基过氧自由基。这两种自由基都是高反应性的,可诱导复杂的细胞改变,从而导致肝毒性损伤、炎症、纤维化、肝硬化和肝细胞癌。
CCl4在肝脏中被细胞色素P450超家族的单加氧酶(CYP家族)代谢为三氯甲基自由基(CCl3*)。随后,这种自由基与核酸、蛋白质和脂质发生反应,从而损害关键的细胞过程,导致脂质代谢改变(脂肪变性和脂肪变性)和蛋白质含量降低。CCl 3 *和DNA形成加合物,进一步触发突变和HCC的形成。
CCl 3 *氧化产生的三氯甲基过氧自由基(CCl 3 OO*)会增加 ROS 水平,导致肝细胞中膜磷脂的过氧化降解,并导致细胞膜完整性受损。ROS 还会导致肝细胞坏死和凋亡。因此,所有细胞室(线粒体、内质网和质膜)的膜通透性降低,出现以炎症、纤维化、肝硬化和肝癌为特征的全身性肝损伤。
CCl4 的毒性有三个或四个不同的阶段。前两到三周主要表现为坏死,表现为肝脏特异性酶活性升高和假胆碱酯酶值降低。在接下来的两到三周内,肝脏脂肪大量堆积,血清甘油三酯和天冬氨酸氨基转移酶 (AST) 水平显着升高,而肝功能降低。在第三阶段,AST 继续增加,发现羟脯氨酸和甘油三酯水平升高,整体肝功能进一步下降。在最后阶段,假性胆碱酯酶的值进一步降低,并观察到肝脏萎缩。这可能与血清白蛋白的显着降低和体重减轻相结合,这表明在长时间纤维化过程中肝功能进行性丧失。
(3)其他:如AFB1
3. 移植型:注射癌细胞,包括易位移植原位移植,异种移植和同种移植。
4. 转基因模型
肝细胞癌的临床前小鼠模型:概述和更新 - ScienceDirect

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








