
欢迎来到“生信学术纵览”!在当前科研领域,细胞衰老无疑是国自然热门方向,其在肿瘤及非肿瘤疾病中的探索热度持续高涨,吸引众多科研人员投身其中。
生信分析作为科研中的有力工具,巧妙地结合热点,不仅能为研究注入创新性活力,更能显著提升文章冲击高分期刊的潜力。今天,特别为大家带来一篇聚焦非肿瘤疾病衰老方向、发表于二区的 SCI 文章剖析,让我们一同抽丝剥茧,深入探究其中隐藏的科研奥秘。
DOI: 10.2147/JIR.S504040

正式介绍
基本信息
-
论文标题:衰老在溃疡性结肠炎发病机制中的作用:聚焦ETS1作为有前景的生物标志物
-
发表期刊:Journal of Inflammation Research,中科院医学大类分区2区,IF=4.1998
-
发表日期:2025年2月6日在线发表
研究背景
溃疡性结肠炎(UC)是一种慢性复发性炎症性肠病,严重影响患者生活质量,已成为全球公共卫生问题。随着人口老龄化,老年UC患者数量增加,其临床管理复杂,治疗风险高,且目前缺乏针对老年UC患者的有效药物。衰老过程中,肠道干细胞、肠道黏膜和肠道微环境发生结构和功能变化,导致肠道免疫系统失调,慢性炎症增加,进而增加UC发病风险。虽然衰老相关基因(ARGs)在胃肠道肿瘤诊断和治疗反应预测中有一定价值,但衰老导致UC的具体机制尚未明确,因此探究ARGs在UC发病机制和诊断预测中的作用意义重大。
研究思路
从GEO数据库获取四个基因表达数据集,从多个公共数据库收集ARGs和UC相关基因。通过差异表达分析筛选UC相关差异表达ARGs(DE-ARGs),利用GSVA分析JAK/STAT信号通路活性,用CIBERSORT评估免疫细胞浸润情况。基于DE-ARGs进行一致性聚类分析,筛选衰老相关分子亚型,并分析不同亚型免疫微环境和信号通路差异。运用WGCNA筛选关键模块基因,再通过LASSO和随机森林算法确定UC相关特征基因,构建诊断模型。最后在DSS诱导的UC小鼠模型中进行实验验证,探究关键基因在UC中的作用机制。
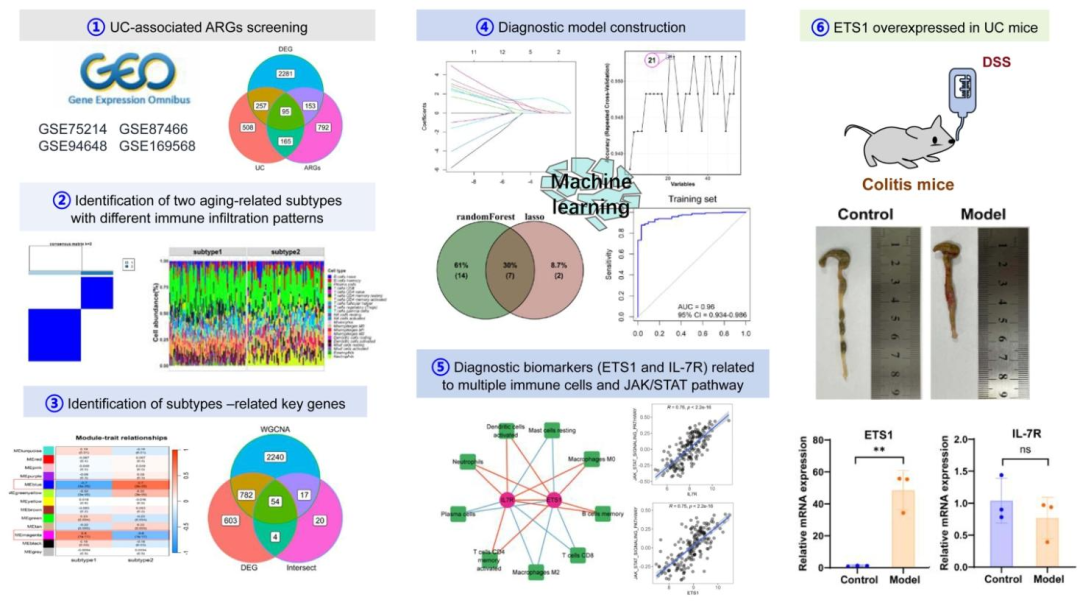
图文摘要
研究亮点
本研究首次构建了基于ARGs的UC预测模型,挖掘出ETS1和IL7R等关键特征基因,为UC早期诊断提供了新方向;深入剖析衰老、免疫失调与UC进程之间的潜在关联,发现了不同衰老相关分子亚型具有不同免疫浸润模式,为理解UC发病机制提供了新视角。综合运用多种生物信息学方法和动物实验,从多层面系统研究UC与衰老的关系,研究方法全面且深入。
数据来源和生物信息方法
1、数据来源
基因表达数据来自GEO数据库,包括GSE75214、GSE87466、GSE94648和GSE169568。ARGs来自CellAge、GenAge和Aging Atlas数据库。UC相关基因来自GeneCards、DisGeNET和CTD数据库。
2、生物信息方法
差异表达分析使用R包limma;GSVA分析利用R包GSVA;免疫浸润分析运用CIBERSORT工具;一致性聚类分析借助R包ConsensusClusterPlus;WGCNA使用R包WGCNA;LASSO分析通过R包glmnet;随机森林分析使用R包randomForest;诊断模型采用逻辑回归算法,评估模型效果用pROC包绘制ROC曲线。
主要结果
1、UC与正常样本差异基因筛选
去除批次效应后样本均匀分散(图1A)。从三个数据库中鉴定1025个共享UC相关基因(图1B),Limma分析筛选出2786个差异表达基因(DEGs),其中1624个上调,1162个下调(图1C),展示了前30个DEGs的热图(图1D)。通过Venn分析确定95个DE-ARGs(图1E),GSVA显示UC样本中JAK/STAT信号通路异常激活(图1F)。小结:筛选出UC相关差异表达基因和DE-ARGs,发现UC样本中JAK/STAT信号通路异常激活,为后续研究奠定基础。
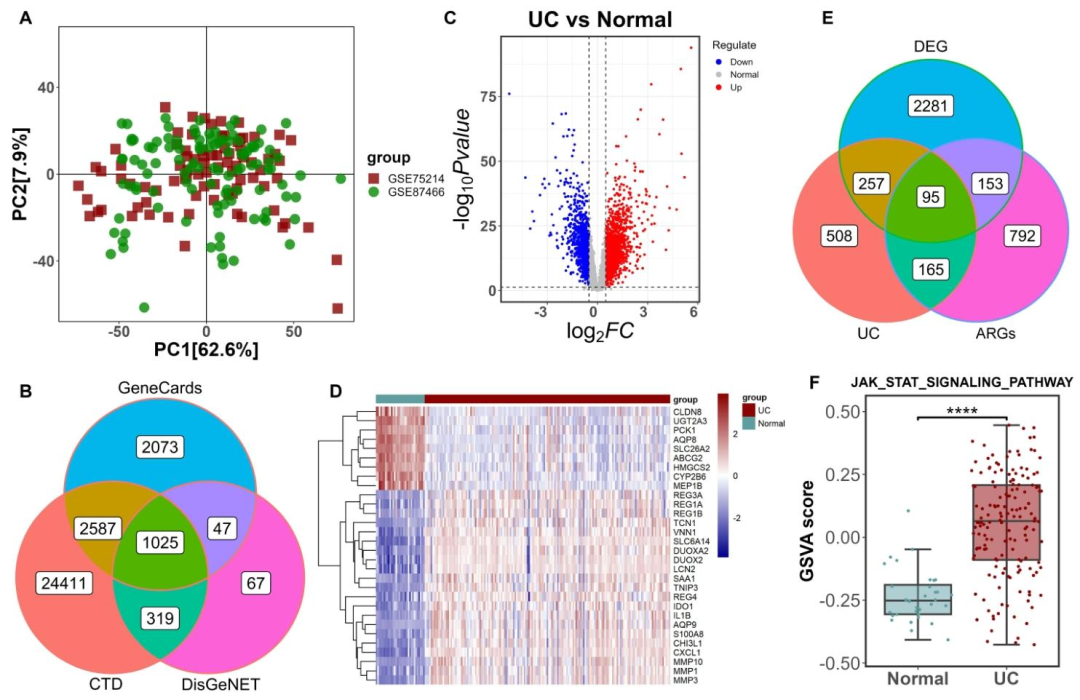
图1:UC与正常样本中差异表达衰老相关基因(DE-ARGs)的鉴定
2、UC与正常样本免疫细胞浸润分析
血浆细胞、M2巨噬细胞和静止肥大细胞在正常和UC样本中浸润比例较高(图2A)。UC和正常样本免疫细胞浸润谱差异明显,有14种免疫细胞类型存在差异。如UC样本中记忆B细胞、M1巨噬细胞和活化树突状细胞丰度增加,M2巨噬细胞和静止肥大细胞水平降低(图2B)。小结:明确了UC与正常样本免疫细胞浸润的差异,表明免疫失调在UC发病中起重要作用。
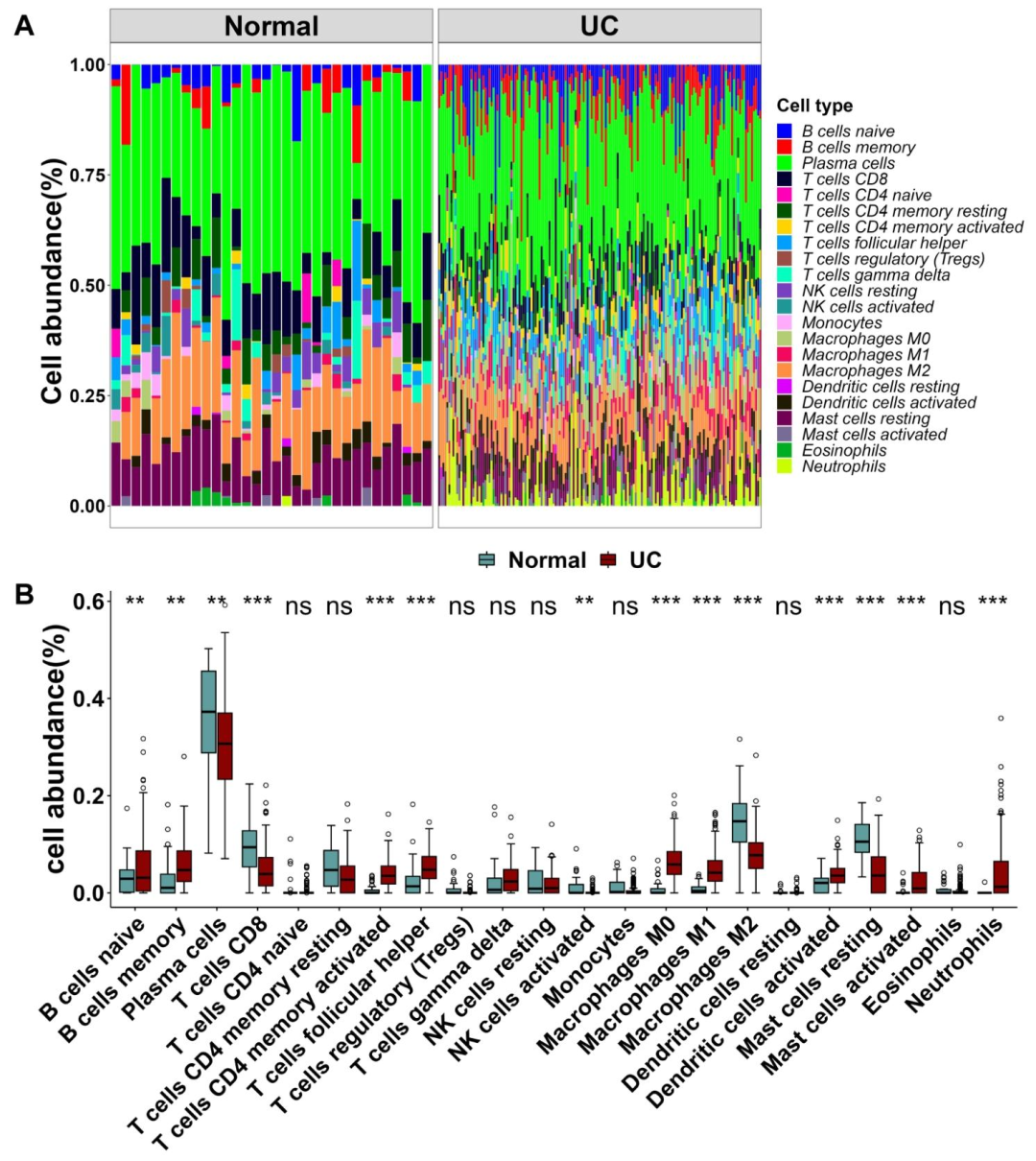
图2:UC与正常样本中免疫细胞浸润分析
3、UC中两种衰老相关亚型筛选
基于95个DE-ARGs的表达进行一致性聚类分析,CDF曲线显示k=2时聚类结果可靠(图3A),将样本分为两个衰老相关亚型(图3B),PCA进一步证实可区分(图3C)。两个亚型免疫细胞浸润模式不同,浆细胞和M2巨噬细胞在其中均占优势(图3D),11种免疫细胞在亚型1和2中丰度差异显著(图3E)。GSVA显示JAK/STAT信号通路在亚型2中显著富集(图3F),差异表达分析在两亚型间鉴定出1443个DEGs(图3G、H)。小结:筛选出UC中两种具有不同免疫浸润模式和JAK/STAT信号通路活性的衰老相关亚型。
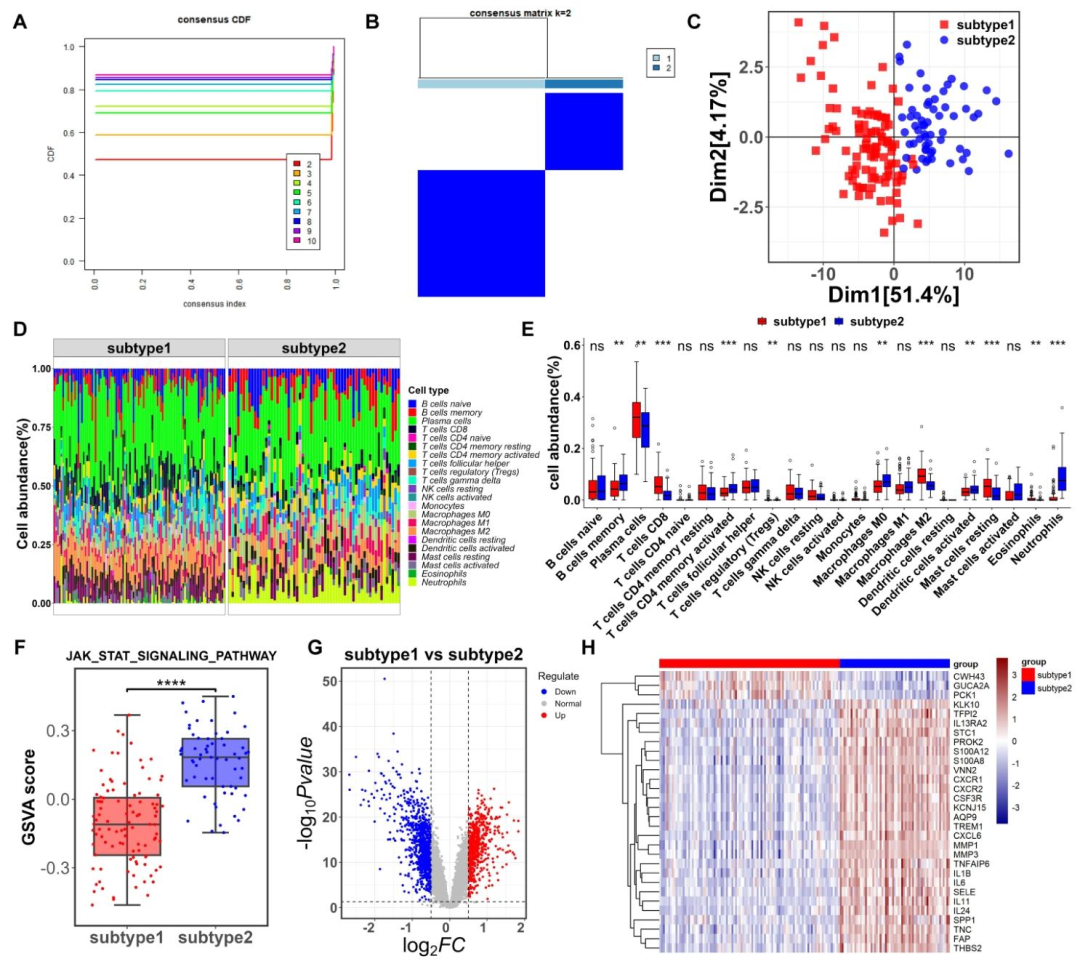
图3:通过一致性聚类分析筛选衰老相关亚型
4、通过WGCNA鉴定关键模块
确定软阈值为6时,生物网络达到无标度,构建模块(图4A)。检测到13个与亚型相关的聚类,蓝色和品红色模块与分子亚型关联最强(图4C)。Venn图显示WGCNA、亚型DEGs和DE-ARGs有54个重叠基因(图4D)。小结:筛选出与UC衰老相关亚型相关的关键模块和基因,为后续筛选特征基因提供候选。
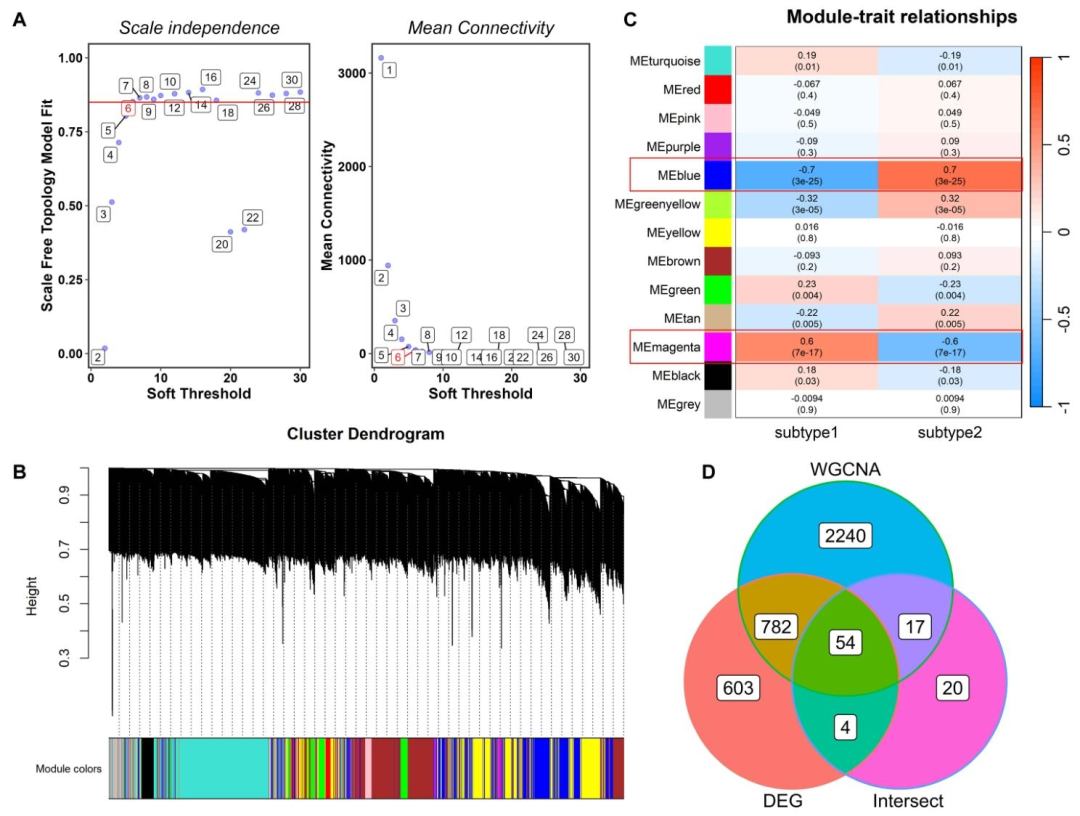
图4:加权基因共表达网络分析(WGCNA)
5、UC诊断生物标志物筛选
LASSO分析确定了9个关键的变量(图5A、B),随机森林模型筛选出了21个基因(图5C),基于MeanDecreaseGini对随机森林模型中的基因进行重要性排序(图5D)。整合两种算法鉴定出7个共享生物标志物(图5E),基于其中两个变量(ETS1和IL7R)构建的逻辑回归模型诊断准确性高,在训练集和两个验证集中,AUC值分别为0.96、0.817和0.882(图5F、G)。小结:筛选出UC诊断的关键生物标志物,构建的诊断模型对UC诊断具有较高准确性。
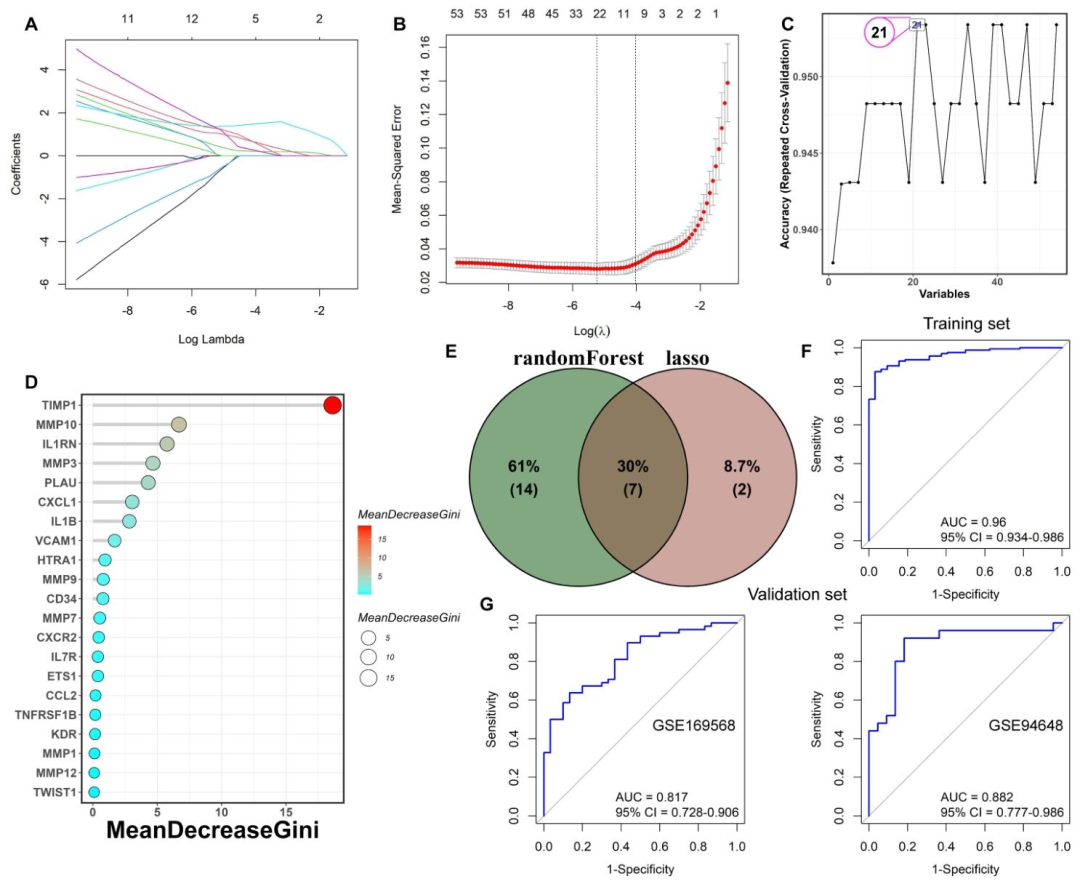
图5:通过机器学习算法筛选UC诊断生物标志物
6、两个诊断基因与生物学特征的相关性分析
ETS1和IL7R与活化树突状细胞、中性粒细胞等免疫细胞呈正相关,与静止肥大细胞、M2巨噬细胞等呈负相关(图6A)。这两个基因的高表达显著促进JAK/STAT信号通路活性(图6B、C)。小结:揭示了诊断基因与免疫细胞浸润和JAK/STAT信号通路的关联,为理解UC发病机制提供线索。
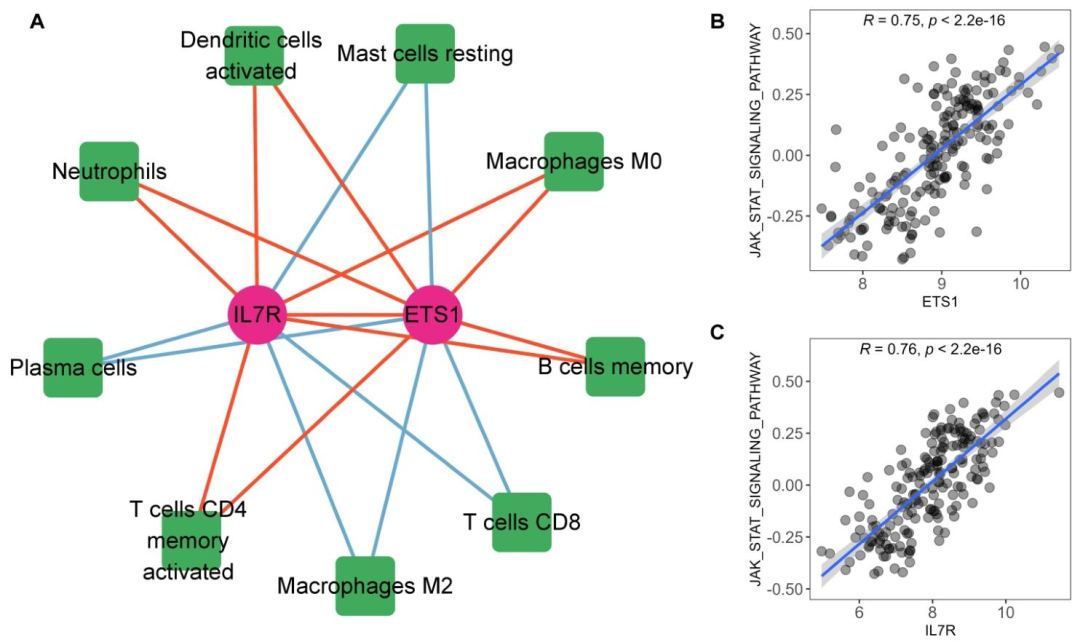
图6:两个诊断基因与生物学特征的Pearson相关性分析
7、实验性结肠炎中关键基因表达水平的验证
与对照组相比,模型组小鼠体重显著下降(图7A),DAI评分持续升高(图7B),出现抑郁、腹泻、便血等症状(图7C),结肠长度缩短,肠黏膜受损(图7D、E),CMDI评分显著升高,表明UC模型构建成功。qRT-PCR结果显示,模型组ETS1的mRNA水平显著升高,IL-7R表达虽有下降趋势,但与UC发生无显著关联(图7F)。小结:在小鼠模型中验证了生物信息学分析结果,表明ETS1在UC中可能发挥重要作用。
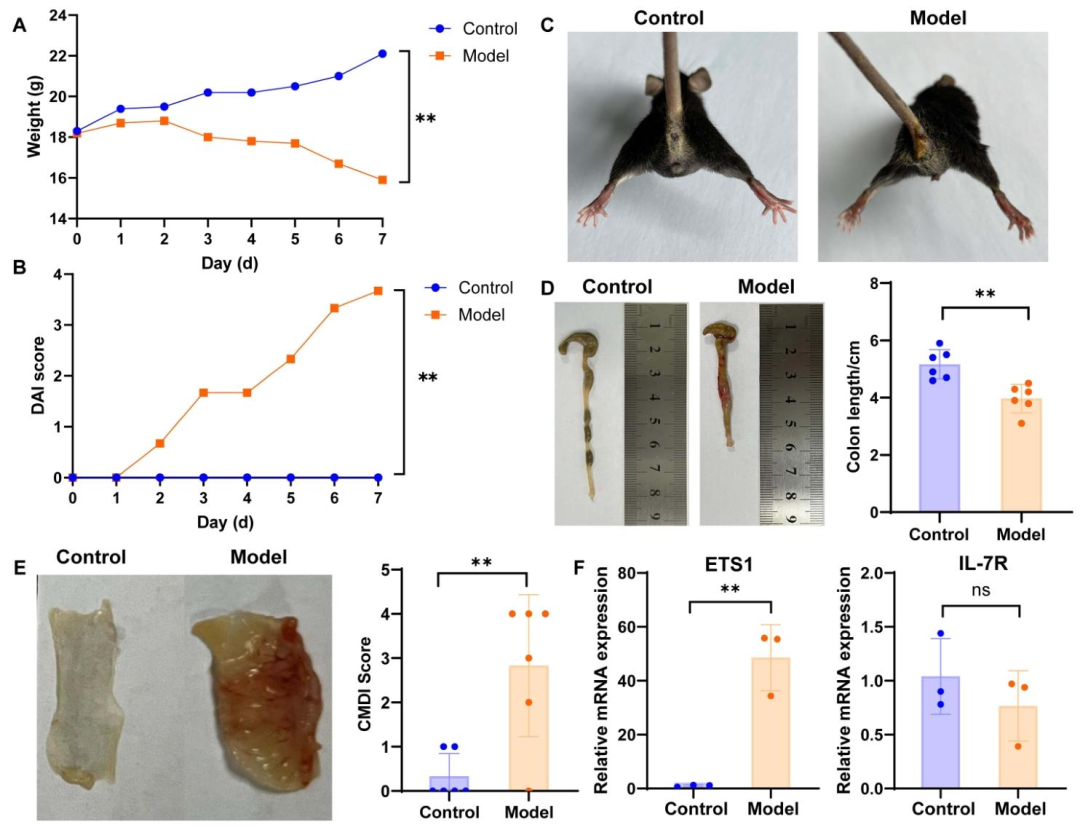
图7:UC小鼠模型中特征基因的表达
研究结论
本研究整合生物信息学分析、机器学习算法和体内实验验证,证实衰老在UC中起重要作用。鉴定出两种具有不同免疫浸润模式的年龄相关分子亚型,亚型间差异表达基因可能通过调节JAK/STAT信号通路影响UC免疫微环境。筛选出ETS1和IL7R两个关键ARGs构建诊断模型,可准确预测UC风险。这两个标志物与多种免疫细胞和JAK/STAT信号通路存在复杂互作,且ETS1在DSS诱导的UC小鼠中显著上调。研究结果为UC治疗中抗衰老靶向药物开发和应用提供重要信息。
研究的局限性和未来方向
局限性:GEO数据库样本缺乏临床信息,无法提供年龄对UC潜在影响的直接临床证据。仅在小鼠模型中进行简单表达验证,ETS1和IL7R影响免疫反应和炎症进而导致UC病理过程的详细机制尚不清楚。
未来方向:未来需进一步开展临床研究,收集更多临床样本和信息,深入探究关键基因的作用机制,以提高研究结果的可信度和临床应用价值。
建议
本研究巧妙整合多种生物信息学方法和动物实验,全面深入地探究了衰老与UC的关系,成功挖掘出潜在生物标志物并构建诊断模型,研究思路清晰、方法严谨,为该领域研究提供了重要参考。这种多组学数据整合和多方法联用的研究模式,充分发挥了生物信息学在挖掘疾病机制和生物标志物方面的优势,值得借鉴。
值得一提的是,在漫长科研征途上,科研人员一定要找准热点思路、运用恰当的研究方法是迈向成功的关键。掌握这些要点,发表SCI并非遥不可及。如果您渴望突破科研瓶颈、加速科研进程,那么请不要犹豫,立即与我们取得联系!我们专业的团队将依据您的课题方向以及临床实际情况,为您提供一对一的精准指导,助力您在科研道路上领先一步,斩获更多科研硕果!
感谢您的阅读,欢迎关注“生信学术纵览”。谢谢您的分享、点赞+在看!
【生信学术纵览】致力于为科研人员和学者精心搜罗并呈现各类生物信息学的学术成果与研究方法!诚邀您关注、投稿、分享、转载。若有投稿或转载需求,关注公众号“生信学术纵览”后私信说明,携手推动科学知识传播交流。觉得内容不错,点赞、在看安排,助力基因和生物信息知识广泛传播!

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








