经颅直流电刺激期间记录神经元峰电活动
1 背景
经颅直流电刺激(tDCS)是一种非侵入性神经调控技术,通过电极将微弱电流经头皮传递以调节皮层兴奋性[1,2]。该技术已被广泛应用于多种行为和临床研究中。例如,在运动任务期间使用tDCS可提高内隐运动学习的速度[3]。此外,tDCS被证明能够提升工作记忆表现并增强选择性注意[4]。在临床方面,tDCS已被证实可改善慢性中风患者和帕金森病患者的运动功能[5][6,7],,缓解抑郁和双相情感障碍[8],,并通过减少药物渴求来治疗成瘾[9,10]。
经颅直流电刺激(tDCS)被认为可在刺激期间调节皮层兴奋性,并产生超过原始刺激持续时间的刺激后效应。通过从初级运动皮层记录运动诱发电位进行测量,阳极经颅直流电刺激被证明可增强皮层兴奋性,而阴极刺激则抑制皮层兴奋性[1]。随着刺激时间的延长,经颅直流电刺激的持续效应更为明显,在刺激时间超过13分钟时,效应可能持续一小时以上[11]。使用钠通道阻滞剂或钙通道阻滞剂的药理学干预可消除tDCS的短期效应,而使用NMDA受体拮抗剂的干预仅消除其长期效应。该发现表明,tDCS的短期效应主要与膜极化效应相关,而长期变化则具有突触性质[12]。
然而,经颅直流电刺激产生效应的精确神经生理机制目前仍不十分清楚。文献中的一个重要空白在于对经颅直流电刺激期间神经元峰电活动的基本理解。造成这一空白的主要原因是方法学上的限制:经颅直流电刺激需要在目标区域的头皮上放置电极,而单细胞记录则需要直接接触同一位置的大脑组织。一种解决方案是使用直径为1 mm的小型直流刺激电极,将其直接放置在皮层表面,并靠近用于记录峰电活动的微电极[13]。在这种猫实验模型中,克雷茨菲尔特等人发现,对皮层表面施加至少200 μA的阳极刺激可使深度达3 mm的神经元放电频率增加,而阴极刺激则降低放电频率。然而,
刺激电极的小尺寸产生的电流密度比现代经颅直流电刺激头皮电极组合高出几个数量级。
在此,我们开发了一种新方法,用于在直流电刺激期间和之后对直接位于经颅直流电刺激海绵电极下方的皮层神经元进行体内微电极记录(MERs)。该装置包括两个制作的颅腔室和两个腔塞,每个腔塞容纳一个用于刺激的海绵电极以及一个用于将微电极插入皮层的线性槽。
2 方法
我们选择使用恒河猴(清醒且处于静息状态)进行设备测试,因为它们在灵长类动物研究中被广泛使用。猕猴模型在大小、几何结构和功能方面与人脑具有高度的形态学相似性,并且还提供了在复杂行为和/或认知任务期间评估经颅直流电刺激细胞效应的可能性。为了模拟经颅直流电刺激中最常见的电极放置位置,在运动皮层和背外侧前额叶皮层上方进行了标准的微电极记录开颅术,并使用丙烯酸水泥将颅腔固定在颅骨上以保护开颅部位。
通常这些颅腔为金属材质,但我们选择使用聚醚醚酮(PEEK)制造,这种材料具有所需的结构强度且具备电绝缘性。这一选择排除了电流通过颅腔侧面形成未知分流的可能性,确保施加的电流必须穿过大脑才能到达回路电极。
为了模拟经颅直流电刺激期间使用的电极类型,我们设计了一个“插头”,可插入PEEK腔室中,并可用经颅直流电刺激通常使用的相同材料的海绵填充,同时允许微电极插入皮层(图1)。
该插头沿直径方向设有两个通道,用于微电极穿过插头。这两个通道各占据直径的四分之一,一个从插头侧面通向中心,另一个从
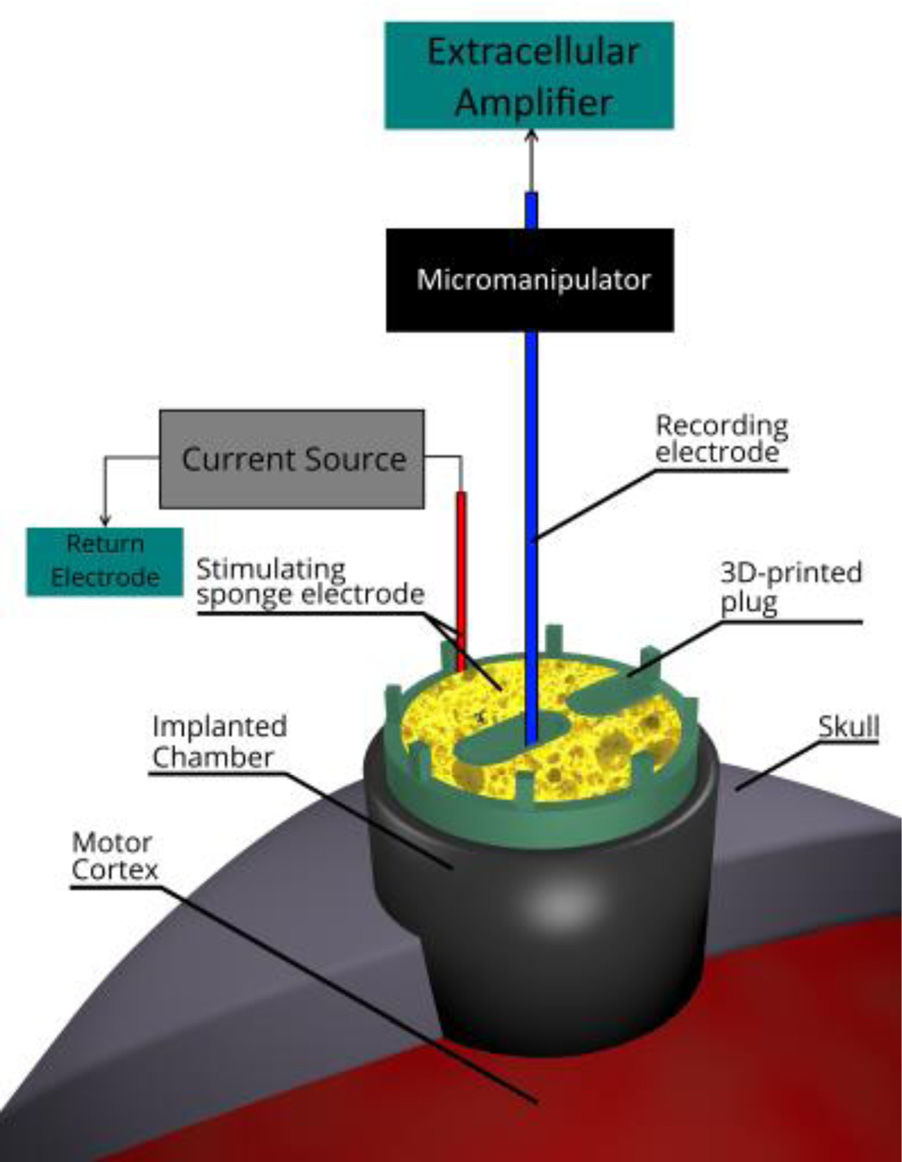
中心朝向另一端。这种设计最大化了可填充海绵电极的塞子面积,并确保海绵电极内部的电连续性。通过在颅腔内旋转塞子,可将微电极输送至腔内的任意位置。该塞子由丙烯腈‐丁二烯‐苯乙烯材料通过3D打印设备(Makerbot Industries,纽约布鲁克林)制造而成。
在插头中加入通道的第二个优点是,可以将生理盐水滴到底部腔室中,以确保海绵与覆盖脑膜的肉芽组织之间保持良好的电连接。刺激器与皮层表面之间建立稳定连接至关重要,以确保驱动所需电流所需的电压不会过高或因电路电阻的变化而出现强烈波动。因此,将银‐氯化银导线嵌入浸有生理盐水的海绵中,从而在刺激装置与浸有生理盐水的海绵之间提供稳定的接口。
使用钨微电极(FHC,鲍德温,缅因州)记录细胞外活动,并通过SNR系统(Alpha Omega,耶路撒冷,以色列)进行记录。单个神经元通过离线分类器(Plexon公司,达拉斯,德克萨斯州)中的主成分分析从记录到的动作电位中分离出来。
3 结果
以下是 在非人灵长类动物中经颅直流电刺激期间初级运动皮层细胞外记录的示例 (图2)。
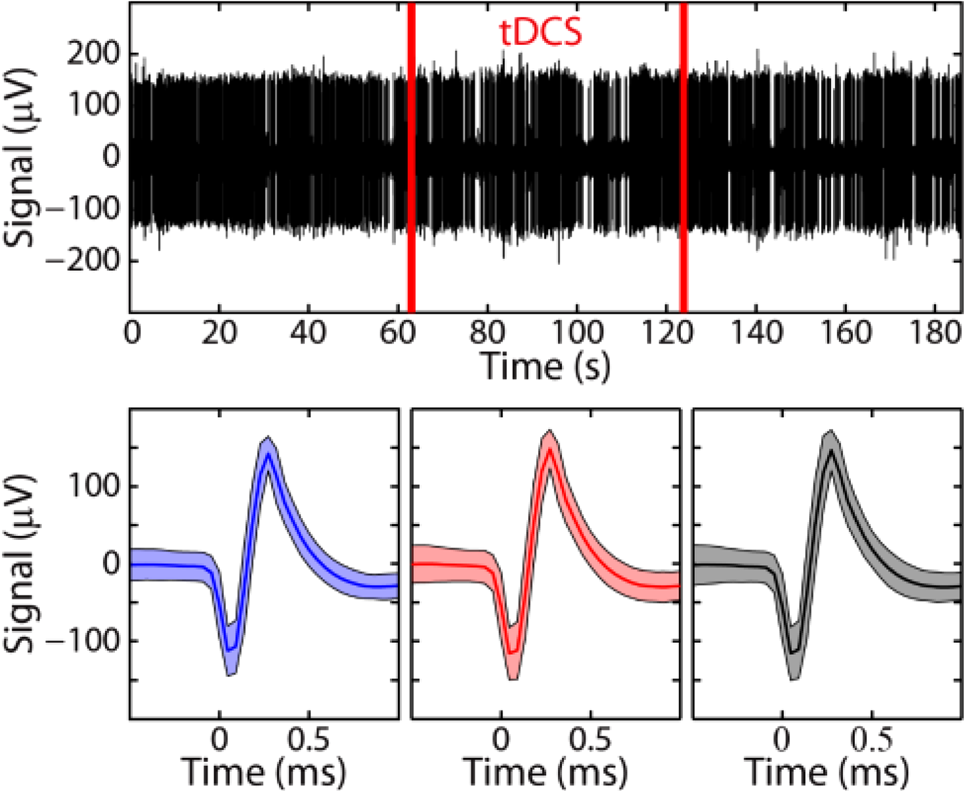
4 解读
使用此方法时还需要其他实验预防措施。为了实现微电极记录,应将参考电极与经颅直流电刺激的回路电极分开,以尽量减少干扰。如果使用导向套管穿透脑膜,则应在施加经颅直流电刺激之前将其撤回,以确保电流会从海绵均匀地扩散到生理盐水,再进入大脑,而不会通过低电阻路径进入皮层。同时,重要的是要确保除回路电极外不存在其他返回路径(即避免向受试者接地),以确保电流会在经颅直流电刺激电极之间的皮层区域流动。
当前设计存在若干不足之处:最明显的是刺激电极与大脑之间缺少了头皮和颅骨;此外,“海绵塞”的表面积也小于标准经颅直流电刺激电极的表面积。为了消除这些差异,可以采用数学模型(如达塔等人提出的模型[14])来估算经皮肤和颅骨分流的电流,计算标准经颅直流电刺激期间皮层表面的电流密度,并调整施加的电流以达到预期数值。尽管该方法与在人体中进行的经颅直流电刺激并不完全等同,但它确实提供了一个重要机会,能够在复杂的行為和认知范式背景下,评估直流电刺激对单个神经元自发活动的影响,从而剖析并优化经颅直流电刺激的生理机制,用于基础与临床应用。
 tDCS下神经元活动记录新法
tDCS下神经元活动记录新法























 15
15

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








