一:缓冲溶液
1:同离子效应:
在一个弱电解质(弱酸或者弱碱)的平衡体系里面加入与弱电解质具有相同离子的强电解质,可以降低弱电解质的电离程度。
也即:
在弱酸溶液中加入该酸的共轭碱,或在弱碱的溶液中加入该碱的共轭酸时,可使这些弱酸或弱碱的解离度降低。
因为加入了具有相同离子的强电解质,造成了平衡左移,导致了弱电解质溶解度下降。
比如:
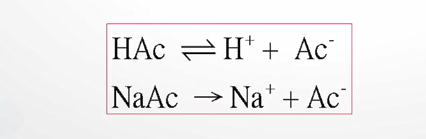
醋酸是弱电解质,醋酸钠是强电解质两者含有共同的元素醋酸根。当二者共同存在于溶液中时,醋酸的溶解度降低,此时就会使溶液的pH值基本保持不变。
2:
缓冲溶液:
能抵抗外加适量的强酸,强碱或稍加水稀释而溶液的pH值基本保持不变的溶液,称为缓冲溶液
组成:弱酸,强碱弱酸盐(弱碱,强酸弱碱盐)共轭酸碱对的混合溶液。
3:缓冲溶液的作用原理:
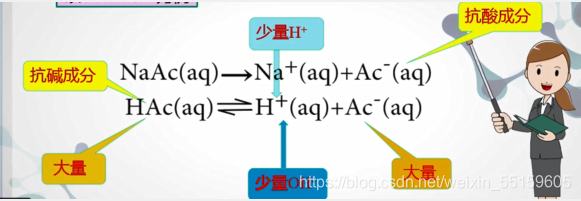
当溶液中存在这对缓冲物质时,
如果向溶液中增加酸,分解的氢离子会和醋酸根反应生成醋酸以维持溶液的pH值。
如果向溶液中增加碱,分解的氢氧根离子会和氢离子反应生成水,此时根据








 本文详细阐述了缓冲溶液的原理、作用及计算方法,包括同离子效应如何影响弱电解质溶解度,并举例人体内的缓冲系统。同时,介绍了溶度积常数、溶解度与溶度积的关系,以及溶度积规则在判断沉淀溶解平衡中的应用。讨论了同离子效应和盐效应对溶解度的影响,并给出了不同条件下溶解度的计算和预测方法。
本文详细阐述了缓冲溶液的原理、作用及计算方法,包括同离子效应如何影响弱电解质溶解度,并举例人体内的缓冲系统。同时,介绍了溶度积常数、溶解度与溶度积的关系,以及溶度积规则在判断沉淀溶解平衡中的应用。讨论了同离子效应和盐效应对溶解度的影响,并给出了不同条件下溶解度的计算和预测方法。
 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章

















 1万+
1万+

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








