背景补充
- 早期激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)乳腺癌的研究流程
- 乳腺癌病理分析及建模预测复发评分的过程
- 利用自监督学习算法Barlow Twins从癌症基因组图谱(TCGA)结肠腺癌数据集中提取特征的流程
- 基于 TCGA 训练集、AVANT 临床试验集的结肠腺癌图像分析流程
- 基于组织病理学图像的癌症相关模型流程
一、Orpheus:基于 H&E 图像预测乳腺癌复发评分的新利器

| 作者类型 | 姓名 | 单位 |
|---|---|---|
| 第一作者 | Kevin M. Boehm Omar S. M. El Nahhas Antonio Marra | 1. 计算肿瘤学服务部,纪念斯隆凯特琳癌症中心,美国纽约州纽约市东61街323号 2. 放射肿瘤学系,纪念斯隆凯特琳癌症中心,美国纽约州纽约市约克大道1275号 3. 德国德累斯顿工业大学卡尔·古斯塔夫·卡鲁斯医学院,Else Kroener Fresenius数字健康中心,德国德累斯顿费切尔大街74号,邮编01307 |
| 通讯作者 | Sarat Chandarlapaty Sohrab P. Shah Jakob Nikolas Kather | 1. 计算肿瘤学服务部,纪念斯隆凯特琳癌症中心,美国纽约州纽约市东61街323号 2. 人类肿瘤学和发病机制项目,纪念斯隆凯特琳癌症中心,美国纽约州纽约市约克大道1275号 3. Marie-Josée和Henry R. Kravis分子肿瘤学中心,纪念斯隆凯特琳癌症中心,美国纽约州纽约市约克大道1275号 4. 德国德累斯顿工业大学卡尔·古斯塔夫·卡鲁斯医学院,Else Kroener Fresenius数字健康中心,德国德累斯顿费切尔大街74号,邮编01307 5. 德国海德堡大学医院国家肿瘤疾病中心(NCT),医学肿瘤学,德国海德堡新海德堡菲尔德460号,邮编69120 |
文献概述
“Multimodal histopathologic models stratify hormone receptor - positive early breast cancer”发表于Nature Communications,通过开发多模态深度学习工具Orpheus,利用苏木精和伊红(H&E)全切片图像推断Oncotype DX复发评分(RS),为激素受体阳性早期乳腺癌的风险分层和治疗决策提供了新方法。
-
研究背景:激素受体阳性、HER2阴性(HR + /HER2-)的早期乳腺癌是最常见亚型,Oncotype DX®复发评分(RS)在预测和预后评估方面价值显著,但成本高、检测周期长限制其应用。已有基于临床病理特征的预测模型效果不佳,因此研究旨在用深度学习算法分析H&E全切片图像预测RS。
-
研究方法
-
- 数据组装:收集三个机构6172例HR + /HER2-早期乳腺癌患者数据,包括H&E染色、免疫组化分析、RS计算及部分基因组数据,分为训练验证集和外部验证集。
- 模型训练:构建基于transformer的模型,通过自监督学习和适应transformer架构训练,预测RS。分别训练视觉、语言和多模态模型,多模态模型融合图像和文本信息。
- 模型评估:用Pearson相关系数、一致性相关系数等评估模型预测RS的能力,对比Orpheus与临床病理列线图及RS识别远处转移复发的能力。
-
研究结果
-
- 模型性能良好:视觉模型在不同队列稳健推断RS并识别高风险疾病;语言模型有一定预测能力;多模态模型性能最优,识别高风险疾病(RS > 25)的AUC达0.89,优于列线图(0.73)。
- 预测复发优势明显:对于RS ≤25的患者,Orpheus + 模型预测远处转移复发的能力强于RS,MSK - BRCA队列中,Orpheus + 的平均时间依赖性AUC为0.75,RS仅为0.49。
- 可解释性与生物学一致:通过注意力机制可视化,发现模型关注肿瘤相关区域和关键病理信息。高风险疾病肿瘤微环境有显著特征,与基因特征相关。
- 临床应用有潜力:Orpheus识别低风险患者敏感性高,识别高风险患者有一定特异性,可减少基因检测,指导辅助化疗决策。
-
研究结论:Orpheus可从常规H&E全切片图像近似RS,多模态方法优势明显,为乳腺癌精准医疗提供支持,有助于扩大精准医学覆盖范围、优化治疗和随访策略。
早期激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)乳腺癌的研究流程
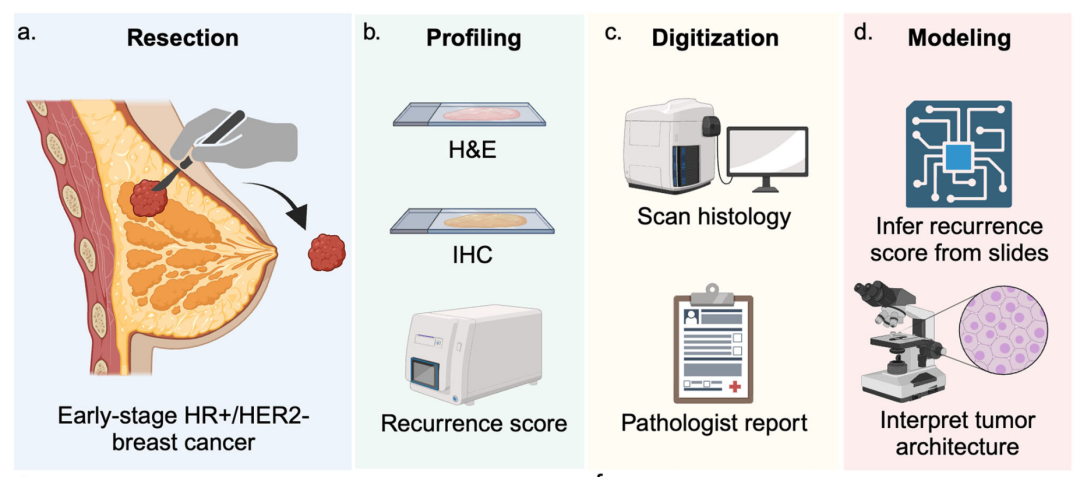 image-20250312082348464
image-20250312082348464
共分为4个步骤:
- a. 切除(Resection):切除早期HR+/HER2-乳腺癌组织样本。
- b. 分析(Profiling):对样本进行苏木精 - 伊红(H&E)染色和免疫组织化学(IHC)分析,计算复发评分。
- c. 数字化(Digitization):对组织学切片进行扫描,并生成病理报告。
- d. 建模(Modeling):通过切片推断复发评分,并解读肿瘤结构。
乳腺癌病理分析及建模预测复发评分的过程
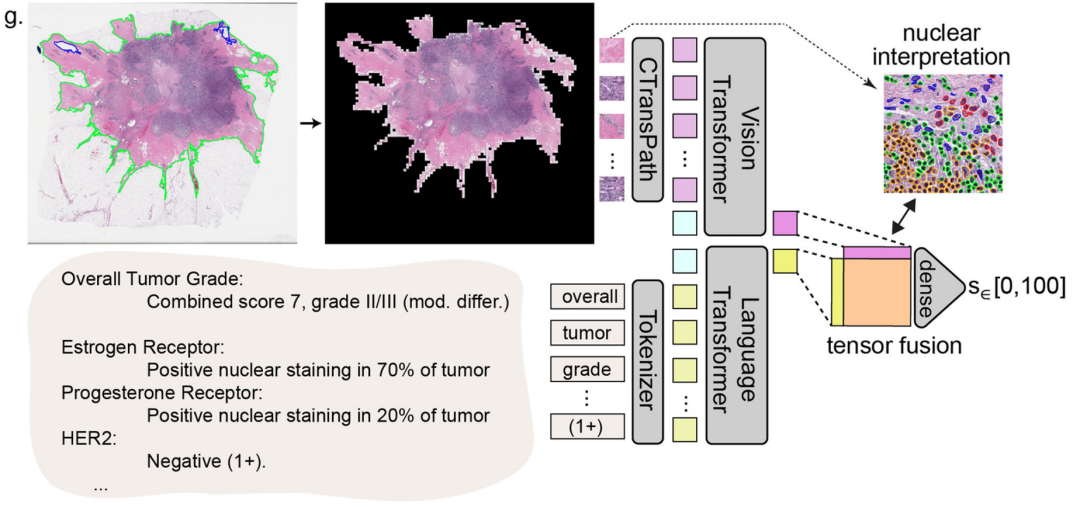 image-20250312082519834
image-20250312082519834
- 病理信息:肿瘤综合评分7,等级II/III(中度分化);雌激素受体在70%的肿瘤细胞核中呈阳性染色;孕激素受体在20%的肿瘤细胞核中呈阳性染色;HER2为阴性(1+)。
- 分析流程:左侧是苏木精 - 伊红(H&E)染色的组织切片图像,经处理后提取图像特征(CTransPath)进入视觉Transformer模型进行细胞核解读;同时,病理文本信息经标记器(Tokenizer)处理后进入语言Transformer模型,最后将视觉和语言模型的输出通过张量融合(tensor fusion)得到一个在0到100之间的分数(s),用于预测复发评分。
二、自监督学习挖掘结肠癌治疗相关的组织形态学模式
 https://doi.org/10.1038/s41467-025-57541-y
https://doi.org/10.1038/s41467-025-57541-y
一作&通讯
| 作者身份 | 姓名 | 单位 |
|---|---|---|
| 第一作者 | Bojing Liu、Meaghan Polack | Bojing Liu:1. 卡罗林斯卡学院医学流行病学与生物统计学系;2. 纽约大学格罗斯曼医学院应用生物信息学实验室 Meaghan Polack:1. 莱顿大学医学中心外科;3. 纽约大学格罗斯曼医学院病理学系 |
| 通讯作者 | Aristotelis Tsirigos | 2. 纽约大学格罗斯曼医学院应用生物信息学实验室;6. 纽约大学格罗斯曼医学院病理学系 |
文献概述
文章《Self-supervised learning reveals clinically relevant histomorphological patterns for therapeutic strategies in colon cancer》发表于Nature Communications,*利用自监督学习(SSL)从结直肠癌苏木精 - 伊红染色全切片图像(WSIs)中提取和分析组织形态学特征,构建了与临床治疗及预后相关的组织形态表型簇(HPCs),为结直肠癌个性化治疗提供依据*。
-
研究背景:传统结直肠癌诊断依赖病理学家镜检,且预后预测复杂。深度学习(DL)虽有帮助,但存在可解释性难题。SSL可自动从无标注数据提取图像特征,本研究旨在用SSL从WSIs提取临床相关组织学模式并探究其与患者结局及分子表型的关联。
-
研究方法
-
- 数据处理与特征提取:用TCGA结肠腺癌(TCGA - COAD)数据集训练SSL Barlow Twins算法,将WSIs处理为小图像补丁(图块),提取128维特征向量。
- 构建HPCs:运用Leiden社区检测算法对特征向量聚类,构建HPCs,并在AVANT试验数据集验证。
- 评估与分析:对HPCs进行组织病理学评估和特征描述,从定性和定量评估其一致性和稳健性。用Cox回归构建HPCs与总生存期(OS)的预测模型,结合SHAP值分析重要HPCs。通过计算Spearman相关性和基因集富集分析(GSEA),探究HPCs与免疫特征、致癌通路的联系。
-
研究结果
-
- HPCs构建与验证:成功构建47个HPCs,可分为8个超级簇,在TCGA和AVANT队列中表现出良好的一致性和稳健性。
- HPCs与OS的关系:HPCs分类器在预测OS方面表现出色,是独立预后因素,不同治疗组中与OS相关的HPCs具有不同组织学特征。
- HPCs与免疫及致癌通路的关联:与OS相关的HPCs与肿瘤微环境免疫特征相关,AVANT - 实验组中,HPCs与致癌通路联系紧密,部分HPCs与贝伐单抗治疗反应相关。
-
研究结论:研究识别并验证了结直肠癌中与预后相关的组织病理学特征,强调肿瘤微环境重要性,提出影响患者治疗敏感性的机制。HPCs有临床应用前景,但研究存在局限性,未来需提高预测准确性并验证相关机制。
利用自监督学习算法Barlow Twins从癌症基因组图谱(TCGA)结肠腺癌数据集中提取特征的流程
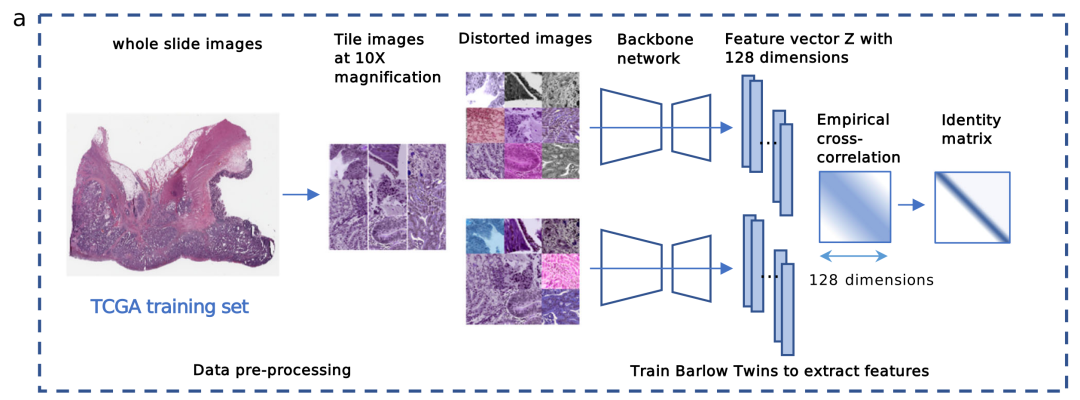 image-20250312083102215
image-20250312083102215
- 数据预处理:以TCGA训练集的全切片图像(whole slide images)为起始数据,将其处理成10倍放大的图块图像(Tile images at 10X magnification),然后生成畸变图像(Distorted images )。
- 特征提取:将畸变图像输入主干网络(Backbone network),得到128维的特征向量(Feature vector Z with 128 dimensions),计算经验互相关(Empirical cross-correlation),并与单位矩阵(Identity matrix)对比,训练Barlow Twins算法来提取图像特征。
基于 TCGA 训练集、AVANT 临床试验集的结肠腺癌图像分析流程
这张图展示了基于TCGA训练集和独立的AVANT临床试验数据集,利用训练好的主干网络对结肠腺癌组织图像进行处理和分析的流程:
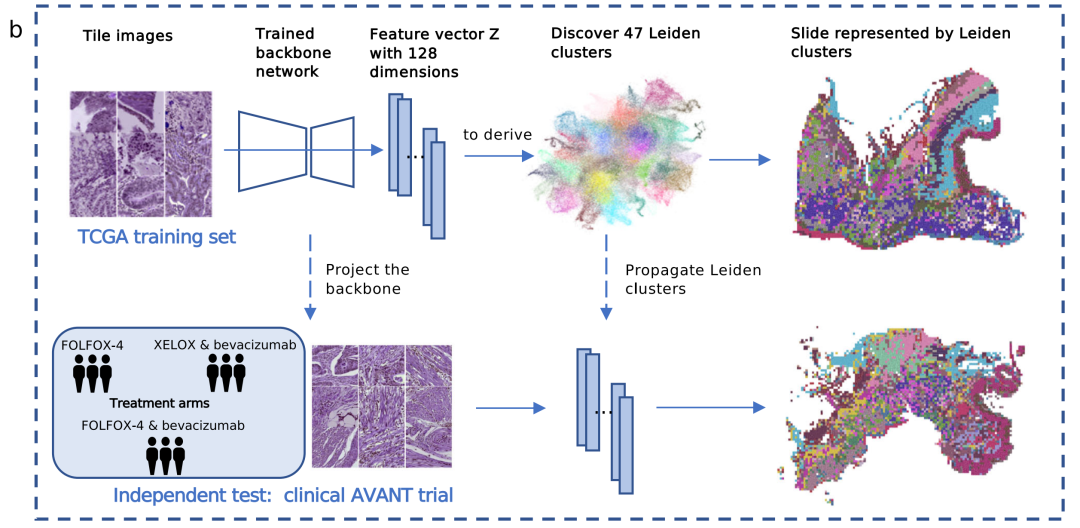 image-20250312083154216
image-20250312083154216
- TCGA训练集处理:将图块图像(Tile images)输入训练好的主干网络(Trained backbone network),生成128维的特征向量(Feature vector Z with 128 dimensions),通过这些特征向量发现47个莱顿簇(Leiden clusters),并将全切片用莱顿簇表示。
- 独立测试(AVANT临床试验):该试验有FOLFOX - 4、XELOX & 贝伐单抗(bevacizumab)、FOLFOX - 4 & 贝伐单抗等治疗组(Treatment arms)。对试验中的图像同样经过主干网络投影(Project the backbone),再利用莱顿簇分析,得到相应的图像表示结果,以此验证相关分析结果的有效性 。
三、BEPH 模型:从组织病理图像实现癌症诊断与生存预测的新基础模型
 https://doi.org/10.1038/s41467-025-57587-y
https://doi.org/10.1038/s41467-025-57587-y
一作&通讯
| 姓名 | 身份 | 单位(中文) |
|---|---|---|
| Zhaochang Yang | 第一作者 | 上海交通大学生命科学与生物技术学院生物信息学与生物统计学系 |
| Yue Zhang、Zhangsheng Yu | 通讯作者 | 1. 上海交通大学生命科学与生物技术学院生物信息学与生物统计学系 2. 上海交通大学 - 耶鲁大学生物统计学与数据科学联合中心 3. 上海交通大学医学院转化科学研究所生物医学数据科学中心(Yue Zhang、Zhangsheng Yu) 4. 上海交通大学数学科学学院(Zhangsheng Yu) 5. 上海交通大学医学院临床研究院(Zhangsheng Yu) |
文献概述
研究提出基于自监督学习的基础模型BEPH,利用1100万张未标记的组织病理学图像进行预训练,在多种癌症检测任务中表现出色,为癌症诊断和生存预测提供了有效工具,推动了计算病理学在临床和研究中的应用。
-
研究背景:计算病理学利用全切片图像进行病理诊断,但现有方法受标注数据稀缺和组织学差异限制。基础模型通过对大量无监督数字病理图像预训练,学习图像潜在结构和关系,有监督学习和自监督学习是主要训练策略。
-
BEPH模型构建:从TCGA收集32种癌症的11760张病理图像,构建1177万个224×224像素的预训练补丁数据集。*基于BEiTv2,利用自监督学习技术在自然图像和病理图像上预训练,学习病理图像的通用表示,再针对不同任务微调* 。
-
实验结果
-
- 补丁级分类:在BreakHis数据集上,BEPH的患者级和图像级平均准确率比最新CNN和弱监督模型高5 - 10%;在LC25000数据集上,对肺癌亚型分类准确率达99.99%±0.03,优于其他模型,表明其泛化能力强。
- WSI级分类:在肾细胞癌、非小细胞肺癌和乳腺癌亚型分类任务中,BEPH的10折宏观平均测试AUC表现优异,虽在部分结果上略逊于UNI和GigaPath,但整体稳定性和泛化能力强,且零样本能力出色。
- 标签效率:训练数据减少时,BEPH性能仍优于多数模型,使用约50%训练数据时,性能与其他用大量数据训练的模型相当,能有效应对数据稀缺问题。
- 生存预测:在六种癌症类型的生存预测中,BEPH的C指数最高,在区分高风险和低风险患者方面表现出色,且无需病理图像注释或额外基因组信息。
- 模型可解释性:通过UMAP降维分析和注意力热图可视化,发现BEPH能有效提取特征,注意力热图与病理学家注释高度一致,消融实验证明病理图像预训练和MIM的重要性。
-
研究展望:未来计划构建更大规模、更多样化的预训练数据集,探索多模态基础模型整合多领域数据的价值,以推动病理学人工智能发展。
基于组织病理学图像的癌症相关模型流程
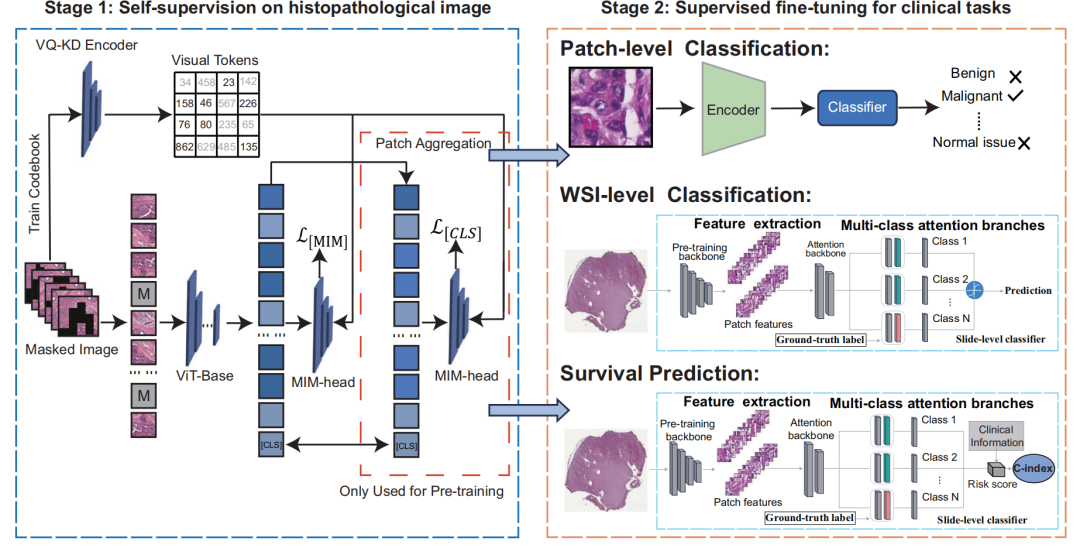 image-20250312083501382
image-20250312083501382
第一阶段(Stage 1: Self-supervision on histopathological image)
对组织病理学图像进行自监督学习。
使用VQ-KD编码器将图像转换为视觉标记,通过掩码图像(Masked Image)输入到ViT-Base模型中,利用MIM-head(Masked Image Modeling head)计算损失函数 L [ M I M ] L_{[MIM]} L[MIM]和 L [ C L S ] L_{[CLS]} L[CLS],进行预训练。
此阶段的一些组件如Patch Aggregation等用于处理图像块。
第二阶段(Stage 2: Supervised fine-tuning for clinical tasks)
针对临床任务进行有监督的微调,包含三个任务:
- Patch-level Classification(图像块级别分类):将图像块输入编码器,再经过分类器,判断图像块对应的组织是良性、恶性还是正常组织。
- WSI-level Classification(全切片图像级别分类):先进行特征提取,通过预训练的主干网络得到图像块特征,再经过多类注意力分支和切片级分类器,结合真实标签进行预测。
- Survival Prediction(生存预测):与全切片图像级别分类类似,先提取特征,然后通过多类注意力分支和切片级分类器,结合临床信息计算C-index和风险分数,预测患者生存情况 。
如何学习大模型 AI ?
由于新岗位的生产效率,要优于被取代岗位的生产效率,所以实际上整个社会的生产效率是提升的。
但是具体到个人,只能说是:
“最先掌握AI的人,将会比较晚掌握AI的人有竞争优势”。
这句话,放在计算机、互联网、移动互联网的开局时期,都是一样的道理。
我在一线互联网企业工作十余年里,指导过不少同行后辈。帮助很多人得到了学习和成长。
我意识到有很多经验和知识值得分享给大家,也可以通过我们的能力和经验解答大家在人工智能学习中的很多困惑,所以在工作繁忙的情况下还是坚持各种整理和分享。但苦于知识传播途径有限,很多互联网行业朋友无法获得正确的资料得到学习提升,故此将并将重要的AI大模型资料包括AI大模型入门学习思维导图、精品AI大模型学习书籍手册、视频教程、实战学习等录播视频免费分享出来。

第一阶段(10天):初阶应用
该阶段让大家对大模型 AI有一个最前沿的认识,对大模型 AI 的理解超过 95% 的人,可以在相关讨论时发表高级、不跟风、又接地气的见解,别人只会和 AI 聊天,而你能调教 AI,并能用代码将大模型和业务衔接。
- 大模型 AI 能干什么?
- 大模型是怎样获得「智能」的?
- 用好 AI 的核心心法
- 大模型应用业务架构
- 大模型应用技术架构
- 代码示例:向 GPT-3.5 灌入新知识
- 提示工程的意义和核心思想
- Prompt 典型构成
- 指令调优方法论
- 思维链和思维树
- Prompt 攻击和防范
- …
第二阶段(30天):高阶应用
该阶段我们正式进入大模型 AI 进阶实战学习,学会构造私有知识库,扩展 AI 的能力。快速开发一个完整的基于 agent 对话机器人。掌握功能最强的大模型开发框架,抓住最新的技术进展,适合 Python 和 JavaScript 程序员。
- 为什么要做 RAG
- 搭建一个简单的 ChatPDF
- 检索的基础概念
- 什么是向量表示(Embeddings)
- 向量数据库与向量检索
- 基于向量检索的 RAG
- 搭建 RAG 系统的扩展知识
- 混合检索与 RAG-Fusion 简介
- 向量模型本地部署
- …
第三阶段(30天):模型训练
恭喜你,如果学到这里,你基本可以找到一份大模型 AI相关的工作,自己也能训练 GPT 了!通过微调,训练自己的垂直大模型,能独立训练开源多模态大模型,掌握更多技术方案。
到此为止,大概2个月的时间。你已经成为了一名“AI小子”。那么你还想往下探索吗?
- 为什么要做 RAG
- 什么是模型
- 什么是模型训练
- 求解器 & 损失函数简介
- 小实验2:手写一个简单的神经网络并训练它
- 什么是训练/预训练/微调/轻量化微调
- Transformer结构简介
- 轻量化微调
- 实验数据集的构建
- …
第四阶段(20天):商业闭环
对全球大模型从性能、吞吐量、成本等方面有一定的认知,可以在云端和本地等多种环境下部署大模型,找到适合自己的项目/创业方向,做一名被 AI 武装的产品经理。
- 硬件选型
- 带你了解全球大模型
- 使用国产大模型服务
- 搭建 OpenAI 代理
- 热身:基于阿里云 PAI 部署 Stable Diffusion
- 在本地计算机运行大模型
- 大模型的私有化部署
- 基于 vLLM 部署大模型
- 案例:如何优雅地在阿里云私有部署开源大模型
- 部署一套开源 LLM 项目
- 内容安全
- 互联网信息服务算法备案
- …
学习是一个过程,只要学习就会有挑战。天道酬勤,你越努力,就会成为越优秀的自己。
如果你能在15天内完成所有的任务,那你堪称天才。然而,如果你能完成 60-70% 的内容,你就已经开始具备成为一名大模型 AI 的正确特征了。
这份完整版的大模型 AI 学习资料已经上传CSDN,朋友们如果需要可以微信扫描下方CSDN官方认证二维码免费领取【保证100%免费】

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








