小罗碎碎念
本期推荐的文章是《CT-based radiomics prediction of complete response after stereotactic body radiation therapy for patients with lung metastases》,由Savino Cilla等人撰写,发表在《Strahlentherapie und Onkologie》2023年第199卷上。
文献信息
- 文章的DOI是10.1007/s00066-023-02086-6
- 接收日期为2023年2月6日
- 接受日期为2023年4月11日
- 在线发表日期为2023年5月31日
文献简介
这篇文章介绍了一项关于使用基于 CT 的影像组学来预测肺转移立体定向放射治疗 (SBRT) 后完全反应的研究
要点和关键论点如下:
- 目的:开发一种基于机器学习的预测模型,用于接受 SBRT 的肺寡转移性癌症患者的完全缓解。
- 方法:分析
56例患者80例肺寡转移的CT图像,提取影像组学特征,并使用逻辑回归和分类以及回归树分析评估其与完全缓解的相关性。 - 主要发现:四个影像组学特征(表面体积比、偏度、相关性、灰色归一化水平均匀性)与完全缓解相关。机器学习模型的准确度、精确度和召回率分别为 0.644 和 0.750、0.644 和 0.651 以及 0.635 和 0.754。
- 结论:治疗前CT扫描的影像组学特征可以预测SBRT后肺寡转移的完全反应,突出了影像组学在预测治疗反应方面的潜力。
总体而言,该研究证明了影像组学分析在预测肺转移 SBRT 后治疗反应方面的效用,为肺癌患者的个性化治疗计划提供了见解。
一、引言
立体定向体部放疗(SBRT)作为早期不可治愈的非小细胞肺癌(NSCLC)和肺转移瘤的黄金治疗标准,已得到广泛实施,这得益于成像、放疗计划及放疗传递技术的进步[1, 2]。特别是在肺转移瘤的治疗中,SBRT的使用允许给予高消融剂量,有望实现更长的局部控制和总体生存期。一些研究表明,孤立性或少量肺转移瘤的局部控制率在1年内可达70-100%[3-5]。
知识点补充:立体定向体部放疗
立体定向体部放疗(Stereotactic Body Radiation Therapy,简称SBRT)是一种高度精确的放射治疗方法,主要用于治疗身体某些部位的肿瘤,尤其是肺癌、肝癌和脊柱旁的肿瘤等。
SBRT的特点是能够给予肿瘤高剂量的放射治疗,同时最大限度地减少对周围正常组织的影响。
-
精确定位:使用先进的成像技术(如CT、MRI或PET/CT)对肿瘤进行精确定位,确保放射治疗的精确性。
-
治疗计划:根据肿瘤的大小、形状和位置,以及周围正常组织的特性,制定详细的放射治疗计划。
-
高剂量分割:SBRT通常涉及较少次数的治疗(通常为1至5次),但每次治疗给予的放射剂量较高,这与传统的放疗(需要多次治疗,每次剂量较低)不同。
-
立体定向技术:使用立体定向技术,确保放射束精确地对准肿瘤,有时使用特殊的设备(如体部框架或呼吸控制技术)来进一步减少对周围正常组织的损伤。
-
图像引导放疗(IGRT):在每次治疗前,使用成像技术确认肿瘤的位置,以确保治疗的精确性。
-
治疗过程:患者平躺在治疗台上,放射治疗机器会根据治疗计划精确地将放射线束对准肿瘤。
-
治疗后的监测:治疗后,患者将定期进行影像学检查和临床评估,以监测治疗效果和及时发现任何可能的副作用。
SBRT的优势在于它能够提供有效的局部控制,对于无法手术切除或手术风险较高的患者来说,是一种重要的治疗选择。此外,由于治疗次数少,SBRT还可以减少患者的整体治疗时间和相关费用。
然而,SBRT也有其局限性和风险,包括可能对周围正常组织造成损伤,以及存在一定的副作用,如疲劳、皮肤反应、疼痛和吞咽困难等。因此,SBRT的适用性需要根据患者的具体情况和肿瘤的特性来决定。
近期报告指出,胸廓SBRT后的病理完全缓解(CR)率低于之前的预测,这种情况不仅发生在早期非小细胞肺癌中[6],也发生在肺寡转移瘤的情形中[7-9]。因此,迫切需要一种能够识别在接受SBRT治疗肺转移瘤后,处于不完全/部分缓解高风险(或复发高风险)的患者分层方法。这样的方法可以帮助设计针对患者特定疾病特征的治疗计划,通过在治疗前选择剂量增强或额外的系统治疗,从而改善治疗窗口。
目前,对于肺SBRT临床结果的准确预测模型仍然较少[10-12]
在肺转移瘤的情况下,Tanadini-Lang等人[10]开发了一个预测SBRT后2年总体生存期的列线图。Karnofsky表现指数、原发肿瘤类型、原发肿瘤控制情况、最大直径和转移瘤数量被确定为显著的预后因素。该列线图的计算一致性指数为0.73。
在原发肺癌的情况下,Baker等人[11]开发并验证了一个预测早期肺癌SBRT后总体生存期的列线图。该列线图基于六个预后因素:年龄、性别、Karnofsky表现状态、可手术性、Charlson合并症指数和肿瘤直径,提供的一致性指数为0.64。最后,Ye等人[12]创建了一个预测接受SBRT的I期NSCLC患者治疗前预后的列线图。作者显示,2年局部区域控制和无进展生存期与肿瘤大小和最大标准化摄取值显著相关。该列线图在模型组和验证组的一致性指数分别大于0.8和0.7。
近年来,放射组学作为一种新兴方法,能够从医学影像中提取大量定量特征,对于评估肿瘤表型显示出巨大潜力[13]。这些数学特征可作为诊断、分期、预后和预测肿瘤反应的影像生物标志物。尽管针对肺转移瘤的放射组学仍大多处于探索阶段[14],但已有一些研究成功获得了预测淋巴结复发和复发率的放射组学特征[15-18]或总体生存[19-22]。
然而,各种开发算法的临床影响仍低于预期,主要是由于结果的可重复性较差,且缺乏来自其他机构数据的外部验证[23]。专注于SBRT治疗后治疗反应的研究更为罕见。Cheung等人[24]在经SBRT治疗的肺寡转移瘤患者中识别出两个放射组学治疗反应预测因子(偏度和均方根),并开发了一个用于预测目的的机器学习模型。他们的支持向量机模型提供了74.8%的准确率。
鉴于SBRT在治疗肺寡转移瘤中的全球广泛应用,基于放射组学分析的新强有力预测模型将是区分对治疗有反应和无反应肿瘤的受欢迎工具。
当前研究的目的是对肺转移瘤进行探索性的基于CT的放射组学分析,以识别能够预测SBRT后放射学和功能反应的放射组学特征。此后,生成两个机器学习模型,以预测基于选择的放射组学特征和临床特征后的SBRT治疗反应。
二、材料和方法
2-1:患者
在2010年1月至2020年12月期间,我院对56名患有80处肺寡转移瘤的患者进行了SBRT治疗。这些患者被纳入之前的一项前瞻性I-II期研究(DESTROY-1)[25],该研究得到了天主教大学机构审查委员会的批准(Destroy-1: P#594/CE)。所有患者均签署了书面知情同意书。
研究排除了ECOG表现状态>3的患者,或有与非恶性疾病相关的医疗问题,这将限制患者完全遵守研究的患者,以及之前接受过SBRT的患者。
知识点补充:ECOG表现状态
ECOG表现状态(Eastern Cooperative Oncology Group Performance Status,简称ECOG PS)是一种广泛使用的评分系统,用于评估癌症患者的一般健康状况和日常活动能力。
这个评分系统最初是为了在临床试验中标准化患者的功能状态而开发的,但现在已经广泛应用于临床实践,帮助医生了解患者的整体健康状况,并作为治疗决策和预后评估的一个因素。
ECOG表现状态评分从0到5,具体定义如下:
- 0:完全活动,能够进行所有正常的活动,没有限制。
- 1:有症状,但能够完全自理,轻度限制。
- 2:中度限制,能够进行轻度活动,但不能进行所有正常活动。
- 3:重度限制,只能进行有限的自我照顾,不能进行正常活动。
- 4:卧床不起,完全需要他人帮助,除非上厕所。
- 5:死亡。
ECOG PS评分通常由医生或医疗专业人员根据患者的自我报告和观察来进行。这个评分系统简单、快速,能够为医疗团队提供患者功能状态的快速概览。ECOG表现状态评分较高的患者可能意味着健康状况较差,可能无法耐受某些治疗,或者可能预后不佳。因此,ECOG PS评分是癌症治疗决策中一个重要的考量因素。
2-2:CT图像的获取、分割以及计划
在本次研究中,患者接受了计算机断层扫描(CT)模拟,使用的是128层扫描仪(Brilliance 128,飞利浦医疗保健,荷兰贝斯特)。CT图像的获取采用了2毫米厚的切片。所有患者均采用仰卧位进行模拟。所有病变均由资深放射科医生(A.P.)和资深放射肿瘤科医生(F.D.)在治疗计划系统上手动分割。
临床靶区(CTV)定义为计划CT和/或CT-PET和/或MRI上确定的总体肿瘤体积(GTV)。内部靶区(ITV)是基于呼吸运动分析(自由呼吸或腹压或深吸气屏气)定义的。根据患者设置可重复性的量化,设置边界设定为3mm,如前所述[25]。图像引导放射治疗用于每次分割的患者设置。
所有患者接受的治疗方案为40-50 Gy的剂量,分五次连续给予,相当于BED10为80至100 Gy。SBRT计划使用固定野强度调制(IMRT)或体积调制弧治疗(VMAT)技术,以及6-MV X射线能量束生成。采用了一种统一的处方等剂量表面(IDS)选择方法。
对于每个计划,IDS被选为满足以下两个条件的最大IDS:95%的PTV体积达到100%的处方剂量,99%的PTV达到至少90%的处方剂量。GTV内的最大剂量不应超过处方剂量的140%。计划计算使用了坍缩锥卷积算法和1.5mm的剂量网格大小。
知识点补充:坍缩锥卷积算法
坍缩锥卷积算法(Collapsed Cone Convolution algorithm,简称CCC算法)是一种用于放射治疗剂量计算的先进算法。它被设计用来更精确地计算放射线在人体组织中的剂量分布,尤其是在处理复杂几何形状和不规则密度分布的区域时。以下是坍缩锥卷积算法的关键特点:
-
基于卷积的方法:CCC算法使用卷积原理来模拟放射线与物质相互作用的物理过程。卷积是一种数学操作,它将放射线的分布(如X射线或质子束)与组织对射线的响应结合起来,以计算剂量分布。
-
坍缩锥模型:该算法使用坍缩锥模型来近似放射线在不同组织中的穿透和散射。这个模型考虑了射线在通过组织时的衰减和散射效应,但不直接模拟射线的详细路径。
-
快速计算:与蒙特卡洛模拟等更精确但计算成本更高的方法相比,CCC算法提供了一个相对快速的剂量计算解决方案,使其适用于临床实践。
-
组织异质性:CCC算法能够处理组织异质性,即不同类型和密度的组织对放射线吸收和散射的影响。
-
剂量分布:算法输出的是三维剂量分布图,这可以帮助医生和物理师评估治疗计划的质量,比如剂量是否充分覆盖了肿瘤,以及对周围正常组织的潜在损伤。
-
临床应用:CCC算法常用于放射治疗计划系统中,以帮助设计和评估治疗计划,确保患者接受安全有效的放射治疗。
-
限制:尽管CCC算法在计算效率和准确性之间取得了平衡,但它仍然有局限性,特别是在模拟低能光子或非常复杂几何形状的情况下。在这些情况下,可能需要使用更精确的算法,如蒙特卡洛模拟。
坍缩锥卷积算法是一种在放射治疗领域广泛使用的剂量计算工具,它帮助医疗专业人员更好地理解和优化治疗计划,以提高治疗效果并减少对患者的伤害。
2-3:治疗反应评估
本研究的主要临床结局是放射学治疗反应,通过SBRT后4个月的形态学对比增强CT进行评估。根据RECIST(实体肿瘤反应评估标准)系统v1.0[26],这一时间点被认为是评估早期和晚期反应恶性肿瘤都合适的。
- 完全缓解(CR)定义为CT扫描中病变消失;
- 减少超过30%被视为部分缓解(PR);
- 任何生长的、不易归因于纤维化的病变被报告为疾病进展(PD)。
2-4:放射组学分析
CT DICOM图像包含GTV的分割,用于提取放射组学分析的所有特征。
图像处理使用的是软件包Pyradiomics 2.0.1[27]。该软件允许提取IBSI(图像生物标志物标准化倡议)[28]定义的标准化特征。
预处理包括使用B样条插值函数将CT图像重采样为1mm^3的等距体素。每个病变自动提取总共107个特征,包括:
一阶统计特征(强度直方图,IH):19个- 基于形状的直方图特征:26个
- 灰度共生矩阵,GLCM:24个特征
- 灰度行程长度矩阵,GLRLM:16个特征
- 灰度大小区域矩阵,GLSZM:16个特征
- 邻域灰度差异矩阵,NGTDM:5个特征
- 灰度依赖矩阵,GLDM:14个特征
2-5:特征选择、建模与统计分析
本研究通过以下三个步骤来避免共线性、降低维度,并识别必要的放射组学特征。
首先,我们计算了由放射科医生和放射肿瘤科医生对30个随机选择的病变进行的两次分割得到的基于ROI的放射组学特征之间的符合相关系数(CCC)。将CCC>0.90的特征定义为稳定特征,并纳入后续分析。
其次,我们使用Spearman等级系数(ρ)评估放射组学特征之间的成对相关性。所有|ρ|≥0.8的特征被视为冗余特征,并在后续分析中剔除,只保留与临床结果在单变量分析中最强相关的特征。
最后,通过逐步向后消除方法确定剩余特征的相关重要性。在这个过程中,根据赤池信息准则(AIC),考虑从解释变量集合中减去一个特征。
知识点补充:赤池信息准则
赤池信息准则(Akaike Information Criterion,简称AIC)是一种用于统计模型选择的准则,由日本统计学家赤池弘次提出。AIC旨在评估给定数据集的不同统计模型的相对质量,它基于似然函数的概念,并考虑了模型复杂性的影响。AIC被广泛应用于各种领域,包括生态学、经济学、信号处理和医学研究。
AIC的定义如下:
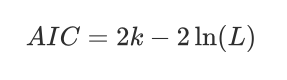
其中:
- ( k ) 是模型中参数的数量。
- ( L ) 是模型的最大似然估计值。
AIC的核心思想是,一个好模型应该在拟合数据(即最大化似然函数)和保持模型简洁(即参数数量较少)之间取得平衡。AIC通过惩罚模型中参数的数量来实现这一点,因为参数数量越多,( k ) 越大,AIC值也就越高。
在实际应用中,研究者会比较多个模型的AIC值:
- 一个模型的AIC值越低,表示该模型在拟合数据和保持简洁之间取得了更好的平衡。
- 当面对多个候选模型时**,AIC值最低的模型通常被认为是最合适的模型**。
AIC的一个主要优点是它提供了一种相对简单的方法来选择最佳模型,而不需要对模型的似然函数进行复杂的比较。然而,AIC也有局限性,它假设所有模型都是正确指定的,即模型的形式和分布假设都是正确的。如果模型的假设不正确,AIC可能会导致错误的模型选择。
在机器学习和统计分析中,AIC常用于模型选择,尤其是在变量选择、特征选择和决策树剪枝等场景中。通过最小化AIC,可以帮助识别对数据拟合最好且最简洁的模型。
使用Mann–Whitney U检验评估治疗反应与所选放射组学特征之间的关联。统计显著性设置为p值0.05或更低。
最终显著的放射组学特征用于构建两个模型,以分类响应或非响应病变,包括逻辑回归(LR)和分类与回归树分析(CART)。
LR是一种经典的机器学习算法,通常用于二分类任务。该模型使用逻辑方程提供数据集中两个类别(0或1)之一的类别成员概率。LR的快速训练是其众所周知的优势,输入变量可以是离散的或连续的。
分类与回归树(CART)是一种基于决策树的方法,广泛应用于数据挖掘。它能够揭示数据关系,并自动搜索模式以发现即使是在高度复杂数据中的隐藏结构。CART模型的典型表示是一个二叉树,其中每个根节点代表一个输入特征及其在该特征上的分割点。树的叶节点包含用于预测的输出变量。最佳分割点通过Gini不纯度(GI)指数识别。
Gini指数的值介于0和1之间,其中0表示分类的纯度(即所有元素属于一个指定类别),1表示元素在各个类别中的随机分布。Gini指数值为0.5表示元素在类别间的均匀分布。
模型使用五折交叉验证进行验证。这是一种重采样程序,主要用于估计机器学习模型在未见数据上的技能。这种方法涉及将观察集随机分成k组(在我们的情况下是五折)大约相等的大小。第一个折被视为验证集,方法在剩余的k-1个折上拟合。这个过程重复十次,旨在减少交叉验证结果的方差,并降低仅一次运行得到过于乐观结果的机会。
模型的性能通过接收器操作特性曲线(ROCs)、准确度、精确度、召回率和F1度量评估指标来评估。
统计分析包括机器学习训练和测试,使用XLSTAT统计包(Addinsoft,纽约,纽约,美国)进行。
知识点补充:XLSTAT统计包
XLSTAT是一款强大的统计分析软件包,它作为插件运行在Microsoft Excel中,为Excel用户提供了丰富的统计分析功能。XLSTAT的主要目标是简化复杂的统计分析过程,使其更加易于接近和使用,特别是对于那些没有深入统计学背景的用户。以下是XLSTAT的一些关键特点:
-
用户界面:XLSTAT提供了一个直观的用户界面,用户可以通过简单的菜单导航和对话框来选择所需的统计测试或分析。
-
数据分析:XLSTAT支持广泛的数据分析方法,包括描述性统计、回归分析、方差分析、时间序列分析、生存分析、聚类分析、多变量分析等。
-
结果输出:分析完成后,XLSTAT能够将结果以表格、图形或模型摘要的形式直接输出到Excel工作表中,方便用户查看和进一步处理。
-
数据导入:XLSTAT能够处理来自Excel工作表的数据,也可以导入外部数据文件,如CSV、TXT等格式。
-
定制报告:XLSTAT允许用户定制分析报告,包括选择显示哪些统计量和图形,以及如何格式化输出结果。
-
高级功能:除了基本的统计分析,XLSTAT还提供了一些高级功能,如敏感性分析、蒙特卡洛模拟、六西格玛分析等。
-
教学和研究:XLSTAT在教学和研究中也很有用,因为它可以帮助学生和研究人员快速执行复杂的统计分析,而无需深入了解底层的统计理论。
-
支持多种语言:XLSTAT支持多种语言,使其能够服务于全球用户。
-
更新和支持:XLSTAT提供定期的更新和技术支持,以确保软件的统计方法保持最新,并解决用户可能遇到的任何问题。
-
成本:XLSTAT是一款商业软件,用户需要购买许可证来使用其全部功能。但是,它通常提供免费试用版,让用户在购买前能够测试软件的功能。
XLSTAT通过将强大的统计分析工具集成到熟悉的Excel环境中,使得没有专业统计软件背景的用户也能够执行复杂的数据分析,这在商业、科研和教育等多个领域都非常有用。
三、结果
3-1:患者情况
从2010年至2020年,共招募了56名患者(38名男性和18名女性),中位年龄为72岁(范围38-90岁)。
分析的总肺转移瘤数量为80个,其中36个达到完全缓解(CR组)。另外31个转移瘤达到部分缓解,10个被认为是稳定疾病,3个被认为是进展性疾病——这44个转移瘤被认为是非完全缓解者(NCR组)。
大多数转移瘤来自肺(44个转移瘤)和结直肠(20个转移瘤)肿瘤。在组织学方面,大多数是腺癌(35个病变),其次是鳞状细胞癌(7个病变)。表1报告了患者的特征。

以下是根据表格内容对患者特征的分析:
-
患者数量 (No. of patients): 共有56名患者参与了这项研究。
-
年龄 (Median age, years): 患者的中位年龄是72岁,年龄范围从38岁到90岁。
-
性别 (Gender, M/F): 其中38名为男性,18名为女性。
-
吸烟状况 (Smoker, Y/N): 23名患者是吸烟者,而33名患者不是。
-
病变数量 (No. of lesions): 总共分析了80处病变。
-
病变位置 (Location, central/peripheral): 病变位置分为中心型和周围型,分别是17处和63处。
-
患者病变数量 (Number of lesions, patients):
- 有46名患者有1处病变。
- 12名患者有2处病变。
- 3名患者有3处病变。
- 1名患者有4处病变。
-
原发肿瘤的病变数量 (Number of lesions, primary tumor):
- 44处病变源自肺部肿瘤。
- 11处源自直肠肿瘤。
- 9处源自结肠肿瘤。
- 8处源自妇科肿瘤。
- 2处源自乳腺癌。
- 2处源自皮肤肿瘤。
- 4处源自其他类型的肿瘤。
-
肿瘤体积 (Median GTV, cc): 肿瘤的中位总体积(Gross Tumor Volume, GTV)是5.3立方厘米(cc),范围从0.2到61.9 cc。
-
计划治疗体积 (Median PTV, cc): 计划治疗体积(Planning Target Volume, PTV)的中位数是27.5 cc,范围从4.9到215.7 cc。
-
处方剂量 (Median prescribed dose, Gy): 中位处方剂量是50 Gy,范围从30到50 Gy。
-
处方等剂量百分比 (Median prescribed isodose, percentage): 中位处方等剂量百分比是81%,范围从73到89%。
-
生物等效剂量 (Median BED, Gy): 生物等效剂量(Biological Equivalent Dose, BED)的中位数是100 Gy,范围从48到100 Gy。
这些患者特征为研究提供了重要的背景信息,有助于理解研究的参与者群体,并可能对分析研究结果和解释治疗响应的影响因素提供线索。例如,吸烟状况可能与肺癌的发展有关,而肿瘤的位置、数量和体积可能会影响SBRT治疗计划和治疗结果。
3-2:放射组学特征及选择
从每个病变中提取了总共107个放射组学特征。
整体平均符合相关系数(CCC)为0.97 ± 0.14。两位临床医生之间形状特征的平均CCC为0.98 ± 0.08,表明对肺转移瘤分割的观察者间可重复性良好。在所有30个分析的转移瘤中,强度和纹理特征的平均CCC均≥0.89。
特征之间的成对Spearman相关性分析揭示了整个数据集中高度相互依赖性,超过85%的特征与至少一个其他特征在|ρ| > 0.8的水平上相关。因此,经过这两步,我们从107个特征中获得了15个初级特征集。随后,根据逐步向后消除方法,选择了四个最终特征用于构建预测模型,即:
- 表面体积比(SVR)
- 偏度(Skew)
- 相关性(Corr)
- 灰度归一化水平均匀性(GNLU)
这四个放射组学特征与两组病变的关联在单变量分析(Mann–Whitney U检验)中报告了统计学意义(p< 0.05)。这些四个特征的详细诊断准确性统计数据在表2中报告,包括:
- 曲线下面积(AUC)
- 敏感性
- 特异性
- 阳性预测值
- 阴性预测值
- 准确度
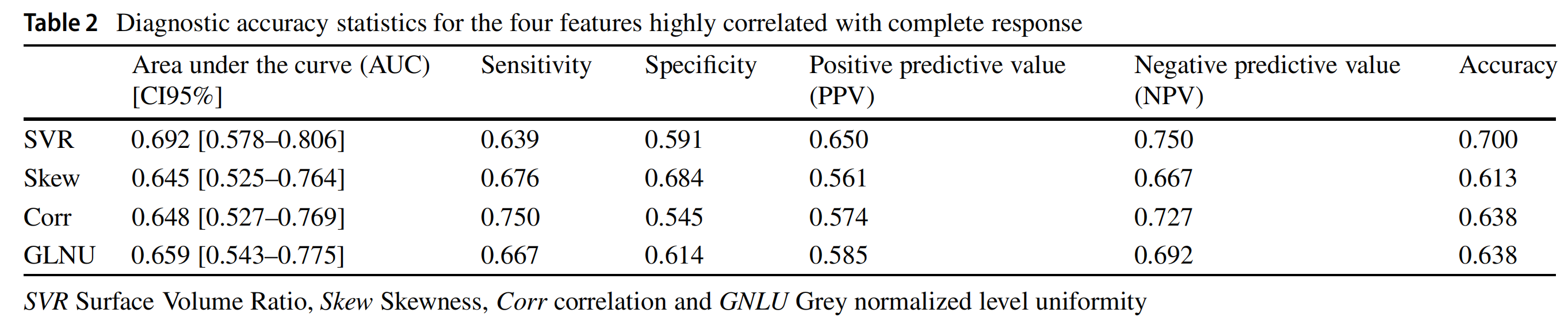
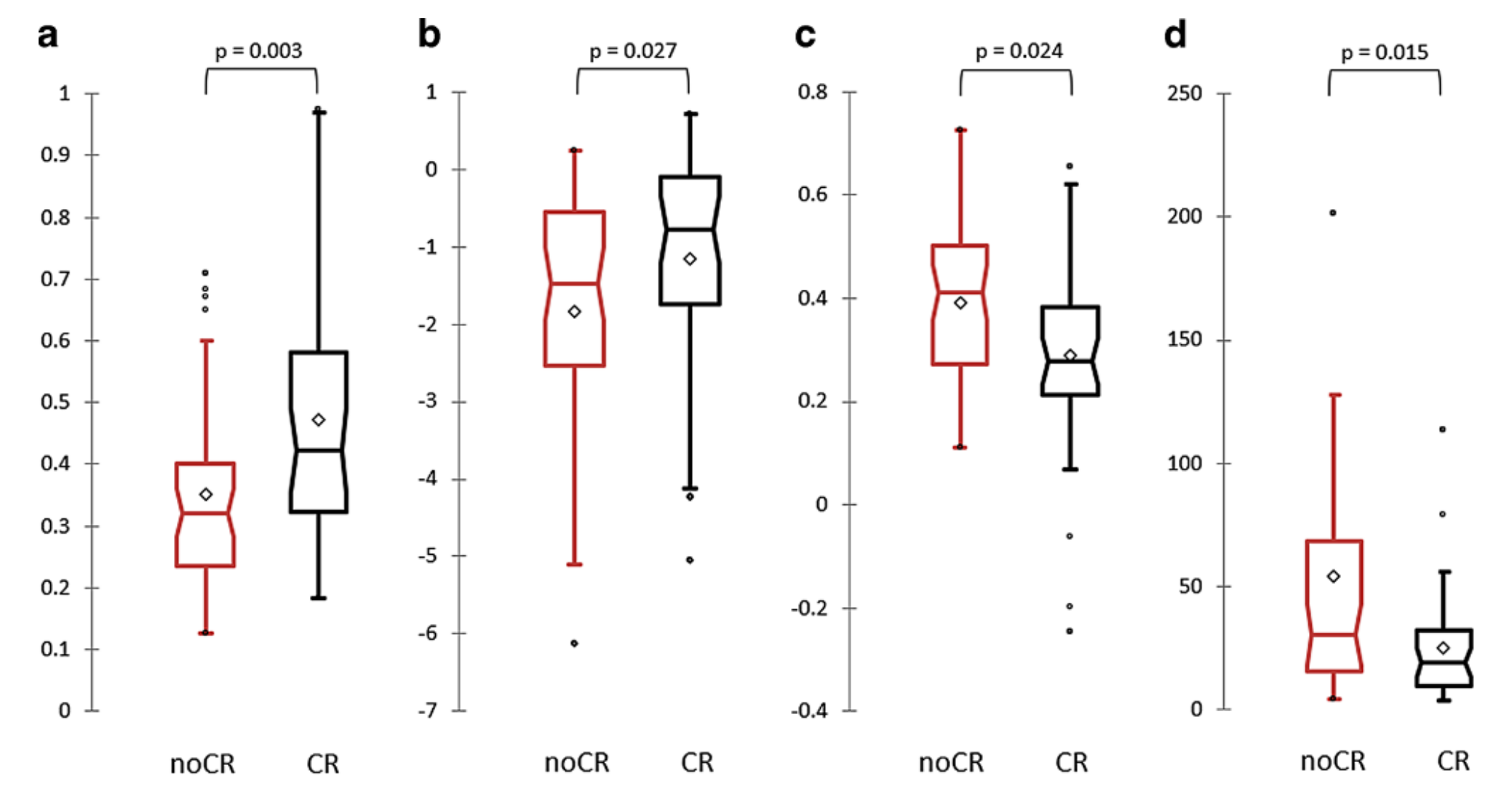
Fig. 1 展示了四个与治疗反应结果相关联的放射组学特征的箱形图(Box-and-whisker plots),这些特征在单变量分析中与完全缓解(CR)和非完全缓解(noCR)相关。每个箱形图代表了一个特定的放射组学特征,并且比较了CR组和noCR组之间的差异。以下是对这些图表的分析:
-
表面体积比率 (Surface Volume Ratio, SVR):
- 箱形图a展示了表面体积比率的分布情况。
- SVR是一个描述肿瘤形状的放射组学特征,较高的SVR值表明肿瘤具有更不规则的边缘。
-
偏度 (Skewness, Skew):
- 箱形图b展示了偏度的分布情况。
- 偏度是衡量数据分布不对称性的统计量,正偏度表示数据分布的尾部向右延伸,负偏度则向左延伸。
-
相关性 (Correlation, Corr):
- 箱形图c展示了相关性的分布情况。
- 相关性是衡量肿瘤内部结构均匀性的指标,高相关性表明肿瘤内部的像素强度值更加一致。
-
灰度非均匀性 (Grey Level Nonuniformity, GLNU):
- 箱形图d展示了灰度非均匀性的分布情况。
- 灰度非均匀性是衡量图像中灰度分布不均匀性的指标,较高的值表明肿瘤内部的灰度变化更大。
每个箱形图通常包含以下元素:
- 中位数 (Median): 箱形图中的中线表示数据的中位数。
- 上四分位数 (Upper Quartile): 箱子的上边缘表示数据的上四分位数(75%分位数)。
- 下四分位数 (Lower Quartile): 箱子的下边缘表示数据的下四分位数(25%分位数)。
- 异常值 (Outliers): 箱子外的点通常被认为是异常值。
通过比较CR组和noCR组的箱形图,研究人员可以评估这些放射组学特征是否能够区分两种不同的治疗反应。如果CR组和noCR组的箱形图有显著差异,这可能表明相应的放射组学特征对于预测治疗反应具有潜在的预测价值。例如,如果CR组的SVR值普遍高于noCR组,这可能表明具有较高SVR值的肿瘤更有可能在SBRT治疗后实现完全缓解。
需要注意的是,为了确定这些放射组学特征的预测价值,研究人员还会进行统计测试(如Mann–Whitney U test),以评估两组之间的差异是否具有统计学意义。
Fig. 2 展示了两个不同患者的肺部病变的轴向CT图像和3D图,以及它们的放射组学特征值。这些特征值用于区分完全缓解(CR)和疾病稳定(stable disease)的治疗结果。
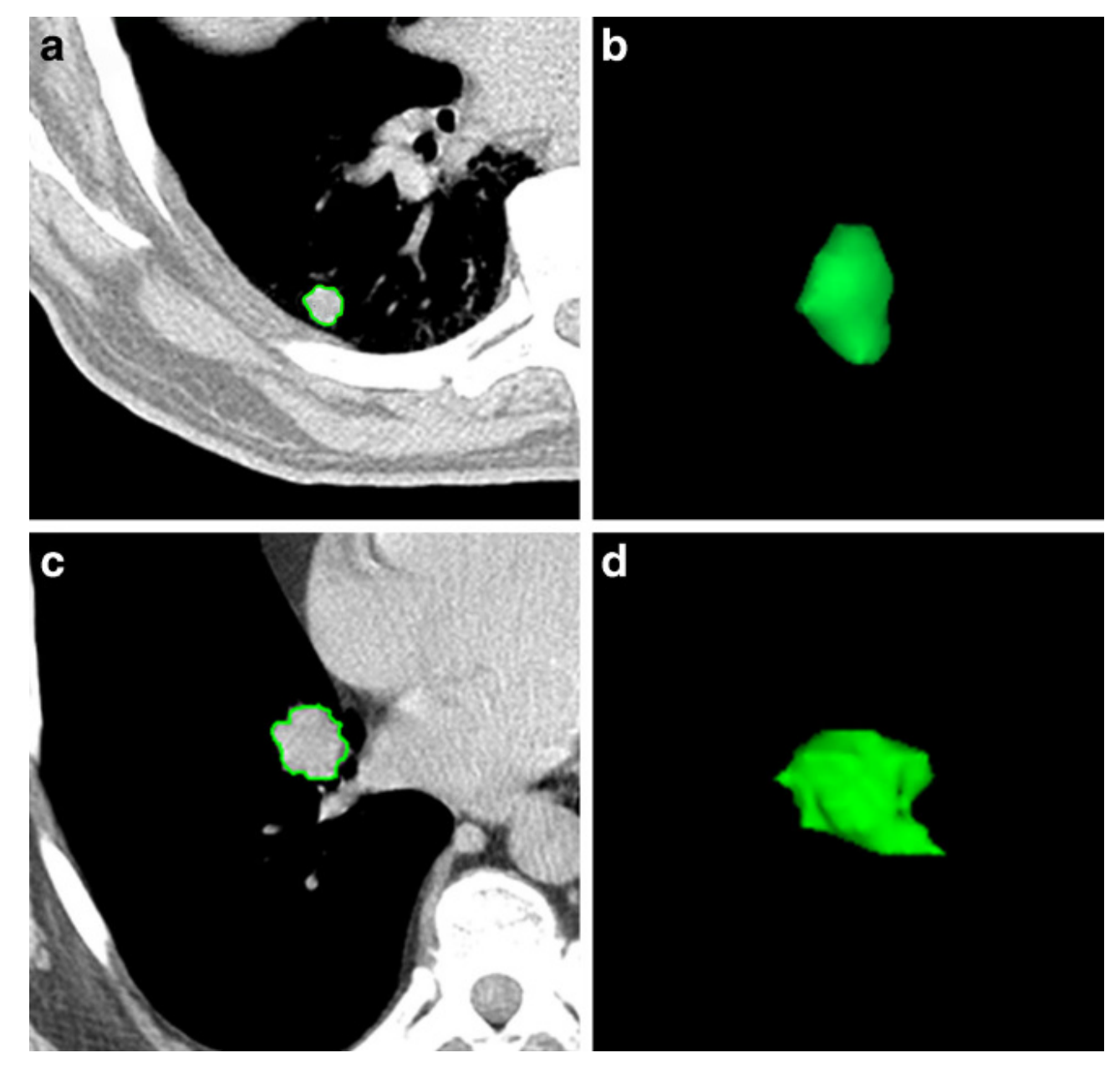
以下是对图2中信息的解释
- 患者1 (a, b):
- 年龄:78岁,男性。
- 治疗结果:完全缓解(CR)。
- 患者2 (c, d):
- 年龄:75岁,男性。
- 治疗结果:疾病稳定(stable disease)。
概念解释
- 轴向CT图像:展示了病变在CT扫描中的实际图像,可以帮助观察者直观地看到病变的位置和大小。
- 3D图:通过三维重建技术,提供了病变形态的三维视图,有助于更好地理解病变的空间结构。
放射组学特征值对比
通过比较两组病变的放射组学特征,研究人员可以寻找与治疗反应相关的模式。例如,CR组的病变可能具有较高的SVR值和较低的灰度非均匀性,而疾病稳定的病变可能具有较低的SVR值和较高的灰度非均匀性。
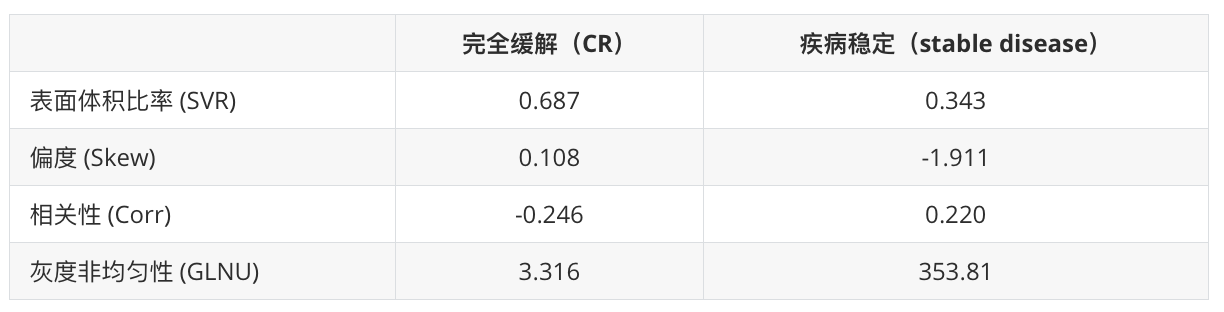
这些观察结果可以帮助研究人员理解哪些放射组学特征可能对预测SBRT治疗的反应更有帮助。
需要注意的是,虽然图2提供了两个病变的直观比较,但为了得出统计学上显著的结论,研究人员需要分析更大样本量的病变数据,并可能使用机器学习等高级分析技术来建立预测模型。
值得注意的是,没有发现与完全响应相关的临床变量。与两组响应相关的唯一非放射组学变量是病变的体积,较小的体积与完全响应显著相关。然而,正如预期的那样,发现这个变量与SVR特征共线性,因此被排除在后续分析之外。
3-3:机器学习模型
LR和CART模型的分类性能在表3中报告了训练和内部验证数据集。CART分类器表现最佳,准确度、精确度、召回率和F1分数分别为79.2%、78.4%、80.3%和78.5%。
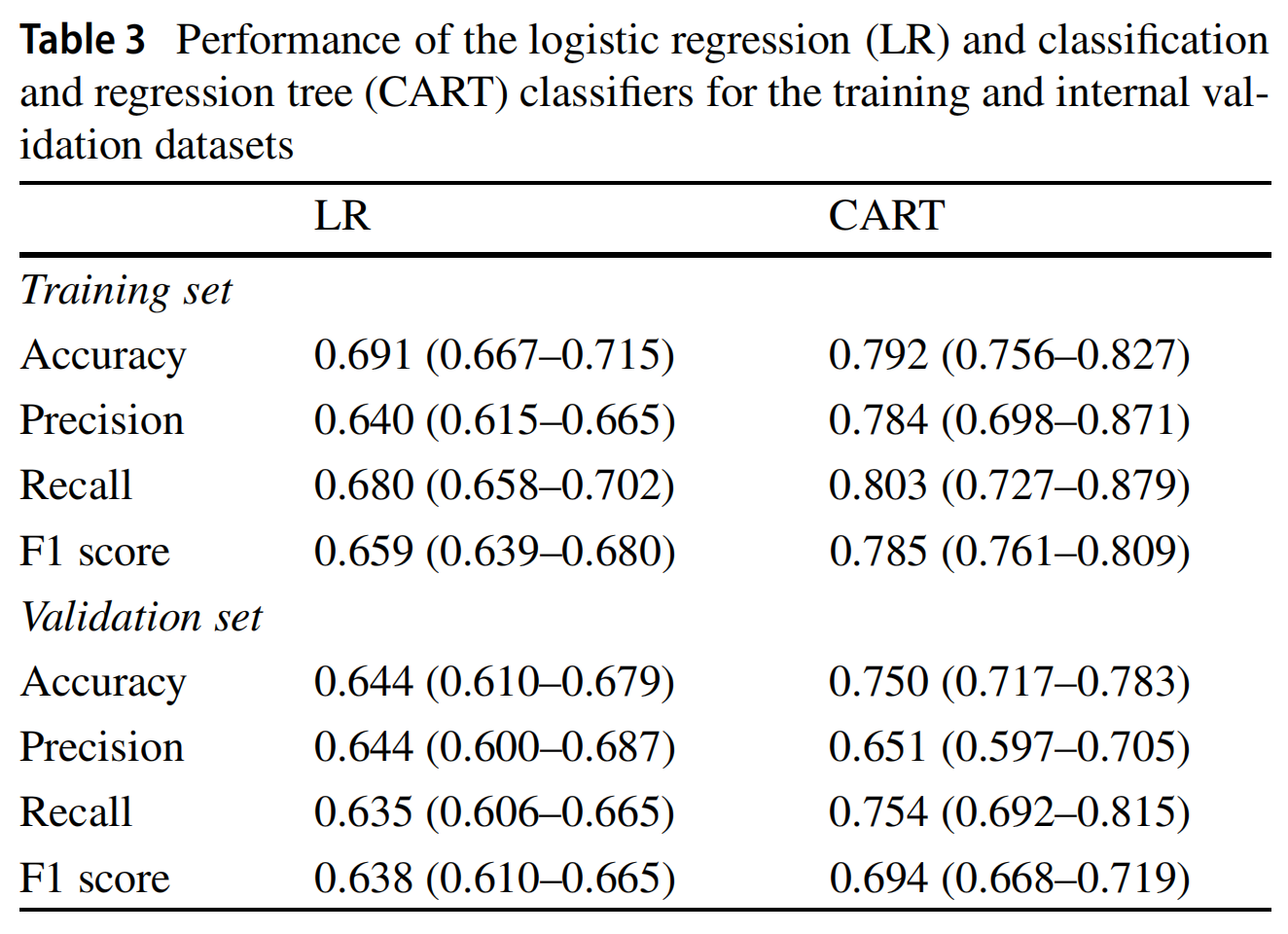
两个模型的接收器操作特性(ROC)曲线交叉验证结果在图3中展示。LR和CART模型的曲线下面积(AUC)分别为0.707(95% CI: 0.633–0.817)和0.753(95% CI: 0.675–0.836)。
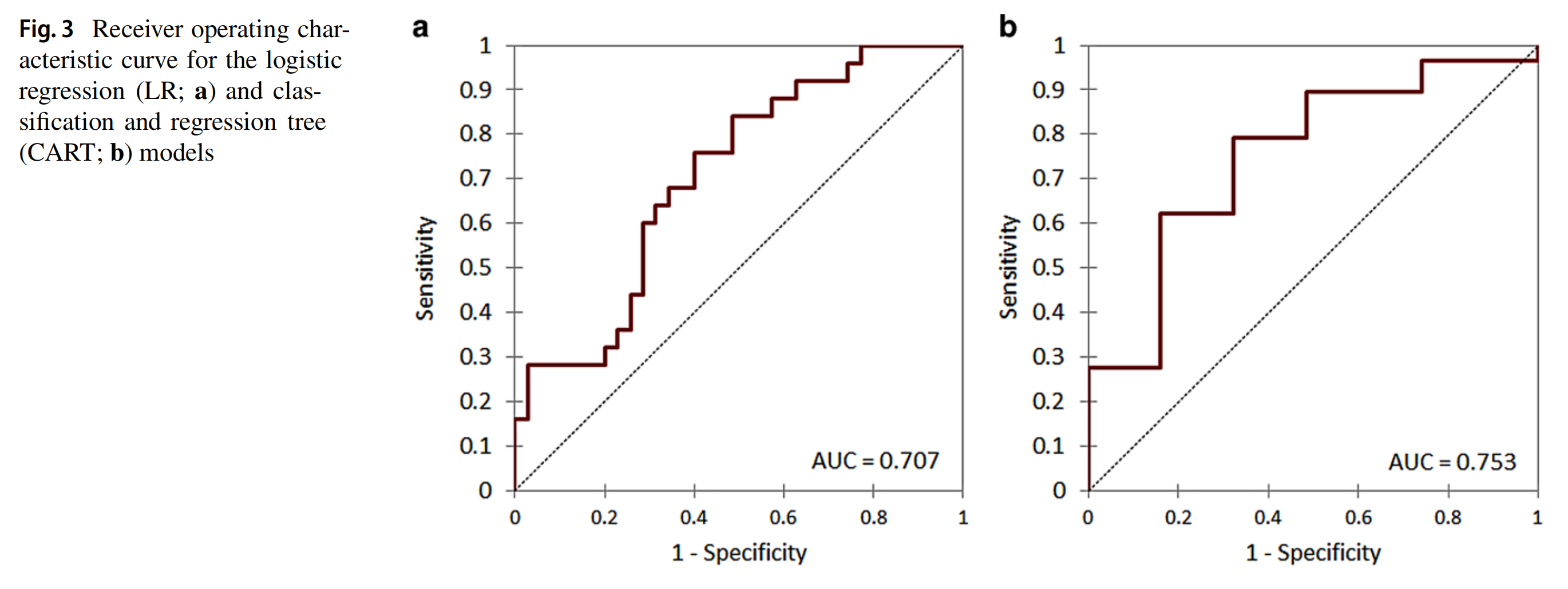
Fig. 4 中的分类回归树分析(Classification and Regression Tree Analysis,简称CART)是一种决策树的可视化表示,它展示了如何使用放射组学特征来预测肺转移瘤患者在接受立体定向体放射治疗(SBRT)后的完全缓解(CR)。CART模型是一种监督学习算法,它可以识别出哪些放射组学特征对于区分CR和非CR(noCR)最为重要。
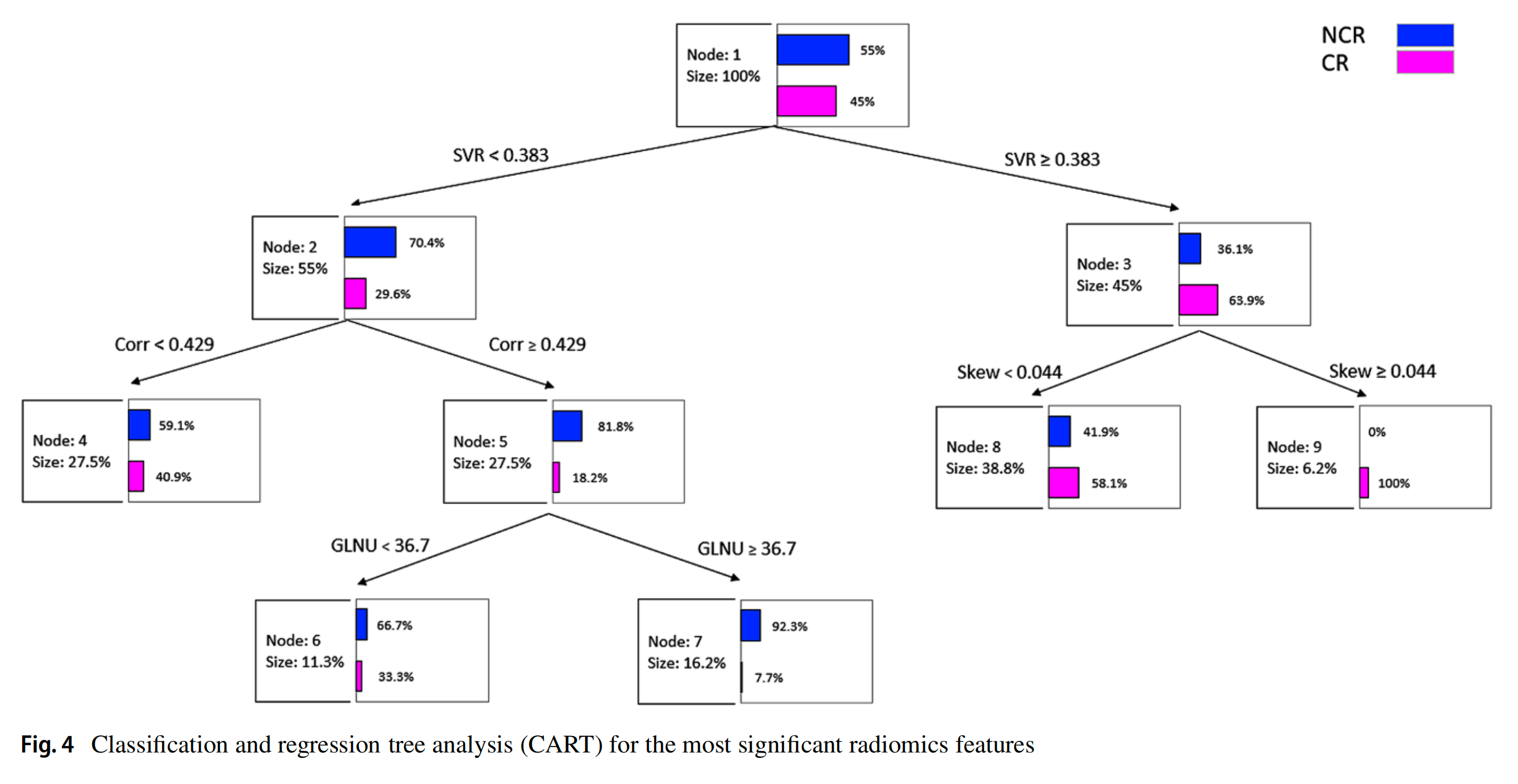
CART模型的决策树通常包括以下元素:
-
根节点 (Root Node): 决策树的起始点,通常基于一个单一的特征进行分割,该特征在所有考虑的特征中对分类结果的预测能力最强。
-
分支 (Branches): 从每个节点延伸出来的分支代表基于特定特征的不同阈值的分割。
-
内部节点 (Internal Nodes): 表示基于某个特征的分割点,每个内部节点都会根据该特征的值将数据分为两部分。
-
叶节点 (Leaf Nodes): 决策树的末端,代表最终的分类决策,即预测的响应类别(CR或noCR)。
-
分割点 (Split Points): 每个内部节点都会根据某个特定特征的值进行分割,分割点是该特征用于区分不同类别的特定阈值。
-
纯度 (Purity): 叶节点的纯度,即该节点下所有样本属于同一类别的程度。纯度越高,表示该节点的预测越可靠。
-
基尼不纯度指数 (Gini Impurity Index): CART使用基尼不纯度指数来评估节点的纯度,并选择最佳的分割点。
CART模型的一个优点是它的可解释性,即人类专家可以相对容易地理解模型的决策过程。通过分析CART图,医生可以更好地了解哪些放射组学特征对于预测治疗反应最为重要,并且可以据此做出更有针对性的治疗决策。
四、讨论
肺癌是一种高度异质性的疾病,不仅在细胞和组织学水平上存在差异,而且在同一患者内的不同病变之间以及同一病变的不同部分之间都存在显著的变异。因此,仅研究临床特征可能无法捕捉到肺部病变的异质性。目前的研究表明,高度异质性的肿瘤更具侵袭性,而具有不规则棘状边缘的肿瘤更可能是侵袭性肿瘤。
总的来说,这些发现暗示,内部密度更高且异质性更低的病变可能对治疗有更积极的反应。此外,区分原发性肺癌和肺部转移瘤在临床上是至关重要的,因为它们在预后和治疗方面存在显著差异。从这个角度来看,放射组学具有巨大的潜力,能够通过描述组织学和遗传特征以及捕捉肿瘤内部异质性,为癌症结果提供可靠的预测。然而,放射组学是一个相对较新的研究领域,其对肺部转移瘤的潜在临床应用仍然是一个相对较小的子领域,这从相关研究的匮乏中得到了证明。
本研究的主要目标是探索放射组学在预测接受SBRT治疗的肺部转移瘤完全缓解方面的可行性。为了提高预测模型,我们还尝试整合了诸如年龄、吸烟状况、肿瘤组织学类型和分期等临床特征,但没有发现任何临床变量与病变反应相关。
尽管没有任何临床特征预示着完全缓解,我们发现四个放射组学特征(表面体积比、偏度、相关性和灰度非均匀性)与完全缓解显著相关,突出了放射组学分析在预测SBRT治疗后肺部转移瘤结果方面的潜力。
表面体积比是形状特征中与完全缓解相关性最高的。特别是,我们发现SVR值较高的病变在SBRT后有更高的完全缓解概率。这并不令人意外,因为已有充分报道指出,体积较大且不规则的肿瘤在总体生存和局部控制方面预后较差。有趣的是,偏度和相关性也在之前的放射组学研究中被确定为肺肿瘤的主要放射组学特征。
据我们所知,只有一项由Cheung等人[24]进行的研究评估了放射组学在预测SBRT治疗后肺寡转移瘤反应方面的作用。作者报告说,偏度和均方根是放射学治疗反应的预测因子,准确率为74.8%。另一方面,一些研究专注于将放射组学应用于原发性肺癌,以识别预测放射组学特征。例如,Bousabarah等人[22]报告了CT放射组学分析在110例不可手术的早期NSCLC患者中的应用,这些患者接受了SBRT治疗,旨在预测局部控制、总体生存和无病生存。具体来说,作者报告说,具有高偏度(即Hounsfield值较低的病变占主导地位)的肺肿瘤局部失败的风险较低,生存概率较高,而具有高相关性(组织同质性的度量)的肺肿瘤更可能导致局部失败。这些结果与我们发现的完全一致。
此外,Coroller等人[36]发现偏度是化疗放疗后早期肺癌病理学大体残留疾病的一个显著相关特征。同样,Chong等人[37]证明了偏度在预测化疗放疗后肺腺癌病理学非应答患者方面具有预测价值。最后,Caruso等人[38]测试了胸部CT上CT纹理分析的能力,以识别恶性肺结节。作者报告说,除了峰度之外,恶性结节与良性结节纹理参数之间最显著的区别是偏度,恶性病变的偏度值统计上更高。
由于不同放射组学研究中偏度值可能与不良预后相关,一些研究人员实际上正在探索放射组学特征背后的生物学基础,这些特征可能具有特定的放射学外观。特别是,偏度被发现与NSCLC中的KRAS突变相关,这标志着预后不良和治疗抵抗的肺癌[39]。目前的假设是,“偏斜”肿瘤观察到的较差预后至少部分是由KRAS突变驱动的,例如通过诱导类似癌症干细胞的表型,导致放射抵抗。
使用这四个顶级特征,我们训练和评估了两个机器学习模型,使用LR和CART分析方法。最佳的诊断性能是由CART分类器实现的,其在训练集和评估集中的准确度、精确度和召回率分别为0.792、0.784和0.803。获得的CART模型具有明显的优势,即易于解释,与机器学习或深度学习的其他方法不同。我们使用四个放射组学协变量,通过九个节点和三个深度级别构建了CART模型,以产生一个直接和紧凑的决策树。CART分析选择SVR大于0.383的病变与完全缓解相关。随后,偏度和相关性在提高病变分类率方面发挥了重要作用,高偏度和低相关值有利于完全缓解。
由于这种高分类准确度,我们认为这个CART模型可能代表了一个有价值的工具,用于放射科医生在为肺部病变制定SBRT策略时选择有效的治疗方案。
局限性
尽管结果令人鼓舞,但本研究仍存在一些局限性,需要指出并讨论。
首先,这是一个回顾性研究,患者队列(80个病变)的规模并不大。这是许多定量放射组学研究的一个典型缺点。因此,我们选择了简单的二元分类来定义反应结果(完全缓解与所有其他反应),以便为每个组提供一个合理的样本量。未来,我们的目标是收集更多的病变,以便在提出的二元分类之外更好地分层反应(即完全缓解、部分缓解、稳定疾病和进展性疾病)。
其次,我们的研究仅限于一个机构,这意味着图像采集、靶区定义和临床结果评估可能在不同机构之间存在差异。在靶区定义方面,准确的病变分割对于确保提取特征的可靠性至关重要。因此,为了量化特征的可重复性,我们计算了两名独立医生获得的两个分割集的放射组学特征的符合相关系数(CCC)。非常高的CCC值(平均0.972)是可靠靶区定义的标志。此外,评估RECIST反应的内部和外部观察者不确定性可能导致整体反应的误分类。然而,据很好地报道,与其它部位相比,肺部病变的反应可重复性要高得多。
最后,有限的病变队列不允许在独立的患者数据集上评估模型的性能。为了部分克服这一限制,我们进行了一个可靠的内部验证,采用了五折交叉验证过程。这是一种众所周知的重采样技术,用于评估基于有限数据样本的机器学习模型,即估计模型在训练模型时未使用的数据上进行预测的预期性能。另一方面,必须强调的是,交叉验证无法严格评估回顾性研究中的选择偏差,这可能导致预测性能的过高估计。然而,一项专注于开发放射组学模型以分类恶性肺肿瘤的研究报告称,内部验证的模型(AUC > 0.89)在外部验证中的AUC为0.82。
综上所述,即使需要使用独立数据集的外部验证来确认我们模型的稳健性和普适性,但我们的研究提供了一个可靠的证明,即放射组学分析可能提高预测SBRT治疗反应所需的精确度。


























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








