1.化学势其实就是偏摩尔吉布斯方程,它是偏摩尔量,符合吉布斯杜亥姆方程
上面将要介绍如何由一个组元的活度求得另一个组元的活度 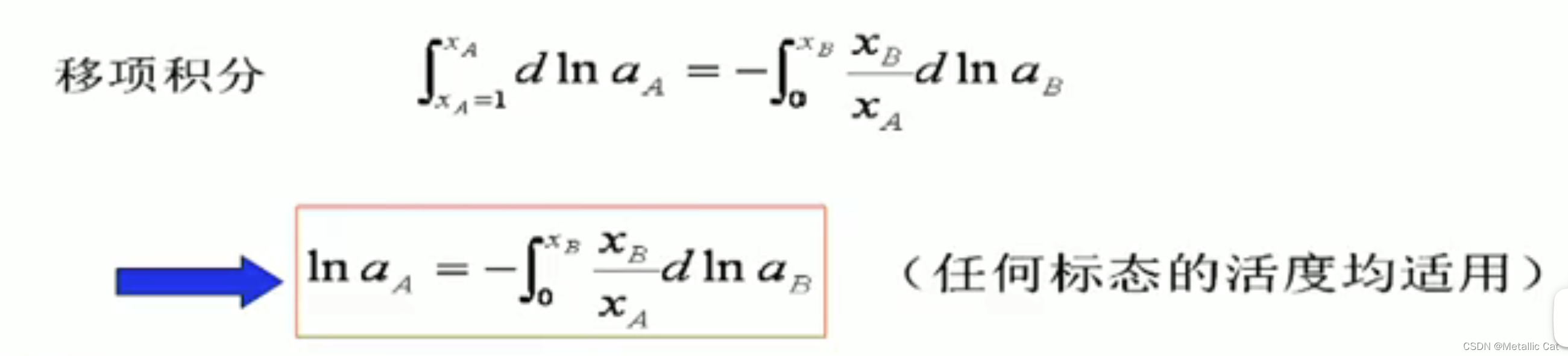
但是上面这种求法存在如下这些缺点: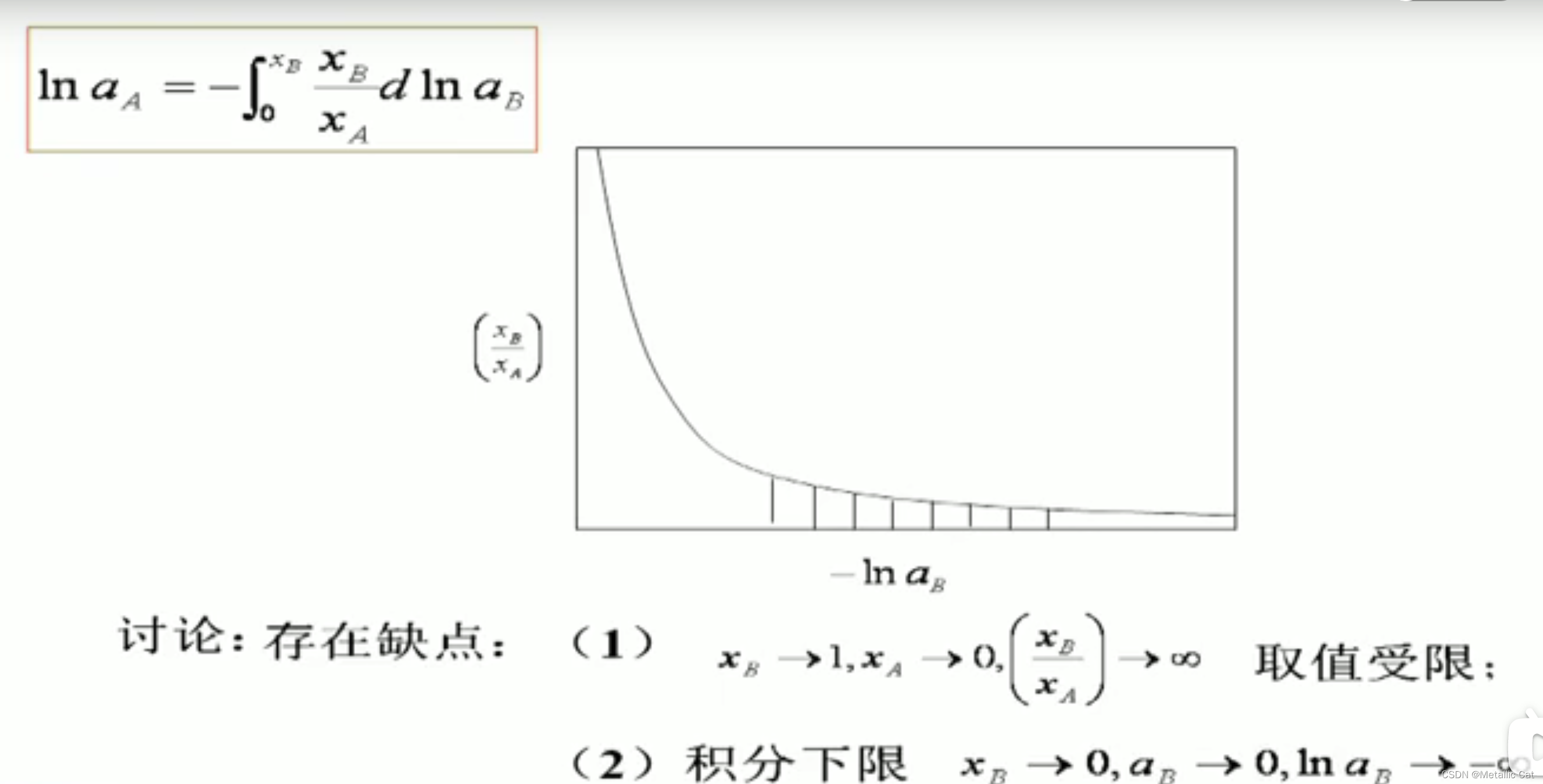
简单来说就是无法确认积分的上限和下限
为了解决上面这个缺陷,我们不妨先从活度系数入手,由一组元的活度系数来求另一组元的活度系数:
最重要的是方框中推理出来的公式
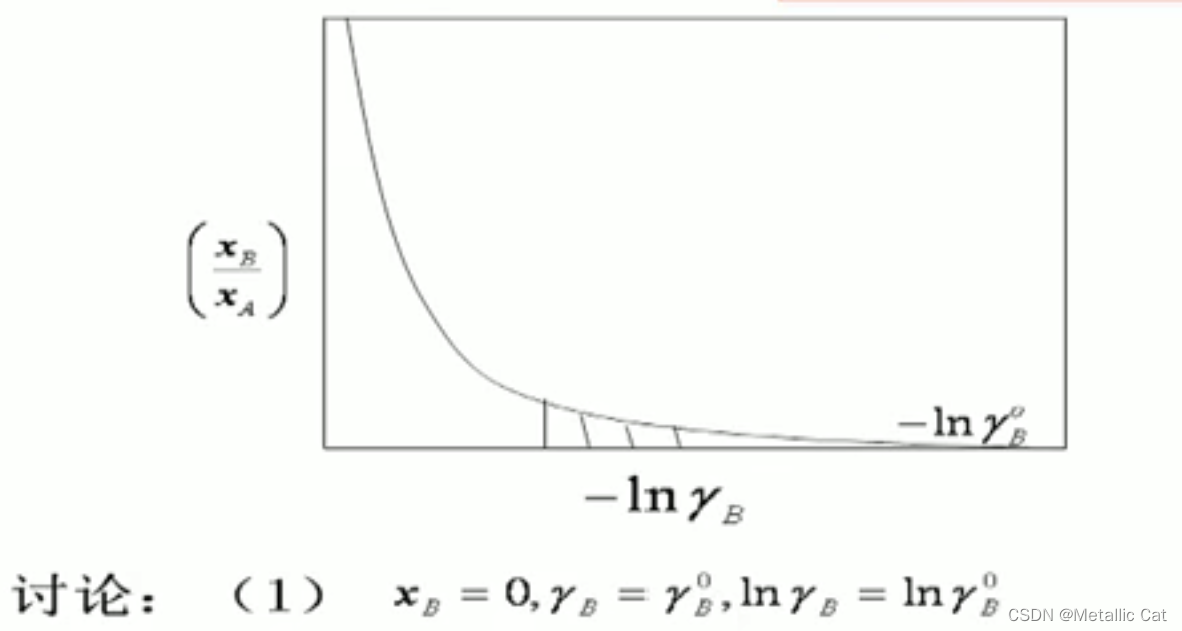
通过求活度系数的方式我们就解决了第一个方法中的一个问题 --- 就是当Xb趋于0的时候,下限无法确认的问题。
在上面这张图中,当Xb趋于0的时候,也即是说此时对于组元B而言,溶液变为了一个极稀溶液,此时符合亨利定律,活度系数等于1,此时有了活度系数和组元摩尔浓度,我们要求的活度也就出来了
但是问题仍然存在那就是积分的上限仍未确认
这第二个问题是采用α函数法来解决的:

从Xa积分到Xa等于1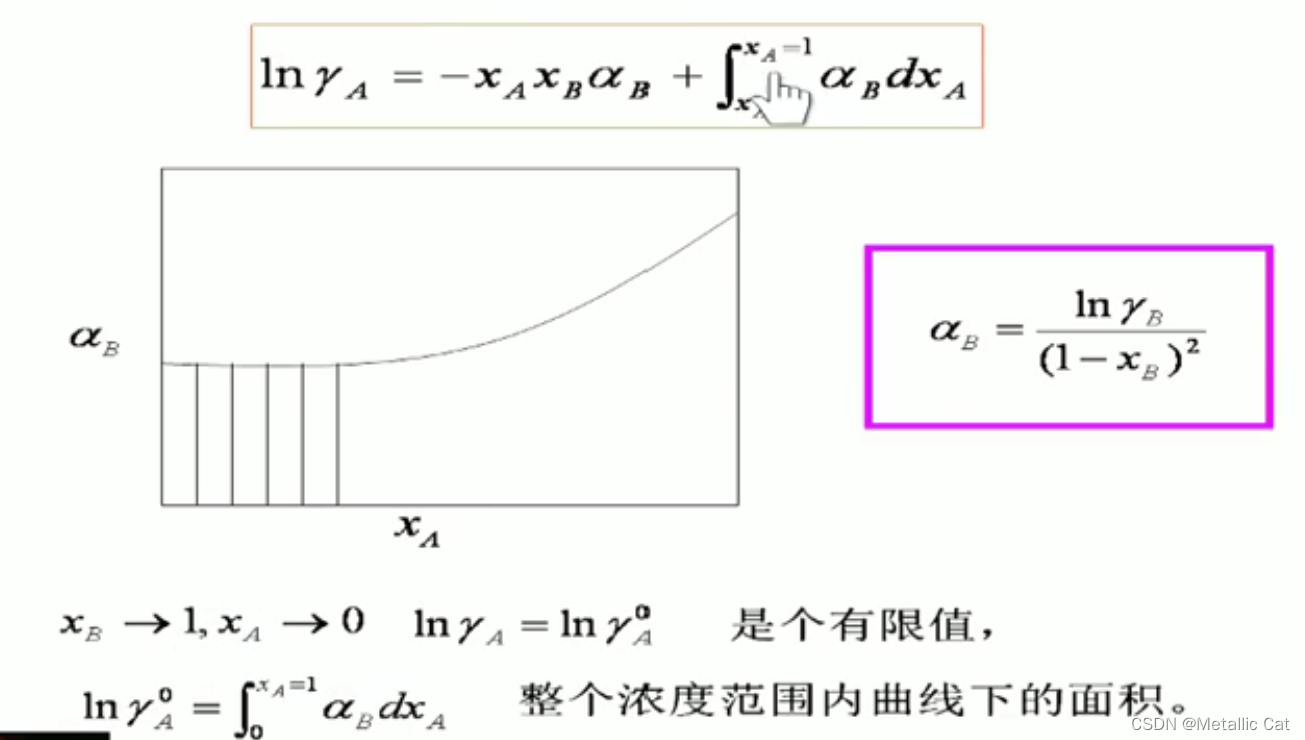
最重要的是α函数法,一次性解决了上限和下限两个问题
恒温恒压下R值一定与组成有关,一定是一个组成的函数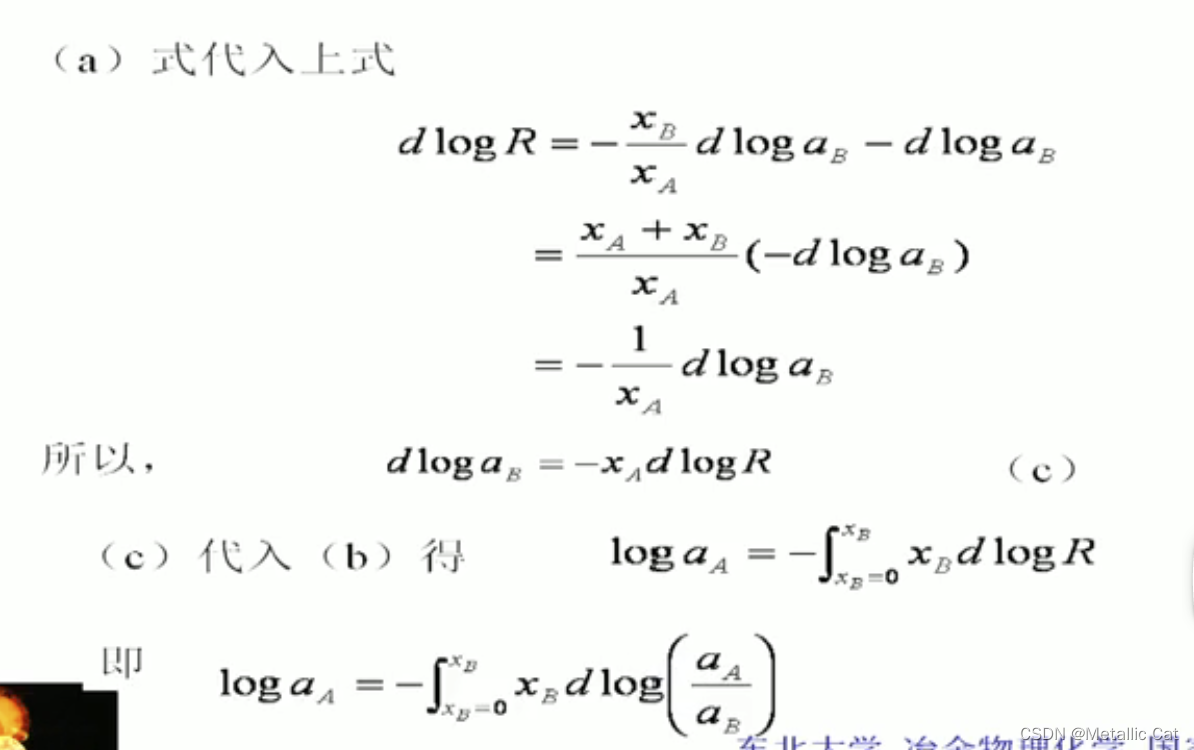
最重要的是下面这两个公式和R表示的是什么 ---
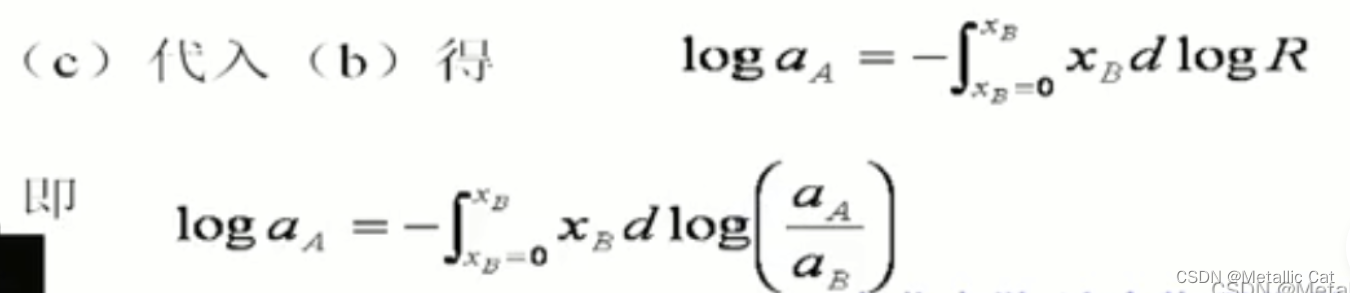
接下来开始介绍的活度的实验测定: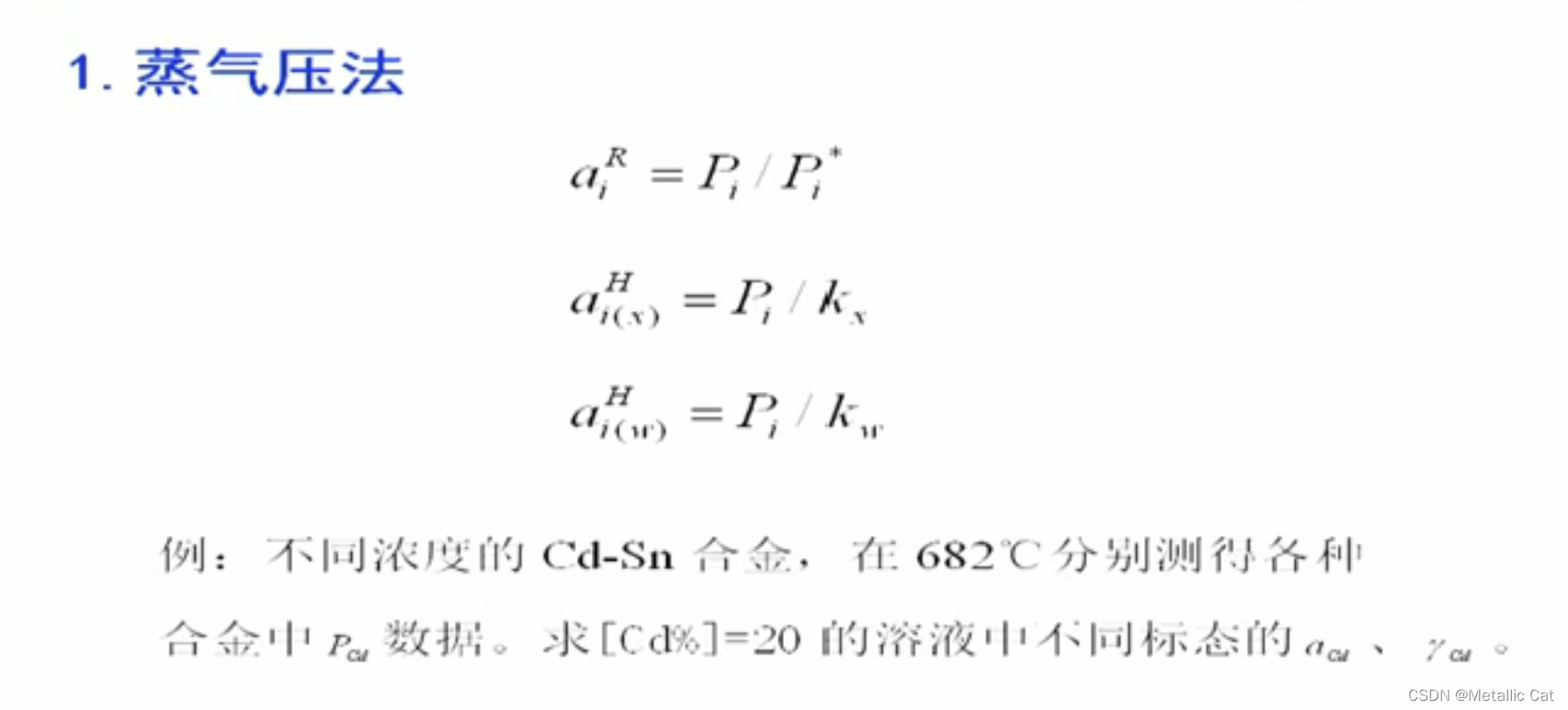
蒸气压法是根据活度的定义来直接获得活度 --- 获得活度的最直接的方法
用蒸汽压法时我们不仅要测出一些相关值,同时还要测出求活度时必不可少的一些常数量
Pi*指的是i为纯物质时的分压 --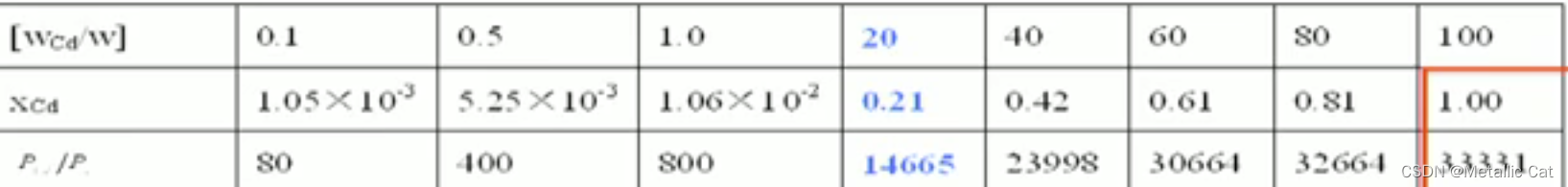
首先找到Xcd等于1 --- 表明是纯物质,然后再找出等于1时对应的分压值,即1下面的那个3.3331,这个值就是我们想要的Pi* 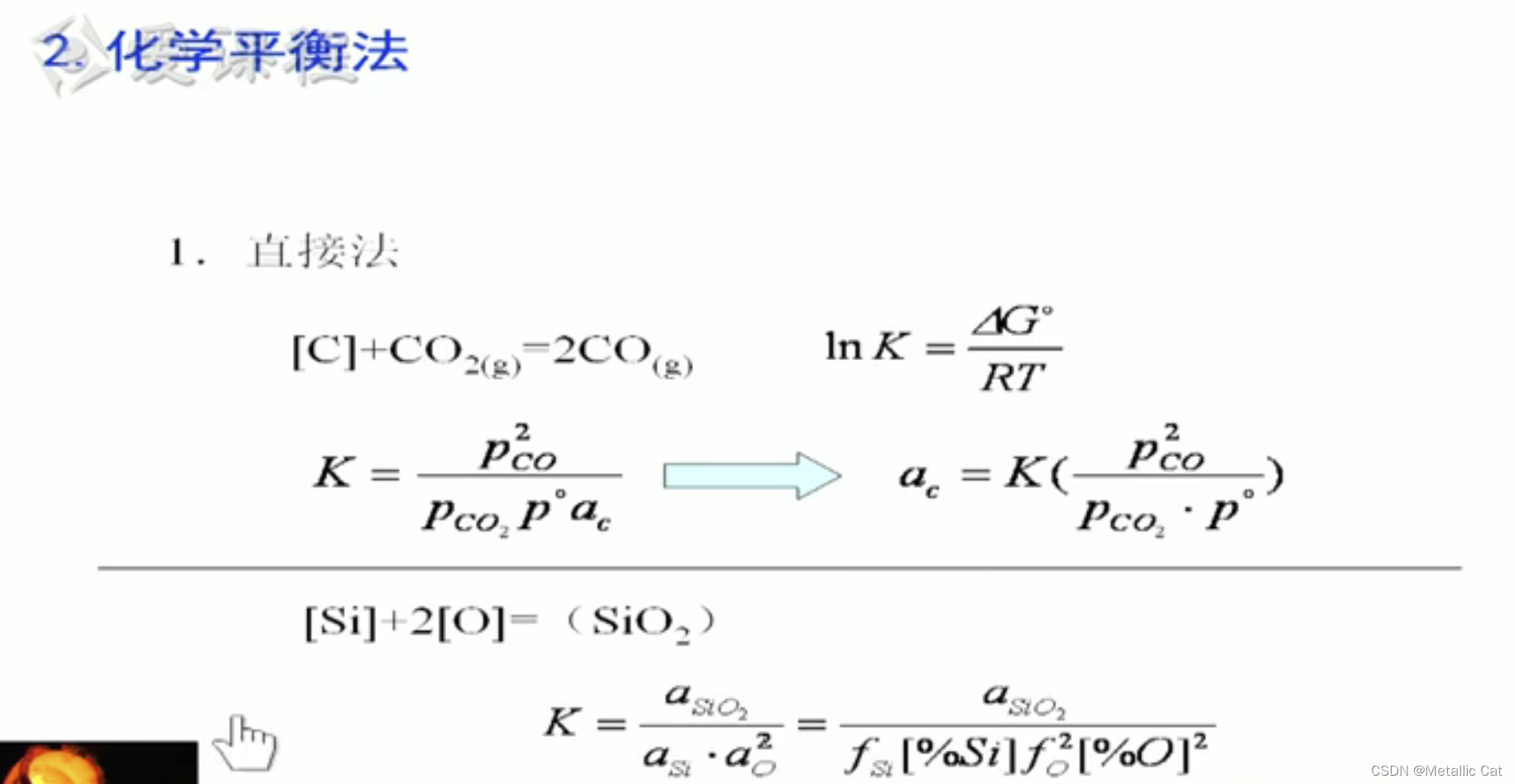

上面这个 【%a】就是a的质量分数表达
使用直接法的前提是:我们要提前知道反应的吊塔G0等于多少,否则用不了

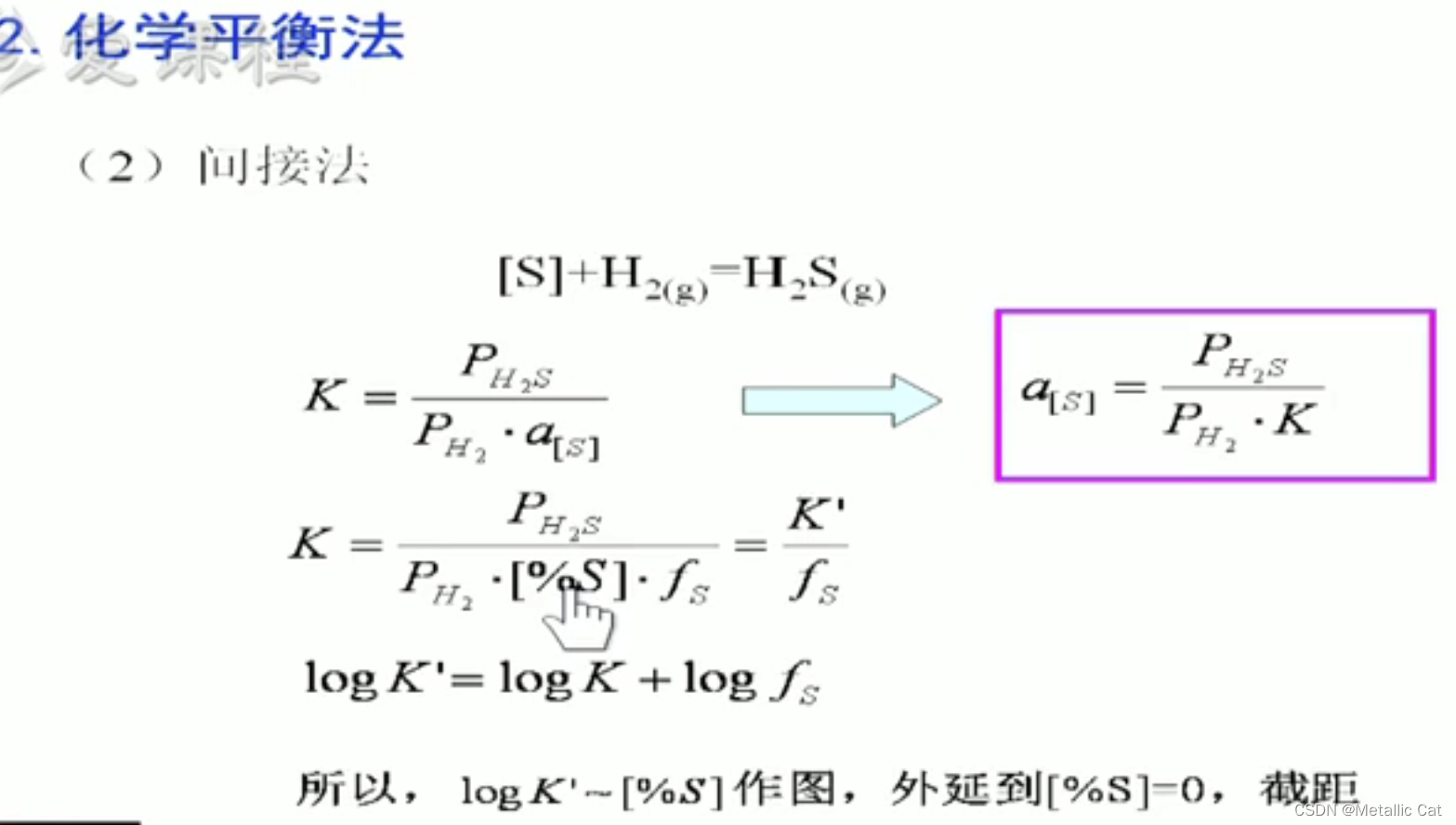
K‘ 是表观平衡常数
exp【a】 --- 表示的是自然底数e的a次方
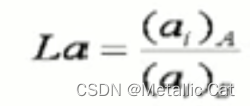
这个分配常数是一个适用于任何浓度下的常数,它的求解方式是先在极稀浓度下求出,然后适用于所有浓度的情况 
通过测量电动势的方式来测得待测液体的活度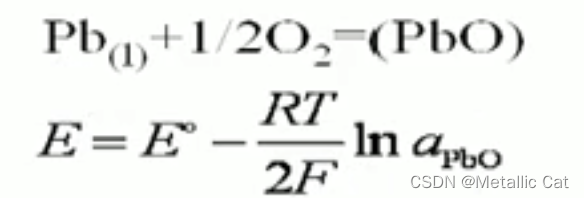
E是电动势,E0是标准电动势,F是法拉第常数 ,2则表示上面那个化学反应得失电子的数
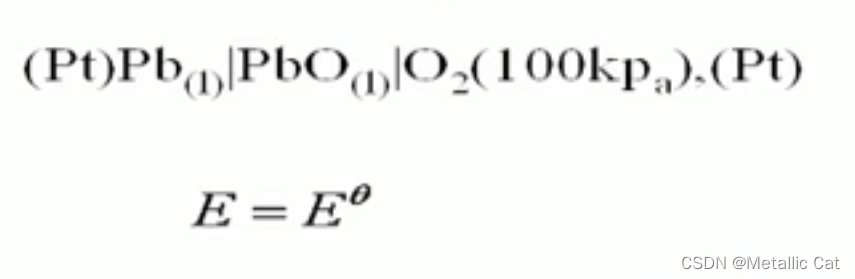
上面这个电池的电动势就是标准电动势
此时有了标准电动势和电动势之后,我们就可以根据公式直接反推活度了





















 2414
2414











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








