绘制脑连接图的神经影像学方法的发展改变了我们对精神疾病、脑刺激的分布效应以及如何最好地利用经颅磁刺激靶向和改善精神症状的理解。与此同时,神经影像学研究表明,像前额叶皮层这样的高阶脑区(代表了精神疾病最常见的脑刺激靶点)在大脑连接方面表现出了一些最高水平的个体差异。这些发现为基于个体特异性脑网络结构的个体化靶点选择提供了理论基础。最近的进展使确定可重复的个体化靶点成为可能,其精度为毫米,采集时间为临床可掌握。这些进展使空间个性化经颅磁刺激靶向的潜在优势得以评估并转化为基础和临床应用。在这篇综述中,我们概述了目标位点个性化的动机、初步支持(主要在抑郁症中)、来自其他脑刺激模式的聚合证据,以及抑郁症和前额叶皮层之外的普遍适用性。最后,我们将详细介绍方法学建议、争议和值得注意的替代方案。总体而言,虽然这一研究领域看起来很有前景,但个性化靶向的价值仍不清楚,使用经过验证的方法学进行专门的大型前瞻性随机临床试验是至关重要的。
经颅磁刺激(TMS)是一种很有前景的治疗神经和精神疾病的方法,但其疗效仍存在差异。对于难治性抑郁症,即使在临床特征相似的患者之间,结局也有差异,缓解率(即症状改善50%)通常为35% ~ 50%。尽管在难治性人群的背景下,这一结果非常令人鼓舞,但这些比率仍有很大的改善空间。治疗结局的差异可能与临床或人口统计学因素相关,但这些关联已被证明是不一致的,并且不能通过改变来改善个体结局。平行的研究试图确定治疗反应的神经生物学底物,以及是否可以通过针对个体差异的个体化治疗来提高临床疗效。近年来,技术进步和新的数据集推动了这一领域的发展,帮助揭示了个体水平的脑网络结构和计算技术的进步,现在为在空间和时间尺度上实现精确的个性化靶向提供了手段。抑郁症作为TMS最常见的临床应用,其研究引领了这一领域的进展,并在其他临床和基础研究应用中进行了转化和探索。回顾性和初步研究的结果很有前景,但仍需要大型前瞻性随机临床试验;该限制和其他限制将在后面的限制、争议和常见问题中讨论。
1. TMS的功能对齐空间定位
抑郁症的传统脑刺激疗法通常采用著名的基于头皮的启发式方法,在左背外侧前额叶皮层(DLPFC)确定一个适合所有人的单位点TMS靶点。其中一个方法确定了DLPFC TMS靶点在运动皮层前方5 ~ 6 cm,但我们发现这经常完全错过DLPFC,导致了Beam F3启发式(Beam F3 heuristic)的发展,它估计额叶F3电极的大致位置。虽然这些方法成本低且实施迅速,但它们导致不同个体的靶向皮质位点存在很大差异(图1A)。这些方法没有考虑神经解剖和脑网络结构的个体差异,可能无意中涉及不同个体的不同功能性脑网络(图1B),这可能导致临床结局的差异。
运动皮层提供了一个有用的类比来说明适当的空间定位的潜在功能意义,在这里,刺激侏儒内不同的运动表征导致相应肌肉的肌肉抽搐。同样,神经调节性TMS对受刺激的肌肉代表的效果最大,并且随着与线圈的距离增加而逐渐减弱(图1C)。此外,不能单纯基于头皮测量来预测运动热点,热点位置存在个体差异,TMS线圈位置的微小偏移会使线圈脱靶,从而不再诱发运动诱发电位。值得注意的是,在个体中,躯体运动区是同质性和空间保守性最高的区域,而最常见的TMS治疗靶点前额叶区域是异质性最高的区域(图1D-F)。这些观点强调了空间定位的基本原理,与个体特定的脑功能结构适当匹配。
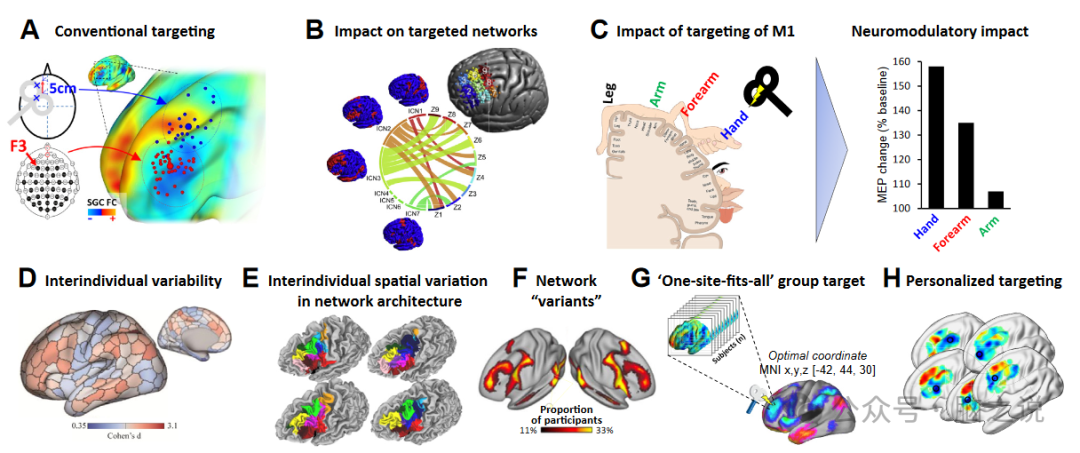
图1 基于脑连接的个性化定位原理
2. 基于脑连接的神经影像靶向证据
随着神经影像学方法的发展,我们对精神疾病的现象学、脑刺激的分布效应以及TMS如何更有效地改善精神症状的理解发生了改变。神经影像学已经清楚地表明,TMS效应的传播远远超出了即刻刺激部位 (图2A),从而调节分布式脑网络(图2B)。与此同时,TMS治疗一系列疾病的结果越来越明显地与刺激部位与疾病相关的下游互联区域和脑回路之间的脑连接有关,如果不是受其支配的话。这方面的大部分工作是在抑郁症领域率先开展的,其中TMS的临床结果似乎与DLPFC TMS靶点与膝下扣带回皮质(SGC)之间的静息态脑功能连接(FC)相关。FC是大脑区域之间相关活动的常用测量方法,当参与者躺在磁共振成像(MRI)扫描仪中时,它很容易被记录下来。已知SGC与异常的情绪处理、悲伤、抑郁严重程度以及对各种抗抑郁治疗的反应有关。DLPFC- SGC连接和TMS结果之间的关联已经在多个独立的临床队列中被报道,并且在不同的临床中心、扫描仪、刺激器和DLPFC靶向方法中似乎相当稳健。这种关系在假TMS和一系列对照部位中不存在。最近的研究表明,或者更确切地说是重申,SGC是分布式抑郁网络的核心组成部分。这一研究方向导致了一系列基于回路的靶向策略(稍后将在《从种子到基于回路的神经调节》中描述)。
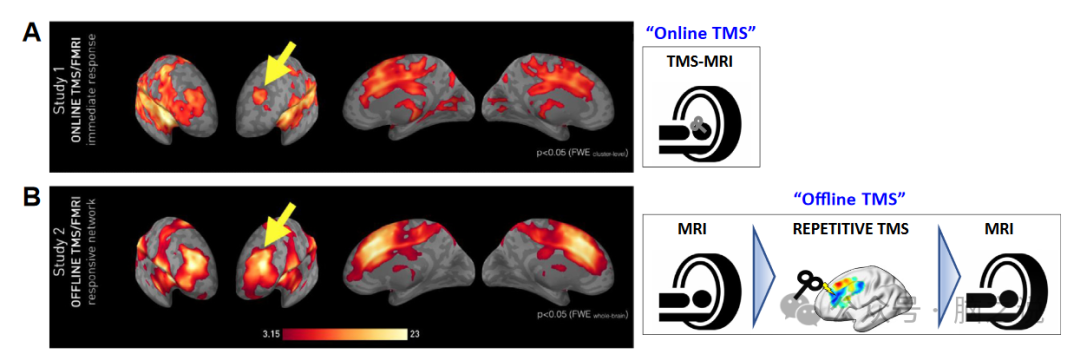
图2 经颅磁刺激(TMS)的效应传播到即时刺激部位以外的空间分布的互联脑区。
3. 基本原理:群体水平与基于个性化连接的目标
基于上述研究,有人提出根据与SGC或相关回路的连接来前瞻性地对齐DLPFC靶点,可能会改善重性抑郁障碍(MDD)的TMS治疗结果。最直接的方法是确定一个适合所有个体的单一位点DLPFC靶点,该靶点对所有个体都有效,通过整个DLPFC的SGC FC的人群平均图定义(图1G)。这种靶向方法的一个潜在缺点与大脑网络结构的个体间差异有关,尤其是在PFC内(图1D-F),这对应于该大脑区域内的进化发展增加。大脑连接可以变化到这样的程度,以至于可以根据他们的连接组“指纹”从大样本中可靠地识别个体。此外,作为精神疾病最常见的脑刺激治疗靶点,PFC等高阶脑区在细胞结构、结构形态、神经功能和连接方面表现出一些最高水平的个体间差异。来自群体平均FC地图的单一坐标可能为一些个体提供有效的靶点,但FC结构的巨大个体间差异可能导致许多其他个体的靶向性不佳。因此,任何将上述发现转化为更好治疗结果的尝试都可能需要将刺激靶点与个体特定的脑网络结构相匹配。关键的是,一些研究使用神经导航将TMS递送到基于组平均SGC-FC或使用纯粹解剖学定义的靶点的单一靶点坐标,与其他传统靶点相比,并没有显示出任何令人信服的治疗效果改善。这些发现可能提示非个体化靶向不足以提高TMS的疗效,尽管靶向方法的直接比较仍有待进行。
4. 为什么要花这么长的时间来测试个性化定位
由于一系列技术和计算方面的挑战,实现个性化靶向的进展受到了阻碍。直到最近,似乎需要90分钟的功能MRI (fMRI)数据来揭示皮质-皮质下关系的功能网络结构的个体差异,相应地,大的扫描时间可能需要确定精确的个性化目标。这是由于与fMRI信号相关的固有噪声,以及需要捕捉足够的大脑活动变异性来可靠地估计FC。然而,MRI采集时间过长降低了临床可行性。初步工作还表明,定义基于连接的DLPFC目标的误差范围是几厘米,这使得传统的计算方法无法有效地实现个性化治疗。
此后的一些进展使确定可重复的个性化目标成为可能,包括更擅长去除非生理噪声的高级预处理策略,以及为个性化目标量身定制的计算管道的开发。现在,我们可以在15 ~ 20分钟的临床可控静息态扫描时间内,以毫米精度确定稳健且可重复的个性化DLPFC靶点(图S1)。基于Fox等人的重要工作,我们在人类连接组计划数据集的1000个个体中验证了我们为特定个体识别的位点在第二天或一年间隔的重复扫描之间的差异中位数为2毫米——这相当于一个脑体素的长度。这些方法学上的进步有助于通过标准静息态功能磁共振成像(resting-state fMRI)方案在临床环境中实现个体化靶向治疗。有趣的是,人类连接组计划的家族数据表明,同卵双胞胎的目标比异卵双胞胎、非双胞胎兄弟姐妹和无关个体更相似,这表明这些目标是稳定的,至少部分受遗传控制。
与此同时,用于个性化靶向的计算策略也被其他不同的研究团队开发或扩展,包括基于功能分区的靶向和基于TMS电场的微调靶向。开发可靠的方法并非易事,而且至关重要的是要证明个性化靶点在特定个体的不同扫描中是可重现的,并且个性化靶点的个体间空间差异是明显的,这表明在追求靶点再现性的过程中,脑网络结构的个体差异并未被侵蚀(图3)。这暗示了可靠性和个性化之间的重要权衡:通过限制个性化目标在个体之间的差异程度(例如,所有坐标必须位于固定坐标的一定半径内),个性化目标可以变得更可靠;然而,过度限制可行搜索空间或放松其他参数(如簇阈值或探照灯球直径)不可避免地导致所有个体收敛到一个共同的目标(图3,面板3)。
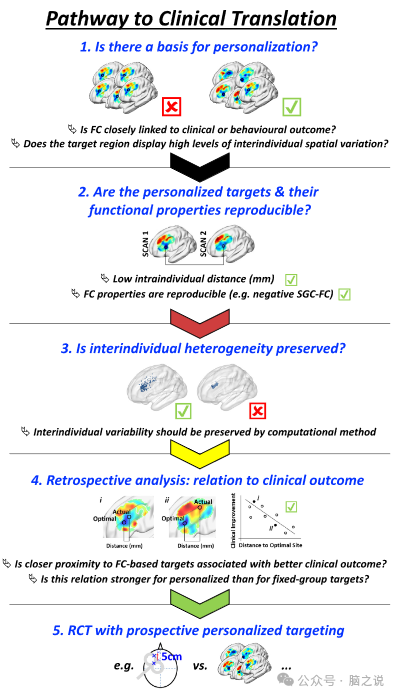
图3 临床转化的理想路径,指出了采用目标站点个性化的重要方面。
5. 个性化脑刺激的初步回顾性证据
在这方面的第一项研究中,我们采用了我们的计算方法来回顾性探索现有数据是否提供了个性化靶向治疗潜在临床价值的证据。我们在一组抑郁症患者中进行了这项分析,这些患者之前接受了一疗程的常规(F3)TMS靶向治疗。已知每个个体的实际Beam F3 TMS靶点坐标。每个患者在治疗前都接受了MRI检查,因此我们也能够回顾性地计算出每个个体基于连接的最佳个性化TMS靶点。数据表明,对于那些偶然接受治疗的患者,TMS的抗抑郁疗效显著地更接近他们最佳的基于个性化连接的DLPFC靶点。最优性是指与SGC环路表现出最强FC反相关的位点(种子图)。重要的是,当我们转而计算与任何传统的单部位适用于所有人群的靶点的接近程度时,TMS的临床结局没有关系。这一发现随后在其他几个队列中得到了验证(图4)。这些研究的效应量范围为R = 0.47 ~ R = 0.6(平均R = 0.55)。这些回顾性研究的一个局限性是,数据仅代表与治疗应答相关的数据。

图4 基于个性化连接的靶向的回顾性证据
6. 初步前瞻性证据
基于脑连接的最佳刺激位点的前瞻性定位和靶向提供了一个机会,可以直接将之前的基础研究转化为更好的临床结果,量化个性化靶向的潜在临床和经济效益,并检验脑连接和治疗反应之间的因果关系。目前有初步的前瞻性证据表明,基于连接的个性化靶向治疗可能通过侵入性和非侵入性脑刺激方式提高临床结局。
采用个性化TMS靶向治疗抑郁症的前瞻性研究在方法上有所不同,但重要的是,这些研究的应答率始终高于传统靶向治疗的预期。这似乎不太可能是与所涉及的额外技术(即MRI和神经导航TMS)相关的安慰剂效应,因为其他使用类似高科技方法的研究,但采用了单一的“一位点适合所有”而非个性化靶点,并没有观察到治疗结局的任何额外改善。然而,我们需要进行直接比较。
这些研究的局限性包括队列规模小、未采用盲法以及仅在少数研究中纳入了对照条件。此外,虽然临床结果可能密切依赖于所采用的个体化方法的准确性和可重复性,但迄今为止,没有一项针对个体化TMS靶点的前瞻性研究证明了其靶点的可重复性。考虑到个体化靶向治疗的成本和不便,有必要开展专门的、具有足够功效的前瞻性随机双盲对照试验,以确定这些因素是否充分证明了临床和经济收益。这一成本可以通过我们团队和其他人开发的更快、更高效的TMS方案来部分抵消。这些研究的数据还可用于指导和完善目标策略,或开发替代和更简单的方法。
7. 来自侵入性脑刺激的聚合证据
回顾性研究表明,脑深部电刺激(DBS)的临床结果与刺激电极的连接特征密切相关,并且可以从刺激电极的连接特征中预测。然而,重要的是要认识到,DBS是一种相当多的焦点刺激方法,可以实现毫米精度的瞄准,而TMS可能会从线圈焦点扩展到一厘米或更多。DBS研究还产生了其他有趣的见解,包括强迫症的多个不同的DBS靶点可能通过调节相同的大脑网络来缓解症状。基于个体特异性连接特征的前瞻性个性化DBS电极植入治疗抑郁症的反应率为81%,而先前发表的基于解剖的靶向治疗的反应率为41%。最近的研究也表明,通过个性化的靶点选择,强迫症的临床改善更快,缓解率达到80%。这些数据仍是初步的,尚未开展大型前瞻性试验。
8. 普适性—超越MDD和PFC
一个关键问题是,个性化TMS靶向的潜在益处是否可以推广到PFS之外的其他临床和行为学脑刺激应用。新兴研究表明,个性化TMS的潜在优势是1)多日顶叶皮层TMS在增强联想记忆表现方面,与皮质-海马记忆网络的靶向一致;2)左侧DLPFC的渴求经颅磁刺激过程,与独立衍生的渴求回路对齐;3)孤独症谱系障碍,左侧DLPFC经颅磁刺激与杏仁核连接一致;(4)卒中后失语,左侧或右侧额上回TMS与语言环路一致。综上所述,这些发现表明,基于个性化连接的靶向技术可能在多个临床TMS应用和脑区中具有优势。
9. 从种子到基于回路的神经调节
精神症状的定位和调节已逐渐从主要关注单个脑区转向关注分布式脑网络和环路疾病。这一基于网络的框架得到了几行证据的支持,最显著的发现是,分布在同一脑网络内不同部位的病变可以引发类似的症状,这一发现在包括抑郁症在内的一系列神经精神疾病中得到了证实。因此,这些病变的连接性可用于描述与症状表达有因果关系的共同脑网络。在抑郁症的病例中,这些数据有助于描绘出一个汇聚的脑回路,由此连接到该回路的空间发散病灶与症状表达相关,使用DBS或TMS成功靶向这一回路与治疗反应相关。
有趣的是,当我们从抑郁症文献中包含过去20年任务型影像学异常的独立数据导出脑回路时,该数据与上述汇聚脑回路非常相似(图5A)。值得注意的是,该回路的统计学阈值显示了共同的TMS和DBS靶点(图5B)。在几个独立衍生的压低回路中有明显的(统计学显著的)收敛(图5A)。图6说明了如何不仅基于与单个种子区域的连接,而且基于与分布式脑回路的连接来导出个性化或组水平的脑刺激目标。因此,我们能够证明,在一个独立的现有数据集中,更接近基于该回路的个性化靶点与更好的TMS治疗结果相关。换句话说,更有效地靶向这一抑郁环路与更好的治疗结果相关。
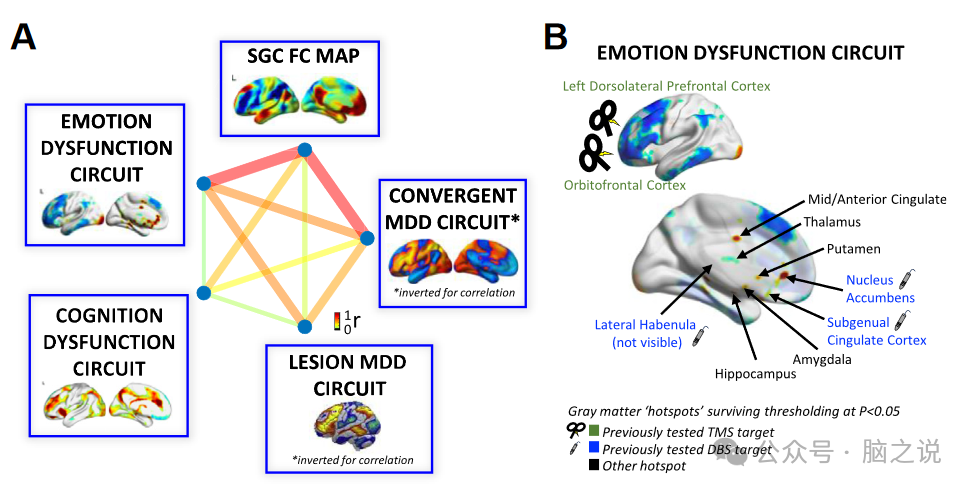
图5 (A)这张示意图显示了来自独立数据集和方法的跨抑郁回路的显著收敛。(B)情绪功能障碍环路的统计阈值揭示了热点,其中许多与已在临床研究中测试过的TMS和DBS靶点相一致。
随着抑郁症中汇聚回路证据的积累,它为SGC种子图的实现带来了一个全新的视角(图6,iii)。SGC种子图是SGC FC的规范全脑图,最初被提出作为一种巧妙的方法来增加SGC时间序列的信噪比。有趣的是,我们最近证明了SGC种子图非常接近上述的抑制回路模型(图5)。这意味着之前通过计算实现的SGC FC图来推导DLPFC TMS靶点无意中提供了一种靶向抑制环路而不是单独靶向SGC的方法。
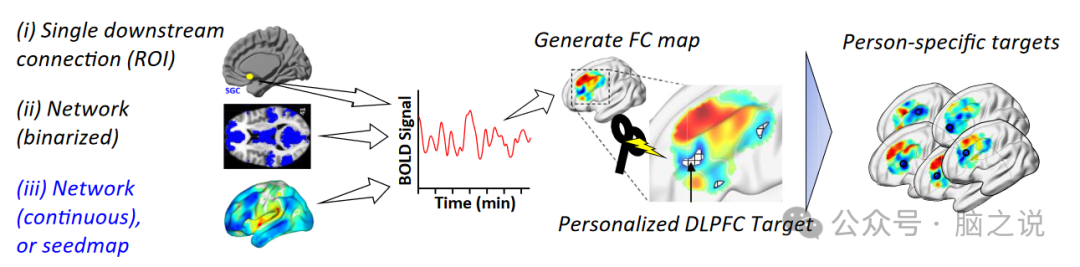
图6 个体化经颅磁刺激靶点的计算
10. 基于症状群的个性化神经调控
抑郁症是一种高度异质性的综合征,两名患者可以有相同的诊断,但没有共同的症状。理想情况下,治疗可针对每例患者的特定症状或症状群量身定制。为此,Siddiqi等人勾画了介导焦虑和焦虑躯体症状的回路,从而能够分别针对这些症状。我们对抑郁症的研究已经描绘出了与认知、情绪、积极和消极情绪异常相关的回路。已经明确了其他环路,包括烦躁不安、快感缺失、反刍思维和认知控制等核心症状。这些回路提供了更有效地解决所关注症状的潜在机会,但这种方法是否有效,或者这些回路是否可以跨诊断仍有待确定。只需将感兴趣的靶点或环路代入之前描述的计算方法(图3和6),即可在单个体或组水平得出相关靶点(图3和图6)。在为帕金森病选择DBS靶点时,考虑主要症状和合并症(例如神经认知障碍、抑郁病史),基于症状的类似靶向方法已经成为常规方法。临床实施可能包括先后靶向多个环路或靶向环路重叠部位。当有合并症时,TMS的临床结局(至少对于抑郁症)往往不那么积极,这表明仍有更多的复杂性需要解决。下一节将详细介绍如何修改这种方法以适应其他症状和障碍。
11. 如何将该方法应用于其他疾病和应用
上述研究中概述的靶向方法可用于为其他疾病、症状或基础研究应用生成个性化或群体水平的目标,只需将感兴趣的目标或回路代入现有的计算方法(图3和5)。可通过多种方式推导出与临床(或行为表现)结局相关的回路。简而言之,这些可以来自体素相关图,即r图,将DBS、TMS或病变的位置与临床(或行为)结果联系起来;任务型(或其他)神经影像数据;或潜在的荟萃分析神经影像数据库(例如Neurosynth [https://neurosynth.org/])。理想情况下,这些环路应在多个独立数据源之间进行交叉验证(图5A)。与感兴趣环路连接最优的皮质刺激靶点可以使用集群、探照灯或替代靶向算法自动定位在个体或组水平。新的管道在未来也可能被证明是更好的,并且可以很容易地使用回顾性方法进行比较。
12. 实际考虑和建议
为了计算环路衍生的个性化靶点,我们的数据提示,15 ~ 20分钟的fMRI数据就足够了(图S1)。随着扫描时间的减少,精度和可靠性变得越来越不确定,这可能会排除早期研究中收集的数据用于确定精确的个性化目标的效用。使用多回波平面成像序列可以进一步缩短扫描时间,从而提高皮层下区域的数据质量和信噪比。这一讨论在其他地方进行。
13. 局限性、争议和常见问题
如前所述,现在可以计算稳健的个性化目标,这些目标次日甚至1年后仅变化2 mm(图S1)。这种毫米级的再现性并不意味着这代表了TMS本身的空间精度或定位功能离散区域所需的空间精度。个性化定位的目的仅仅是可靠地为给定的个体确定最佳patch的位置,然后将TMS发送到该区域(图7)。最大限度地减少计算管道中的误差是有价值的,因为在稍后的程序中,如神经导航和手持定位可能会引入误差。与此相关,值得注意的是,通常描述的电场模型的空间范围随着输入参数的变化而变化。实验研究表明,线圈位置的偏移0.5 cm具有功能显著性,人类运动皮层的TMS同样表明,偏移0.5 ~ 1 cm具有功能显著性(如图1C),而TMS激活的表面积估计在1.5 ~ 2 cm2范围内,空间分辨率为0.5 ~ 2 cm。
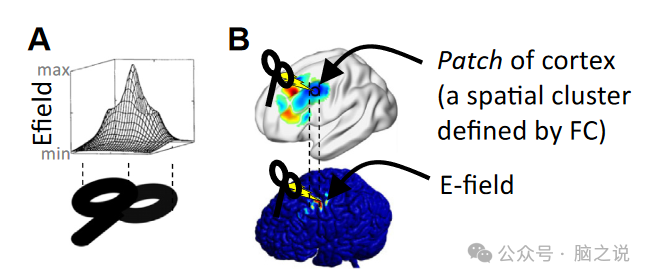
图7 个体化靶向和经颅磁刺激空间精度。
获得高质量fMRI可能会限制fMRI引导的靶向治疗在临床的广泛推广。神经导航设备也很昂贵。规避神经导航费用的潜在方法正在开发中,包括一种将蒙特利尔神经研究所(Montreal Neurological Institute)坐标转换为头皮测量值的基于网络的工具(https://transcranial-brain-atlas.org/mni2cpc/)。改进的fMRI采集序列和技术,以及执行目标个性化的全自动化软件平台,将缓解这些挑战。这些将在另一份出版物中加以阐述。
虽然SGC-DLPFC FC和治疗结果之间的关系已在一系列研究中得到验证,但一个数据集的效应量在R = 0.16 (p = .006)时要低得多。这种情况的潜在原因值得考虑,特别是可用的样本(N = w300)比以前可用的样本大得多。首先,需要注意的是,来自该数据集的临床方案使用了组平均Fox坐标;换句话说,治疗中使用的刺激靶点已经根据SGC FC定义。这可能减少了检测SGC FC和治疗反应之间关系所需的统计学差异。其次,这个数据集的体素尺寸相当大(5 mm)。典型的2毫米的体素尺寸相当于8 mm3 /体素,而5毫米的体素尺寸相当于125 mm3 /体素。空间分辨率的降低可能会影响连通性计算,并影响精确定位最佳坐标的能力。作者提出,较小的(即之前的)样本可能有更大的效应量方差。虽然这在原则上是正确的,但对于之前研究SGC FC和治疗结局之间的关系,或者那些研究个体化靶点和治疗应答之间的关系,这似乎不是问题,每项研究都报告了在0.47 ~ 0.6范围内的可比相关系数(如图4C)。作者还提出,呼吸异常可能影响某些个体的整体信号,并驱动DLPFC-SGC FC与治疗反应之间的关系。这很奇怪,因为1)在这个数据集的扫描过程中没有记录呼吸,这使得这一结果很有推测性;2)这些伪影通常在预处理过程中被回归出来;3) DLPFC-SGC FC之间的关系先前被证明在刺激位点上具有空间特异性,这意味着它不是整体信号波动的伴随现象。上述因素在原文章中没有讨论,值得考虑,但目前尚不清楚它们是否促成了这篇其他方面很强的文章的结果。我们的团队和合作者同时对该数据集进行了调查,同样没有发现更好的临床结局和接近环路衍生的个性化目标之间的关系。3d数据集中出现这些差异的原因最终仍不清楚。尽管前一项研究的效应量较弱,但DLPFC-SGC FC与治疗结果之间的关系是显著的,并且支持基于连接的靶向治疗的证据似乎具有很好的普遍性。然而,这项研究提出了不确定性,并强调了大型前瞻性随机对照试验的必要性,使用回顾性验证的方法,以明确个性化靶向是否值得,并量化其临床和经济价值。
14. 显著替代基于FC的个性化目标定位
FC并不是唯一可以用来指导TMS靶向的指标。目标也可以来自基于任务的激活,并且与功能相关区域的连接隐含在这种方法中。然而,与任务表现相关的区域可能是有益的、代偿性的、抑制性的或仅间接参与给定的任务。重复的TMS是否会增强或破坏(例如虚拟病变)任务相关活动至关重要,但很难事先确定。应考虑到患者和健康人之间的组间差异导致的TMS靶点可能无意中破坏患者有益的代偿功能活动。
还可以基于结构连接(SC)来定义靶点,SC描述了区域间白质的连接。DBS的临床结果与刺激靶点的SC和FC广泛相关。然而,对于DBS来说,SC是一个明显的指标,因为电极通常直接植入白质束。相比之下,TMS电场主要扩展到浅层灰质,这为关注神经元(灰质)集群之间的FC提供了理论基础。SC不太擅长追踪多突触通路,例如介导DLPFC和SGC之间通信的通路。然而,整合SC和FC信息或使用基于结构连接的多突触通信措施可能提供克服这些问题的手段。
另一个有趣的测量方法是大脑可控性,在这种情况下,它可以用于确定哪个目标最有可能引导大脑进入一个不同的、可能更规范或更健康的大脑状态。广义而言,这种方法假设,高度连接的中枢区域可以更有效地将大脑转移到更容易到达的状态,而弱连接的区域可以在将大脑转移到难以到达的状态方面有用。个性化模型已经被提出来推进这一方法;然而,在数学基础和可控性的适用性方面也产生了争议。而不是个性化的刺激靶点,另一种选择是使用一个空间特异性较低的线圈来刺激更宽的DLPFC。理想情况下,大多数或所有个体的最佳位置应该在受刺激区域的范围内。这种方法具有降低成本、增加可行性和可及性的优点。然而,这种霰弹枪瞄准方法的潜在缺点是,多个焦点的刺激可能会潜在地导致有害或意想不到的影响。例如,刺激多个与SGC既相关又不相关的DLPFC位点,可能导致刺激效应相互干扰。奇怪的是,最近的研究表明DLPFC与SGC的正连接位点也可能与抑郁症患者的正TMS结果相关;最简单的解释可能是,任何与SGC及其环路的连接(通路)都是有益的,尽管这需要进一步研究。与此相关,最近的一项研究表明,使用h线圈的加速方案具有较高的应答率和缓解率,h线圈比8字形线圈刺激的区域更大、更深。这些结果提示,局灶性较小的线圈可以提供个体化靶向治疗的替代方案,但本研究未确定缓解和缓解标准,因此比较不太清楚。对于更常见的8字线圈TMS设置,我们的印象是,个性化靶向和加速方案都可以独立(或协同)改善治疗结果。
还需要对DLPFC以外的目标进行更广泛的探索。这些区域可能不太容易发生个体间的差异,并且更受空间限制,可能避免了对个性化靶向的需求。例子包括颞顶交界、顶下小叶和眶额皮质,它们具有潜在的相关连接。
另一种替代方案是神经心脏引导的DLPFC TMS,该TMS是个体化的,可诱导心率的急性变化。据推测,这种心率的变化表明,TMS靶点连接到额叶迷走神经脑网络,该网络与上述环路有一些相似之处。临床疗效的研究正在进行中。
15. 基于时间脑动力学的个性化
在本文中,我们重点讨论了TMS定位的空间个性化,以与个人特定的网络架构相匹配。然而,很明显,神经功能是动态的,并且时间特征可能在个体之间存在差异。我们的目标是在其他地方解决这些问题。与合作者一起,我们开发了第一个时间个性化TMS方案,首次提出了相位依赖性可塑性的概念,并开发了一个版本的theta burst刺激,以模拟个体的theta耦合模式。相关的研究已经指向调整TMS(或DBS)的刺激频率,以匹配内源性振荡或提供与脑电图振荡相匹配的脉冲相位。内源性振荡的频率具有一定的动态性,这可能会影响个性化频率匹配的价值。无论如何,这为确定最简单(即最可翻译)但最具临床疗效的TMS治疗方案提供了补充途径。
16. 结论
近年来,脑回路的个性化定位迅速上升到TMS研究的前沿。越来越多的证据初步支持该方法适用于不同的脑刺激模式以及不同的精神和神经疾病。然而,该领域的大多数研究仍然是回顾性的,对于抑郁症,迫切需要采用经过仔细验证的个性化方法进行随机临床试验,以评估其临床和经济价值。
参考文献:Personalized and Circuit-Based Transcranial Magnetic Stimulation: Evidence, Controversies,and Opportunities.
























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








