
长期以来,全球基因研究严重偏向欧洲人群,导致原住民群体在疾病诊断、风险预测和治疗中面临巨大不平等。格陵兰因纽特人作为北极原住民的代表,其独特的遗传历史和生活方式,使得他们的基因图谱长期处于科学研究的“盲区”。
关键问题:
-
人口瓶颈:约1000年前,因纽特祖先从西伯利亚迁入格陵兰,经历了严酷的人口收缩(仅约300人),基因多样性大幅减少。
-
饮食与适应:高脂肪、高蛋白的传统饮食,可能驱动了基因的自然选择(如与脂肪代谢相关的CPT1A和FADS2基因)。
-
医疗困境:缺乏本地基因数据,导致临床筛查困难,欧洲模型预测效果差,误诊风险高。
【重磅发现】北极基因的“高影响力变异”
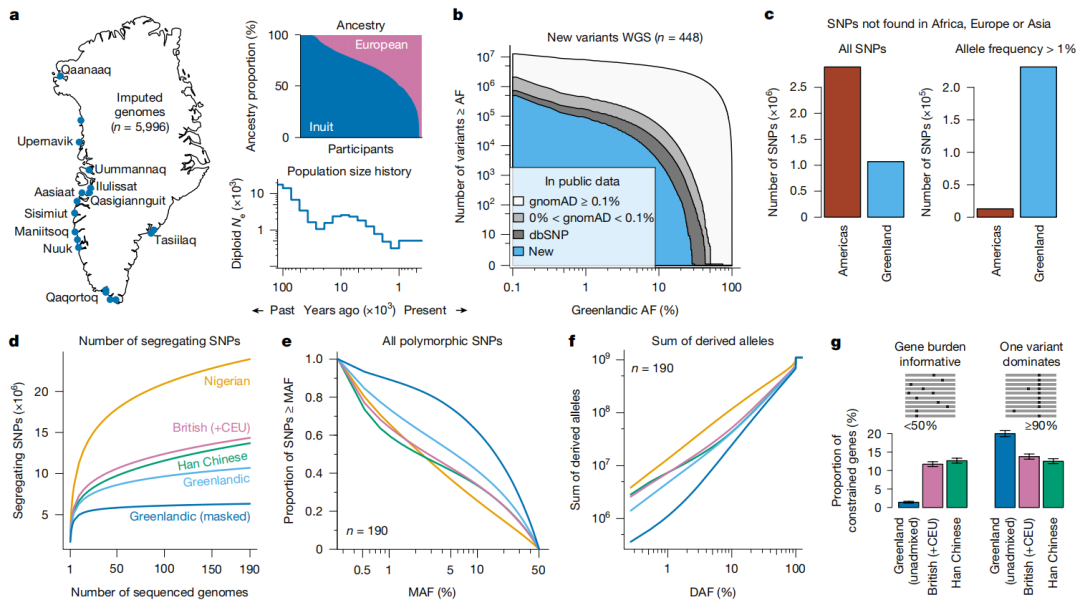
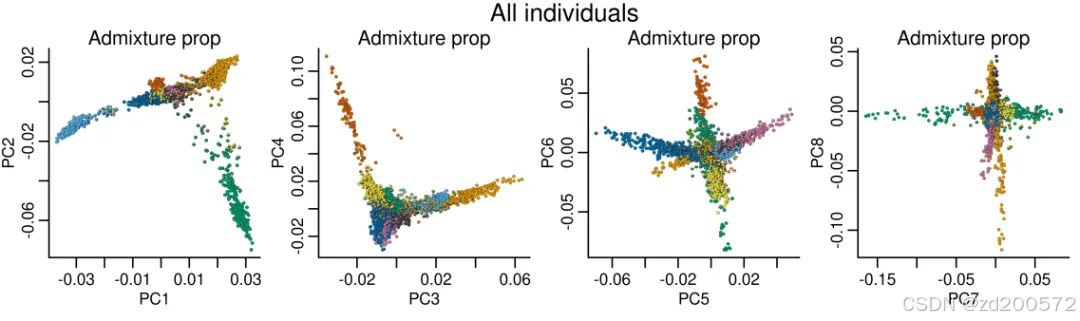
图 遗传结构比较
1. 基因变异的“北极特色”
通过分析5996名格陵兰人的全基因组数据,研究发现:
-
更少但更常见的变异:74%的变异属于“常见型”(欧洲人群仅37-43%),且许多是北极特有。
-
代谢疾病的“关键钥匙”:发现16个与代谢特征强相关的基因位点(如LDLR、TBC1D4),其中8个为北极特有,对糖尿病、肥胖等疾病影响显著。
-
自然选择的痕迹:部分基因(如CPT1A)因适应高脂饮食被正向选择,解释了变异高频存在的原因。
-
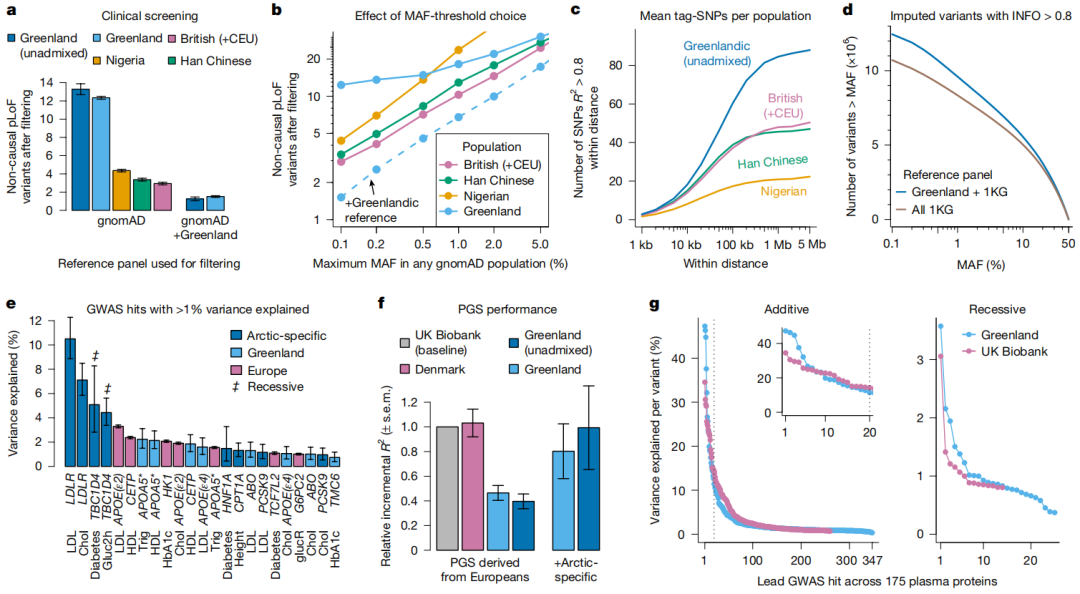
图 基因结构对疾病图谱的影响
2. 医疗应用的突破
-
筛查效率提升:加入本地基因数据后,非致病候选变异减少6倍,误诊风险大幅降低。
-
风险预测“逆袭”:欧洲多基因评分在格陵兰人中的准确度仅为欧洲的一半,但加入北极变异后,预测效果追平甚至反超!
-
隐性疾病的未来曙光:随着人口流动增加,某些隐性遗传病(如ATP8B1相关的胆汁淤积症)发病率或自然下降。
-
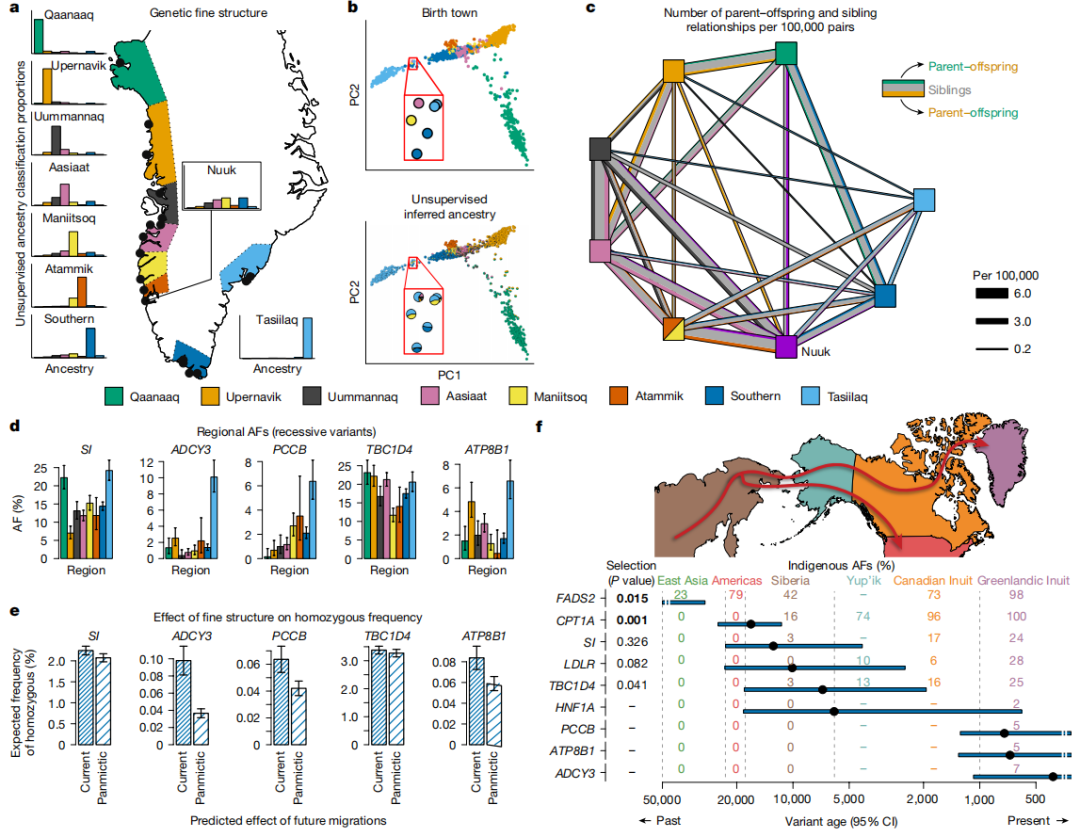
图 遗传精细结构
【基因结构的“北极密码”】
1. 历史的“基因孤岛”
格陵兰不同地区因纽特人存在显著遗传分化,区域间历史迁徙极少。例如:
-
东格陵兰(Tasiilaq)人群基因高度单一,而首都努克(Nuuk)呈现多元混合。
-
这种分化解释了疾病分布差异(如东格陵兰某隐性病高发)。
2. 现代流动的“基因融合”
近几十年城镇化加速,区域间基因交流增加:
-
26%的参与者出生地与现居地不同,努克成为“基因枢纽”。
-
未来人口趋于融合,隐性致病基因携带率或降低,但糖尿病等复杂疾病仍需关注。
-
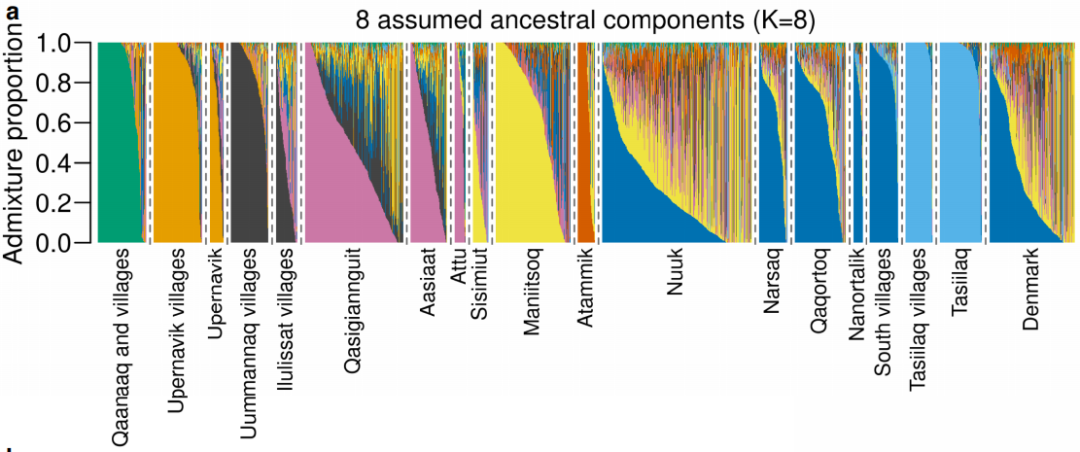
【科学意义】改写医疗公平的北极样本
这项研究不仅是基因科学的突破,更是一场医疗公平的实践:
-
填补北极基因空白:首次系统性揭示因纽特人遗传结构,为北极人群疾病研究提供“导航图”。
-
精准医疗新范式:证明本地化基因数据对诊断、预测和治疗的不可替代性。
-
全球启示:呼吁将更多原住民纳入基因研究,打破“欧洲中心”的医疗不平等。
【未来展望】从基因到行动
-
临床落地:北极变异已用于糖尿病和先天性糖酶缺乏症的筛查,未来或拓展至更多疾病。
-
政策推动:建立北极基因数据库,支持个性化医疗和公共卫生决策。
-
科学伦理:研究全程与格陵兰社区合作,尊重原住民权益,确保成果回馈本土。
结语
格陵兰的冰雪之下,不仅藏着气候变迁的密码,更蕴藏着人类适应极端环境的基因智慧。这项研究如同一盏灯,照亮了北极健康之谜,也为全球医疗公平开辟了新路径——唯有包容多样性的科学,才能真正守护全人类的健康。❄️🧬
























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








