
临床数据管理(Clinical data management,CDM)是临床研究中的一个关键过程,涉及按照监管标准收集、清理和管理受试者数据。CDM的主要目标是从临床试验中生成高质量、可靠且统计上有效的数据。其实,数据管理从逻辑的角度来讲,就是确保数字研究数据长期可查找、可访问、可互操作和可重复使用的所有活动,包括数据管理、归档以及第三方的再利用。关于数据管理的精确定义及其与数据管理的区别,其实还不少专家还存在争议。
常规的临床数据管理的关键方面包括:
- 数据收集:这涉及设计病例报告表(CRF),可以是纸质的或电子的(eCRF),以从研究参与者那里收集数据。
- 数据录入:数据录入员跟踪CRF页面的接收情况并将数据输入数据库。
- 数据验证:数据库程序员创建研究数据库,设计数据录入界面,并编写编辑检查程序以验证数据。
- 差异管理:CDM团队识别并解决数据差异,以确保数据质量和一致性。
- 医学编码:医学编码员标准化不良事件、病史和药物的术语。
- 数据库锁定:一旦所有数据管理活动完成,数据库将最终确定并锁定以进行统计分析。
要进行数据管理
适当的数据管理是开放科学的重要组成部分。通过开放科学促进研究数据的最佳(再)利用是欧盟(EOSC宣言)及相应国家计划的目标之一。科学家、患者和公众将从共享高质量数据中获得新科学知识、治疗方法和应用。此外,数据管理是保护研究科学完整性、满足研究资助者、科学期刊和法律(如《通用数据保护条例》,GDPR)要求所必需的。
作为临床研究者,适当的数据管理将为你带来多方面的好处:
1)CDM确保临床试验中收集的数据准确、完整且一致,这是得出有效结论的基础;
2)它帮助保持对监管标准和指南的遵守,对获得FDA等监管机构的批准至关重要;
3)组织良好且干净的数据使研究人员和医疗提供者能够就治疗和患者护理做出明智决定;
4)通过严格的数据分析,CDM帮助识别潜在的不良事件和评估患者健康趋势,提高整体安全性;
5)通过优化资源分配和减少与数据相关的低效,CDM可显著节省临床研究的成本;
6)CDM自动化数据录入、验证和清理的许多方面,提高了临床研究过程的效率;
7)一个强大的CDM系统确保提交给监管机构的数据准确且合规,提高成功批准的可能性;
8)CDM建立了受控和标准化的数据存储库,便于跨不同研究的数据比较和分析;
9)通过确保高质量数据和高效流程,CDM有助于加快整体药物开发时间表;
10)CDM为生成可靠的证据提供基础,可用于指导医疗实践和治疗指南;
总之,临床数据管理在确保临床试验的成功、可靠性和效率方面发挥着重要作用,最终促进在科学研究、商业开发、验证或医疗保健等行业的良性循环。另外,良好的数据管理计划还确保你能及时获得存储空间和支持人员等资源。
FAIR原则
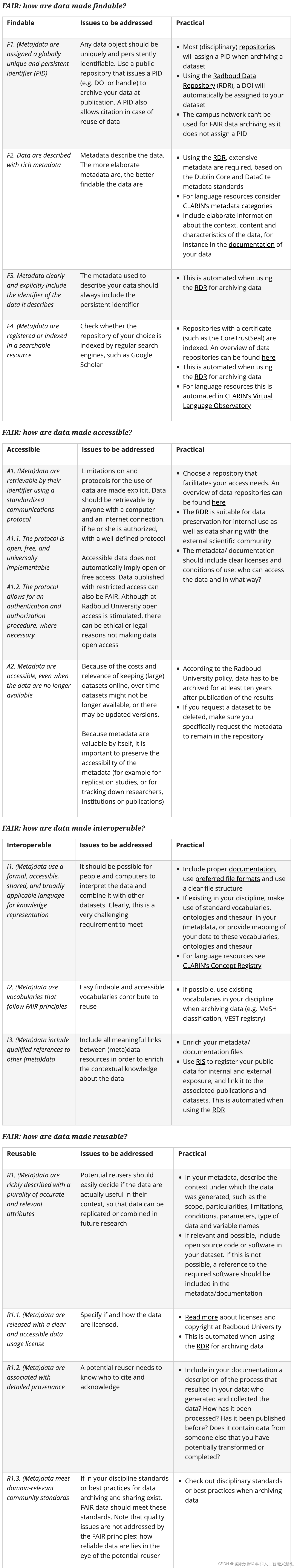
本章根据全球采用的FAIR原则描述了研究数据管理的基本原理。FAIR原则规定研究数据应当:
- Findable(可查找):数据应具有唯一且持久的标识符,其他研究人员应能够找到这些数据。
- Accessible(可访问):应明确数据的使用条件,对人和计算机均可理解。
- Interoperable(可互操作):可互操作性是指非合作资源的数据或工具能够以最小的努力整合或协同工作。数据应为机器可读,并使用该领域常用的术语、词汇或本体。
- Reusable(可重复使用):数据应符合上述要求,并且有足够的元数据和出处信息描述,以便数据源能够与其他数据源链接或整合,并能够进行适当引用。
承担数据管理员职责
作为一名临床研究者,也同样承担着主要的数据管理员角色。这意味着不仅负责数据的收集和分析,还要确保数据从生成到共享的整个过程符合相关法规和伦理要求。在这一过程中,研究对象的隐私保护也是我的重要职责。本文将详细探讨临床研究数据管理的各个方面,包括研究设计、数据收集、分析、存储、共享以及如何确保数据管理的合规性。
研究设计是科学研究的基础。在这一阶段,我们需要确定研究问题、设计实验方法、选择研究对象,并制定详细的数据管理计划。这些计划应包括数据的收集方式、存储地点、数据的保密性措施以及数据的共享策略。确保研究设计符合伦理要求和法律法规是非常重要的,特别是在涉及人类受试者的临床研究中。我们需要获得伦理委员会的批准,并确保研究对象签署知情同意书。在数据收集阶段,我们需要严格遵循预定的研究方案,确保数据的准确性和完整性。数据收集的方式可能包括问卷调查、临床测试、实验室分析等。在这个过程中,必须保护研究对象的隐私,确保数据收集过程的透明度和可追溯性。所有的个人数据都需要匿名化或假名化处理,以减少隐私泄露的风险。另外,数据分析是研究过程中的关键环节。分析结果的准确性直接影响研究结论的可靠性。在进行数据分析时,我们需要使用适当的统计方法,并确保数据分析过程的透明度和可重复性。所有的分析结果都应该经过严格的验证,以确保其可信度。在这一过程中,数据管理员需要确保分析软件和工具的合规性,并确保分析过程的可追溯性。同时,数据存储是数据管理的重要组成部分。我们需要选择安全可靠的数据存储设施,确保数据在存储过程中不被篡改或丢失。数据存储设施应符合相关的法律法规和行业标准,如《通用数据保护条例》(GDPR)和《健康保险可携性和责任法案》(HIPAA)。在数据存储过程中,我们还需要定期备份数据,以防止数据丢失。同时,数据存储设施应具备良好的访问控制机制,确保只有授权人员才能访问敏感数据。
数据共享是促进科学进步的重要手段。通过数据共享,其他研究人员可以重复实验、验证结果,并在此基础上进行新的研究。然而,数据共享需要遵循严格的隐私保护和伦理要求。在共享数据之前,我们需要对数据进行匿名化处理,去除所有能够识别研究对象的个人信息。同时,我们需要签订数据共享协议,明确数据的使用范围和责任义务,以防止数据被滥用。
保护研究对象的隐私是数据管理的核心原则。我们需要采取一系列技术和管理措施,确保个人数据的安全性和保密性。这些措施包括数据的匿名化处理、数据访问控制、数据加密以及数据使用的监控和审计。同时,我们需要确保研究对象了解他们的数据将如何使用,并获得他们的知情同意。在数据管理的各个环节,我们都需要遵循最小化原则,即只收集和处理必要的数据,避免不必要的数据处理和存储。
根据《通用数据保护条例》(GDPR)的问责原则,研究机构有责任确保个人数据处理的合规性,并能够证明其合规性。这意味着研究机构需要制定和实施适当的数据管理政策,配备必要的设施和专业知识,以确保数据管理的各个环节符合GDPR的要求。研究机构还应指定一名数据保护官员,负责监控机构的GDPR合规情况,并处理与数据保护相关的问题和投诉。
不遵守数据管理原则的后果
不遵守数据管理原则可能带来严重的后果,包括声誉损害、法律责任以及失去或必须退还研究经费。声誉损害可能导致研究机构在学术界失去信誉,影响未来的研究合作和资金申请。法律责任可能包括高额罚款、诉讼费用以及对受影响个人的赔偿。失去研究经费则可能导致研究项目中止,影响研究成果的产出。因此,研究机构和研究人员必须高度重视数据管理的合规性,采取一切必要措施确保数据管理符合相关法规和伦理要求。
一些研究机构已任命正式的数据管理员,负责促进或提供数据管理方面的建议。这些数据管理员通常具备丰富的数据管理经验和专业知识,能够为研究人员提供技术支持和指导。研究人员可以将部分数据管理任务委托给这些数据管理员,以确保数据管理过程的合规性和高效性。数据管理员的职责包括数据管理政策的制定和实施、数据管理培训、数据安全监控和审计等。
| 角色 | 责任 |
|---|---|
| 研究人员 | 对研究数据负责;控制整个研究数据流;尽可能重复使用现有数据;在整个研究项目中与患者组织合作;保护研究对象的隐私和安全;应用FAIR原则;保护研究质量和可重复性;利用现有专业知识和推荐的基础设施;提前考虑知识产权;负责任地共享数据。 |
| 研究机构 | 雇佣提供数据管理程序和技术系统的专业人员(如数据管理员、数据经理、IT专家、统计学家);有负责管理和协助专业人员的机构经理;有监督机构如医学伦理审查委员会和隐私官员;与提供数据的患者和公民互动;提供保护数据的设施以符合GDPR。 |


























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










