
FDX1参与了铜相关的细胞死亡方式——铜死亡,这可能会影响肿瘤进展,如铁死亡和焦亡。然而,FDX1在肿瘤中的作用仍需探索。本研究从泛癌症的角度,基于综合生物信息学,调查了FDX1的表达特征以及与预后、肿瘤分期、免疫微环境和铜死亡的相关性。
1. FDX1模式的表达及其在泛癌症中的临床特征
首先,为了研究FDX1在肿瘤和正常组织中的差异表达,作者从TCGA数据库获取了FDX1的mRNA表达数据。差异表达分析结果显示,在胶质母细胞瘤(GBM)、脑低级别胶质瘤(LGG)和胃腺癌(STAD)中,FDX1在肿瘤组织中的表达水平高于正常组织(图1A)。而在乳腺浸润性癌(BRCA)、胆管癌(CHOL)、结肠腺癌(COAD)、肾嗜铬细胞瘤(KICH)、肾透明细胞癌(KIRC)、肾乳头状细胞癌(KIRP)、肺腺癌(LUAD)、肺鳞状细胞癌(LUSC)、前列腺腺癌(PRAD)、直肠腺癌(READ)和甲状腺癌(THCA)中,肿瘤组织中FDX1的表达水平降低(图1A)。接下来,作者根据GTEx数据集分析了FDX1在正常组织中的表达情况。结果显示,肾上腺、肝脏和甲状腺中FDX1的表达水平较高,而血液、大脑和胰腺中的表达水平较低。然后,肿瘤细胞系中FDX1表达的结果显示,根据CCLE数据库,它在肠道、胃、造血和淋巴组织中表达最高,在胸膜和上呼吸道中表达最低。
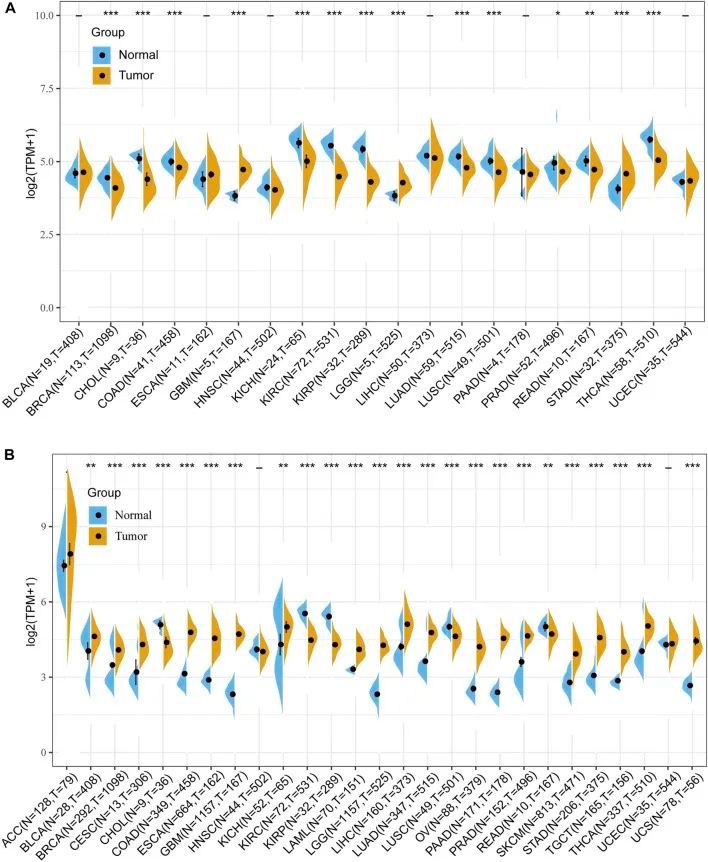
图1 根据癌症基因组图谱(TCGA)和基因型组织表达(GTEx)数据库,FDX1在人类泛癌中的差异表达情况
由于TCGA数据库中正常样本数量较少,作者进一步整合了TCGA和GTEx数据库来评估FDX1的差异表达。如图1B所示,FDX1在膀胱尿路上皮癌(BLCA)、乳腺癌(BRCA)、宫颈鳞状细胞癌和子宫内膜腺癌(CESC)、结直肠腺癌(COAD)、食管癌(ESCA)、胶质母细胞瘤(GBM)、肾上腺皮质肿瘤(KICH)、急性髓系白血病(LAML)、低级别胶质瘤(LGG)、肝细胞癌(LIHC)、肺腺癌(LUAD)、卵巢浆液性囊腺癌(OV)、胰腺腺癌(PAAD)、前列腺癌(PRAD)、皮肤切除性黑素瘤(SKCM)、胃腺癌(STAD)、睾丸生殖细胞肿瘤(TGCT)、甲状腺癌(THCA)和子宫肉瘤(UCS)中上调,在胆管细胞癌(CHOL)、肾透明细胞癌(KIRC)、肾盂细胞癌(KIRP)、肺鳞状细胞癌(LUSC)和直肠癌(READ)中下调。在肾上腺皮质癌(ACC)、头颈部鳞状细胞癌(HNSC)和子宫体内膜癌(UCEC)中,FDX1的表达没有差异(图1B)。
此外,作者根据GEPIA2.0在不同癌症阶段探索了FDX1的表达情况。结果显示,FDX1在甲状腺癌(F值=11,Pr(>F)=5.15e-07)、肝细胞癌(F值=6.11,Pr(>F)=0.000467)、肾透明细胞癌(F值=5.7,Pr(>F)=0.000759)、胰腺导管腺癌(F值=4.9








 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章



















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










