获得2020年诺贝尔化学奖的CRISPR/Cas9基因编辑系统,作为第三代基因编辑工具,自2012年面世以来,极大简化了基因编辑操作,降低了研究门槛,让基因编辑迅速成为热门领域。随之大量基于CRISPR/Cas系统的实验方法被开发出来。例如对RNA的编辑,实现了基因编辑从DNA到RNA水平的跨越,由于其仅对基因转录产物mRNA编辑,而不改变基因组DNA,为基因表达调控研究提供了新思路;单碱基编辑(base editor, BE),绕过HDR同源重组修复的低效率,为真正意义上的单碱基突变基因的精准修复提供了可能。
针对CRISPR/Cas9基因编辑系统的改造优化中,提高特异性、减少脱靶、简化操作流程、使科研人员可以专注于研究本身是CRISPR技术研发的永恒追求。
Cas9稳转细胞株(即Cas9稳转细胞系、Cas9预置稳转株),通过将Cas9核酸酶基因转染入各类常用细胞株中,筛选单克隆,构建了可以稳定表达Cas9核酸酶的细胞株,使CRISPR/Cas9基因编辑实验步骤进一步简化。实验中,仅需转染gRNA/sgRNA,即可实现基因敲除,而转染gRNA/sgRNA和供体DNA,即可实现基因敲入,绕过了RNP核糖核蛋白复合体大分子转染效率较低的问题,显著提高基因编辑效率。
Cas9稳转细胞株基因编辑流程:
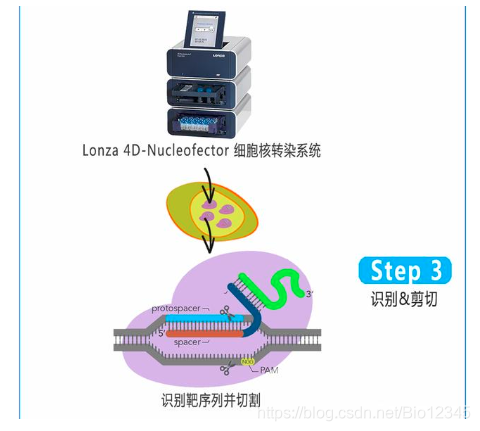
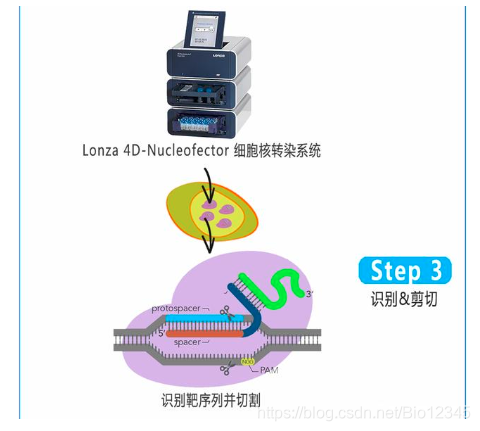
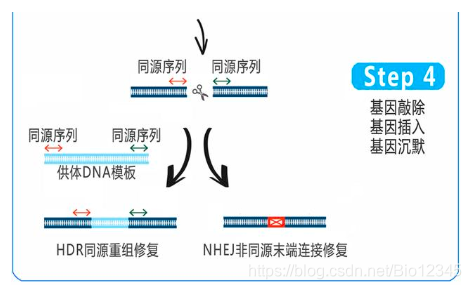
Cas9稳转细胞系:
CRISPR-Cas9自面世以后,完全改变了基因编辑所需的门槛:大量的基于CRISPR-Cas9 系统的实验方法被开发出来,极大的促进了基础研究的进步。
将Cas9核酸酶基因转染入细胞系中,通过筛选单克隆,可以得到稳定表达Cas9的细胞系。这时CRISPR-Cas9的基因编辑实验步骤可以进一步得到简化。在实验中,仅需转染向导RNA,即可实现基因敲除。转染向导RNA和供体DNA,即可实现基因敲入。因此,稳定表达Cas9的细胞系是基因编辑研究的利器,可以极大的简化实验。























 205
205

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








