在人的一生中,大脑会发生与年龄相关的显著变化,个体的衰老速度会显示出明显的个体间差异,从而产生作为大脑特征在特定认知领域上的大脑标记。这些是由各种各样的因素形成的,既有内部的,也有外部的。最近,研究人员通过使用机器和深度学习(DL)技术,可以从神经成像内表型中获得对大脑年龄(BA)的准确预测。预测模型在准确估计年龄的同时,还揭示了哪些特征对最终预测贡献最大,这是揭示大脑老化模式演变潜在机制的关键。同时,可解释的人工智能(XAI)方法正在成为不同领域的使能技术,在生物医学中也不例外。在此框架内,本文考察了BA研究,并对可解释机器学习(ML)/ DL(深度学习)方法的开发方面的最新进展进行了全面回顾,强调了主要的未决问题,并为未来方向提供了提示。本文发表在IEEE SIGNAL PROCESSING MAGAZINE杂志。
介绍
一个人的大脑的脑龄是多少?这个看似简单的问题隐藏着一个极其复杂的系统,其中不同类型的内生变量和外生变量以一种未知的方式相互作用。在本文中,作者旨在通过关注一个具体的案例来提供一些见解:解释神经成像衍生的内表型对脑龄确定的影响,即大脑的“大脑特征”或“指纹”,同时利用XAI揭示主导该过程的主要因素。
大脑老化的研究最近在科学界引起了关注,因为通过神经成像数据并结合特定的统计分析来开发准确的大脑老化生物标志物,在不同领域开辟了新的视角,使我们能够从疾病特异性变化中理清年龄相关的变化,并在单个受试者水平上跟踪疾病进展。
预测模型通常是在大样本对照上训练,输入候选内表型,并输出估计或预测的年龄。然后定义了一个由预测年龄和历史年龄之差给出的脑龄-delta。delta[以下称为大脑预测年龄delta (brain-PAD)]反映了个体与人群常模的偏差,突出了加速老化(正delta)和对老化的弹性(负delta),从而提供了关于大脑健康的信息。脑龄测量对于评估正常老化和疾病具有价值,最近的研究揭示了几种神经和精神病理学中更快老化的模式,甚至在明显的疾病表现之前。一个重要的例子可以在神经退行性疾病的背景下找到,作者的一项初步研究证明了对照组/稳定轻度认知障碍(MCI)和阿尔茨海默病(AD)患者的脑龄评分之间的显著差异,以及当使用脑龄评分而不是神经心理学测试时,对AD转化的预测更准确。
为了解决这个问题,不同的研究者已经提出了不同的解决方案,从内表型的选择到预测BA的方法。在现有技术(SOA)中,这些方法从经典的线性回归到处理单/多模态数据的ML模型。公共可用的大型异构数据存储库的出现需要新的方法来处理高维数据,而DL是首当其冲的。这使得模型结果的可解释性变得至关重要,尤其是考虑到BA估计固有的神经生理学基础的缺乏。因此,本文的主要目的是综述当前主要的BA研究结果,以及DL(深度学习)和XAI(人工智能)最新的进展如何促进BA的研究。
基于神经影像的BA预测在本节中,概述了当前文献中使用的最常见的图像衍生内表型(IDPs ),作为预测BA的成像特征,重点是基于磁共振成像(MRI)的特征。神经成像技术是评估遗传和环境因素对大脑结构和功能影响的天然工具。T1加权(T1w) MRI图像已经证明,大脑在其一生中会遇到进行性萎缩。过早的解剖变化与几种疾病有关,如神经退行性疾病、高血压和肥胖,这标志着脑龄是表征一个人健康的手段。
在目前的文献中,大多数BA的预测模型依赖T1w图像作为输入,因为T1w图像具有更高的可用性、可靠性和易于解释。14份被审议的文章采用了这种方法,而另外8篇文章考虑了其他模态的数据。机器学习方案下的研究通常从T1w图像中提取几个特征以用作BA模型中的预测特征。而最简单的解决方案是原始全脑T1w数据,避免特征工程步骤。但考虑到这些数据的高维性,这种框架仅在DL框架下是可行的。有六篇论文采用了这种方法,使用了3D卷积神经网络(CNN)。
在本文所选的九篇文章中,研究者们首先分割T1w图像以导出灰质(GM)/白质(WM)组织概率图,以用作3D输入或在矢量化之后使用。此外,两项工作对T1w数据进行了基于张量的形态测量,以使用推导出的雅可比行列式的图作为新的内表型。相反,在10项研究中,作者从基于体素的方法转向基于区域的方法,提取不同感兴趣区域(ROI)的汇总统计数据,特别是皮质厚度、表面积和体积。总的来说,依赖于这些特征的模型利用了关于萎缩水平的信息,如组织体积的变化、皮质变薄和脑沟变宽,以提供准确的BA预测。
除了常规T1w MRI之外的神经成像模式可以补充T1w图像无法提供的信息,并提供其他相关方面的信息,如组织微结构和脑功能。关于结构磁共振成像,T2加权(T2w)图像代表了T1w数据的一个可行的补充。英国生物库(UKB)的数据处理尤其遵循了这种方法。从这样的图像得到的主要特征由T1w/T2w表面比表示,在给定ROI中的所有体素上平均,以提供髓磷脂含量和WM损伤体积的简单测量。扩散加权成像[扩散MRI (dMRI)]是一种先进的结构技术,可捕捉活体脑组织的微结构特征。通过将原始dMRI信号拟合到特定的表示模型,可以得到几个微结构指数。这里考虑的所有文章都采用了简单的张量模型,从该模型中导出了分数各向异性(FA)和扩散率测量值,如平均扩散率和径向扩散率。
值得注意的是,各向异性指的是水分子的运动方向,而扩散率衡量的是水分子如何在给定的方向上自由扩散。UKB还包括来自神经突起定向分散和密度成像模型(NODDI)的额外信息,例如细胞内体积分数、各向同性体积分数和定向分散,而在一项工作中,指数来自平均表观传播因子(MAP)模型,提供不同的测量,包括广义FA (GFA)、非高斯性(ng)、正交ng和平行ng指数。从这些脑图出发,通常提取的IDP由跨WM地图或沿不同区域计算的平均值表示,后者通过基于区域的空间统计或追踪图进行识别。总的来说,包含这些特征的BA模型捕获了WM微结构中与年龄相关的变化,例如各向异性的降低,这主要反映了脱髓鞘、轴突变性或通过水肿形成的神经炎症。
除了分析大脑结构,还可以通过基于血氧水平依赖对比(BOLD)和动脉自旋标记(ASL)的功能性MRI (fMRI)来提取关于功能性的重要信息。在四篇文章中采用了基于BOLD fMRI数据的IDP,以及那些采用UKB数据的研究。FMRI扫描可以在给定任务的执行期间(任务-功能磁共振成像)或休息时(休息-功能磁共振成像)获得。在此处选择的文章中,任务相关的IDP仅在UKB框架内使用,并通过组水平图(即百分比信号变化和z统计的中值和第90百分位)得出的区域中的激活测量来表示。相反,基于静息功能磁共振成像数据的研究在很多研究单位都已经进行了这方面的研究。虽然在一项工作中报道了与低频波动幅度和区域同质性相关的测量,但在此类研究中通常采用功能连接(FC)模式的特征。
具体来说就是,从预处理的静息fMRI数据中提取信号,然后使用不同的统计方法进行分析,其中Pearson全相关和偏相关是最常见的,反映了区域中配对之间的同步性。然后,导出邻接矩阵,并使用这种连接矩阵的条目来作为BA预测模型的输入。只有一项研究突出了使用协方差作为连通性测量。相比之下,Rokicki等人开发了基于ASL的脑血流局部测量(CBF ),它与神经元活动密切相关,反映了微血管的完整性/功能性,并将其用作BA预测因子。最后,有两篇文章提出了将MRI与从电生理测量(如脑磁图(MEG ))获得的特征相结合的尝试。在这种情况下,IDP由功率谱密度、振幅包络相关、层间耦合、源活动性(如信号功率)和源连通性(如信号协方差)等特征构成。
影响BA预测的主要问题之一是人数和样本量之间的不平衡,这可能导致模型过度拟合。为了克服这一瓶颈,通常在将IDP输入预测模型之前进行降维。这通常基于主成分分析(PCA)、典型相关分析(CCA)和独立成分分析(ICA)。这些都是作为模型的补充来人为设置的,如值得注意的是,虽然PCA沿着最大方差的维度投影数据,但是CCA最大化了数据之间的给定相似性度量,最常见的是相关性。当ICA用于降维时,数据被投影到一个空间中,在该空间中,分量被假设为非高斯的并且尽可能独立。这种数据预测可以提供关于群体的额外信息,反映其内在差异和相似性。
大规模生物医学数据库,例如阿尔茨海默病神经成像倡议(ADNI)、UKB、剑桥衰老和神经科学中心(Cam-CAN)的相关研究被纳入到本文中。在被考虑的论文中没有使用其他的内表型。事实上,与衰老过程有明显联系的特征(如性别、教育、血压和临床变量)仅被用作协变量,并在预测BA后用于进行关联研究,本文将在“BA预测建模:从统计方法到DL”和“BA发现的关联研究”部分详述这一内容。
总的来说,关于当前BA研究的要点可归纳如下:
1)在BA研究中大量采用结构T1w数据,提供从基本组织概率图到量化皮质厚度、表面积、体积和沟宽度的更复杂测量的形态测量信息。
2)DMRI、BOLD fMRI和ASL代表了更先进的技术来补充传统的基于T1w的IDP。它们有助于获得描述微结构、功能和血液动力学脑模式的大量特征,这些特征目前正在BA领域中进行,并具有有希望的结果。
3)不同性质的内表型的使用,例如基于电生理学测量的内表型,仍然是有限的,而没有研究开发出与衰老过程有明确联系的其他特征。
4)研究中的人数和样本量之间可能存在的不平衡是一个重要问题,可能会使预测产生偏差,需要加以考虑(例如,通过维度缩减方法)。
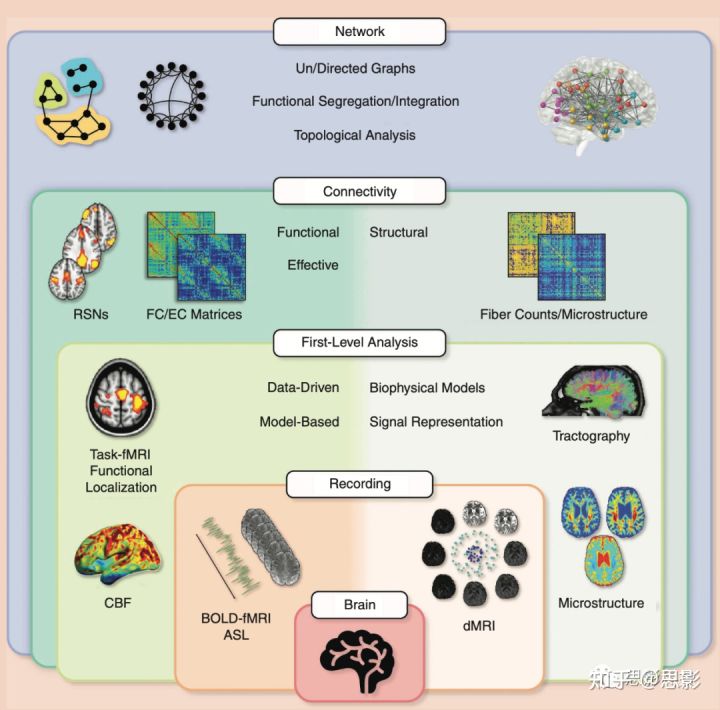
图S1 使用脑影像方法对不同层面的人脑特征进行提取并用于预测脑龄
一阶段特征:扩散磁共振成像(dMRI)是结构磁共振成像的一种变体,它通过将数学模型(分析模型或房室模型)来拟合原始数据,提供微结构特性的详细信息(图S1)。此外,可以通过跟踪每个体素中的主要扩散方向来建立结构连接。血氧水平依赖的功能磁共振成像(fMRI)是记录大脑功能活动的最常见的无创方法,而动脉自旋标记(ASL)代表了另一种可行的替代方法,能够导出定量脑血流图以及可比的功能信息。这两种技术都可以在特定任务的执行过程中或休息时应用(休息状态fMRI)。为了获得有意义的模式,可以使用各种计算/统计方法(例如,任务功能磁共振成像和相关功能定位的一般线性模型,以及静息状态功能磁共振成像的独立成分分析);
连接水平的特征:通过静息态数据或者结构数据可以构建以脑区为节点,以脑区间的功能耦合或白质连接作为边,可以提供网络连接水平的特征,包括功能连接强度或者白质连接的纤维束counts等;
网络水平的特征:在前一步的网络构建的基础上,可以通过图论方法提供一些网络水平的特征,包括模块化、不同网络的整合和分离等,更进一步的可以使用图的拓扑属性来作为特征的描述。
BA预测建模:从统计方法到DL
在本节中提供了BA估计框架的详细概述,首先介绍了更传统的统计/ML方法和相关发现,然后说明了迄今为止在BA领域开发的基于DL的方法。越来越多的研究机构将几种有监督的、线性的和非线性的技术应用于BA预测问题。多变量分析有助于准确地检测出个体中与预期年龄相关的大脑模式的细微偏差。 2010年开发的“BA gap estimation”方法首次从T1w数据中量化了个体大脑衰老的加速/减速,揭示了不同研究中有希望的结果。正如将在本节下面总结的那样,最近已经设计出了几种替代方案,超越了传统的统计/ML方法,并且利用了DL方法的巨大潜力。
统计方法
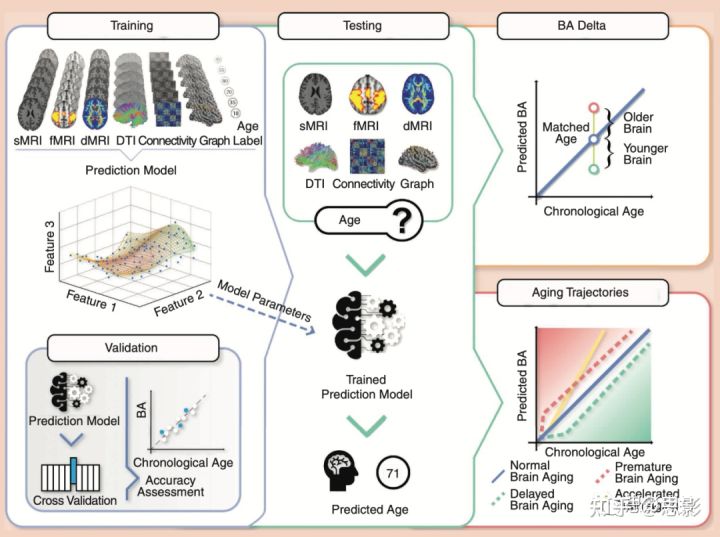
图1使用监督ML对BA预测范式的概述
训练:直接从多种模式获得的神经成像数据,或作为健康个体的次级特征,使用参与者的实际年龄标记,并作为回归模型的输入。验证:k-fold交叉验证过程,将训练样本分成k份,使用k- 1份数据进行训练,使用hold out流程进行预测。然后,该程序在所有folder中迭代,并将预测的年龄与按时间顺序排列的年龄进行比较,以评估模型的准确性。
测试:将训练得到的模型系数/权重应用于测试集的参与者数据,以产生个体BA预测。
BA delta:然后从预测的BA中减去实足年龄,得出一个单一的总括测量(大脑脑龄)。
衰老轨迹:不同的大脑衰老轨迹已经被许多研究证明提供了一个人的健康状况的信息。每个人的大脑老化轨迹可能不同,偏离所谓的“健康老化”。事实上,一个人的基因和发育/环境因素可能会导致其一生中更高的衰老率(早衰;红色虚线)或者相反,延迟大脑衰老(绿色虚线)。此外,某些人可能会经历一些特定的事件,从而决定大脑老化的加速轨迹(黄线)。
如图1所示,预测BA的一般过程依赖于对“训练集”的健康受试者(无神经精神病学、神经学和其他健康疾病)的大样本的识别,通常采取以下步骤:
预测模型的定义:从设计角度来看,大多数BA研究使用受试者的大型训练集,在监督学习框架内建立年龄预测模型,将大脑IDPs(图像衍生内表型)作为独立(预测)变量,将实际年龄作为因变量(结果)。简单线性回归及其适应多个预测因子的扩展[多元线性回归(MLR)]已被提出作为模拟变量统计关系的简单而有效的方法。给定n个受试者和p个大脑特征,MLR可以被模拟为:
Y = Xb+f = B0+X1*B1+X2*B2+g+Xp*Bp+f,(1)
其中Y 是响应变量的向量(年龄),X 是独立变量矩阵(大脑特征),bp是权重向量(待估计的未知系数),f是随机误差的向量。
然而,考虑到目前可用的神经成像特征的高维度,传统的普通最小二乘(OLS)回归方法可能不合适(很容易导致模型的过度拟合)。因此在实际使用时以多变量方法为主,这些方法能够处理大量特征和大数据储存库。基于八种不同ML方法的BA模型在本文中进行了研究,包括正则化回归模型[岭、最小绝对收缩和选择算子(LASSO)和弹性网]、高斯过程回归(GPR)、支持向量回归(SVR)、相关向量回归(RVR)、随机森林(RF)和梯度提升回归(GBR)。
训练和验证:在这个阶段,来自训练集的IDPs(图像衍生内表型)和参与者的按时间顺序的年龄被输入到选择的ML模型中。为了验证BA模型,大多数研究采用交叉验证方法,在该方法中,来自整个训练组的一部分样本被排除(通常在10%和20%之间),而剩余的最大部分用于训练BA模型。然后将其应用于被排除在外的群体,以预测个人年龄。执行该操作直到探索整个不相交分区集。模型的性能是根据预定义的测量值进行评估的,通常是估计的BA和年代之间的平均绝对误差(MAE)、均方根误差和皮尔逊相关系数(r值)。虽然这些指标主要用于评估模型的准确性,但应谨慎解释,尤其是在比较跨研究的结果时,因为它们受几个因素的影响,包括样本的年龄范围,这可能会导致表现的变化。
将预测模型应用于独立的测试集:通常,最好的模型被保留用于在一组看不见的样本(测试集)上进行测试,该组样本包括健康和/或患病的受试者,并且生成个体预测。该操作使得能够进一步验证BA模型,并证明其跨可能来自不同来源和数据库的若干样本的可推广性。最后,提取脑龄作为由预测年龄和年代年龄之间的差异给出的单一代表性度量。
使用统计/最大似然估计方法的BA研究的主要结果
此处包含的关于统计/最大似然预测的所有相关研究(17篇论文加上两项比较DL和最大似然预测的研究)遵循了前面描述的一般路径。这些发现表明输入的大脑特征本身的差异可能比模型选择方法有更大的影响。
关于不同的IDP,在成人中最精确的研究报告了使用基于T1w结构IDP的单模模型的4-5年的MAE,当使用皮质下和基于体素的形态测量(VBM)特征时结果会稍好。此外,在涵盖儿童早期和成年早期年龄范围的研究中,预测通常达到更好的准确性,MAE值仅为1-2年。一些研究发现了健康成人的类似结果,其中作者额外强调了评估几个参数对BA估计框架的影响的重要性。特别是训练样本的数量对准确性有最大的影响,而处理参数,包括从T1w图像中导出结构特征的方法和使用PCA的维数减少,对MAE值只有轻微的影响。
近年来,研究人员还试图探索额外的大脑IDP产生BA预测的潜力。最近的横断面研究通过简单地组合所有特征或使用结构性MRI结果作为基准,调查了大量健康成人样本的不同MRI数据和相应的IDP。后面的这些研究表明,基于dMRI的单模态预测往往达到与使用传统T1w数据相当的性能,而基于fMRI测量的模型只能解释有限的年龄差异,并且达到最低的预测精度。此外,在Rokicki等人的研究中,基于CBF的模型仅表现出中等性能,这是唯一一个将ASL的预测准确性与结构性测量结果进行比较的模型。
除了单一模态,所有这些横断面研究都调查了在多模态模型中合并来自不同MRI数据的信息是否有助于实现更准确的BA预测。集成了不同模态和特征集的模型在所有这些研究中产生了最佳拟合。使用多模态叠加模型得到了类似的发现,当在基本模型上叠加MEG或fMRI时,多模态叠加模型能够比单独使用MRI更好地预测BA,并且与纯粹基于解剖的预测相比,有助于获得近一年的误差。
虽然合并多个特征以实现准确的BA估计的重要性是不可否认的,但是Smith等人最近指出如何将几个因素组合成单个度量是个重要的问题,因为不同模态特征的融合可能会以丢失用于区分不同生物因素的重要信息为代价,所述不同生物因素会导致大脑在老化时发生不同的变化。因此,除了将所有可用的IDP输入一个达到最佳精度(MAE = 2.9年)的模型之外,作者还分析了由62种模式代表的大脑衰老的不同方面,每种模式反映了不同IDP的组合,并得出了一系列模式对每个受试者的BA估计值。他们的发现证明了通过分别考虑多种模式所带来的附加值,并强调了超越单一总和指标来揭示更具生物学意义的衰老大脑图像的重要性。
深度学习
对更准确的年龄估计的追求和大神经影像数据可用性的增加已经推动研究人员超越传统的ML方法并利用DL的潜力。在过去的一年中,已经发表了一些关于该主题的研究,正如我们在“使用DL方法的BA研究的主要结果”一节中简要总结的,当前的方法显示了使用3D T1w图像作为输入并实现更低MAE值的有希望的结果。然而,在进一步提高预测精度方面,尤其是在训练样本有限的小数据集上,以及在定义最佳架构方面,仍然存在挑战。事实上,在BA任务中,更复杂和更深入的模型是否比更简单的模型表现得更好,以及它们如何处理不同类型的数据,这些都是有待阐明的公开问题。
这里包括的七篇相关论文中的六篇依靠CNN架构使用3D T1w图像来估计BA。尽管当前文献中存在大量的CNN变体,但BA文献中迄今探索的解决方案大多基于VGGnet和ResNet架构的网络(图2)。一般使用的是与ML类似的BA预测的框架,数据样本会被分成训练集、验证集和测试集,用于模型训练和评估。在训练过程中,通常使用随机梯度下降,自适应矩估计来优化CNN,而真实年龄和预测年龄之间的MAE以及kullback-leibler散度被用作在该过程中最小化的损失函数。
在最后一种情况下,BA预测是作为一个软分类问题而不是像最近提出的经典回归问题来考虑的。在这种设置中,年龄标签不被认为是一个单一的数字,而是一个离散的高斯概率分布,以实际年龄为中心,分布σ设置为一个年龄区间的大小,如1-2岁。模型的输出也是一个概率分布,kull backlei bler散度可以用来衡量两个概率之间的相似性。产生的输出具有给定数量的X位数字,代表X个年龄组,每个年龄组覆盖一个特定的年份范围,最终的年龄预测由所有年龄组的平均值给出,该平均值由输出概率加权。这种软分类方法应该实施一种模型来尽可能准确地预测BA。
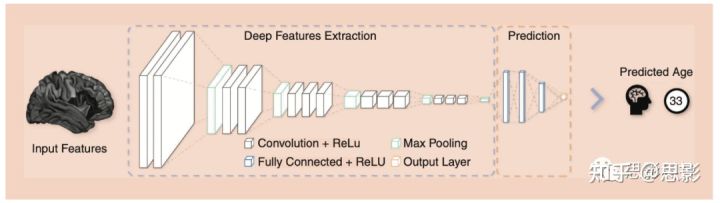
图2 一个用于BA预测的VGGnet架构示例
大脑代表输入的特征。黑框部分是卷积层,后面是ReLU激活层;绿框表示最大池化层,蓝框表示全连接层,然后是ReLU激活层。最后,橙色框表示线性预测器。输出是主体的预测年龄。
为了减少模型对预处理步骤的依赖,如图像重新对齐和配准,所有的研究都倾向于对输入数据仅应用最少的预处理。此外,不同的正则化和数据扩充策略,包括丢失、数据旋转、转换、镜像、缩放和添加随机噪声,通常在训练阶段应用,以避免过拟合和提高泛化能力。最后,如“统计方法/ML”一节所述,通过MAE和r值来评估模型的性能。
使用DL方法进行BA研究的主要结果
在过去的两年中,探索基于CNN的T1w图像年龄预测方法的研究数量有所增加,使得对这一问题的理解有了重大突破。虽然在所有代表性的论文中,CNN架构大多基于前面提到的两个模型,但在每项研究中都提出了具体的设计,以实现精确的估计并更好地解决一些主要的计算问题(例如,总参数的数量、复杂性和内存需求)。一个研究受通用VGGnet架构的启发,设计了3D CNN,将来自覆盖大量成人的大型聚合数据集的全脑T1w体积作为输入。尽管与使用DL框架的其他研究相比,该模型没有达到最佳预测结果,但该模型在来自同一人群的保留测试集和另一个独立数据集(MAE ~ 4年)中表现良好。然而,正如作者所认识到的,主要的焦点不是准确性本身,而是对训练集中年龄分布(均匀/不均匀)的贡献的评估。研究结果表明,均匀分布的数据集将导致准确的估计,而不会明显偏向某一年龄组,同时保持良好的训练效率,应当将此类标准纳入更广泛的BA研究。
相反,彭等人最近发表的一项研究旨在提出一种新的3D CNN架构,以实现可能的最佳性能,正如作者参加2019年BA forecast-casting预测分析挑战赛所证实的那样,他们在比赛中名列第一。他们开发了一种轻量级的DL架构,即简单的完全卷积网络(SFCN),基于完全卷积网络和VGGnet,其特征是参数数量相对较少,并以全脑3D T1w图像作为输入。他们创造性的设计能够降低计算复杂性和内存成本,即使训练对象数量很少,在UKB数据集也可以达到良好的精度值。他们还将他们的SFCN与更复杂的CNN架构(例如ResNet18和ResNet50)进行了比较,证明了在这种预测任务中,更深的模型并不比浅的模型表现得更好,并且用他们的轻量级模型达到了最低的MAE。最后,他们证明,无论训练集大小如何,SFCN都能够胜过一个调整良好的弹性网络模型。
这与作者之前对3D CNN和T1w图像的发现一致。在这项研究中,作者首先根据四种不同的结构特征(全脑T1w图像、雅可比图和GM/ WM分割)独立训练他们的模型,根据图像类型实现了4-4.8年的平均MAE。此外,他们将这种方法与八个ML回归模型进行了比较,这八个模型分别基于表面形态测量、VBM和相似性矩阵特征进行了训练,表明DL模型比其他模型预测BA更准确。其他作者已经从各种数据库中报告了健康个体中使用CNN模型的类似的更低的MAE值。有趣的是,Jonsson等人和Peng等人研究了将从T1w图像中提取的不同特征集(如GM/WM图和原始的非线性归一化T1w数据)相加可以提高性能,正如使用ML回归方法预测BA所证明的那样。从用不同特征类型分别训练的单个CNN模型开始,使用多数投票策略形成最终预测并平均单个预测来导出集成模型,并且与使用单个模态相比,两者都通过多模态输入导致性能增益。这再次强调了组合多种数据类型的重要性,因为从不同的特性中收集到的信息是部分独立的。
最后,一些作者已经开始评估迁移学习(TL)方法的可行性,以微调最初在从不同位置和不同成像条件下获取的数据集上训练的BA模型,并获得有希望的结果。事实上,TL可能是提高基于MRI的BA预测模型的可推广性的可行解决方案,特别是当ML/DL典型的大数据要求未得到满足时,以及当处理更复杂的测量时,例如那些来自dMRI和f MRI数据的测量,其经常经历更大的站点间可变性。一个重要的例子是通过使用来自dMRI数据的基于区域的测量(tensor和更高级的特征,如GFA和ng)将CNN模型应用于预测BA。一旦定义了模型,就应用TL将dMRI老化模型从源域(Cam-CAN)转移到目标域[NTUH(国立台湾大学医院)、IXI-HH(哈默史密斯医院)、IXI-盖伊],目标域代表具有不同采集方案/参数的四个独立数据集,这些数据集对微结构dMRI图有明显的影响,并会排除脑老化模型的一般化。他们的结果表明,使用源域建立的预训练模型可以转移并微调到其他三个数据集,具有令人满意的预测性能和良好的重测信度。 总体而言,关于BA预测建模的要点可总结如下:
1)基于多重统计/最大似然方法的BA模型仍然是大多数研究中的常见选择。
2)使用不同数据集的文献发现表明,输入的特征类型比采用什么ML方法对BA估计具有更高的影响,因此需要仔细选择。
3)基于DL方法的BA预测正在出现,并在许多方面带来附加值,包括直接使用原始神经成像数据的可能性,如果数据集足够丰富则避免特征工程,处理大量数据/特征的能力,对输入和输出变量之间的非线性关系建模的可能性,以及与传统ML方法相比BA预测的更高精度。
4)与单一模态相比,在ML或DL框架中组合不同特征类型的多模态方法通常实现更高的准确性。
可解释的人工智能(即可解释的深度学习方案)
XAI最近成为理解ML/DL算法结果的“为什么和如何”的最热门话题之一。然而,这个领域在很大程度上仍未被探索,特别是在大脑老化领域,尽管它可能有助于理清不同特征对最终估计的影响,并提供传统方法无法捕捉的关于老化机制的其他线索。24份入选本文综述的论文中有16份采用XAI框架。在处理这个问题之前,我们试图阐明文献中仍然不清楚的一个方面,即explainability和interpretability之间的区别,这两个概念在描述不同的概念时可以互换使用。然后,对BA预测中最常用的方法进行了概述,并回顾了解决以下问题的相关文献:什么是XAI,它如何用于评估和理解模型结果?
可解释的能力(Interpretability,)、可因果性和可解释性(explainability)
Interpretability和explainability的概念很难被区分开来,通常被ML研究者认为是可以互换的。文献综述的查询结果也提出了这种模糊性。事实上,关键字explainability没有返回任何结果,而interpretability返回了本节中讨论的论文。因此,需要对这些术语进行明确的定义,以就其在本文中的含义达成一致,并得出主观或客观的评估标准。要注意的是,本文作者并没有假装要解决这个需要哲学思考的问题,而是围绕一个可能的意义来展开有意义的讨论。
Interpretability与模型输出背后的人类直觉相联系,声称模型的Interpretability越强,就越容易理解出系统输入和输出之间的因果关系。这个定义与可因性的概念密切相关,可因性与医学领域密切相关。可因果性被定义为“在特定的使用环境中,对人类专家陈述的解释达到特定水平的因果理解的有效性、效率和满意度的程度。”相反,explainability将与ML系统的内部逻辑和机制的解码相关联。特别是有研究者将可解释性定义为突出算法表示的决策相关部分和算法模型中的活动部分的具体计算,这些部分有助于弄清在训练集或特定预测的模型准确性的原因。但它与人类的理解没有必然联系。
因此,对于ML,interpretability并不必然导致explainability,反之亦然,如下。图3(b)试图说明这两个概念之间的区别。从训练数据开始,可以遵循两个方向来获得模型解释:
1)使用可直接解释的模型,例如决策树或线性回归模型,其底层逻辑易于遵循和理解,并且解释(即explainability)可以直接从模型系数中导出;
2)应用黑盒模型(例如,深度模型,例如CNN),随后是事后可解释性模型来导出解释(interpretability,例如显著图),不一定需要理解底层模型机制。
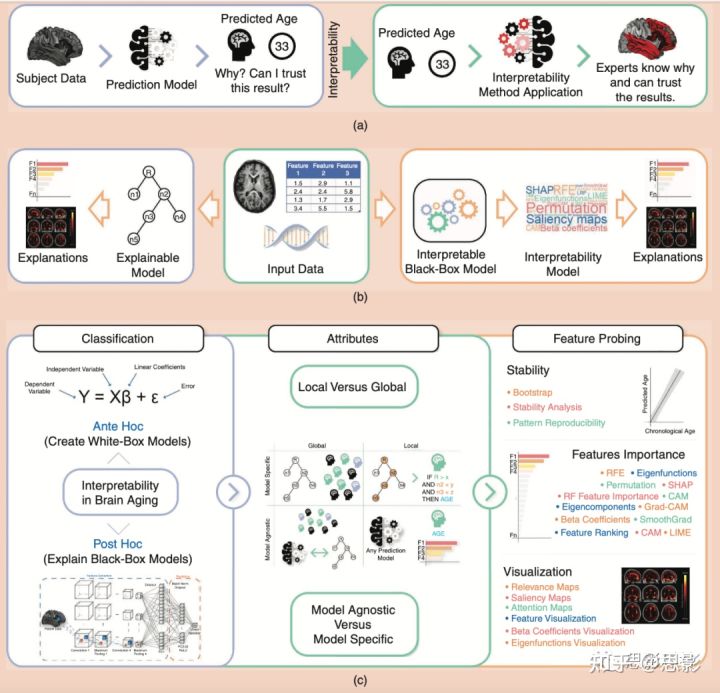
图3 可解释性方法的概述
(a)黑盒模型(DL)可以获得最佳预测,但它们不能促进完全理解。可解释性方法的应用使检索和解释最重要的特性成为可能。
(b)说明Interpretability 模型和explainability模型之间的区别的示意图。
(c)可解释性方法分为事前和事后。局部的、全局的、模型无关的和特定于模型的属性以及特性探测的属性被举例说明。Shapley加性解释;Gradient- cam:梯度加权类激活映射;LIME:局部可解释的模型;LRP:分层关联传播;RFE:递归特征消除。
Holzinger等人指出,数据、对象和图形表示,例如图像和文本,是可以直接理解的,因此可以由人类来解释。特征探测方法可以提供解释以实现模型的解释。以下三个特性是相关的:
通过使用重采样方法和交叉验证来测量在保留数据集上训练的多个模型中每个特征贡献的稳定性的方法来评估特征稳定性,通过评估特征对预测输出的影响而获得的特征重要性的排序,以及特征可视化,包括提供重要性的可视化呈现的策略,例如显著性图。虽然第二个和第三个属性旨在使模型结果人类可以理解,但第一个属性可以被视为评估解决方案的鲁棒性(可推广性)的一种方式。在这方面,通常在训练/验证阶段采用自举法。
在接下来的内容中回顾了一些本文认为与此相关的可解释性模型的附加属性。可解释性模型可以是模型不可知的,也可以是模型特定的。前者试图给出一些关于模型潜在功能的见解,而不考虑模型结构,后者只能应用于特定的预测模型和架构。此外,可解释性模型可以是局部的,也可以是全局的,这分别取决于解释是涉及单个预测还是整个模型或系统的一小部分。最后提出的另一个相关分类区分了事后模型和事前模型。
事前模型
这一类包括可解释模型,如线性、决策树和基于规则的模型,以及同样透明的更复杂的模型。应用XAI的16篇论文中有6篇使用了事前可解释推理模型来解释它们的结果。在BA预测中,如“BA预测建模:从统计方法到DL”一节所述,线性回归模型(如OLS、岭和LASSO)被广泛使用。它们具有可解释性,因为它们可以根据它们在局部和全局上的b系数被直接解释。假设数据已经标准化并且模型不包含截距,b的大部分可以被解释为与回归任务相关的特征。值得注意的是,解释能力受到共线独立变量的影响,因为在这种情况下,与目标变量无关的特征会被赋予较大的权重。如非负性和正则化可以用来限制解集,从而可能简化模型并提高可解释性。
事后可解释模型
事后模型代表了最广泛的一类可解释性方法,并被10个选定的论文应用。关于ML模型,基于特征排列的特征排序方法通常被用作可解释性技术。排列特征重要性是一种模型检验技术,当数据是特定的时,可用于任何拟合的估计量。特征重要性被定义为当单个特征值被随机打乱时模型分数的降低。模型得分的下降表明了模型对该特征的依赖程度。这种技术得益于模型的不可知性,并且可以用不同的特征排列进行多次计算。
广泛使用的黑盒模型可解释性方法是基于扰动的方法,如SHAP,旨在为黑盒模型建立替代模型,为它们提供可解释性。SHAP利用Shapley值的思想对模型特征影响评分,考虑实例的所有可能预测,使用所有可能的输入组合。由于这种详尽的方法,SHAP可以保证一致性和局部准确性。
在DL领域,显著图(Saliency map)起着核心作用。基本方法是依靠梯度,每个梯度量化每个输入维度的变化将在多大程度上修改输入周围小邻域中的预测。输出是对应于输出神经元相对于给定类别的梯度的图像特定类别的显著图。从这个共同点出发,开发了多种方法来从DL模型生成显著图。BA预测中最流行的是SmoothGrad。它首先通过添加正态分布噪声来扭曲输入图像,然后提取每个体素相对于训练模型输出的偏导数。这个过程被重复多次,以从多个梯度图导出平均显著图。
类似的方法是类别激活映射(CAM),这是一种为CNN开发的方法,用于指示CNN用来获得输出的图像的区别区域。具体而言,通过计算和连接位于最终输出层之前的卷积特征映射的激活平均值来创建特征向量。这个向量的加权和被馈送到最后一层。图像区域的重要性可以通过将输出层的权重投影回卷积特征图上来评估。梯度加权CAM (Grad-CAM)建立在CAM之上,可以应用于所有CNN模型,可以在任何架构的显著图中实现改进的特征定位。
可解释模型
在BA预测中,一些可解释性模型开始被用来更深入地了解导致预测BA的主要因素。它们包括以下内容:
事前模型:事前可解释的方法在这个领域广泛传播。在这一类别中可以找到五个主要贡献:
线性模型:Treder等人利用回归系数来解释模型预测,证明这些系数能够捕捉整个BA预测中的有意义的特征(参见“BA预测建模:从统计方法到ML”一节)。潜在变量模型:常见的推导将潜在变量模型作为特征缩减方法。潜在的空间成分增强了模型的可解释性。在[22]中,PCA被用作依赖于fMRI特征的线性模型的初步步骤。潜在变量对应于描述连通性模式的FC网络。Smith等人提出了一种类似的方法,使用PCA和ICA提取62种主观可变性模式,作为老化大脑的指纹。每种模式代表了大脑老化的不同方面,表现出不同的大脑功能/结构变化模式,以及与遗传、生活方式、认知、身体测量和疾病的选择性关联。
在帕尔马等人提出的图像标量法中,获得的特征函数编码了健康、轻度认知障碍和阿尔茨海默病受试者之间的主要差异。例如,作者观察到,第一特征函数有助于区分侧脑室和大脑的其他部分,从而得出结论,该特征函数的得分可能与诊断和实际年龄相关。最后,作者直接使用CCA来可视化显著影响BA预测的特征。
稳定性评估:Cole在LASSO系数上使用了bootstrapping技术来突出他的工作中包含的多模态变量中最具信息性的变量,得出多模态模型优于单模态模型的结论。这表明多模态提高了性能,尽管许多与年龄相关的变异可以被一小部分特征捕获,包括T1w和dMRI内表型。
事后模型:即使事后模型仍未被充分探索,本文中仍旧包括了已有的10篇文章,以给出迄今为止应用的技术的完整概述:
基于排列的方法检验特征的重要性:从使用单一模态的方法开始,作者使用排列特征重要性来分析不同WM/GM区域的相关性,以预测健康队列的BA。他们强调了在认知和记忆(海马体)、情绪调节/突出(杏仁核)和生理稳态(脑岛)中起核心作用的区域。相反,De Lange等人和Rokicki等人都开发了多模态BA预测模型。虽然作者利用基于置换的特征重要性进行初始特征约简,使用这种技术揭示了整合所有模态的模型的预测准确性主要由皮质厚度、T1w/T2w比率和皮质下体积驱动。
在文献[21]中遵循了类似的方法,其中通过回归模型的R2的减少来计算特征重要性。最后,Engemann等人在他们的混合模型中,研究了在MEG和fMRI表现型之间存在附加成分时的可变重要性。他们的特征重要性分析表明,脑磁图提供的在功能磁共振成像中难以获取的快速脑节律的信息是有意义的,这与预期相符。基于扰动的特征重要性:在文献[33]中,作者通过训练预测模型评估了空间脑龄模式的特异性,每次仅使用分别来自枕叶、额叶、颞叶、顶叶、扣带回、脑岛和小脑区域的特征子集。他们强调了被分析的11个不同临床组的不同空间模式。这项分析表明,在神经发育(精神分裂症)和神经退行性(多发性硬化(MS)和痴呆)疾病中,不同地区的相对老化表现出相反的模式。只有一项研究利用SHAP方法来评估青春期人群的特征相关性。作者在多种ML方法中使用了SHAP,揭示了一组共同区域的解剖变化驱动了年龄的模型预测,而与模型类型无关。通过追踪最重要的特征发现的区域反映了儿童和青少年时期大脑皮层的发育生长模式。
显著图:关于基于梯度的方法,文献[7]的作者利用SmoothGrad为他们的CNN模型制作解释图。他们分析了15个不同的数据库,包括健康和病理队列,并能够创建基于人群的综合解释图。评估每对解释图之间的相似性,并应用聚类来突出对年龄预测贡献最大的大脑区域。这些区域显示出与脑龄的最高相关性,表明导出的图对它们的模型的特异性。
最后,Wang等人和Feng等人从他们的基于T1w的CNN中检索Grad-CAM注意图,以显示不同区域对于BA预测的相对重要性。具体来说,文献[8]中的工作发现,虽然网络观察整个GM,但注意力模式相当复杂,这表明在预测BA时,brain-PAD更多地与特定特征相关,而不是与GM体积的全局测量相关。冯等人向前进了一步。除了事后的Grad-CAM导出的显著图,他们还应用了专注于部分输入数据的消融分析方法。他们强调了正常老化的神经解剖学贡献模式,为成年人一生中所有年龄阶段额叶区域的突出提供了证据。
总之,我们可以说Interpretability、可因果性和explainability不是同义词,它们提供了模型的不同观点。在BA评估中采用XAI的关键方面可以总结如下:可解释的模型,如线性回归和正则化回归,在BA估计中得到了广泛的应用,但它们各自的解释仍然没有得到广泛的推导。
在最近的论文中,潜在空间中的模型系数的可视化(如tSNE)被越来越多地开发。基于排列和扰动的特征重要性在提取解释中具有中心作用,尤其是那些用于DL模型的解释方法。显著图的方法在DL模型中也被使用,并且主要依赖于基于梯度的方法。
与BA结果的关联研究
在本节中介绍了关于BA的发现和几个影像/非影像变量(例如,临床、环境和遗传因素)之间关联研究的主要论文,目的是提供证据支持这种新的脑龄测量与其他生物学指标之间的相关性。脑龄测量的生物学相关性确实仍在争论中。考虑到BA估计依赖于使用残差预测误差(即来自统计分析的残差)作为汇总测量,一些作者认为基于此的解释可能有缺陷,因为更精确的模型会理想地降低该值。确定其相关性的一个关键因素在于外部验证,特别是将该指数与在相同个体中测量的其他特征相关联,尤其是具有明显的老化显著性的特征。例如,这可能与认知、身体、生活方式和遗传领域有关。
作为最初的尝试,一些作者研究了脑龄值和多种影像特征之间的联系,如皮质厚度、体积、纤维束和FC测量。特别是前者提供了证据,表明脑龄与几个皮质区域的厚度显著相关,包括额叶/颞叶和楔前叶的区域。这些在正常老化中有着突出的作用,支持了脑龄的鲁棒性和相关性。越来越多的大型资料库,包括除神经影像数据以外的信息,给该领域带来了巨大的好处,促进了对更详细和多样化变量的相关性的研究,如UKB资料库的情况。该数据集包括广泛的非成像数据,例如遗传、生活方式因素(例如,锻炼、吸烟状况和酒精摄入)、认知/生物医学测量(例如,流体智力得分、试跑测试、收缩压/舒张压、体重和体重指数)以及来自卫生保健系统的健康结果信息。
文献[3]和[4]的作者是第一批探索这一深度资源并评估他们估计的brain-PAD值和5000多个非成像变量之间关系的人,他们依靠简单的相关性分析和线性回归模型来解释不同的混杂因素。有趣的是,作者证明了较老的大脑与较高的收缩压/舒张压、中风史、糖尿病诊断、吸烟和饮酒有关。值得注意的是,在另一项不同数据集的研究中,这些心血管风险因素和脑龄之间的显著正相关的相同结果也得到了证实,为这些发现的普遍性提供了证据。认知测试中的几项指标也与大脑加速老化显著相关,这是人们在所有情况下都可能预期的方向。这些认知表现的结果与之前的一项研究[13]一致,该研究证明了脑龄与三项重要认知测试(数字替代、试走和反应时间测试)中的较差表现有关,从而证明了这一汇总指标与认知障碍高度相关。
最后,Engemann等人同样在Cam-CAN数据集中发现了脑龄与个人认知健康之间的相关性,较高的脑龄与较低的记忆和快速思维任务分数相关。最近文献[11]也研究了与UKB中选择的特征相关的脑龄,并使用孟德尔随机化分析来研究一些关联的潜在因果性质。结果证明了舒张压升高和大脑老化之间的因果关系,表明预防高血压将对大脑老化产生积极影响。此外,已经在不同的患者组中评估了brain-PAD和几个临床评分之间的关系,例如MS中的扩展残疾状态量表(EDSS)和MCI和AD中的简易精神状态检查(MMSE)。这些研究的重要发现进一步强调了脑龄作为衰老的候选生物标志物和追踪疾病进展的预后工具的重要性。
除了这种趋同的证据,在最近三项关于UKB数据的研究中,作者们更进一步,提出使用脑龄作为遗传关联研究的信息表型。事实上,由于这种测量的生理学基础可能是多种多样的,遗传分析提供了探索影响表型变异的因素的机会,从而能够更深入地理解大脑老化过程及其纵向变化。在[13]中,brain-PAD的全基因组关联研究(GWAS)产生了两种不同的遗传序列变体[也称为单核苷酸多态性(SNPs)];在这项研究中,它们是rs1452628-T和rs2435204-G]与脑沟深度和WM表面积的减少相关。事实上,GWAS有助于任何变量(例如,脑龄)和大量SNP之间的相关性分析,以突出任何显著的现有关联。
此外,文献[13]的作者通过GWAS汇总统计分析调查了遗传力。他们证明了脑龄是可遗传的,这表明了生物相关信号的捕捉,与早期的发现一致[33]。在后一项研究中,作者进行了进一步的分析,以评估brain-PAD和常见脑疾病的遗传底物之间的重叠,从几种疾病的GWAS汇总统计数据开始,如AD、MS和精神分裂症。他们的结果揭示了几个重要的独立基因座,它们是染色体上的特定基因位置,显示了脑龄和所有包括的疾病之间的多效性(即一个基因对许多明显不相关的表型特征的影响)。大多数确定的位点与精神分裂症相关。这第一次证明了对照组的脑龄和普通大脑疾病之间存在重叠基因。最近文献[10]也进行了类似的分析,其中作者探索了62种大脑老化模式提供的丰富信息(参见“基于神经成像的BA预测表型”部分),并使用不同模式的delta估计值进行了单独的遗传分析。有趣的是,虽然单一的全合一脑龄估计没有报告显著的结果,但62种 GWASs的脑老化模式导致了总共156个显著的峰关联。其中,发现了与rs429358的遗传关联,RS 429358是决定载脂蛋白E (APOE)基因等位基因是否为E3的SNP,是与几种神经退行性疾病(包括AD和MCI)相关的主要位点。这些结果证实了评估脑龄的遗传影响的重要性,但同时表明,当产生一个单一的度量标准时,生物特异性可能会被淡化,再次突出了脑龄的附加价值。 分别考虑多模式和多模式BA模式。
总之,与BA研究相关的主要方面有:
1)使用在相同个体中测量的其他特征来验证BA框架和相关测量对于证明脑龄度量的生物学和临床意义是至关重要的。
2)已经证明,在脑龄和一些心血管风险因素以及生活方式测量之间存在积极的显著关联,这意味着,除了其他因素之外,看起来更老的大脑与吸烟/饮酒量增加和高血压有关。
3)遗传分析可以提供深入研究影响个体间预测BA估计值变化的因素的机会。
神经退行性疾病与BA
在这一节中将通过展示最相关的BA研究与一些常见神经退行性疾病特征之间关系的贡献,来理解BA评估的临床相关性问题。研究大脑疾病发作的标记物是BA模型的可能转化应用之一,该模型已经在几项研究中进行,特别是在神经退行性疾病的背景下。事实上,由于这些条件很可能影响生物衰老的速度,BA代表了一种直观和简单的方法来评估这一过程的程度,并可能将年龄相关因素与疾病特异性变化分开。正如预期的那样,在这些文章的大部分中,BA估计值来自MCI和AD患者组。
在他们的开创性工作中,Franke等人证明了与ADNI数据库中的对照组相比,AD患者的大脑PAD明显更高,这表明AD患者的大脑更老。Lowe等人更近一步,将ADNI受试者分为对照组、稳定/进展型MCI患者和AD患者,并进一步分为APOE4携带者/非携带者。特别是,这是APOE基因的等位基因形式,已被证明与AD发病有关。健康和稳定的MCI受试者的估计脑龄分数被证明与进行性MCI和AD受试者的脑龄分数显著不同,这表明在这两类受试者在加速脑老化过程。在同一项研究中,作者分析了几个纵向时间点,表明进行性MCI和AD患者的衰老速度明显快于其他两类患者,APOE4携带者也明显快于非携带者。作者还通过使用整个样本指出了brain-PAD和认知评分之间的现有联系,并使用BA指标而不是APOE4携带者/非携带者的认知表现更准确地预测向AD的转化。帕尔马等人最近报告了类似的发现。此外,利用特征函数可视化,他们显示了不同区域如何根据疾病表型对相关脑龄做出贡献。类似地,Rokicki等人使用几个BA模型和基于排列的特征探测,展示了BA估计值的差异如何能够表征神经退行性疾病的不同病理生理学方面。事实上,他们观察到,使用来自全局T1w图像的脑龄值可以获得区分对照和AD患者的最佳准确性,而来自基于CBF的模型的值对于MCI和控制组来说更具区分力。
Beheshti等人研究了与AD和帕金森病(PD)相关的BA预测。他们的研究表明,从基于GM的模型得到的脑龄值在AD受试者中比在PD受试者中更大,而当从WM得到时,它们在两个类别中更相似(尽管在AD患者中也更高)。有趣的是,这两个模型对PD患者产生了明显不同的结果,这表明多区域BA预测可能有助于更好地描述衰老过程。与帕金森病患者相比,阿尔茨海默病患者与正常人的偏差更大,这表明受试者的大脑看起来更老。作者还进行了脑龄和认知评分之间的部分相关性测试,结果仅与帕金森病受试者的单一认知评估测试显著相关。
尽管MS是一种多因素自身免疫性疾病,但它经常被列为神经退行性疾病,已经在不同的研究中进行了研究。在[33]中,作者纳入了各种大脑疾病,并报告了脑龄值的增加,在精神分裂症、多发性硬化症、轻度认知障碍和痴呆症中观察到最强的影响。他们还使用从感兴趣区域的子组中获得的特征来测试相同的模型,以评估跨组的空间脑龄模式的特异性。他们的发现表明,区域性的估计与全脑分析的估计基本相当,不同疾病之间有一些显著的空间差异。特别是,根据小脑-皮质下特征计算的脑龄在痴呆和MS受试者中更高。此外,关联研究显示,从MS全脑特征得出的脑龄估计值与用于评估残疾程度(EDSS)的主要临床评分相关,而从全脑和小脑皮质下特征得出的脑龄估计值分别与MCI和痴呆患者的MMSE认知功能评估值相关。
最后,Cole等人最近提出了一项对不同MS表型的BA模式的深入分析,并显示与那些受临床孤立综合征影响的患者相比,诊断的MS患者的估计脑龄显著增加。此外,一项纵向分析显示,越来越大的脑龄评估与较差的残疾评估分数呈正相关(EDSS)。他们的发现也证明了这一总结性指标作为残疾状态的预测指标的重要性,以及与原发性进展型MS患者相比,影响复发-缓解型MS患者的更快衰老的存在。
总之,BA在神经退行性疾病中的主要发现是:
1)预测的BA和相应的脑龄是不同条件下的生物学信息测量,代表有待进一步开发的新生物标记。
2)与健康对照组相比,包括MCI、AD和MS在内的几种疾病表现出显著更高的脑龄(即,看起来更老的大脑)。
3)通过使用基于ROI的方法导出多个区域的特征的BA估计值并评估跨疾病组的空间脑龄模式的特异性,出现了有希望的结果。
未决问题和研究方向
大脑老化是一个精致的多维主题,可以从基因到行为的不同尺度上进行研究,它的评估在临床(包括神经科学)和社会层面上跨越了多个领域。正如[2]中所强调的,BA估计的美妙之处在于,它是一个老化的生物标志物,以一个非常容易理解的数字概括复杂的信息,尽管[10]中讨论了它所有可能的局限性。这非常符合XAI的框架,在一个概念(老化)的实例中浓缩了不同信息处理的结果,这个概念包含了基本的认知范畴,因此传达了一个明确的信息。此外,它可以与目前正在研究的其他形式的“身体年龄”相结合,例如,基于生物化学和生理测量,以提供对生物衰老过程的更广泛和更全面的评估[2]。正如一些作者所承认的,仍然有一些相关的问题值得研究。在本节的剩余部分,提供了进一步的研究方向。
BA框架内的新方法
BA预测这一新兴领域正在迅速发展,在过去几年中关于这一主题的论文数量不断增加就证实了这一点。虽然已经探索了不同的方法并取得了满意的结果,但是可以设想对该框架的每个构件进行进一步的开发,从额外的IDP开始,例如,从dMRI/fMRI/ASL数据的基于图形的网络分析以及它们的联合建模开始,这些在当前文献中仍然是未开发的。转到预测方法本身,如[37]中所示,多模态数据的变分自动编码器嵌入可以通过分析BA上下文中获得的潜在空间来改善对输入特征之间的关联的理解,并生成有效模态融合的固有特征聚合。
值得注意的是,建立处理多模态数据的方法是一个重要的方面,应在未来的研究中进一步探索。例如,在[13]中,作者使用CNN模型集成策略,并通过结合一组更简单的基础模型的优势建立预测模型。特别是,他们通过使用多数投票方案和线性回归数据混合器来组合在四个基于T1w的图像上训练的CNN,以组合BA预测,并证明以这些方式组合预测可以减少过拟合并提高准确性。
在可解释性方面,诸如用于特征排序的局部可预测模型不可知解释和用于特征可视化的Grad-CAM++或分层相关性传播的方法仍未得到充分探索,但在BA预测和基于MRI的DL模型中显示出有希望的初步结果。除了所有这些方面,仍然需要对BA级联中的特定元素进行进一步的研究,例如年龄偏差校正、适当的混杂模型、BA模型的外部验证以及定义最佳训练年龄范围等问题。越来越多的大型数据集(其中一些涵盖成年人的寿命和不同的疾病)将有助于进一步挖掘这些方法问题,并巩固BA估计的稳定性。
深入研究遗传学
从“基于神经影像的BA预测表型”和“BA预测建模:从统计方法到DL”部分的调查中可以明显看出,遗传决定子(GDs)的利用还处于起步阶段。虽然有大量文献可用于将brain-PAD与遗传变异联系起来的关联研究,无论是作为单独的SNPs还是在多基因风险评分中的blow down,但将此类信息纳入建模大多是未经探索的,但对它的研究可以为BA预测中GDs与非GD特征(如IDPs)的相对权重带来有价值的见解。XAI将是这方面的使能技术,因为它提供了工具来“打开复杂模型的盒子”,如深度CNN,并解释处理结果以及对有助于结果的特征进行排序并量化其影响。
对GDs的利用也可以在许多其他方面得到有效利用。正如[2]中提到的,端粒长度有可能成为衰老的生物标志物。目前有一些证据表明,端粒长度随着年龄的增长而减少,尽管这两个变量之间的联系仍有待阐明。以间接的方式对此进行评估,例如,通过孟德尔随机化调查IDPs和端粒长度之间的联系,可能会对该主题有所启发。同样,脱氧核糖核酸甲基化也可能发挥作用,这一事实被用来塑造所谓的表遗传时钟。这些研究可以提供新的特征,有助于修剪整个衰老相关特征集的树,从而在特征空间星座中追踪从测量到脑龄的最佳路径。最后,将XAI方法提供的与BA预测最相关的区域特征信息与Allen人脑图谱中的基因表达(包括与中枢生物功能相关的几个基因的核糖核酸强度)相结合,可能会为更深入地了解影响脑老化的特定遗传因素打开新的视角。
总结:
BA预测范式的框架已被证明在理解个体生物年龄的基础元素方面具有重要价值,因此在描述不同的老化轨迹方面也具有重要价值。与此同时,它提供了一种简单而有效的方法来捕捉对大脑机制的新见解,有可能及时识别未来认知老化和年龄相关的大脑疾病的风险。在这种情况下,ML和DL方法显示出巨大的前景,强调了向多种方法联运转变的重要性。但与此同时,有必要进一步探索对非典型群体(例如老化疾病或者发育疾病)提供的具体BA估计数。XAI的应用不仅是有用和必要的,而且也为BA预测提供了巨大的机会。一方面,线性和潜在变量模型中的XAI有助于在一个对人类友好的框架中直接检测和可视化,阐明最重要的特征,而另一方面,它使复杂和深度模型的应用成为可能,可以通过增强它们的可信度来减少它们的不透明性。




 本文探讨了大脑年龄预测方法及人工智能可解释性在该领域的应用。研究利用神经成像技术和机器学习方法准确预测个体大脑年龄,并通过AI可解释性技术揭示预测背后的生物学机制。
本文探讨了大脑年龄预测方法及人工智能可解释性在该领域的应用。研究利用神经成像技术和机器学习方法准确预测个体大脑年龄,并通过AI可解释性技术揭示预测背后的生物学机制。

















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








