1、原子结构
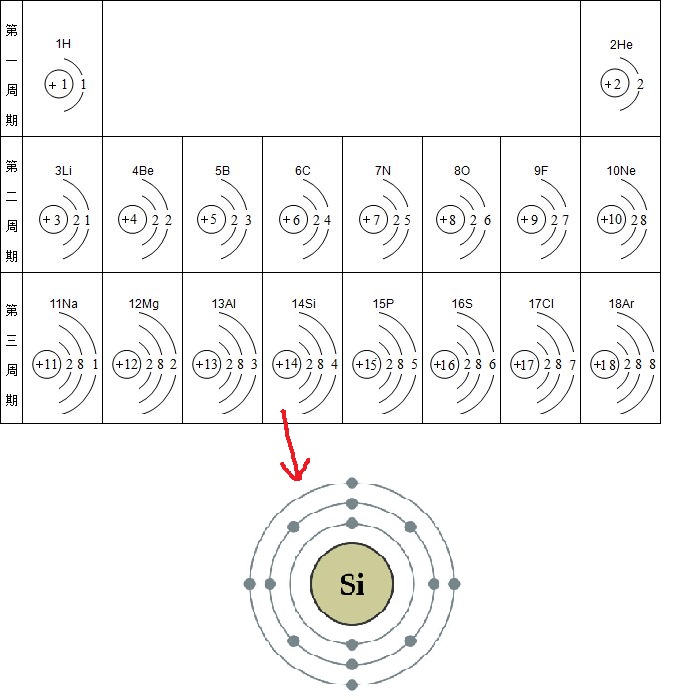
原子由原子核和围绕原子核旋转的电子构成。如果将原子比作一棒球场,那么原子核大大小不比一个棒球大,但原子的所有重量都集中在原子核上,而电子只相当于棒球场上的苍蝇,所占空间相比来说也是极小的。原子核带正电荷,电子带负电荷。原子内正电荷和负电荷数量相等,所以原子整体是中性的。电子围绕原子核运动,和地球围绕太阳远行相似。在核的引力作用下,电子分成几层(又叫能带 energy band)按完全确定的轨道运行,而且各层所能容纳的电子数目也有一定规律。以硅元素为例,原子核周围的14个电子组成三层环,围绕原子核运动。从里往外数,第一层环上有其2个电子,其余依次为8、4个电子。凡是环上的电子数为2、8、18时.这些环上的电子总是比较稳定的,这类元素一般形成绝缘体。若环上的电子数不等于以上各数时,这些环上的电子总是不太稳定。于最外层的价电子离核比较远,所受引力最小,所以最容易受外界影响而形成自由电子。导体和半导体都是靠最外层的自由电子进行导电的。
而每个原子核除了吸引自己的价电子外,还吸引相邻原子的价电子。因此,两个相邻原子的价电子便成对地存在。这一对电子同时受这两个原子核的吸引,为它们所“共有”。这两个相邻原子也通过这个电子对被联系在一起。这样,电子对就好像起了键(联结)的作用,我们叫它共价键。每一个硅原子以其4个价电子与其他4个硅原子的价电子组成4个共价键而达到稳定状态。在理想情况下,硅晶体中所有的价电子都织成了电子对,因此没有自由电子,这时硅晶体是不易导电的。纯硅晶体也不是像绝缘体一样完全不导电,所以这类固态成为半导体。在外力作用下电子会逃脱共价键,形成空穴和自由电子,均被称作载流子。以硅晶体结构为例:








 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章















 8973
8973











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








