随着新法规和新政策的密集出台,医疗器械行业正迎来一场深刻的运营模式变革。2023年6月,随着医疗器械唯一标识(UDI)的推进,行业迎来了关键转折点。
一、UDI实施,医疗器械“实名制”管理
自2023年2月起,国家药监局、卫健委、医保局联合发布《关于做好第三批实施医疗器械唯一标识工作的公告》,明确了103种临床需求量大、涉及集中带量采购和医疗美容等领域的第二类医疗器械,作为UDI实施的重点品种。这些品种覆盖了超声、激光、高频/射频手术设备等多个关键领域。
从2024年6月1日起,相关医疗器械需具备UDI,并遵循严格的管理流程。企业需在注册系统中提交产品标识,确保数据真实、准确、完整、可追溯。这一变革不仅提升了医疗器械的监管水平,更为患者提供了更加安全、可靠的医疗保障。
二、UDI信息查询,保障合规与可靠
查询UDI信息,可通过国家药监局官网、医疗器械注册证查询平台或第三方数据库等工具(如数
屿医械数据库)您可以使用这些工具便捷地查询UDI信息。

在选定查询途径后,请按照平台或工具的提示,输入医疗器械的相关信息进行查询。
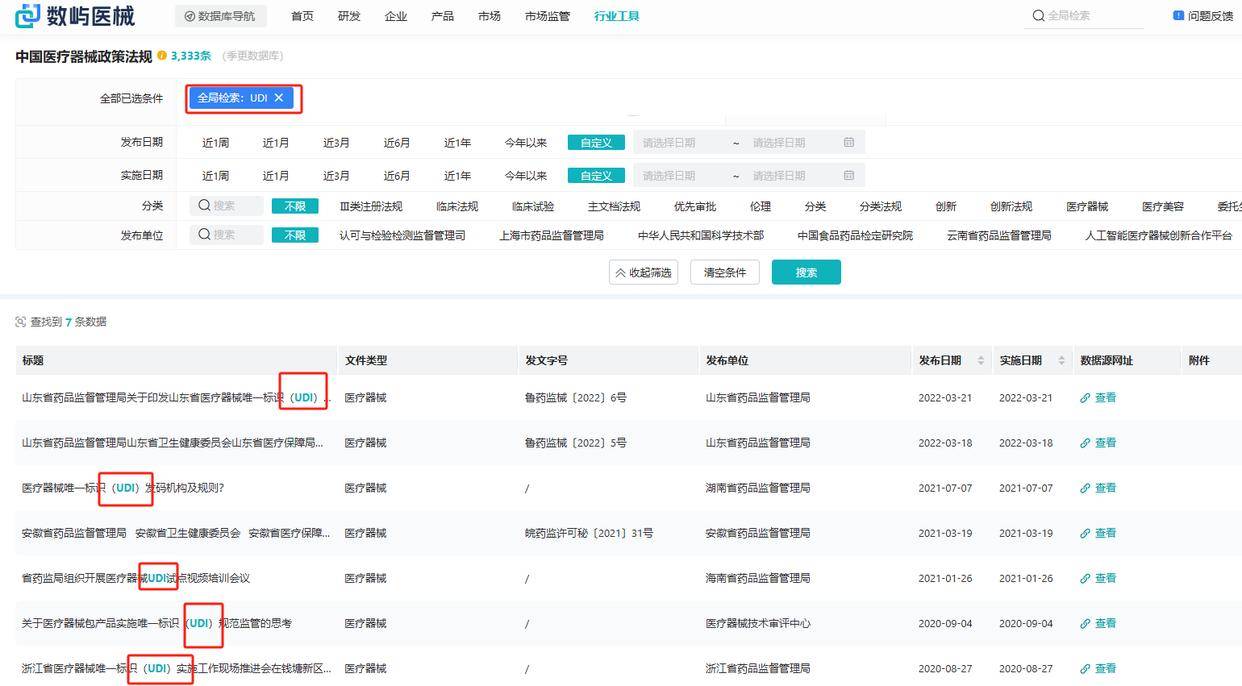
通常,输入器械的名称、型号、注册证号码等详细信息,可以获取更精确的查询结果。
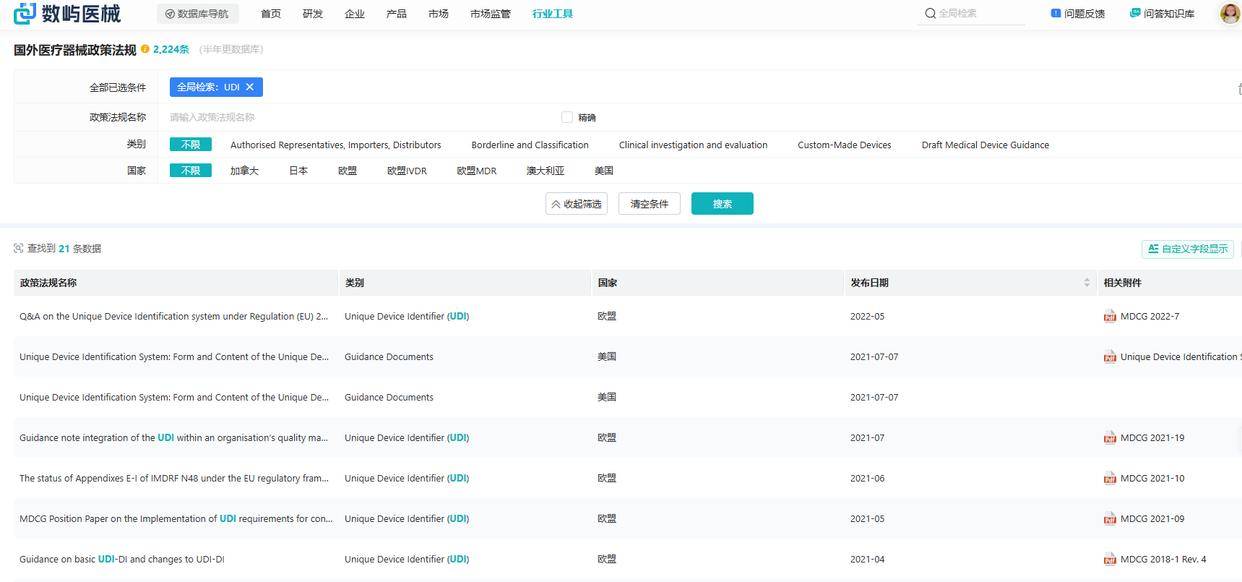
国外的相关UDI数据查询,政策法规相关附件。

查询完成后,您将获得包含器械生产商、生产日期、有效期限、批次号等信息的UDI数据,从而更全面地了解该医疗器械的合规性和可靠性。
输入准确的医疗器械名称、型号或注册证号码,即可获取包含生产商、生产日期、有效期限等关键信息的UDI数据。
三、医疗领域政策动态更新
- 耗材国采落地:2024年5-6月,第四批耗材国采结果将正式落地,涉及人工晶体类及运动医学类耗材,市场规模庞大,为患者带来经济实惠的治疗选择。
- 全国耗材集采执行:浙江医保局牵头的冠脉血管内超声诊断导管和输注泵两类耗材集采结果将在2024年5-6月全国范围内开始执行,覆盖32+29个省份。
- 县域医共体建设:到2024年6月底前,全国将全面推开紧密型县域医共体建设,提升基层医疗服务能力。
- 政府采购新方式:2024年6月1日起实施全新的政府采购方式,鼓励医疗器械研发创新。
- 医疗器械委托生产新规:自2024年6月1日起,医疗器械委托生产实施新规定,强化注册人主体责任。
- 新修订《公司法》施行:2024年7月1日起,新修订的《公司法》正式施行,规范公司治理结构。
这一系列政策的出台与实施,将进一步推动医疗器械行业的健康发展,为患者带来更加安全、高效、经济的医疗服务。





















 594
594

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








