qEV尺寸排阻外泌体分离柱是一种用于分离和纯化外泌体的实验工具,通过尺寸排阻色谱(Size Exclusion Chromatography, SEC)技术实现外泌体的高效分离。这种方法基于颗粒大小的不同将样本中的外泌体与其他成分(如蛋白质、脂质体、微粒等)分离开来。以下是关于qEV尺寸排阻外泌体分离柱的详细介绍:
qEV尺寸排阻外泌体分离柱的原理
qEV分离柱通过一个多孔的填料实现分离,填料的孔径设计允许特定大小的分子通过。样本溶液通过柱子时,大分子(如外泌体)由于体积较大,不能进入填料的孔隙,因而较早从柱子中流出;而小分子(如小分子蛋白质等)则会进入填料孔隙,路径较长,因而较晚流出。通过这种方式,可以实现对不同大小的分子的分离。
| qEV尺寸排阻外泌体分离柱-操作流程(点击观看视频)
-
用洗脱缓冲液冲洗柱子。
-
装入500μL样品。
-
最开始的3ml是空隙体积,继续向分离柱中添加PBS以洗脱囊泡(外泌体)。
-
收集空隙体积后的1.5mL液体为高纯度外泌体。
| qEV尺寸排阻外泌体分离柱-优势
● 高纯度:去除99%以上的可溶性蛋白质,去除95%以上高密度脂蛋白
● 无损伤:保持细胞外囊泡的完整性和生物功能
● 标准化:每根分离柱均经过标准化、质量保证,并通过ISO13485标准认证
● 可靠性:只要15min就可以得到完整外泌体样本,已经在大规模的实验室试验得到证实
● 适用性:适用于多种类型样品的外泌体提取,包括:血清、血浆、尿液、细胞上清、脑脊液、唾液等;尤其适用于外泌体功能研究中,用于细胞培养或动物注射的高纯度外泌体的获得
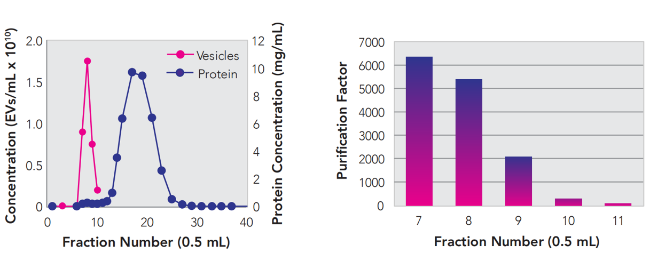
如上图所示,血清样品中收集的组分,用qNano其进行定量测量。在280纳米处用吸光度法测定蛋白质的相对浓度。数据表明,收集的第7至9组分具有最高浓度的囊泡(外泌体),而污染的血清蛋白洗脱的分数为第11至30组分(左图)。通过比较分离前和分离后的囊泡(外泌体)与蛋白质浓度比,第7组分的囊泡富集量为蛋白质的6000倍(右图)。根据样品的不同,如果下游分析分别需要更高的囊泡(外泌体)纯度或更高的囊泡(外泌体)产量,可将第7至9部分或第7至11部分汇集在一起。
| qEV尺寸排阻外泌体分离柱-产品规格

qEV与超速离心技术的对比
案例1 尺寸排阻SEC比超离UC获取外泌体的纯度更高

该文献通过对滑膜液经过相同的预处理后,分别使用超离、密度梯度离心和尺寸排阻进行外泌体的分离。并通过WB、TEM对其进行鉴定分析。
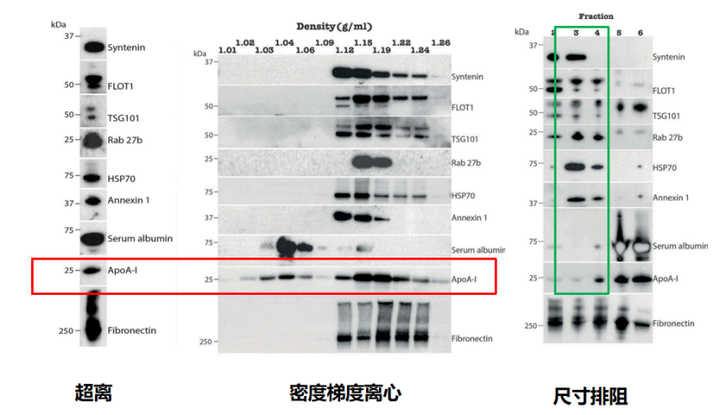
上图中红框所示的ApoA-1是HDL的标志物,可以发现UC和DGC都无法有效去除HDL,而SEC的WB图中,外泌体标志物的出现和HDL标志物和血清白蛋白的出现几乎不存在时间上的重叠,所以SEC可以收集到比较纯净的外泌体。
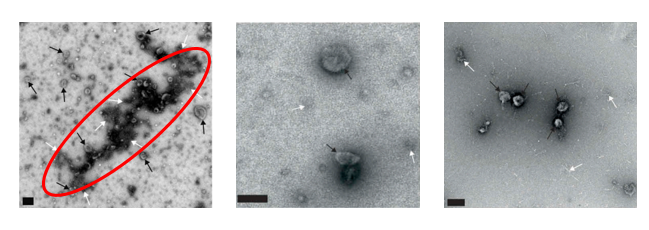
上图中超离电镜下的图像,不仅背景杂质多,而且发生了聚集现象,这种聚集会对下游分析产生较大不利影响。相比之下,SEC的背景纯净,外泌体特征明显。
案例2 尺寸排阻SEC比超离UC获取外泌体生物活性更强

该实验研究了使用超离UC和尺寸排阻SEC分离的心肌祖细胞(HMECs)培养液的外泌体的功能可能的差异。通过外泌体刺激细胞,诱导EKR磷酸化,然后通过比较外泌体刺激后的pEKR和EKR的比率,来评价不同分离方法制备外泌体的功能活性。
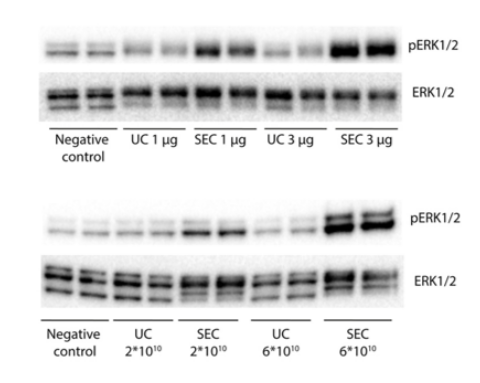
上图WB显示,在相同条件下,无论总蛋白量变化还是粒子数变化,用SEC的方法比超离他的pERK / ERK比率更高,表明SEC收集到的外泌体具有更高的生物活性。
案例3 尺寸排阻SEC比超离UTC更适合进行血浆外泌体蛋白质组学分析
该文献通过高分辨质谱分析,比较了SEC和UTC分离的血浆外泌体,在五次技术重复中鉴定的蛋白数量、信号强度等方面的差异。结果发现,相较于超离,SEC得到的外泌体,蛋白鉴定数量更多(图A,SEC 1,268±102,UTC 319±45),相同蛋白的定量CV值更小(图B,SEC 562种蛋白质的CV低于25%,而UTC只有73种蛋白质达到这一阈值),且相同外泌体marker蛋白,SEC信号值普遍比UTC更高(图C)。
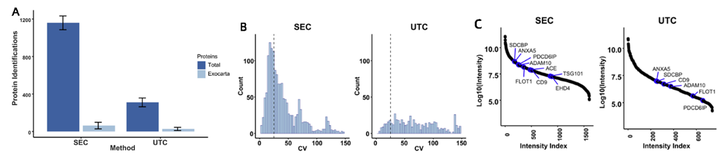
添加图片注释,不超过 140 字(可选)
上述几篇文献将尺寸排阻SEC与超离UC、密度梯度离心DGC在收集到外泌体的纯度、生物活性和得率方面作比较,通过实验数据、电镜图、WB图像,发现SEC相较于其他两种分离方法,获取的外泌体纯度更高、生物活性更强、更适合蛋白组学实验。
结语
qEV尺寸排阻外泌体分离柱以其高效、简便、非破坏性的特点,成为外泌体研究中的重要工具。通过这种技术,研究人员可以获得高纯度的外泌体样本,进一步推动外泌体在基础研究、临床应用和药物开发中的应用。华盈生物致力于提供高品质的外泌体研究服务,帮助科研人员在这一领域取得更多突破性成果。






















 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








