虽然功能性磁共振成像(fMRI)研究主要集中在灰质上,但最近的研究一致发现,血氧水平依赖(BOLD)信号可以在白质中可靠地检测到,功能连接(FC)已被组织成白质中的分布式网络。然而,尚不清楚这种白质FC是否反映了潜在的电生理同步。为了解决这个问题,我们使用了16例耐药癫痫患者的颅内立体脑电图(SEEG)和静息状态功能磁共振成像(fMRI)数据。我们发现BOLD FC与SEEG FC在白质中相关,并且这一结果在每个参与者的广泛频段范围内是一致的。通过纳入扩散谱成像数据,我们还发现SEEG和fMRI的白质FC与白质结构连通性相关,表明解剖纤维束是白质功能同步的基础。这些结果为白质BOLD FC的电生理和结构基础提供了证据,它可能是精神和神经疾病的潜在生物标志物。
功能性磁共振成像(fMRI)已被广泛用于基于人脑血氧水平依赖性(BOLD)对比来定位神经活动。虽然fMRI研究主要集中在灰质上,但最近来自多个独立研究的证据表明,在静息状态和各种任务状态下,BOLD信号可以在白质中可靠地检测到。这些研究一致表明,白质BOLD信号并非像之前认为的那样是噪声,而是表现出与通道和任务特定功率谱不同的模式,这可能与潜在的神经活动有关。此外,最近的研究利用BOLD fMRI表征了白质的血流动力学反应功能和神经可塑性。通过测量两个白质区域之间静息状态BOLD信号(称为“功能连接(FC)”)的时间同步,先前的研究发现,白质显示出一种相互作用的功能网络的内在组织,类似于灰质。例如,Peer等人将白质分成12个对称的功能网络,这些功能网络被组织成三层,与皮层灰质功能网络的关联程度不同。Huang等人进一步证明,白质功能网络在两个独立的数据集上具有高度可重复性,并且这些网络被组织成具有反相关连通性的两组。此外,研究表明,白质BOLD FC受解剖白质束结构的限制,并在基因表达谱中编码。先前的研究还表明,白质BOLD FC可能是多种精神和神经疾病的神经标志物,包括精神分裂症、抑郁症、阿尔茨海默病和帕金森病。然而,目前尚不清楚白质BOLD FC是否反映了白质中颅内电生理信号的潜在神经同步,还是仅仅是一种血管现象。颅内脑电图(IEEG)是一种记录大脑局部场电位(LFP)的侵入性方法,可用于确定耐药癫痫发作的确切来源。它通常包括皮质电图(ECoG),包括在暴露的皮质表面植入的电极网格,以及立体定向脑电图(SEEG),包括穿透大脑的深度电极。在一项具有里程碑意义的研究中,Betzel等人证明颅内电生理FC(定义为来自两个ECoG电极的LFP时间序列之间的相关性)与灰质中的BOLD FC具有相似的网络结构。然而,目前尚不清楚白质是否也是如此。与ECoG相比,SEEG电极通常通过白质穿透大脑,具有4-18个触点,两个相邻触点之间的中心到中心间距为2-10 mm,为记录白质组织中的LFP提供了机会。最近,Revell等人发现,尽管SEEG数据中白质信号较弱,但白质FC比灰质FC更强。然而,本研究并未寻求电生理信号与白质BOLD FC之间的相关性。
在这项研究中,我们旨在利用SEEG数据为白质BOLD FC的颅内电生理基础提供证据。由于先前的研究一致表明,白质连通性是大脑区域之间功能通信动态的结构基础,我们假设BOLD和SEEG白质FC都受到潜在白质结构连通性的限制。我们使用来自16名耐药癫痫患者的多模态数据集来测试这些预测,每个患者都完成了颅内SEEG,无创静息状态BOLD fMRI和高质量扩散谱成像(DSI, ~24分钟采集)。我们的研究结果表明,在每个参与者中,BOLD白质FC与SEEG白质FC在很宽的频带范围内高度相关,并且BOLD和SEEG FC都与白质结构连接高度相关。
1. 结果
1.1 BOLD和SEEG白质FC
我们研究了16例需要SEEG定位癫痫发作的耐药癫痫患者间歇期的颅内SEEG记录。每个参与者有6-12个电极,每个电极有5-16个接触点。使用先验白质分割图(WMPM)图集,我们发现白质接触主要集中在颞叶、额叶和顶叶颞叶区域。所有参与者术前均进行了结构MRI、功能MRI、DSI和x射线计算机断层扫描(CT)。我们根据MRI和CT的结构数据定位所有接触点的坐标,然后识别白质内的接触点。与之前的工作一样,SEEG数据被处理并过滤成7个频段(1-4、4-8、8-13、13-30、30-40、40-70和70-170 Hz)。我们计算了所有白质接触时间序列之间的Pearson相关性,以生成SEEG白质FC。接下来,我们通过计算所有ROI的BOLD fMRI时间序列之间的Pearson相关性来估计BOLD白质FC, ROI被定义为以白质接触为中心的球体。
1.2 在单个参与者中,BOLD和SEEG白质FC高度相关
我们首先评估了单个参与者的BOLD和SEEG白质FC之间的对应关系。为了可视化白质FC,我们显示了两个白质接触点(图1a)的SEEG (1-4 Hz)和BOLD信号的时间序列,分别具有MNI坐标(46,−14,−20)和(34,−4,−23)。通过目视检查,SEEG和BOLD时间序列高度同步,表明BOLD fMRI (r = 0.52)和SEEG (r = 0.55)数据显示两个白质接触之间存在FC。接下来,我们并排描绘了BOLD和SEEG (1-4 Hz)白质FC矩阵的上三角形,它们呈现出高度相似的模式(图1b)。特别是,BOLD FC中具有强连通性的区域对在SEEG FC中也具有强连通性。我们接下来使用Spearman的秩相关来评估两个FC矩阵之间的相似性,因为FC不是正态分布的。在评估相关性之前,我们回归了两个矩阵中区域对之间的欧几里得距离,正如之前的研究报道的距离与FC之间的关联。我们发现BOLD和SEEG白质FC显著相关,跨越所有区域对(图1c)。最后,我们观察到,BOLD和SEEG白质FC之间的Spearman 's秩相关在所有频段均显著(图1 d)。
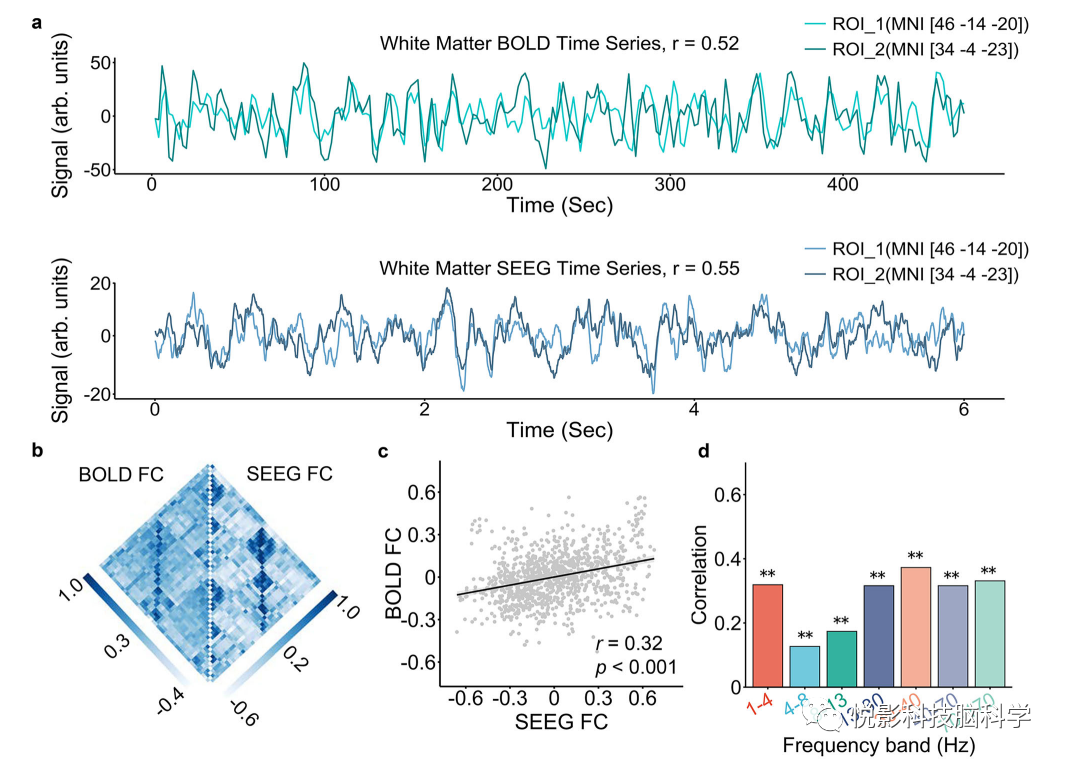
图1 BOLD和SEEG白质FC在单个参与者中是相关的
1.3 每个参与者的BOLD和SEEG白质FC均相关
在证明了BOLD和SEEG白质FC在单个参与者中高度相似之后,我们接下来评估了这一现象是否可以在其他15名参与者中重现。通过重复上述过程,我们发现对于其他15名参与者,在从两个FC矩阵中回归欧氏距离后,BOLD和SEEG白质FC在所有频段的所有区域对中都是显著相关的(图2)。总体而言,所有参与者的BOLD和SEEG白质FC之间的中位数Spearman等级相关性在所有频段中都高于r = 0.19 (1-4 Hz:中位数r = 0.19;4-8 Hz:中位数r = 0.23;8-13 Hz:中位数r = 0.21;13-30 Hz:中位数r = 0.31;30-40 Hz:中位数r = 0.31;40-70 Hz:中位数r = 0.28;70-170 Hz:中位数r = 0.25。图2)。这些结果表明,与灰质一样,BOLD FC也反映了白质中颅内电生理信号(LFP)的同步性,为白质BOLD FC的电生理基础提供了证据。
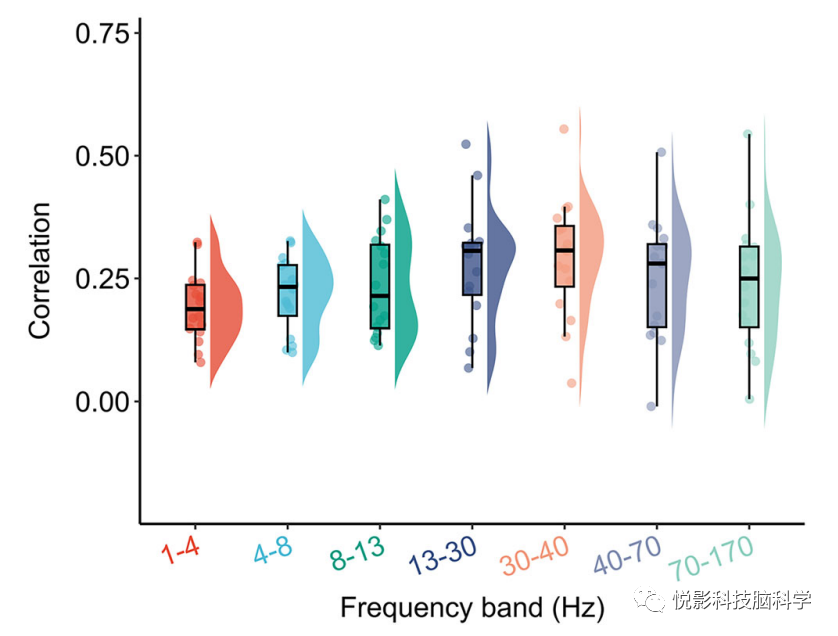
图2 所有16名参与者在所有频段的BOLD和SEEG白质FC之间的相关性
1.4 敏感性分析
我们进行了一系列额外的分析,以验证我们的结果对方法变化的稳健性。有关所有结果的详情,请参阅补充资料。简而言之,我们证明了我们的结果对fMRI处理中参数的变化具有鲁棒性,包括在原生空间而不是标准空间中分析数据,使用0.01-0.08 Hz的带通滤波范围而不是0.01-0.2 Hz,在预处理期间回归出全局和CSF信号。并使用7个体素邻居或27个体素邻居来定义用于BOLD FC计算的ROI。
我们的结果对SEEG数据处理过程中参数的变化也具有鲁棒性。我们使用了10段连续的SEEG时间序列数据,每段数据的长度分别为6 s。在这里,我们分别测试了10个长度为4 s或8 s的片段,结果与我们的主要结果相似。在主要分析中,我们使用Pearson’s相关性来评估SEEG FC,在这里我们发现基于相干的SEEG FC也与BOLD FC表现出类似的相关性。
1.5 结构连接限制了BOLD和SEEG白质FC
在证明了白质BOLD FC的潜在颅内电生理基础之后,我们检查了白质FC的结构连接基础。使用高质量的DSI数据(~24分钟扫描),我们重建了每个参与者的全脑白质纤维束。接下来,我们通过将网络节点定义为以每个接触点坐标为中心的球体,并将网络边缘定义为两个球体之间的白质束的数量,构建了结构连接矩阵(或结构网络)。目测显示,白质结构连通性的网络矩阵与BOLD白质FC相似,通常表现为高FC和高结构连通性(sub1,图3a)。值得注意的是,结构网络是稀疏的,有许多零连接,这表明许多FC是通过沿着结构连接的间接通信出现的。通过定量评估具有非零结构连接的区域对之间的Spearman等级相关性,我们发现在回归到两个矩阵的距离后,结构连接与BOLD白质FC显著相关(sub1, r = 0.16, pFDR<0.001图3b)。最后,我们的结果显示,在剔除距离后,所有参与者的结构连通性都与BOLD白质FC相关(中位数r = 0.30,图3c)。我们接下来评估了结构连通性和SEEG白质FC之间的耦合,并将两者之间的距离进行了回归。与BOLD FC相似,SEEG白质FC (1-4 Hz)也显著相关,具有非零结构连接的区域对之间的结构连通性(sub1,图3d, e)。我们还发现,所有参与者的SEEG白质FC与结构连通性之间的中位数Spearman等级相关性在每个频段(1-4 Hz:中位数r = 0.22;4-8 Hz:中位数r = 0.23;8-13 Hz:中位数r = 0.31;13-30 Hz:中位数r = 0.34;30-40 Hz:中位数r = 0.33;40-70 Hz:中位数r = 0.33;70-170 Hz:中位数r = 0.31;图3 f)。对于其他7名参与者,相关性是显著的,3名受试者5个频带差异均显著。其余1名参与者(sub08)无显著相关性。总的来说,这些结果表明结构连通性和SEEG FC之间的耦合在不同的频段和个体之间大多是可复制的。
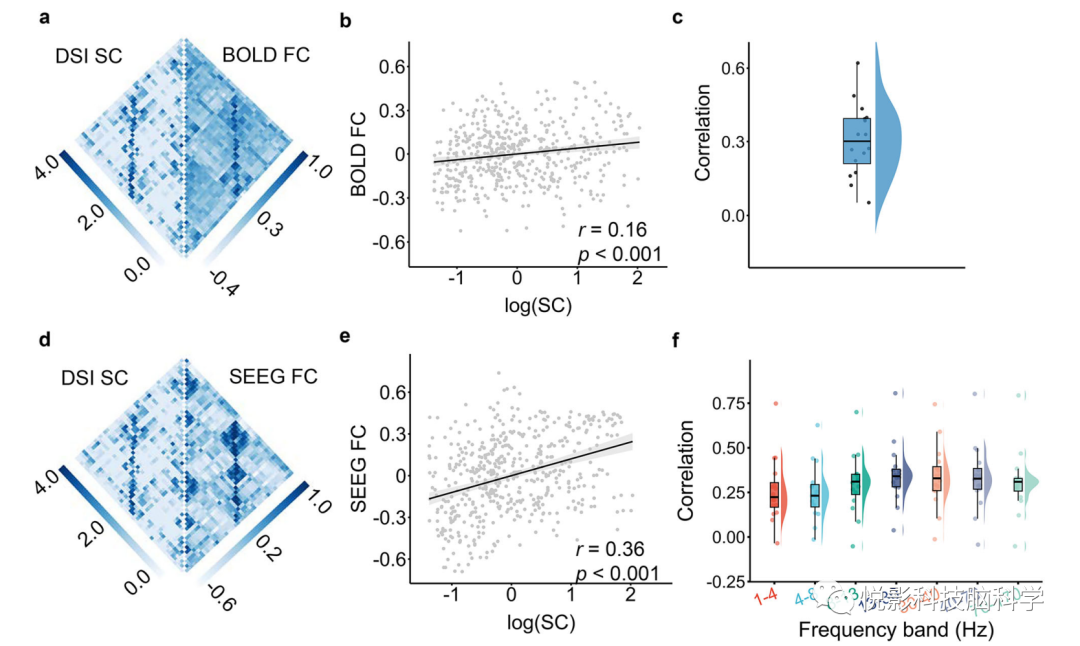
图3 白质结构连通性限制了BOLD和SEEG白质FC
2. 讨论
本研究利用多模态数据集(包括颅内SEEG、静息态fMRI和DSI),从16例耐药癫痫患者中证实了白质BOLD FC的电生理和结构基础。我们发现,BOLD FC与白质中的SEEG FC相关,并且这一结果在广泛的频段范围内对每个参与者都是一致的。此外,SEEG和BOLD fMRI的白质FC与所有区域对的结构连通性呈正相关,表明解剖结构连通性限制了白质的功能动态。我们的研究建立在最近的工作基础上,表明BOLD fMRI信号可以在白质束中可靠地检测到,白质束对任务负荷表现出不同的反应。与灰质一样,BOLD信号的自发波动在白质中两个空间分离的区域之间同步,这种功能连接被组织成内在的功能网络。先前的研究表明,白质中的BOLD FC可能是精神疾病和神经疾病的潜在神经标志物。我们的研究结果表明,白质BOLD FC反映了白质中潜在的颅内神经活动(即LFPs)的同步,为这些研究提供了颅内电生理基础。我们的研究结果表明,白质BOLD FC与白质电生理FC相关,这是通过颅内SEEG记录计算的。这种关联在广泛的频带范围和每个参与者中都是显著的,这有力地表明了白质中BOLD FC的电生理基础。这一结果与先前在灰质中的发现一致。Logothetis等人在一项具有里程碑意义的研究中发现,灰质中的BOLD fMRI信号反映了潜在的LFPs,为基于BOLD fMRI的神经科学研究奠定了基础。最近,Betzel等人证明皮质区域之间的FC在BOLD fMRI和颅内ECoG数据之间是相似的。然而,这些发现仅限于灰质,而我们的工作提供的证据表明,这也适用于白质。几十年来,白质在功能性脑研究中一直被忽视;然而,我们目前的工作和最近的一系列研究一致表明,白质携带特定的、同步的功能信号。例如,最近的研究描述了白质中的BOLD血流动力学反应功能,它显示任务和通道特异性模式,与灰质中的不同。研究还表明,BOLD fMRI可以检测运动学习引起的白质束功能性神经可塑性。最近的一项研究发现,尽管白质信号较弱,但白质中的FC高于灰质。既往研究一致表明,神经元细胞体存在于白质组织深部,神经递质囊泡直接释放到白质,这可能是白质功能信号的潜在神经生物学机制。我们发现,BOLD fMRI和SEEG数据中的白质FC与结构连通性高度相关,这是使用高质量DSI数据集对白质束进行确定性纤维跟踪构建的。先前的研究一致发现,灰质区域之间的FC受到结构连通性的限制,我们的研究结果表明,白质区域之间的FC也是如此。更重要的是,无论是使用BOLD fMRI还是颅内SEEG,白质FC都与结构连通性一致,强调了观察结果的稳健性。我们的结果也与最近的研究一致,表明不同的白质束在静息状态和对刺激的反应中表现出不同的BOLD激活模式。
这项研究有几个潜在的局限性。首先,我们使用了16例耐药癫痫患者的小样本。然而,应该注意的是,每个参与者都进行了SEEG,静息状态BOLD fMRI和DSI采集。更重要的是,我们的结果几乎可以在16名参与者中复制。因此,我们期望这个结果在大范围的样品中是可重复的。其次,临床确定的SEEG记录在接触次数有限的白质中分布稀疏,因此只覆盖了一小部分离散的大脑区域。然而,由于每个参与者在不同的白质区域有接触,当我们汇总所有参与者的结果时,我们的数据覆盖了大脑的很大一部分。未来的研究应该利用大量耐药癫痫患者的SEEG记录来收集全脑数据。第三,我们的BOLD fMRI和SEEG数据是在不同的会话中获得的,这可能会引入额外的可变性。未来的研究应通过同时获取BOLD fMRI和SEEG来评估白质BOLD信号的电生理基础。第四,本文报道的研究结果是在癫痫发作严重程度需要手术干预的难治性癫痫患者中进行评估的。我们的结果是否可以推广到健康人群还不清楚。最后,SEEG测量神经群的LFP,未来的研究可能会进一步评估BOLD FC是否也反映了使用阵列等其他技术的神经元尖峰。尽管存在这些局限性,但我们为白质BOLD FC的颅内电生理和结构基础提供了证据,这清楚地表明白质BOLD FC反映了神经活动的同步,并受到潜在结构连接的约束。我们的数据为白质中BOLD信号同步的起源和解释开辟了一条途径,并为探索白质BOLD FC作为精神和神经疾病的潜在神经标志物提供了基础。
3. 方法
3.1 被试
我们纳入了首都医科大学宣武医院耐药癫痫患者,这些患者需要SEEG监测以确定癫痫发作的确切来源。从84名参与者的数据库中,我们选择了16名具有完整的临床SEEG记录以及术前结构,扩散,功能数据的患者核磁共振成像和术后x线CT。参与者年龄从19岁到37岁,平均年龄28.2岁,标准差(SD)为4.9岁;该样本包括9名男性和7名女性。所有受试者均提供知情同意,所有研究程序均经首都医科大学宣武医院机构审查委员会批准。
3.2 MRI数据预处理
使用fMRIPrep工具箱和可扩展连接管道(XCP) Engine对结构和功能图像进行预处理,其中使用的工具来自FSL、AFNI、ANTs和FreeSurfer (https:// surfer.nmr.mgh.harvard.edu/).)该流程包括(1)t1加权图像的强度非均匀性校正和颅骨剥离;(2) T1分割为灰质、白质和脑脊液;(3)切片定时校正;(4)磁场不均匀性引起的磁化率畸变校正;(5)将所有帧重新排列到选定的参考帧;(6)将功能数据与结构图像进行共配准;(7)归一化到MNI标准空间;(8)淡化和删除任何线性趋势;(9)对24个运动参数进行回归,包括6个逐帧运动估计、每一个参数的导数、每一个参数的二次项及其导数;(10)通频带在0.01 ~ 0.2 Hz之间的带通滤波。我们从数据中删除了最初的五个帧。最后,为了便于分析,数据被重新采样到2毫米各向同性分辨率。DSI数据集使用QSIPrep pipeline进行预处理,该管道工具箱是基于FSL和ANTs等其他工具箱进行弥散MRI数据处理的管道工具箱。预处理步骤包括:(1)将所有图像和bvecs转换成一致的方向系统;(2)采用Marchenko-Pastur (MP)-PCA、Gibbs去环和B1偏置校正对图像进行去噪;(3)对所有b = 0图像的强度进行归一化;(4)利用SHORELine技术对头部运动进行估计和校正,该技术首先将非0图像对齐到0图像,然后使用留一程序创建目标信号图像,并将留一图像及其对应向量配准到目标;(5)生成b = 0的模板图像,并将所有扩散加权图像配准到模板中;(6)将所有图像配准到单个t1加权图像。
3.3 BOLD和SEEG白质FC计算
在白质内的每个接触点,从一个半径为3mm的球体中提取白质BOLD信号的平均时间序列,该球体由相邻表面和边缘的19个相邻体素组成。白质BOLD FC被计算为每对白质接触时间序列之间的Pearson相关。对于SEEG数据,我们采用带通滤波将信号滤波到7个不同的频段(1-4 Hz、4-8 Hz、8-13 Hz、13-30 Hz、30-40 Hz、40-70 Hz和70-170 Hz)。白质SEEG FC被估计为每对白质接触的SEEG信号之间的Pearson相关性。最后,我们获得了每个参与者的白质BOLD FC和SEEG FC矩阵。BOLD FC和SEEG FC矩阵共享相同的大脑区域,这些区域由接触的位置定义,使两种矩阵具有可比性。对于每个参与者,我们选择了一个长度为60秒的SEEG时间序列,并将其分为10个片段,每个片段包含6秒的窗口大小。为了提高SEEG数据的稳定性和信噪比,我们计算了十个片段的平均SEEG时间序列。最后,我们根据这个平均时间序列计算白质SEEG FC。
3.4 使用DSI构建结构连接体
我们使用DSI Studio (http://dsi-studio.labsolver.org)为每个参与者构建了一个结构连接矩阵。我们首先将b表中的方向与总体平均模板进行了比较,并量化了受限扩散。采用广义q采样成像方法,生成扩散采样长度比为1.25的方向分布函数(ODF)图。基于ODF,我们使用基于定量各向异性的确定性纤维跟踪算法重建了全脑白质束。我们使用随机定量各向异性阈值。为了构建白质连通性矩阵,我们将ROI定义为半径为1体素的球体,其中包括7个相邻体素的表面,围绕着白质中的接触点。每个连通性的强度定义为每个ROI对之间互连光纤束的数量。
参考文献:Intracranial electrophysiological and structural basis of BOLD functional connectivity in human brain white matter.




















 6922
6922











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








