
本公号文献全部由作者自解读,欢迎投稿!

A.如何获得蛋白质动态过程的结构信息,以建立蛋白质分子精准的构效关系是一个重大的挑战:
蛋白质分子是生命的基石。生物系统的各种功能,依赖于各种蛋白质分子不同形式和程度的表达。认识蛋白质的功能,建立在对其结构精准认识的基础上。特别是,蛋白质分子动态过程中结构的实时变化,对揭示具体环境中的蛋白质性质、发展现代生命科学和医学药物研究具有至关重要的意义。因此,《SCIENCE》期刊提出的现代科学125个前沿重要问题中就有三个重大科学问题与测定蛋白质结构相关。如何获得蛋白质动态过程的结构信息,以建立蛋白质分子精准的构效关系,是蛋白质结构研究的核心问题。
B.发展快速响应并实时探测蛋白质动态结构的分子光谱技术是一个重要的科学问题:
分子光谱技术,可以通过测量蛋白质对光照的响应信号,利用不同蛋白质的光学特征不同来测定蛋白质结构。比如,X射线光谱,红外吸收光谱,拉曼光谱,圆二色光谱,都可以指认出蛋白质的“光学指纹”。特别是红外光谱,因其对二级结构变化的高敏感度,成为测定蛋白质结构的一种重要手段 (Nature 2020, 577, 52-59;Science 2016, 353,1040-1044;Chem. Rev. 2017,117, 10623-10664)。
利用红外光谱“光学指纹”信息预测结构信息,离不开理论模拟的对比和确认。然而,蛋白质分子光谱的理论模拟面临严重的计算瓶颈问题。蛋白质在溶液中的结构是溶质分子与周围环境相互作用的整体效果的反映,由于原子数多,自由度极大,给精确的光谱计算带来了相当大的挑战,因此限制了实验光谱的解读和原位谱学探测技术的发展。因此,光谱模拟如何帮助实现快速响应和实时探测蛋白质动态结构的分子光谱技术,是一个重要的科学问题。
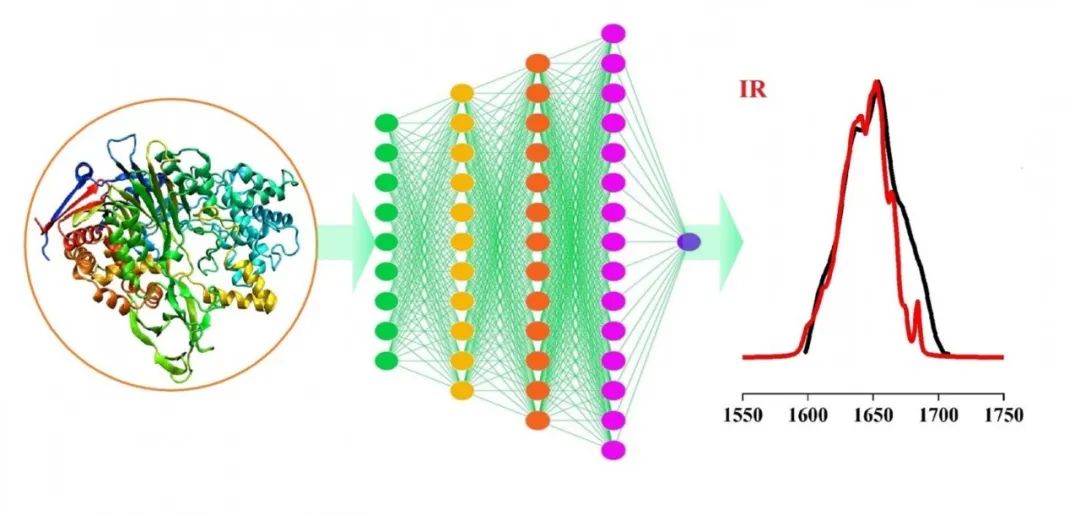 研究出发点
研究出发点
A.蛋白质模型哈密顿量的构建:
蛋白质在红外光谱中有很多特征吸收带,其中酰胺 I 带(1600-1700cm-1),包含了蛋白质丰富的二级结构信息,如α-螺旋、β-折叠、β-转角、卷曲等, 因此测量酰胺 I 带红外光谱可获得蛋白质的“光学指纹”信息。然而蛋白质分子中的原子数成百上千,结构自由度相当大,如果用整个分子的结构信








 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章















 954
954











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








