目录
前言
📅大四是整个大学期间最忙碌的时光,一边要忙着备考或实习为毕业后面临的就业升学做准备,一边要为毕业设计耗费大量精力。近几年各个学校要求的毕设项目越来越难,有不少课题是研究生级别难度的,对本科同学来说是充满挑战。为帮助大家顺利通过和节省时间与精力投入到更重要的就业和考试中去,学长分享优质的选题经验和毕设项目与技术思路。
🚀对毕设有任何疑问都可以问学长哦!
选题指导:
大家好,这里是海浪学长毕设专题,本次分享的课题是
🎯基于U-Net的病理图像中细胞分割技术
设计思路
一、课题背景与意义
病理图像在医学诊断中起着至关重要的作用,细胞分割是病理图像分析的关键步骤之一。准确地分割细胞可帮助医生进行疾病的早期诊断和有效治疗。然而,传统的细胞分割方法往往依赖于人工经验,受到个体差异和图像质量的影响,导致分割结果不够准确。近年来,深度学习技术的快速发展为细胞分割任务提供了新的解决方案。UNet模型,作为一种有效的卷积神经网络架构,特别适用于医学图像分割任务。本研究旨在利用UNet模型对病理图像中的细胞进行分割,探索深度学习技术在提高细胞分割精度和效率方面的应用。
二、算法理论原理
2.1 卷积神经网络
卷积神经网络的核心构建块是卷积层,通过卷积操作提取输入图像的特征。每个卷积层由多个滤波器组成,这些滤波器在输入图像上滑动,计算局部区域的加权和,从而生成特征图。卷积层后通常会接一个激活函数,ReLU,以引入非线性。CNN还包含池化层,用于下采样特征图,减少计算量和参数数量,同时保留重要特征。通过堆叠多个卷积层和池化层,CNN能够学习到越来越复杂的特征。
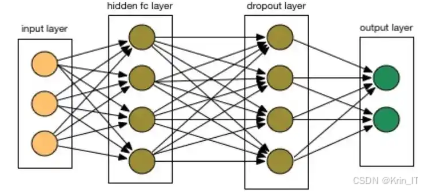
卷积神经网络在图像处理领域具有显著优势,主要体现在参数共享和局部连接上。这种结构使得CNN在处理高维数据(如图像)时较为高效,避免了全连接层带来的庞大参数量。CNN在各种计算机视觉任务中表现出色,如图像分类、目标检测、图像分割和面部识别等。例如,VGG、ResNet和Inception等经典CNN架构在大型图像数据集(如ImageNet)上取得了优越的性能,成为深度学习研究的基石。
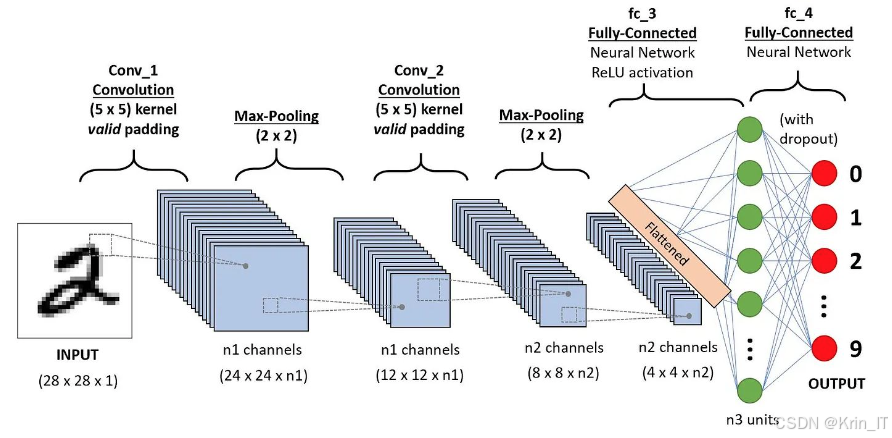
U-Net是一种特定类型的卷积神经网络(CNN),专门用于图像分割任务。它最初是为生物医学图像分割而设计的,但其结构和原理可以广泛应用于其他领域。U-Net的架构呈现出一个对称的U形,主要由编码器(下采样路径)和解码器(上采样路径)组成。编码器逐层提取特征,而解码器逐层恢复空间分辨率,最终输出与输入图像相同尺寸的分割结果。U-Net的一个显著特点是使用跳跃连接(skip connections),即在编码器和解码器之间连接相同层的特征图。这种连接能够保留高分辨率的特征信息,帮助模型更好地进行细节恢复。
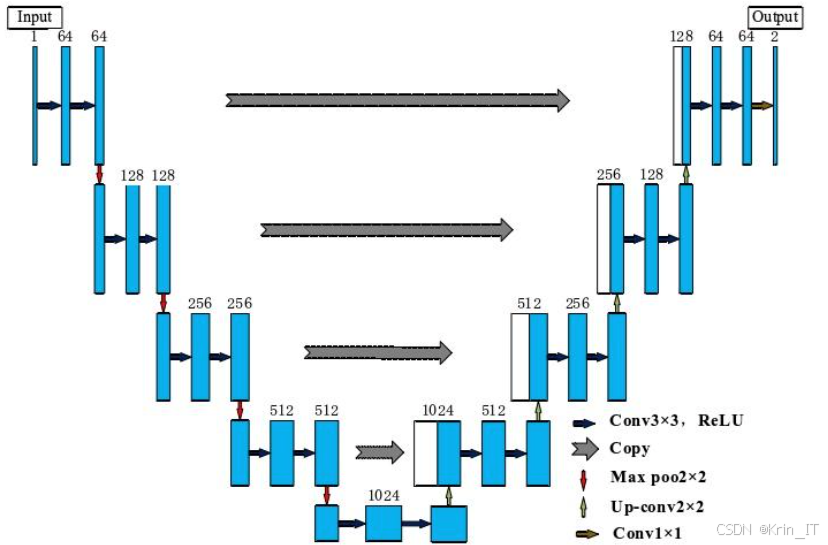
2.2 深度学习模型
Transformer是一种基于自注意力机制的深度学习模型,广泛应用于自然语言处理任务,如机器翻译、文本生成和语言理解。依赖自注意力机制来处理序列数据。自注意力机制是一种计算序列中各位置之间的交互作用的方法,能够让模型直接聚焦于输入数据中的不同部分,以便更好地理解序列之间的关联。例如,每个单词和句子中其他单词之间的关系。
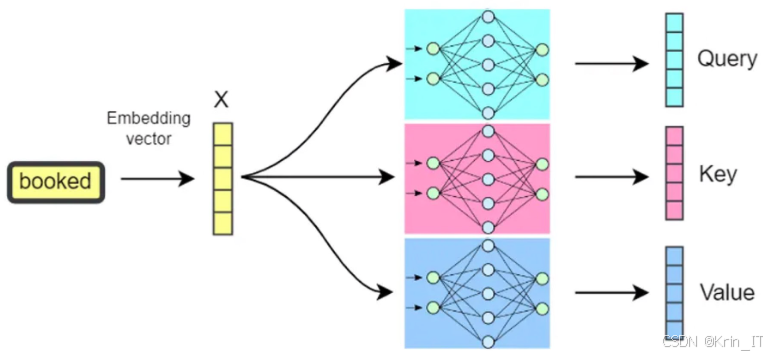
Transformer模型有两大核心部分:编码器和解码器。每个部分都由多个相同的层组成,每一层都含有多头自注意力机制和前馈神经网络。在Transformer中,这两种结构是并行处理的,这使得它能够比递归神经网络在处理长序列数据和捕捉长程依赖关系方面具有更好的性能和效率。Transformer编码器由一系列相同的层组成,每层包含两个关键的子结构:多头自注意力机制和前馈全连接网络。
- 编码器接受一系列输入,通常为嵌入向量的序列。这些向量结合了词嵌入和位置编码,词嵌入捕捉语义信息,而位置编码则使模型能够理解单词在序列中的位置和顺序。在多头自注意力模块中,每个头独立计算输入的注意力得分,允许模型在计算表示的同时,考察输入序列中不同位置的单词。通过计算查询、键和值三个向量的加权求和,注意力权重由查询和键的相似度决定。多头机制使模型能够在多个子空间并行学习信息,增强了表达能力。
- 解码器负责将编码器的输出转化为最终的输出序列。解码器通常由多个相同的层组成,每层包含三个关键的子结构。自注意力机制与编码器中的自注意力类似,但解码器中的自注意力层需保持自回归属性,意味着在生成一个元素时只能访问之前的元素,并通过掩蔽防止未来信息泄露。
Transformer解码器通过结合编码器的上下文信息和已生成序列的信息,逐步预测输出序列的下一个元素,保持自注意力的并行优势,并通过交叉注意力机制有效利用输入信息。
三、检测的实现
3.1 数据集
病理图像中细胞分割数据集的制作首先涉及图像采集阶段。在这一阶段,可以选择自主拍摄和互联网采集相结合的方式。自主拍摄通常使用高分辨率显微镜进行拍摄,确保图像的清晰度和细节捕捉,以便于后续的细胞分析和分割。互联网采集则可以从公开的数据集、数据库中获取已有的病理图像。对采集到的图像进行手动标注,准确地圈出细胞的轮廓和区域。这一过程通常使用专门的标注工具软件,结合病理知识,确保标注的准确性和一致性。标注的结果将为后续的模型训练提供真实的标签数据,从而提高细胞分割算法的性能。
在划分阶段,通常将数据集分为训练集、验证集和测试集,以便于模型的训练、调优和性能评估。常见的划分比例为70%用于训练,15%用于验证,15%用于测试。为了提高模型的鲁棒性和泛化能力,数据增强技术被广泛应用。这包括旋转、平移、缩放、翻转、颜色变换等多种操作,通过这些变换,生成更多的训练样本,从而扩大数据集规模,减少过拟合的风险。
3.2 实验环境搭建

3.3 实验及结果分析
数据准备,这包括图像的采集、标注和预处理。首先,通过自主拍摄或互联网获取高质量的病理图像,确保涵盖不同类型的细胞和病理状态。随后,进行数据标注,病理专家或技术人员使用标注工具对细胞进行精确圈定,并生成相应的标签文件。标注完成后,进行数据预处理,比如调整图像的大小、标准化图像的像素值等,以确保输入数据的一致性。
from PIL import Image
import os
def preprocess_images(image_dir, target_size=(256, 256)):
processed_images = []
for filename in os.listdir(image_dir):
if filename.endswith('.png') or filename.endswith('.jpg'):
img_path = os.path.join(image_dir, filename)
img = Image.open(img_path)
img = img.resize(target_size)
img = img.convert('RGB') # 确保为三通道
processed_images.append(img)
return processed_images
# 使用示例
images = preprocess_images('path/to/image/directory')选择U-Net模型进行细胞分割。模型的架构需要根据输入数据的特征进行设计,通常包括编码器和解码器结构。在构建模型时,可利用深度学习框架(如TensorFlow或PyTorch)来实现所选模型的架构。此外,需定义损失函数和优化器,例如使用交叉熵损失函数和Adam优化器,以便于后续的训练过程。将预处理后的图像和对应的标签划分为训练集和验证集。在每个训练轮次中,通过前向传播计算模型的输出,并与真实标签比较,计算损失。然后,通过反向传播更新模型的参数。训练过程中,定期在验证集上评估模型性能,以监控模型的训练进度,并防止过拟合。通过调整学习率和使用早停策略,可以进一步优化训练过程。
import torch
import torch.nn as nn
import torch.optim as optim
class SimpleUNet(nn.Module):
def __init__(self):
super(SimpleUNet, self).__init__()
# 模型架构定义(简化版)
self.encoder = nn.Sequential(
nn.Conv2d(3, 64, kernel_size=3, padding=1),
nn.ReLU(inplace=True),
nn.MaxPool2d(kernel_size=2, stride=2)
)
self.decoder = nn.Sequential(
nn.ConvTranspose2d(64, 3, kernel_size=2, stride=2),
nn.Softmax(dim=1)
)
def forward(self, x):
x = self.encoder(x)
x = self.decoder(x)
return x
# 模型实例化
model = SimpleUNet()
optimizer = optim.Adam(model.parameters(), lr=0.001)模型训练完成后,需对模型进行评估,使用测试集计算准确率、召回率、F1-score等指标,以了解模型在细胞分割任务中的表现。同时,可以通过可视化工具(如matplotlib)展示模型的分割结果,与真实标签进行比较。如果模型表现不佳,可以考虑进行超参数调优、增加数据增强技术或改进模型架构,进一步提升模型性能。
实现效果图样例:



创作不易,欢迎点赞、关注、收藏。
毕设帮助,疑难解答,欢迎打扰!

























 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








