大家好,这里是专注表观组学十余年,领跑多组学科研服务的易基因。
动脉粥样硬化(Atherosclerosis)是一种慢性血管内膜疾病,是全球发病率和死亡率的主要原因之一。血管衰老是动脉粥样硬化的主要风险因素之一,尤其是内皮细胞衰老在动脉粥样硬化的早期阶段就被观察到,并参与其发病机制。近年来,研究表明表观遗传调控在血管衰老中发挥重要作用,但具体机制尚不清楚。S-腺苷同型半胱氨酸(S-adenosylhomocysteine hydrolase,SAH)是一种强效的DNA甲基转移酶抑制剂,其水平升高与心血管疾病风险增加有关。而S-腺苷同型半胱氨酸水解酶(S-adenosylhomocysteine hydrolase,SAHH)的抑制会导致SAH水平升高,因此SAHH抑制是否加速血管衰老和动脉粥样硬化进展是一个值得探索的问题。
近日,中山大学公共卫生学院营养学系凌文华教授团队研究探讨了抑制SAHH对血管衰老和动脉粥样硬化的影响及其潜在机制。研究结果表明,抑制SAHH会导致血管内皮细胞衰老,并通过表观遗传调控促进线粒体分裂和活性氧(mtROS)水平升高,进而加速动脉粥样硬化进展。研究结果揭示了SAHH在血管衰老和心血管疾病中的重要作用,并为相关疾病的预防和治疗提供了新的靶点。相关研究成果以《Epigenetic modulation of Drp1-mediated mitochondrial fission by inhibition of S-adenosylhomocysteine hydrolase promotes vascular senescence and atherosclerosis》为题发表于《Redox Biology》期刊。易基因科技为本研究提供DNA甲基化测序技术服务。

标题:Epigenetic modulation of Drp1-mediated mitochondrial fission by inhibition of S-adenosylhomocysteine hydrolase promotes vascular senescence and atherosclerosis(通过抑制SAHH对Drp1介导的线粒体分裂的表观遗传调控促进血管衰老和动脉粥样硬化)
发表时间:2023-7-25
发表期刊:Redox Biology
影响因子:IF10.7/Q1
技术平台:WGBS、Target-BS等(易基因金牌技术)

本研究首先通过一项与血管衰老相关的病例对照研究显示,血浆中SAH水平升高与血管衰老风险呈正相关,比值比(OR)为3.90(95%置信区间,1.17–13.02)。在32周龄的SAHH+/-小鼠的动脉中观察到脉搏波速度升高、内皮依赖性舒张反应受损以及衰老相关β-半乳糖苷酶染色增加。此外,在体外和体内实验中,抑制SAHH的血管内皮细胞表现出p16、p21和p53表达增加、线粒体分裂形态以及Drp1表达显著上调。通过siRNA或其特异性抑制剂mdivi-1进一步下调Drp1,可以恢复异常的线粒体形态,并挽救血管衰老的表型。此外,在APOE-/-小鼠中抑制SAHH会促进血管衰老和动脉粥样硬化进展,而这种作用可以通过mdivi-1治疗得到缓解。从机制上讲,SAHH抑制会导致人脐静脉内皮细胞(HUVECs)中DRP1基因启动子区域的低甲基化和DNA甲基转移酶1(DNMT1)下调。
研究结果表明,SAHH抑制通过抑制DNA甲基化在内皮细胞中表观遗传性地上调Drp1表达,从而导致血管衰老和动脉粥样硬化。这些结果表明,SAHH或SAH可以作为血管衰老和心血管疾病的潜在治疗靶点。
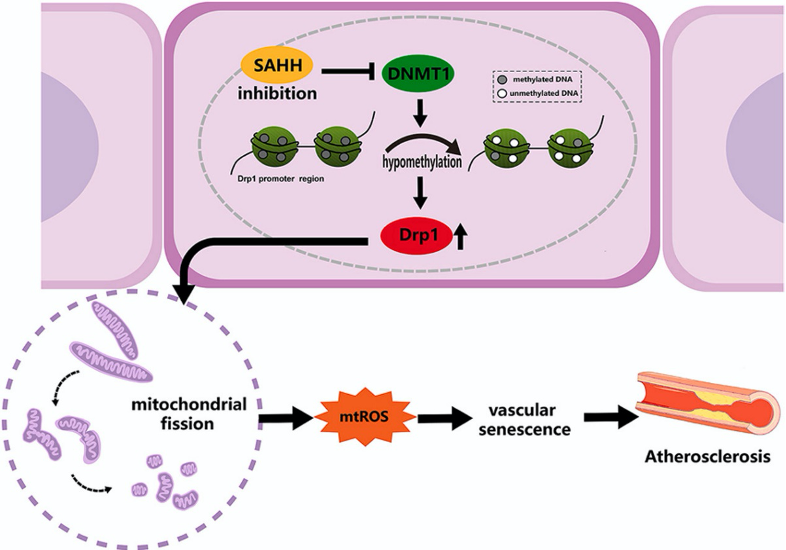
图形摘要
研究方法
病例对照研究:选取40-80岁的中老年人群,通过测量肱踝脉搏波速度(baPWV)确定病例组和对照组,分析血浆中SAH和SAM的水平。
动物实验:使用SAHH杂合敲除小鼠(SAHH+/-)和载脂蛋白E缺陷小鼠(APOE-/-)模型,观察SAHH抑制对血管衰老和动脉粥样硬化的影响。
细胞实验:在人脐静脉内皮细胞(HUVECs)中通过抑制SAHH,观察细胞衰老、线粒体分裂和活性氧(mtROS)水平的变化。
分子机制研究:通过基因表达分析、DNA甲基化测序(WGBS、Target-BS)等技术,探讨SAHH抑制诱导血管衰老的分子机制。
研究结果
(1)血浆SAH水平与人群的血管衰老有关
在一项包含102名年龄和性别匹配的受试者的病例对照研究中,定义臂踝脉搏波速度 (baPWV)≥1400 cm/s为血管衰老。结果显示,病例组的血浆SAH水平显著高于对照组,而SAM/SAH比值则较低。血浆SAH水平与baPWV、颈动脉内膜中层厚度(cIMT)呈正相关,与血流介导的血管扩张(FMD)呈负相关。这表明SAH代谢与血管衰老之间存在相关性。
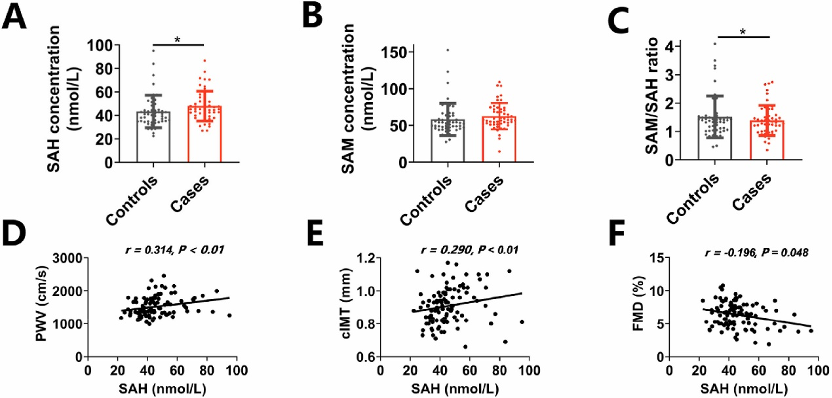
图1:血浆SAH水平与人群血管衰老相关
(2)SAHH 抑制诱导血管衰老
在32周龄的SAHH+/-小鼠中,观察到血浆SAH水平升高,SAM/SAH比值降低,并表现出血管衰老迹象,包括脉搏波速度(PWV)增加、内皮依赖性舒张功能受损以及主动脉中衰老相关β-半乳糖苷酶(SA β-gal)染色增加。此外,细胞衰老主要发生在内皮层。在体外实验中,使用SAHH抑制剂腺苷二醛(ADA)或SAHH siRNA处理HUVECs,也观察到SA β-gal染色增加和衰老标志物p16、p21、p53表达上调。
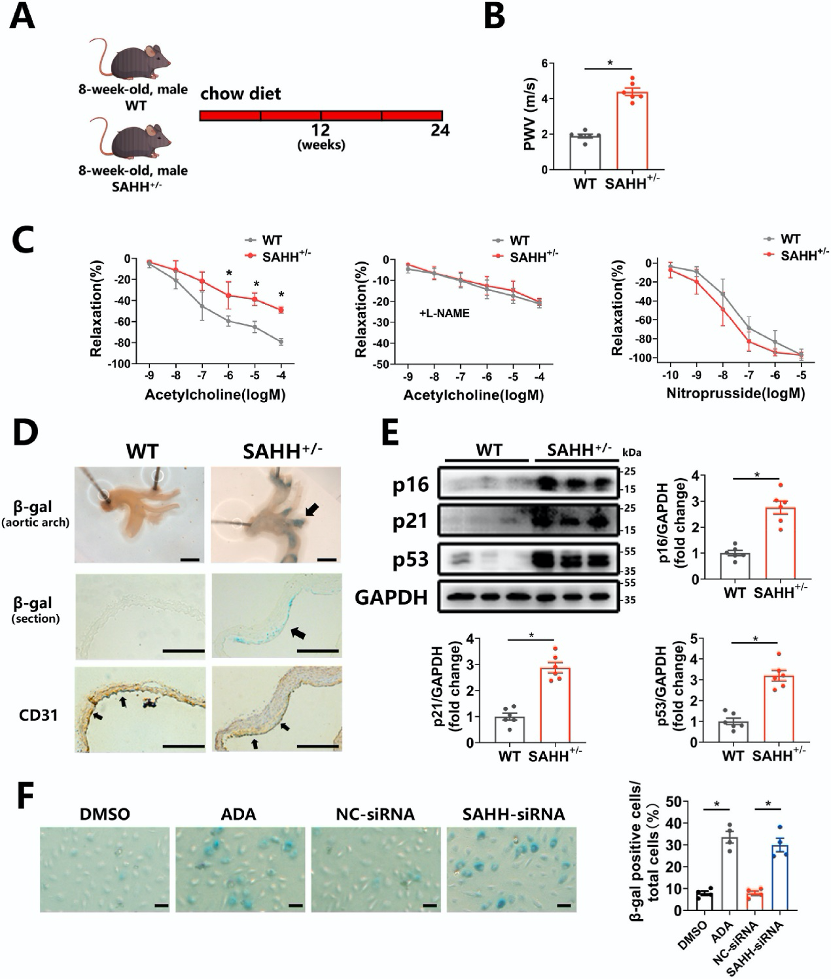
图2:SAHH抑制诱导血管衰老。
(3)SAHH 抑制促进线粒体分裂并介导mtROS水平上调
鉴于SAHH抑制与DNA低甲基化相关,研究者对经SAHH抑制处理的人脐静脉内皮细胞(HUVECs)进行全基因组亚硫酸盐测序(WGBS)以进一步探究其机制。测序结果显示与对照组相比,SAHH抑制组的整体甲基化水平降低。对测序数据集进行的GO富集分析表明,调节线粒体动态的基因可能介导了SAHH抑制诱导衰老的效果。
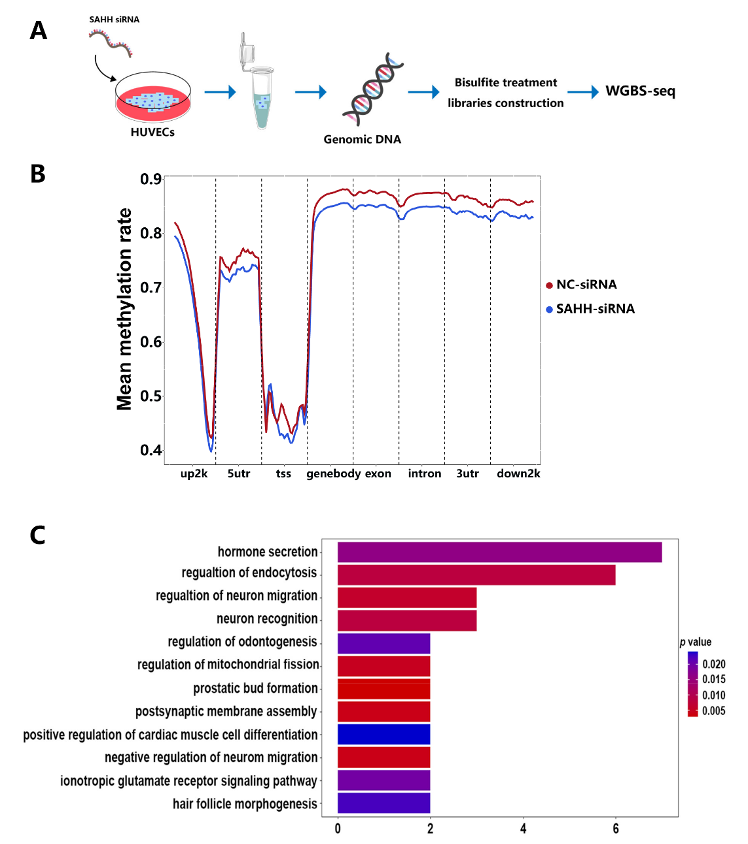
图3: HUVECs细胞转染SAHH-siRNA 48小时。
(A)基因组DNA甲基化测序示意图。
(B)功能基因组区域中甲基化胞嘧啶相对密度的基因组特征。
(C)基于WGBS数据,对NC-siRNA组和SAHH-siRNA组之间差异甲基化区域(DMR)相关基因进行的生物过程GO富集分析。
在SAHH抑制的HUVECs细胞中,通过透射电子显微镜(TEM)和MitoTracker Green染色观察到线粒体形态变短,表明线粒体分裂增加。同时,使用MitoSOX染色检测到线粒体来源的活性氧(mtROS)水平升高。在SAHH+/-小鼠的主动脉中也观察到类似的线粒体分裂形态和ROS水平增加。此外,使用mtTEMPO(一种特异性mtROS清除剂)处理可缓解SAHH抑制引起的细胞衰老表型。
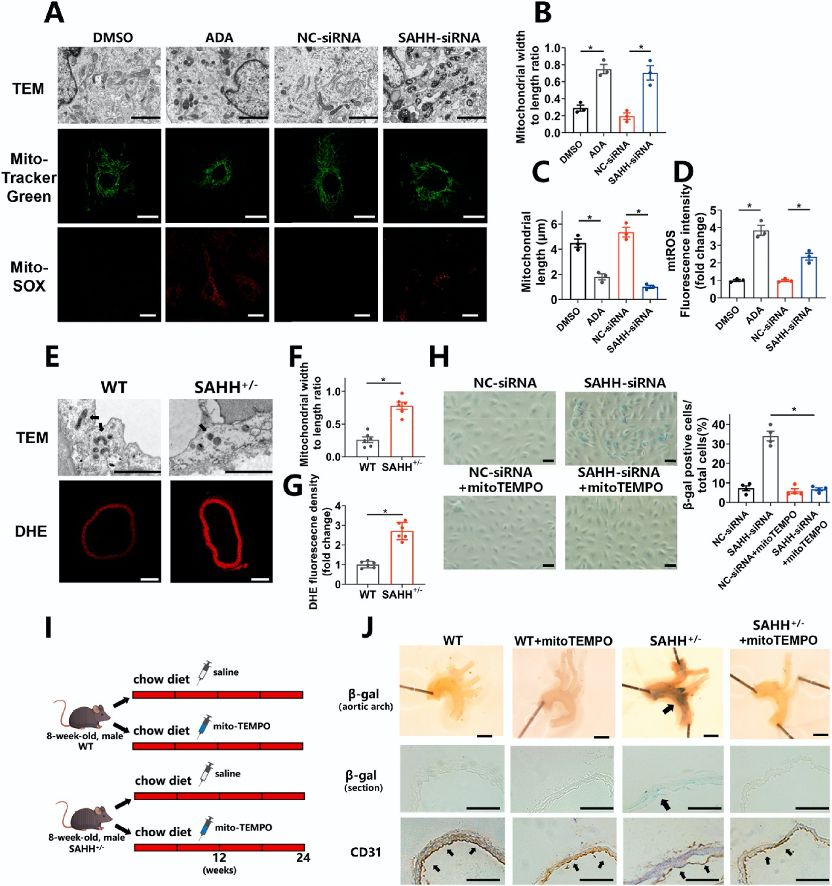
图4:SAHH抑制促进线粒体分裂和mtROS升高。
(4)Drp1-mtROS通路介导SAHH 抑制诱导的内皮衰老
研究发现,SAHH抑制上调Drp1表达,而其他调节线粒体动态的分子(如Fis1、OPA1、MFN1和MFN2)表达未发生变化。通过siRNA或Drp1特异性抑制剂mdivi-1抑制Drp1,可恢复线粒体形态,并减轻SAHH抑制引起的内皮细胞衰老表型。此外,敲低Drp1可抑制SAHH抑制引起的mtROS升高,而清除mtROS对Drp1表达或线粒体形态无影响,表明mtROS增加是Drp1依赖性。
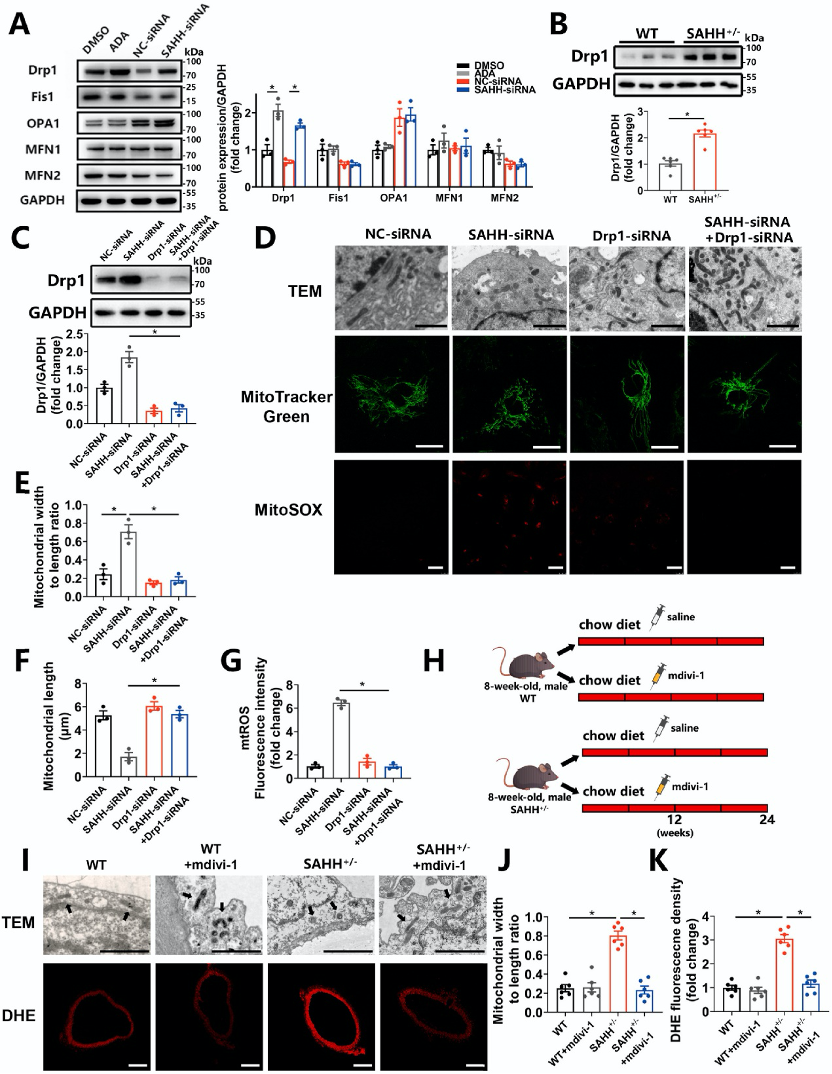
图5:增强的线粒体分裂和mtROS由Drp1介导。
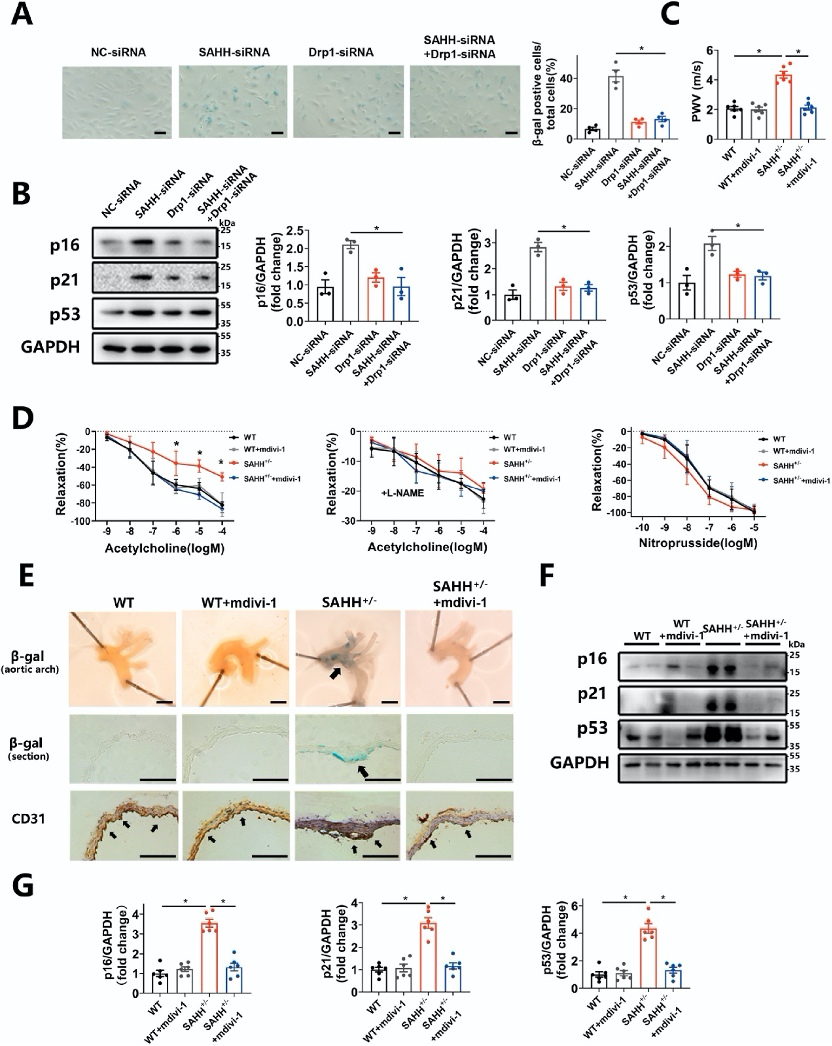
图6:Drp1抑制可挽救SAHH抑制诱导的内皮衰老和血管衰老。
(5)SAHH抑制通过Drp1依赖性通路加速动脉粥样硬化
在APOE-/-小鼠模型中,喂食西方饮食后观察到主动脉中SA β-gal染色增加、p16、p21和p53蛋白表达上调以及斑块形成增加。同时,血浆SAH水平升高,SAM/SAH比值降低,SAHH蛋白表达下降,Drp1蛋白表达增加。在SAHH+/-APOE-/-小鼠中,主动脉中SA β-gal染色和油红O染色的阳性面积增加,表明血管衰老和动脉粥样硬化加剧。而使用mdivi-1处理可减轻这些表型。
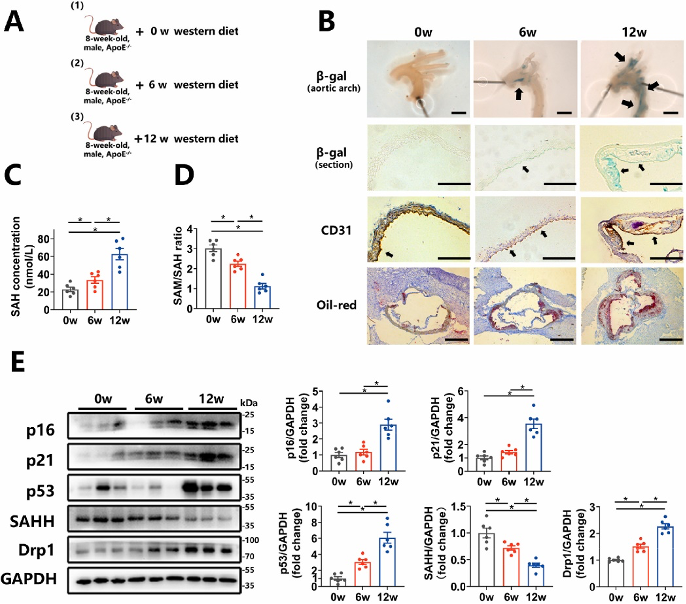
图7:在ApoE-/-小鼠动脉粥样硬化进展过程中,SAHH水平下降且血管衰老加剧。
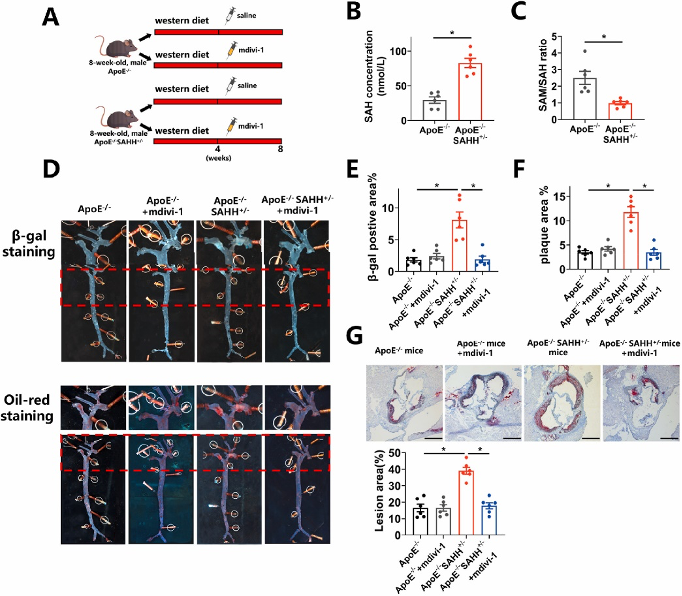
图8:SAHH抑制在Drp1依赖性通路中加速动脉粥样硬化。
(6)SAHH抑制诱导DRP1启动子的低甲基化,并通过抑制DNMT1上调Drp1
在SAHH抑制的HUVECs中,通过靶向DRP1基因启动子区域的亚硫酸盐测序(Target-BS)分析结果表明,启动子区域的甲基化水平降低,与转录激活相关。体外甲基化实验表明,甲基化可抑制DRP1启动子活性。此外,SAHH抑制导致DNMT1表达下调,而过表达DNMT1可抑制SAHH抑制引起的Drp1表达上调。
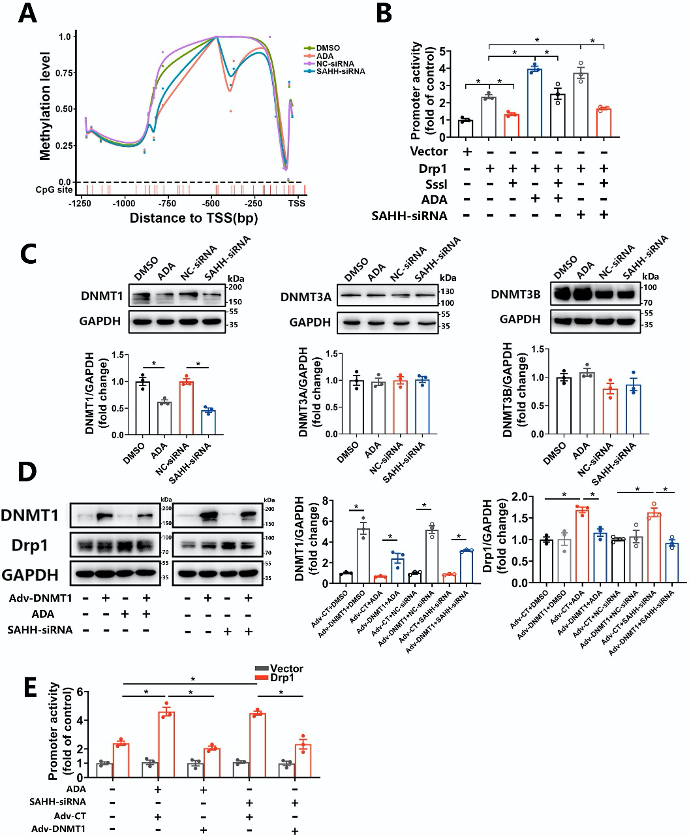
图9:SAHH抑制通过抑制DNMT1诱导DRP1启动子低甲基化和Drp1表达上调。
(A)通过Target-BS检测经ADA(30μM)处理或转染SAHH siRNA 48h的HUVECs细胞中DRP1基因启动子区域的CpG位点甲基化水平。
(B)使用CpG甲基化酶Sss1转染未甲基化或甲基化的DRP1启动子的HUVECs,经ADA(30μM)处理或转染SAHH siRNA 48h。荧光素酶报告基因检测HUVECs中DRP1启动子活性(n=3)。
(C)Western Blot分析经ADA(30μM)处理或转染SAHH siRNA 48h的HUVECs中DNMT1、DNMT3A和DNMT3B的蛋白表达(n=3)。
(D)在ADA和SAHH-siRNA存在的情况下,过表达DNMT1的HUVECs中DNMT1和Drp1的Western Blot分析(n=3)。
(E)转染DRP1启动子或对照质粒的HUVECs感染Adv-CT或Adv-DNMT1 24h,然后用ADA(30μM)处理或转染SAHH siRNA 24h。荧光素酶报告基因检测HUVECs组中DRP1启动子活性(n=3)。
易小结
本研究表明,SAHH抑制通过降低DNMT1表达,减少DRP1基因启动子区域甲基化,导致线粒体动态失衡和mtROS产生增加,最终引起血管衰老和动脉粥样硬化。研究揭示了SAHH抑制通过表观遗传学调控Drp1介导的线粒体分裂,导致血管衰老和动脉粥样硬化的新机制。SAHH或SAH可作为血管衰老和心血管疾病的潜在治疗靶点。这些发现为预防和治疗与衰老相关的疾病提供了新的思路。
WGBS和Target-BS在本研究中发挥重要作用
WGBS:WGBS能够在全基因组范围内以单碱基分辨率检测DNA甲基化水平。本研究通过WGBS发现SAHH抑制组的整体甲基化水平较对照组降低,并鉴定出基因组中因SAHH抑制而发生的差异甲基化区域(DMR)。鉴定出的低甲基化区域与Drp1基因表达上调相关,提示其在血管衰老中的潜在作用。
Target-BS:靶基因DNA甲基化测序(Target-BS)技术在本研究中用于分析SAHH抑制对DRP1基因启动子区域甲基化水平的影响。通过这项技术,研究人员发现SAHH抑制导致DRP1启动子区域的甲基化水平降低,从而促进Drp1基因的转录激活。这一发现揭示了SAHH抑制通过表观遗传学机制调控Drp1表达的分子基础,为理解SAHH在血管衰老和动脉粥样硬化中的作用提供了关键证据。
易基因:DNA甲基化研究基本思路
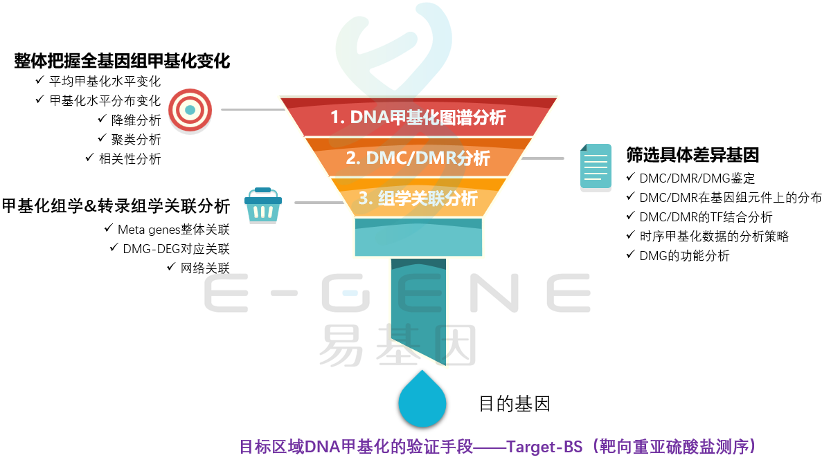
DNA甲基化一般遵循四个步骤:
首先,进行整体全基因组甲基化变化的分析,包括平均甲基化水平变化、甲基化水平分布变化、降维分析、聚类分析、相关性分析等。
其次,进行甲基化差异水平分析,筛选具体差异基因,包括DMC/DMR/DMG鉴定、DMC/DMR在基因组元件上的分布、DMC/DMR的TF结合分析、时序甲基化数据的分析策略、DMG的功能分析等。
再次,将甲基化组学&转录组学关联分析,包括Meta genes整体关联、DMG-DEG对应关联、网络关联等。
最后,对筛选出的目标区域DNA甲基化进行验证,通常采用靶基因重亚硫酸盐测序(Target-BS)。
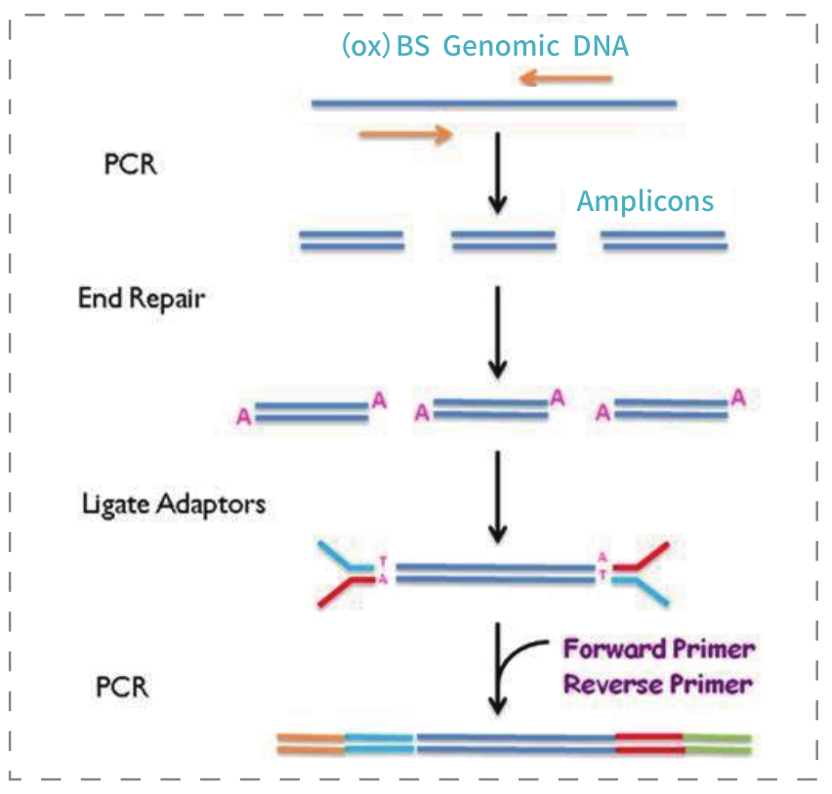
关于易基因靶基因DNA甲基化测序(Target-BS)
对目标基因/CpG 位点甲基化检测,建立灵活的靶向甲基化测序技术。易基因建立的靶基因甲基化高通量测序(Target Bisulfite sequencing,Target-BS)是针对已有目标基因panel组合,运用易基因自主研发的甲基化特异性多重PCR引物设计软件,对亚硫酸盐转化后的目标基因多重扩增,建库后进行超高深度(1000X以上)甲基化精准检测。
应用方向:
Target-BS广泛用于已知位点的甲基化Biomarker筛选、验证及临床转化应用
- 后续目标基因的甲基化验证
技术优势:
- 多基因多重扩增,检测通量高;
- 超高深度亚硫酸盐甲基化测序,相对于传统BSP克隆测序,检测灵敏度、准确性高,可准确检测到样本中低于1%的甲基化水平;
- 样本需求量低,20ng基因组DNA可实现多基因扩增;
- 适用范围广,对基因组DNA、FFPE样本、游离cfDNA等样本均适用;
- 检测费用显著低于现有技术、快周期、超高性价比。
参考文献:
You Y, Chen X, Chen Y, Pang J, Chen Q, Liu Q, Xue H, Zeng Y, Xiao J, Mi J, Tang Y, Ling W. Epigenetic modulation of Drp1-mediated mitochondrial fission by inhibition of S-adenosylhomocysteine hydrolase promotes vascular senescence and atherosclerosis. Redox Biol. 2023 Sep;65:102828. doi: 10.1016/j.redox.2023.102828.
相关阅读:
1、项目文章|靶基因甲基化测序(Target-BS)等揭示特应性皮炎新发现:IL-4表观遗传调控Treg数量和CTLA-4表达
2、项目文章|鸡的chTERT靶基因DNA甲基化检测揭示ALV-J肿瘤发生机制
3、项目文章:Target-BS技术揭示糖尿病引发勃起功能障碍的DNA甲基化调控机制
4、植物靶基因DNA甲基化研究超级问答 | 想知道的都在这里



























 6748
6748

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








