阿尔茨海默症(AD)目前主要依赖于心理测试和临床观察进行诊断。然而,这些诊断方法并不完美,额外的诊断工具(例如,磁共振成像,MRI)可以帮助我们更好地理解阿尔茨海默症,以及提高我们检测该疾病的能力。因此,已有大量的研究投入到阿尔茨海默症的创新诊断方法中。功能性磁共振成像(fMRI)是一种已被用于阿尔茨海默症诊断的神经影像技术;然而,由于fMRI的噪音大、复杂性高,其在临床应用上有所不足。尽管如此,近期深度学习技术的创新可能使fMRI的分析更为简化和高效。
深度学习是一种基于人类神经网络的计算机算法,用来解决复杂问题的人工智能形式。例如,在fMRI研究中,深度学习模型可以自动降噪图像,并通过检测参与者脑部扫描中的模式来对阿尔茨海默症进行分类。在这个系统评价中,我们研究了如何使用fMRI(具体而言,是静息态fMRI)和深度学习方法来诊断阿尔茨海默症。同时,我们概述了文献中常用的深度神经网络、预处理和分类方法。我们还讨论了fMRI深度学习方法的准确性、优点、限制和未来的发展方向。总的来说,我们的目标是为新的研究者总结当前的研究领域,提出未来研究的具体方向,并突出fMRI在辅助阿尔茨海默症诊断方面的潜力。本文发表在Journal of Neuroimaging杂志。
介绍
阿尔茨海默病(AD)是一种严重的神经病症,常常以身体衰退和认知下降为特征。目前,AD尚无治愈之法,此病通常会导致患者死亡。在澳大利亚,AD和其他形式的痴呆症是老年人口死亡的第二大原因。然而,与其他主要的死亡原因不同,AD的衰退过程会持续多年。因此,AD给个人、社会和经济(例如,医疗保健)带来了巨大的负担,影响到每一个人。虽然目前有一些治疗方法可以治疗AD的一些症状,暂时减缓疾病的进展,但目前还没有治疗方法可以停止AD的进展。目前有效治疗手段的匮乏的一个最大原因就是目前的AD诊断状态。在澳大利亚,AD通常通过心理测试和临床观察(例如,访谈和纸笔量表)来诊断。尽管这些诊断方法对于中晚期的诊断大多数情况下是足够的,但对于早期的AD,我们更需要采用可以补充当前策略的方法(例如,MRI,PET)。例如,据估计,如果AD能在早期被诊断出来,通过对疾病的持续治疗和管理,患者可以有一个更好的生活质量。因此,大量的研究已经投入到创新的方法中,以识别早期的AD并补充当前的诊断方法。
在文献中,使用神经影像学、传统生物标记物和神经心理学方法来诊断AD有多种方法。每一种领域在诊断AD时都有显著的优点和局限性。具体来说,传统生物标记物可以直接测量AD的症状(如,β-淀粉样蛋白和tau蛋白)但通常是侵入性的,并且在准确性上存在变异。而神经心理测试易于进行且方便(对临床友好),但可能偏向中晚期诊断。最后,神经影像学方法是非侵入性的并且具有很高的准确性,但分析复杂。在研究中,神经影像学方法通常更受欢迎,因为它们能够以高精度诊断AD并帮助早期诊断。例如,MRI常用于统计模型以预测早期AD。然而,如前所述,神经影像学方法需要复杂的分析,这需要专业的资源。因此,急需改进神经影像学方法以帮助AD的诊断。在这个系统性回顾中,我们特别研究了如何改进功能性磁共振成像(fMRI)以用于AD的诊断。
功能性磁共振成像(fMRI)是一种神经影像学技术,它通过测量脑血氧水平来成像大脑活动。在AD研究中,fMRI主要用于成像大脑区域的活动和大脑区域之间随时间变化的相互作用,后者被称为功能连通性。先前的研究发现,静息态fMRI(没有任务或刺激下进行的fMRI)的功能连通性测量可以准确诊断AD并预测疾病的早期阶段。例如,一些研究发现内侧颞叶和海马的异常功能连通性表明了AD。还有研究建议静息态fMRI(以下简称fMRI)可以区分不同形式的痴呆症并检测早期AD。例如,fMRI可以通过研究不同的神经网络来区分AD和其他形式的痴呆症。因此,研究也显示,AD与默认模式网络(DMN)有关。不同于更传统的结构影像测量(例如,MRI脑容量),有研究认为,功能连通性测量可以在显著的神经退化之前检测出早期AD。据此,证据表明,fMRI测量可以高精度诊断AD,并可能协助临床诊断。
在文献中,传统的fMRI方法通常遵循数据收集、预处理和分析的三个阶段。具体来说,研究通常收集fMRI数据或从像OpenfMRI和阿尔茨海默病神经影像学倡议(ADNI)这样的大型数据库获取数据。然后,使用傅立叶分析和回归等统计技术对fMRI数据进行清理和预处理。这些预处理步骤主要由SPM12、FSL和fMRIPrep等软件包执行。使用的具体预处理技术通常取决于软件包和研究目标。然而,大多数(如果不是全部)研究都会使用预处理技术——如头骨剥离、切片时间校正、运动重新对齐和强度标准化——来清理和转换fMRI数据。这些转换后的数据通常被量化为时间序列(时间内的大脑活动度量)、感兴趣区域(ROI;如对特定体素的分析)或独立组分分析(ICA;时间序列和ROI空间图的混合)测量。使用这些预处理数据,最终分析使用常见的统计技术对比和诊断群体(例如,ANOVA,t-检验,回归)。例如,Koch等人的一项研究以97.2%的准确率对AD和认知正常的对照组(CN)进行了分类。在他们的流程中,Koch等人手动收集了他们的数据,将其预处理成时间序列相关性和ICA测量(使用BrainVoyager软件),然后使用t检验分析他们的组。许多其他研究也使用fMRI以类似的结果诊断AD。
然而,与MRI和PET神经影像学方法相比,fMRI有严重的限制,应用非常有限。例如,与MRI和PET相比,收集、清理、预处理和分析fMRI数据的工作强度非常大。此外,fMRI数据非常混乱(例如,信噪比低),需要高度专业的知识,大型数据库中很少见,而且通常比其他技术(例如,MRI)的准确度低。因此,fMRI方法并不受欢迎,因为它们需要大量的资源、计算能力和技术专长,这些通常与其他技术(例如,认知测试)相比是不合理的。因此,不足为奇的是,fMRI在历史上研究缺乏,不被用于临床AD诊断。然而,fMRI确实提供了对AD的独特视角,例如大脑活动和神经网络的测量。如前所述,这些fMRI测量可以检测早期阶段的AD,并可能在对抗该病的过程中发挥重要作用。因此,通过大幅改进fMRI方法,可以将fMRI的独特信息与当前的技术结合起来,为AD提供更全面的画像,以便在更早的阶段诊断该病。
最近,有人提出使用深度学习技术可以克服fMRI在诊断上的一些限制。深度学习模型使用基于人类学习的计算机算法来解决复杂的问题。在fMRI的情况下,一些研究已经表明,典型的问题——例如清洗和分析fMRI数据所需的高计算成本——可以使用深度学习模型来克服。例如,Parmar等人创建了一个深度神经网络(DNN)模型,可以半自动处理复杂的fMRI数据(例如,4维数据)进行AD诊断。与以前的手动技术(如统计分析和机器学习算法)不同,深度学习方法特别适合处理fMRI,因为它们专门在总结(例如,降维)和分类计算密集型数据上有所长。 此外,一个完全构建的深度学习模型是端到端的,并且在诊断AD时不需要大量的监督或解释。因此,深度学习算法可以被训练来处理fMRI数据并自动分类AD。因此,深度学习方法可以帮助fMRI补充当前的诊断方法,并提高早期AD的检测。
fMRI在AD研究中的应用,无论在临床还是实验中,都相当罕见。处理fMRI也是非常复杂且不友好的。深度学习等方法可以帮助提高fMRI在AD分类中的可行性。然而,这些方法仍然复杂并缺乏操作性。在过去的几年中,使用深度学习和fMRI方法进行AD分类的研究数量正在增加。然而,这些研究在范围、方法和准确性上都有很大的不同。因此,本文系统地回顾了用于AD分类的fMRI和深度学习方法。已有一些其他的评论讨论了使用fMRI和深度学习进行AD诊断的情况; 但是,这些评论通常都是概括性的,因此,往往关注多种疾病、模态和分析技术(例如,自闭症谱系障碍,结构MRI,机器学习)。因此,在这个评论中,我们特别系统地回顾了研究中用于分类AD的静息状态fMRI和深度学习方法。反过来,我们概述了这个领域,并试图给新的研究者提供常见方法、技术、设计、软件以及他们的应用实例的指导。我们希望通过这个基础,研究者将能够应用、适应和创新fMRI和深度学习方法,以帮助对抗AD。我们还特别关注静息状态fMRI,因为这种方法在AD研究中最常见,且对于神经系统疾病患者(与任务基础的fMRI相比)更为友好。
本系统性回顾和指南的其余部分分为六个部分,讨论了本研究使用的方法、我们系统性回顾的结果、fMRI预处理方法、分类设计和方法、常见的DNN,以及结论性讨论。反过来,我们探索以下问题:(1)研究如何量化和预处理fMRI数据以供深度学习模型使用;(2)什么是研究设计和疾病分类的标准方法;以及(3)用于分析fMRI进行AD诊断的常见DNN模型是什么?我们还讨论了fMRI深度学习方法的优点、局限性和未来的发展方向。因此,我们的目标是为新的研究者提供基础知识,并建议进一步研究的途径。
方法
在这个系统性回顾中,我们研究了如何使用fMRI和深度学习方法来诊断AD。对于我们的选择标准,我们将相关的论文定义为那些使用静息状态fMRI数据和深度学习方法来分类AD及其前驱阶段(主观记忆投诉[SMC]或轻度认知障碍[MCI])的论文。我们将深度学习定义为一种使用神经网络和组合特征选择与分类技术的人工智能方法。我们排除了评论文章、未经同行评审的作品、动物研究和非英语论文。所有的文章都来自于2021年5月的Scopus,PubMed(MEDLINE)和Science Direct。我们使用以下关键词来找到相关的论文:(FMRI或“功能磁共振成像”)和阿尔茨海默病和深度学习。最初,我们从搜索中获取了2362篇文章。然而,我们通过过滤掉重复、评论和非同行评审的文章,减少了我们的搜索结果。反过来,我们提取了831篇文章进行筛选。我们的搜索详细信息可以在图1中的系统性评论和Meta-Analyses流程图中看到。
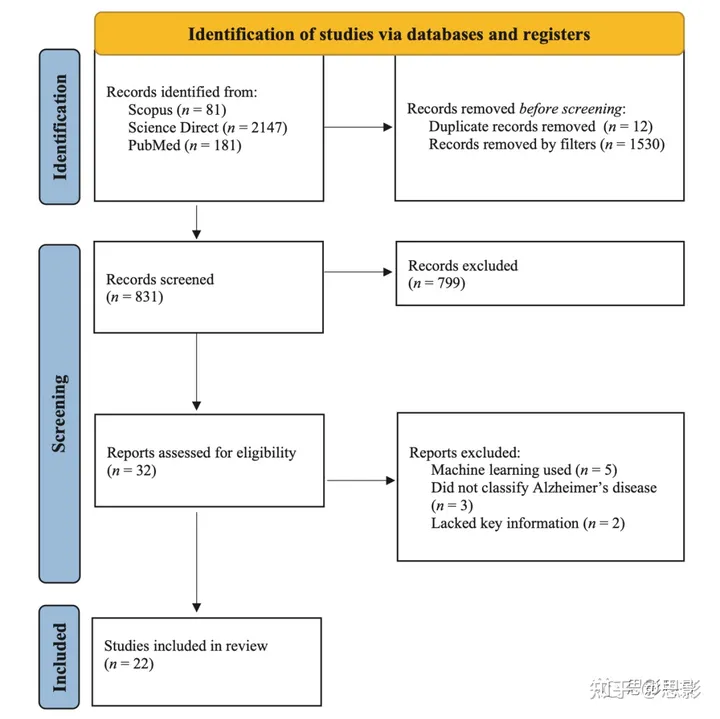
图1 我们使用PRISMA流程图进行系统评审的研究选择过程。
n = 参与者数量。使用此流程图是由系统评审和元分析(PRISMA)推荐的,以符合他们进行系统评审的指南。
我们使用ASReview筛选了所有的文章。ASReview是一种人工智能方法,它使用机器学习算法和研究人员的监督来系统地选择用于审查的文章。对于我们的研究,我们手动筛选了部分文章(根据上述预定义的选择标准)来训练ASReview,然后ASReview筛选了剩余的文章。然后,ASReview将筛选的文章按照适用于训练选择标准的顺序进行排序和输出。我们选择在这个系统评审中使用ASReview,因为它可以帮助我们避免偏见,并自动化审查过程。然而,ASReview并不是一个无偏见的工具,只有在选择标准和停止规则被预定义时,才能提供帮助。在开始我们的ASReview筛选之前,我们决定当连续5%的论文与审查无关(即,不符合上述的选择标准)时,筛选就会结束。因此,在监督阶段,每一篇摘要都被手动阅读并与选择标准进行比较。反过来,我们在达到停止规则之前,使用ASReview筛选了242(29%)篇论文。在831篇筛选的论文中,ASReview找到了22篇符合选择标准的研究。然后对这些研究进行了全面的审查,并提取了相关数据(例如,作者、参与者数量、准确性、分类方法)进行分析。需要注意的是,研究通过比较模型分类结果与参与者的诊断标签来计算准确性。这些标签是由临床诊断定义的(例如,ADNI使用心理测试和临床评估对参与者进行诊断)。有关ASReview的更多信息,请参阅van de Schoot等人的研究。
结果
表1中可以看到22篇选定论文的详细信息,如分类方法、准确性、使用的DNN以及参与者数量。总的来说,大多数评审的研究准确性高,根据所使用的方法,准确性在大约70%至98%之间。大多数,如果不是所有,fMRI深度学习的研究在分类AD时都遵循相同的一般步骤。具体来说,每项研究都从数据库获取数据,使用软件包预处理数据,计算功能连接,然后使用深度学习模型提取特征并分类。一些过程,如数据收集和预处理,在所有研究中都相似。例如,本次评审中的大多数研究(82%)都从ADNI数据库获取数据。然后,研究使用如FSL等计算包处理原始fMRI数据。这些预处理方法将在下一节 进一步讨论。
表1. 审阅的研究摘要
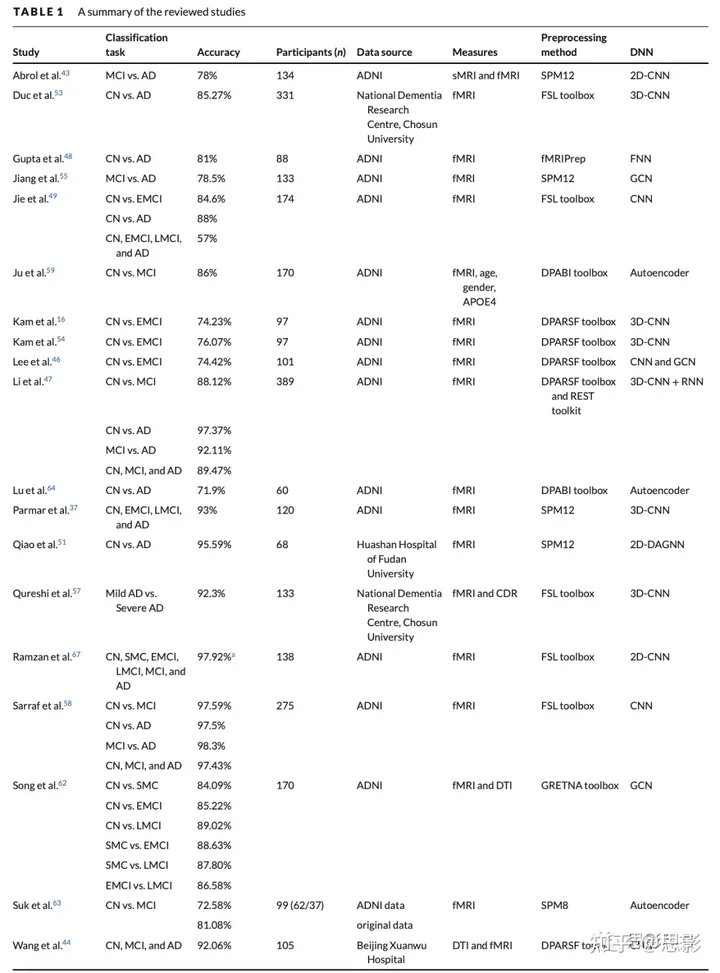
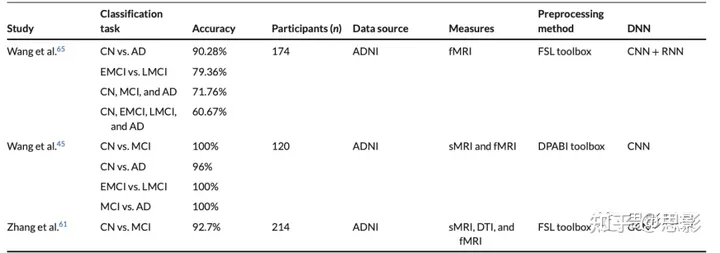
缩略语:AD,阿尔茨海默病;ADNI,阿尔茨海默病神经影像计划;CDR,临床痴呆评定量表;CN,认知正常;CNN,卷积神经网络;DAGNN,有向无环图神经网络;DTI,扩散张量成像;EMCI,早期MCI;fMRI,功能磁共振成像;FNN,前馈神经网络;GCN,图卷积神经网络;LMCI,晚期MCI;MCI,轻度认知障碍;n,参与者数量;RNN,循环神经网络;SMC,主观记忆投诉;sMRI,结构磁共振成像。
a这个准确率是平均准确率。通过将模型分类与参与者诊断标签进行比较来计算准确率(参见方法部分)。
大多数研究的整体设计也存在相似之处。例如,大多数研究(68%)只使用fMRI(功能连接度测量)作为唯一的测量指标,对CN、MCI或AD组进行二元分类。研究还主要使用了SoftMax算法来对群体进行分类(见下文的分类设计部分)。一些研究使用了其他设计,如多变量分类(多个变量)、多类分类(多个组)和其他分类算法。例如,Abrol等人结合了fMRI和结构MRI(sMRI)在一个多变量模型中;王等人在一个模型中对CN、MCI和AD进行了分类;王等人使用了支持向量机(SVM)作为分类层。然而,应当注意的是,与上述二元、单变量和SoftMax方法相比,这些替代方法占的比例较小。一些研究(41%)研究了AD连续谱的早期阶段,如SMC和早期MCI(EMCI)。然而,在所有的组比较中,大多数研究(77%)主要关注了疾病的后期阶段,如MCI、晚期MCI(LMCI)和AD。下文的“分类设计和方法”部分将进一步讨论这些设计选择。
相反,研究在选择功能连接性和DNN(深度神经网络)方法方面存在巨大的差异。在接下来的部分中,我们概述了预处理、研究设计和分类以及DNN方法的典型方法。具体来说,在下一节中,我们详细说明了如何常规地为深度学习分析预处理fMRI信号,并概述了计算功能连接性的方法(量化fMRI的主要方法)。接下来,我们讨论了模型设计和分类技术的方面,如分类层、多变量模型和多类分类。然后,我们概述了流行的深度学习方法,如卷积神经网络(CNN)、图形神经网络(GNN)、自动编码器和循环神经网络(RNN)。我们还提供了一些使用DNN来研究AD的fMRI数据的示例。最后,我们总结和讨论我们的发现,特别关注该领域的局限性以及未来研究的领域。
fMRI预处理
预处理涉及清理和转换fMRI数据,以便进行深度学习分类。如前所述,fMRI研究中使用的预处理方法存在很大的重叠。例如,几乎所有的fMRI研究都使用了如去颅骨和切片时间校正等过程。然而,还有其他一些更专门或具有争议的技术,如全局信号校正和带通滤波。更多关于fMRI预处理中常用的统计检验和技术信息,请参见Strother等人的研究。在fMRI和深度学习研究中,预处理几乎完全是使用如SPM12这样的软件或编程库进行的。在本次回顾中,我们发现大多数研究使用了如FSL(32%)或DPARSF工具箱(23%)这样的预处理库。使用特定的工具箱通常取决于研究的设计。例如,研究者可能会在ICA研究中使用FSL,因为它包含了一个常用的预处理流程(FEAT和BET)和MELODIC(一个用于执行ICA的包)。否则,预处理包大多是可以互换的,取决于研究者的偏好和专业知识。例如,像FSL这样的包需要复杂的视觉检查和手动设置。因此,新的研究者可能会使用需要较少专业知识的自动化工具,如fMRIPrep。如果不喜欢图形用户界面,大多数包也允许进行脚本和命令行预处理。此外,fMRI工具箱通常是开源的,并有专门的网站和社区。因此,我们建议研究者调查上述讨论的工具箱,并决定哪一个最适合他们的技能和研究。
然而,预处理确实有一些限制。具体来说,预处理需要花费相当多的时间和计算资源。例如,使用高端个人电脑(如Intel i9-10900F中央处理单元[CPU],32Gb RAM,Nvidia GTX 1080图形处理单元[GPU])时,fMRIPrep每个被试大约需要25分钟到1小时的时间。此外,当预处理fMRI数据时,sMRI数据也必须进行预处理。因此,参与者数量、硬件和时间可能会大大延长预处理阶段。澳大利亚的许多机构都可以使用超级计算机或研究云(例如,ARDC的Nectar Research Cloud),这可以大大提高预处理的速度。尽管如此,我们理解并非所有的实验室都能接触到尖端的技术。因此,我们建议研究者在进行完整运行之前进行预处理试验,编写他们的预处理脚本,当计算资源有限时将参与者限制在一个有代表性的样本大小,通过在线预处理社区或论坛寻求帮助,并研究不同包的速度(例如,使用fMRIPrep时,FLS在表面处理上比FreeSurfer快)。
功能连接性
在预处理过程中,fMRI数据通常被量化为预处理的血氧水平依赖性(BOLD)信号,或者作为功能连接性的一种衡量。预处理的BOLD信号是fMRI扫描的清洗输出,而功能连接性是从BOLD信号计算出的大脑活动度量。预处理后的BOLD信号被用于一些高维模型;然而,功能连接性度量是最突出的fMRI度量。有不同的方法来量化分析的功能连接性。在本次审查的文献中使用的主要两种度量是:皮尔逊相关性和ICA。历史上,fMRI研究使用相关性分析(例如,大脑区域之间的相关活动)以及预定义的脑图谱来计算和映射功能连接性。这些脑图谱在文献中被广泛使用,以确保不同的大脑能够准确比较。在这次审查中,大多数相关性研究使用了一种形式的皮尔逊相关性分析和自动解剖标签图谱(AAL)来计算功能连接性。然而,这些相关性方法确实有一些局限性。也就是说,它们只能模拟大脑区域之间的简单关系,无法详细描述功能连接体。这些方法在时间上也有限制,通常只采样fMRI时间序列的部分(方法只在一个或几个时间点计算相关性)。相关性分析也存在捕捉功能连接性的高阶特性的问题(相关性是功能连接性的简单总结),大脑图谱可能会丢失对分类重要的个体特征。尽管如此,皮尔逊相关性和大脑图谱已经在fMRI深度学习模型中得到了高度准确的结果。
独立成分分析
在这次的审查中,我们发现大多数研究使用ICA来计算功能连接性。ICA是一种专门用于分离和分类数据的统计技术。在fMRI研究中,ICA可以用来定义功能连接网络,无需预先存在的大脑图谱。ICA也可以提供高度详细的信息,并将大脑划分为多个功能网络。因此,ICA通常被优先于更传统的皮尔逊相关性和大脑图谱技术。一些初步的研究已经暗示,由于ICA能够将功能连接划分为多个区域网络,因此它可以获得更高质量的信息。例如,Kam等人。试图使用fMRI、深度学习(CNN)和ICA技术来诊断EMCI。他们研究了多个功能网络,而不像大多数研究只研究一个网络(例如,DMN)。使用98名参与者(49名EMCI和49名CN)的数据,Kam等人使用ICA构建了参与者功能网络(例如,额-顶网络)的三维(3D)空间地图。然后,这些功能网络被用来训练和测试CNN模型进行疾病分类。Kam等人发现,他们的模型可以以74.23%的准确率将EMCI和CN进行分类。相比之下,其他的深度或机器学习模型只能以平均65%的准确率将EMCI和CN进行分类。他们还将他们的多网络模型与单一功能网络模型进行了比较。他们发现,后者只能以67%-71%的准确率对AD进行分类(DMN和前额-顶叶网络是最好的单一模型)。因此,Kam等人建议使用多个功能连接网络可以强化早期阶段AD的分类。
新兴技术
新兴的研究表明,深度学习方法可以用于计算功能连接性测量。例如,Jiang等人。构建了一个图形卷积神经网络(GCN),可以评估个体和基于人口的功能连接性变化,以分类AD。他们使用两个GCN创建了他们的分类模型。第一个GCN使用fMRI数据自动图形化个体的功能连接网络。然后,第二个GCN通过根据其周围邻居(其他参与者的网络)和他们的连接来调整节点,从而更新功能连接网络。因此,一个人的功能连接网络是根据它与整个样本中其他网络的关系进行改变的。Jiang等人将这个两部分模型称为层次化GCN模型(hi-GCN)。接下来,Jiang等人使用ADNI中133名受试者(99名MCI和34名AD)的数据来训练和测试他们的模型。他们发现,他们的hi-GCN模型可以以78.5%的准确率将MCI和AD进行分类,并且可以超越类似的模型(例如,使用ICA的标准CNN和GCN模型)。因此,他们建议可以使用深度学习方法来计算功能连接性,并且可能优于当前的方法;然而,需要更多关于基于深度学习的预处理方法的研究。
深度学习和AD的fMRI标记物
深度学习和传统的fMRI方法有相似的预处理步骤和技术。然而,深度学习的fMRI在数据类型和提取的特征上有所不同。传统和深度学习数据之间的主要差异在于它们的维度和复杂性。例如,如上文所述,传统的方法可能使用ICA计算功能连接性。ICA的结果通常以脑活动的时间课程和空间图像的形式输出。在传统的研究中,这些ICA的输出通常被转换成Z分数,然后用于分析。另一方面,深度学习方法允许对类似技术进行更高维度的分析。例如,ICA输出的时间序列和空间图可以直接输入到3D深度学习模型中。此外,深度学习模型可以将这两种输出结合起来,形成一个4D模型(空间和时间数据)。除了扩展传统的技术,如ICA,还有一些其他独特的深度学习方法。例如,一些研究使用图论创建用于分析的脑功能连接组模型。这个话题将在下面的图形神经网络部分和上面的新兴技术部分进一步讨论。然而,深度学习为发现、转换和分析AD的fMRI生物标记物创造了新的机会。例如,在我们审查的文献中,研究通常关注AD的生物标记物,如海马活跃度和DMN。我们希望通过这些措施,fMRI和深度学习能够提供复杂且独特的信息,帮助诊断AD。
分类设计和方法
在讨论用于分类AD的特定深度学习模型之前,我们有必要详细了解分类模型的常见设计和层次。例如,预处理和深度学习方法并不是影响分类精度的唯一因素。也就是说,研究的设计、目标和范围也会影响DNN模型的分类精度。因此,我们应该考虑分类的类型(二分类vs多分类)、使用的变量数量(单变量或多变量),以及分类算法(通常被称为DNN的分类层)。在这个部分,我们将讨论常见的分类方法论,例如多类分类,多元分类和分类层。因此,我们的目标是强调分类精度并非是衡量一个模型能力的全面指标。因此,我们强调,在评估fMRI深度学习模型时,考虑研究设计,模型目的和疾病表现(一个研究模仿现实世界诊断场景的准确性)也很重要。
二分类和多分类
多分类模型是一种深度学习算法,可以同时诊断多种条件(例如,CN,MCI,AD)。在AD研究中,多分类模型通常不如二分类方法(例如,AD vs. CN)准确,因为AD是一系列重叠的疾病的连续体。此外,对于深度学习算法来说,二分类任务更简单,因此往往具有更高的准确度。然而,我们认为多分类应该在AD研究中成为常规,因为二分类并不能准确地模拟真实世界中的AD。如果研究人员希望将fMRI和深度学习方法应用到临床实践中,那么模型能够主动评估与AD相关的重叠和相关疾病的能力就至关重要。例如,Sarraf等人使用fMRI构建了一个能够分类AD,MCI和CN的CNN。他们从ADNI获取了数据,其中包括52名AD患者,131名MCI患者和92名CN参与者(N = 275)。fMRI数据使用传统软件进行预处理,并使用PNG无损数据转换将其降维到2维图像。他们发现,他们的CNN的多类分类准确率为97.43%(AD、MCI和CN),二分类准确率为97.5%(AD http://vs.CN)、98.3%(AD vs. MCI)和97.59%(CN vs. MCI)。因此,Sarraf等人表明,多分类方法可以具有高准确度,并能进行更具代表性的AD诊断(即,区分多种相似条件)。
单变量和多变量分类
AD是一种复杂的、多面性的疾病,具有多种症状,没有单一的原因。因此,虽然fMRI深度学习方法可能具有很高的实验准确度,但在临床环境中实现准确诊断还需要进一步的信息。因此,一些模型结合了其他测量手段(例如,认知测试或其他神经影像学方法)和fMRI,以达到更高的分类准确度。大部分多变量研究将fMRI与MRI的其他形式(如sMRI和扩散张量成像(DTI))结合起来。例如,Wang等人使用3D CNN结合sMRI和fMRI数据进行AD分类。他们创建了一个多变量MRI方法,因为他们推测联合方法的分类准确度会优于单独使用sMRI和fMRI。Wang等人使用3D ShuffleNet(为移动设备创建的低强度CNN)构建了他们的模型。sMRI和fMRI数据都使用标准方法(例如,皮尔逊相关性和AAL)进行预处理,并使用核典型相关分析将fMRI和sMRI数据合并到一个分类模型中。Wang等人使用来自ADNI的数据(50个CN,18个EMCI,18个LMCI和34个AD)和一个SVM,发现他们的模型可以以85.2%的准确率将AD从CN中分类出来。他们还发现,他们的多变量模型可以以适中到高的准确度将MCI从AD(84%)、MCI从CN(64.8%)和EMCI从LMCI(53%)中分类出来。与现有的单变量模型相比,Wang等人发现,他们的模型匹敌或超过了大部分(如果不是全部)单变量分类模型。因此,他们表明,多变量深度学习模型可以超越单变量模型,并可能提高fMRI的临床应用可能性。文献中也发现了使用AD的各种测量手段(如APOE4,人口统计学,DTI,认知测试)得出的类似结果。然而,这个探索领域只有少数几个开创性的研究,并需要进一步的研究和验证。请参阅表1,了解此系统评审中包含的多变量研究的摘要。
分类层
分类层是一个数学函数,它将DNN的结果转化为分类输出。在文献中,大多数研究使用SoftMax函数将模型输出转化为分类组。SoftMax函数是一种多类分类函数,它计算输入属于每个结果组的概率。例如,在fMRI深度学习研究中,SoftMax层被用来计算参与者根据其fMRI数据有AD、MCI或是CN的概率。一些其他的替代SoftMax层的方法可以用于深度学习模型的分类。例如,逻辑回归、sigmoid函数和SVM已被用于分类AD。然而,这些方法在机器学习或统计研究中更常见,在评审的文献中没有多大用途。有一些情况下可能会使用SVM,如Wang等人的研究。然而,SoftMax模型是首选,因为它们在面对新信息时可以重新校准,并且可以轻易地融入DNN。SoftMax层可以被替换为类似的方法,如Argmax算法;然而,这些类似的方法并不常见,且超出了本文的范围。还应注意,近来在计算机科学文献中出现了使用自动编码器和聚类技术进行分类的趋势;然而,这些方法尚未广泛应用于AD和fMRI研究。因此,分类层对模型准确度的影响通常是所有讨论过的方法中最小的,但这仅仅是因为SoftMax函数的广泛使用。然而,研究人员在设计fMRI深度学习模型时仍应考虑不同分类函数的优缺点。
深度学习模型
使用fMRI数据对AD进行分类的有各种类型的DNN。在这一部分,我们概述了文献中使用的常见类型的神经网络。具体来说,我们讨论了CNN、GNN、自动编码器和RNN。请参见表2,了解本系统评审中讨论的每种DNN的简要概述。
表2:本系统综述中讨论的每个深度神经网络的摘要
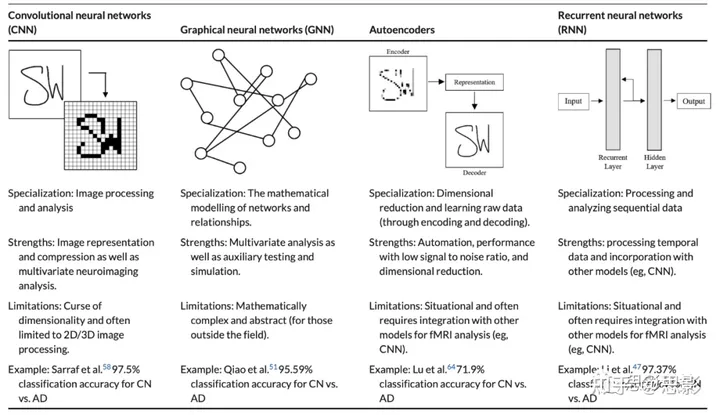
卷积神经网络
卷积神经网络(CNN)是一种专门用于图像处理和分析的深度神经网络(DNN)。与其他方法不同,CNN通过系统性地扫描和总结图像为分类特征来工作。因此,CNN特别适合研究如fMRI这样的复杂数据,并且是fMRI AD文献中最常用的DNN。CNN有多种形式,它们在诸如架构、目的、输入和分类方法等各个方面都有所不同。在fMRI研究中,区分CNN的最简单方法是通过维度。具体来说,CNN可以被归类为2D(例如,像素)、3D(例如,体素)和4D方法(例如,随时间变化的体素)。如前所述,原始fMRI数据本质上是4D的(空间-时间);然而,CNN基本上是设计来研究2D或3D图像的(只有空间信息)。因此,需要在模型复杂性和数据损失之间进行权衡,其中4D数据必须被强制进入一个专门的CNN,或者被降维以适应常见的2D和3D模型。这种权衡通常被称为维数诅咒。
当使用2D CNN时,fMRI数据的维度被大幅度地降低以适应神经网络。这种维度降低通常使用像FSL工具箱这样的预处理软件包进行。二维CNN相对容易使用,不容易出现在高维模型中看到的复杂情况。然而,用于2D模型的剧烈的维度降低可能导致重要数据的大量丢失,这些数据可能对于分类AD至关重要。尽管如此,2D CNN模型在文献中仍有很大的成功。例如,Wang等人创建了一个2D CNN模型,可以使用fMRI数据对CN、MCI和AD参与者进行分类。他们获取了105位(40位CN、30位MCI和35位AD)参与者的数据,并使用DPARSF工具箱(包括维度降低)预处理了他们的fMRI扫描。然后,他们使用皮尔森相关和AAL大脑图谱计算了功能连接度量。结果,Wang等人以82.5%的准确率分类了CN、MCI和AD。
与2D方法相比,3D CNN保留了一个额外的空间维度,但代价是模型更复杂且计算密集。3D CNN可以通过增加的维度信息来提高模型准确性,并帮助区分相似的疾病(例如,EMCI和LMCI),从而证明这种复杂性的增加。然而,需要注意的是,由于深度学习(例如Keras和TensorFlow)和计算机硬件(例如CPU和GPU)的最新进步,3D CNN并不过于密集,且相对容易使用。在文献中,3D CNN是最受欢迎的深度学习模型类型,因为它们平衡了数据丢失和模型复杂性之间的权衡。例如,Qureshi等人使用3D CNN模型和fMRI来分类痴呆的严重程度。具体来说,他们使用临床痴呆评分量表来构建AD严重程度组(轻度和重度)。然后,他们训练一个3D CNN,基于fMRI数据来分类AD的严重程度。该模型是使用TensorFlow架构,133名AD参与者,以及使用群体ICA计算的功能连接数据构建的。因此,Qureshi等人发现,他们的3D CNN可以以92%的准确率分类AD的严重程度。
CNN基本上是设计来研究2D和3D图像的。因此,研究原生(4D)fMRI数据是非常困难的。然而,一些研究已经建议,4D模型的复杂性增加值得为了提高准确性。人们认为4D DNN可能比降维的CNN更准确,因为它们可以利用完整的fMRI时间序列。因此,已经有少数几项研究已经适应了CNN用于4D数据。例如,Parmar等人改编了一个3D CNN模型,以包含4D数据。具体来说,他们使用标准卷积层融入空间信息,并使用一个过滤层(一个排除结构数据的核)输入时间数据。使用这个模型,他们在来自ADNI的120名参与者中对AD连续体的多个阶段(CN,EMCI,LMCI,MCI和AD)进行了分类。最终的4D模型具有93%的多类分类准确性,并且是文献中最准确的方法之一。因此,Parmar等人提出,对于AD分类,4D模型可能比降维模型更好。
图神经网络
图论是由变量及其连接构成的网络的数学建模。这些图网络通常由代表变量(也称为节点)的几何形状和表示关系的连线组成。在fMRI研究中,GNN可以用来模拟功能连接并分类AD。GNN是一种强大的分类工具,因为它们允许复杂现象的简单表示。GNN还允许进行理论测试(例如,病变模拟)和包含各种类型的数据(例如,神经影像,人口统计,生物标记)。此外,GNN可以轻易地包含多变量数据,并可以与其他神经网络方法(例如,CNN)结合。例如,张等人研究了使用GCN的多模式MRI的分类能力。具体来说,他们使用GCN将DTI和fMRI数据结合起来进行AD分类。他们在这项研究中使用GCN,是因为它可以包含和CNN相同的fMRI成像元素,同时也可以加入结构网络信息(DTI)。因此,他们推测,结合空间和时间信息将导致比各种方法单独使用时更高的分类准确性。张等人使用Destrieux脑图谱映射他们的DTI和fMRI数据,以确定区域并创建结构和功能网络图。这些结构图被用作GCN模型的基础,然后使用功能连接数据进行了优化。为了测试他们的模型,张等人从ADNI获取了214名参与者的数据(116名CN和98名MCI),并进行了五折交叉验证。结果,他们发现他们的模型可以以92.7%的准确性将MCI与CN区分开。
通过与各种深度学习方法和AD标记的结合和兼容性,GNN显示出了极大的灵活性。因此,GNN是多变量建模AD的关键(例如,将fMRI数据与其他AD标记结合起来)。此外,GNN还有助于构建和表示功能连接网络。然而,GNN也有一些局限性,如模型设计的复杂性,模拟个体特性(如,参与者疾病严重程度)的困难,以及标准fMRI的噪音问题。然而,GNN的限制正在逐渐被克服。例如,在一篇最近的论文中,宋等人解决了GCN的三个常见限制。具体来说,他们创建了一个模型,该模型可以在分类AD时包含诊断严重性信息,包含参与者相似性数据(例如,参与者之间的相关性),并使用多元MRI数据(DTI和fMRI)。宋等人根据诊断(由ADNI确定)将图模型中的所有节点连接起来,以包含诊断严重性信息。参与者的相似性数据是通过图中节点之间的相关距离以及使用GCN对节点的排名来计算的。最后,多元MRI数据被包含为图的边(连接),并使用两个GCN模型(每种MRI方法一个)进行处理。宋等人研究了来自ADNI的170名参与者(44名CN,44名SMC,44名EMCI,38名LMCI),并使用10折交叉验证来训练,测试,验证他们的模型。因此,他们的GCN模型可以将每个组与其他组进行分类,平均准确度为86.8%。
自动编码器
自动编码器是一种独特的深度神经网络,它通过在隐藏层压缩数据然后寻求重建它来学习特征。在痴呆症研究中,自动编码器可以通过对fMRI数据进行维度缩减然后重新创建功能连接度量来分类AD。因此,对fMRI数据的拆解使自动编码器能够学习指示AD的功能连接网络的基础特性。与某些其他模型不同,自动编码器是无监督的,不需要标记数据,并且可以克服信息损失(例如,丢失的数据)。自动编码器并非固有地构建来分析来自fMRI的4D数据,但可以进行调整。在文献中,自动编码器并未广泛应用于AD和fMRI(与其他技术相比)。尽管如此,自动编码器仍有一些用途,并且仍然可以准确地分类AD。例如,Suk等人提出了一个深度自动编码器模型(包括隐马尔可夫模型),该模型通过对fMRI数据的平均时间序列(随时间的体素)进行采样来分类MCI和CN。他们在来自99名参与者的数据上测试了他们的模型,这些数据是手动收集的,或者是从ADNI获取的。结果,自动编码器模型以81.08%的准确率从CN中分类出MCI。
自动编码器也可以作为维度减少和分类工具。例如,Lu等人使用了一个自动编码器聚类(一种群体排序算法)模型,通过fMRI数据来分类AD。具体来说,他们使用自动编码器进行维度减少,并使用多核模糊聚类进行分类。参与者的数据是从多个数据库中获取的,这些数据库针对各种疾病(自闭症,AD,创伤后应激障碍和注意力缺陷多动症)。对于AD,从ADNI获取了60名AD和CN参与者的混合数据。使用平均时间序列和皮尔森相关性创建了基线功能连接图。在从CN中分类AD时,Lu等人发现他们的模型的准确度为71.9%。他们还发现他们的多核模糊聚类方法与其他聚类方法(例如,k均值,模糊c均值,多项式核模糊聚类)相比,具有最高的准确性。很少有研究使用自动编码器进行基于fMRI的维度减少或分类。
尽管如此,这可能是一个关键的研究领域,它可以实现临床诊断的自动化,并减少深度学习模型中对诊断标签的需求。
循环神经网络
RNN是一种专门的深度学习模型,可以研究随时间变化的数据。RNN可以通过复用模型输出作为未来比较的输入来研究这些数据序列。在fMRI研究中,RNN专门研究功能连接随时间的变化。具体来说,RNN会独立处理随时间变化的fMRI快照,并复用这些快照与序列中的下一张图像进行比较。当与CNN配对时,RNN也发现了极大的用途。因为,通过将RNN与3D CNN配对,可以在4D模型中连续比较3D fMRI图像。例如,Li等人提出了一种使用3D CNN和长短期记忆网络(LSTM)进行4D fMRI分析的方法。他们选择使用3D CNN是因为它专门用于静态图像分析,然后使用LSTM(一种RNN)进行时间分析进行调整。通过结合这些网络,Li等人可以分析fMRI数据的所有四个维度(三个空间和一个时间)。他们的研究从ADNI获取了包含116名AD,99名MCI和174名CN参与者的数据。为了进行比较,他们然后将他们的模型与突出的2D和3D深度学习方法(例如,CNN)进行比较。结果,Li等人发现他们的CNN-LSTM模型优于所有其他模型,并具有以下准确性:AD与MCI的准确率为91.1%; MCI与CN的准确率为88.12%;AD与CN的准确率为97.37%;AD、CN和MCI分类的准确率为89.47%。因此,Li等人显示,涉及RNN的4D fMRI模型非常准确,可能对AD的分类有用。
讨论
在这篇系统性的回顾中,我们研究了fMRI和深度学习方法如何用于诊断AD。我们发现,多项研究已经使用各种类型的DNN以高精度诊断AD的不同阶段。在回顾的文献中,大多数研究使用了如SPM12(用于处理原始fMRI数据)等预处理软件,使用了ICA来计算功能连接性,使用CNN来提取并处理特征,并使用SoftMax激活层来诊断AD。DNN和功能连接度量存在一些差异,然而,这些变化更多的与研究设计有关,而非增加准确性。因此,大多数研究的准确度约为85%,这取决于使用的方法。研究还发现,深度学习方法可以比传统技术(例如,机器学习)更好地分类AD。DNN还具有灵活性(可以使用新数据进行再训练)并可以自动化分析。因此,深度学习方法具有显著的优势,如提高诊断准确性和简化fMRI分析。
然而,深度学习fMRI方法确实存在一些局限性。即,大多数深度学习fMRI的研究都非常新,大多数研究只是概念的证明。例如,大多数fMRI深度学习模型通常都被简化(例如,单变量分析,二分类),并不能真实反映现实世界中的AD诊断。 因此,研究已经提供了实验证据,证明深度学习模型可以使用fMRI数据区分AD连续体的不同阶段;然而,很少有模型检查了对深度学习fMRI模型在现实世界应用中至关重要的临床特征(例如,多阶段诊断)。深度学习和fMRI的当前特性可以帮助临床医生执行半自动化、易于解释且高度精确的诊断模型。然而,为了使fMRI深度学习模型在临床上可行,它们必须能够分类AD的不同阶段(多类别分类),与其他AD标记物结合(多元分类),并能够预测AD的早期阶段。许多被审查的研究也受到他们样本大小的限制。例如,一些高精度模型必须以怀疑的态度对待,因为它们在每个组中只测试了少数参与者。虽然获取神经影像数据很困难,但是研究和他们的诊断模型不能用如此小的样本人群来推广。
这项研究的一些关键局限性也值得强调。首先,应该指出,审查的文献高度依赖ADNI数据库,因此在样本群体中有很大的重叠。这种依赖是由于获取fMRI数据的高昂成本和无法访问其他数据库的情况。例如,英国生物银行有一个大型的fMRI数据集,但访问的成本很高。其次,这项研究提出了深度学习作为改进fMRI分析阶段的一种方法。然而,我们并没有将太多的注意力放在改进数据收集和预处理阶段。这两个阶段仍然需要大量的资源,与其他技术相比,不适合临床分析。我们选择不关注这些问题,因为它们需要超出本文范围的创新。尽管如此,fMRI程序的标准化和自动化的重大进步正在进行中,随着时间的推移应该会有所改进(例如,大型数据库,云计算,超级计算机,自动预处理工具)。第三,应该注意到这篇论文的范围是有限的。fMRI和深度学习研究的内容不仅仅是静息状态测量和分类模型。然而,我们选择关注这些话题,因为我们认为它们是新研究人员容易接触和可获取的重要领域。希望这次审查可以为未来探究前沿fMRI技术和深度学习方法提供基础。最后,我们想强调,这篇评论重点关注了有监督的深度学习模型。这些有监督的模型依赖于由临床测试定义的诊断标签。因此,其中一些模型可能受到定义它们的临床诊断的限制。这种交互需要进行更多的研究和与自动化模型的比较。
未来的研究应在现有的文献基础上进行扩展,并解决上述的限制。我们建议未来的研究应探索诸如早期阿尔茨海默症、多变量诊断模型、痴呆类型分类(例如,血管性痴呆或额颞痴呆与阿尔茨海默症的区别)和高维(4D)模型等领域。我们急需能在早期诊断阿尔茨海默症和区分不同形式痴呆的研究。在阿尔茨海默症诊断的这些领域的创新,可能会极大地改善治疗机会和个体的生活质量。我们还建议未来的研究应通过如多类分类模型、调整潜在的混淆因素(例如,阿尔茨海默症的神经精神症状)和增大样本量等技术来克服目前的限制。样本量的限制是一个大问题,可以通过使用多个数据库、迁移学习、数据增强、数据共享和其他人群来克服。因此,未来的研究可能需要依赖的样本比仅仅ADNI提供的更多,并且应该警惕数据集的过度使用。接下来,我们认为研究者应该投入到与这个话题重叠的更大的领域。这次的审查范围很小,然而,这个话题发生在痴呆、神经影像和人工智能研究的交叉点。这些领域是巨大的,其中一个领域的创新将会影响到其他领域。因此,我们建议研究者拥抱这个领域的跨学科性质,并协同合作来解决阿尔茨海默症问题。最后,我们想强调,未来的研究在分类阿尔茨海默症时,应该平等地考虑模型的准确性、可推广性和临床可行性。分类的内容不仅仅是准确性。因此,我们希望这些模型能在适当的时间内成为临床可行且易于获取的工具。
总之,深度学习技术是当前最先进的技术,正在迅速改变我们(作为一个研究社群)对待阿尔茨海默症诊断的方式。当前,fMRI深度学习方法具有很高的准确性,但它们也非常新颖,需要进行更多的研究。在这个系统综述中,我们讨论了用于阿尔茨海默症分类的fMRI深度学习研究的当前方法。我们希望这个综述能帮助研究人员了解fMRI和深度学习方法在阿尔茨海默症中的应用能力。我们还希望这个综述能帮助新的神经科学家和心理学研究者了解尖端的计算机科学技术。我们希望这项研究能鼓励更多关于fMRI深度学习技术的研究,并最终帮助改善阿尔茨海默症患者的诊断。























 1299
1299

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








