在生物科学的浩瀚星空中,抗癌研究一直是科学家们孜孜不倦探索的璀璨星辰。近年来,随着纳米技术的飞速发展,科学家们利用纳米材料设计出了一系列创新的治疗策略,旨在更加精准、高效地打击癌细胞。今天,我们要探讨的是一项前沿研究——“铁噬”纳米粒子如何通过诱导不可逆的线粒体损伤,为抗癌研究带来新希望。
铁,作为生物体内不可或缺的微量元素,在能量代谢、DNA合成与修复、信号传导等生命活动中扮演着举足轻重的角色。尤其在线粒体中,铁不仅是构成铁硫簇(Fe-S clusters)的关键元素,还直接参与呼吸链的构成,对维持细胞的正常生理功能至关重要。然而,肿瘤细胞对铁的需求异常旺盛,它们通过上调铁转运受体的表达,大肆掠夺铁资源以满足其快速增殖的需求。这一特性,让铁成为了抗癌研究中的“新宠”。
近年来,铁螯合疗法逐渐进入人们的视野。通过剥夺癌细胞所需的铁资源,可以有效抑制其生长。然而,传统的铁螯合剂往往面临生物利用度低、靶向性差等问题,难以在临床应用中大放异彩。因此,开发一种高效、精准的纳米递送系统,成为了科学家们的共同追求。
在这项研究中,科学家们巧妙地将铁螯合剂Dp44mT与自噬抑制剂羟基氯喹(HCQ)结合,设计出了一种名为Dp44mT@HTH的“铁噬”纳米粒子。这种纳米粒子以透明质酸(HA)为亲水外壳,能够特异性地靶向高表达CD44受体的4T1乳腺癌细胞。一旦进入细胞,纳米粒子在活性氧(ROS)的作用下解体,释放出Dp44mT和HCQ,协同作用诱导线粒体损伤。
在实验观察过程中,科学家们使用了AbMole的Hoechst 33342 trihydrochloride这一核酸染料。Hoechst 33342是一种可以穿透细胞膜,并发蓝色荧光的DNA染料。它通过与DNA双链中的小沟结合,显著增强了富含A/T序列的DNA的荧光强度。这一特性使得Hoechst 33342成为细胞核染色和观察的理想工具。在“铁噬”纳米粒子的研究中,科学家们利用Hoechst 33342对细胞核进行染色,清晰地观察到了细胞在纳米粒子作用下的形态变化和凋亡情况。
具体来说,Dp44mT通过螯合细胞内的Fe²⁺,阻断铁硫簇的生物合成,进而扰乱呼吸链功能,导致线粒体功能障碍。与此同时,HCQ不仅减少了Fe²⁺的摄入,还抑制了自噬溶酶体的融合,阻断了细胞通过自噬途径清除受损线粒体的能力。这种“双管齐下”的策略,使得受损的线粒体在体内不断累积,最终引发细胞凋亡。
实验步步为营,揭秘“铁噬”纳米粒子的神奇之旅
-
纳米粒子的制备与表征: 科学家们首先合成了ROS敏感的硫酮(TK)作为连接分子,将HCQ与透明质酸(HA)相连,形成HTH聚合物。随后,通过自组装将Dp44mT包裹在HTH内部,形成Dp44mT@HTH纳米粒子。利用动态光散射(DLS)和透射电镜(TEM)等技术,验证了纳米粒子的粒径、形貌和稳定性。
-
细胞摄取与溶酶体逃逸: 通过荧光标记的纳米粒子与4T1细胞共孵育,科学家们观察到纳米粒子能够高效地被细胞摄取,并在溶酶体内迅速逃逸,进入细胞质中发挥作用。
-
线粒体损伤评估: 利用多种生物化学和分子生物学技术,科学家们系统地评估了纳米粒子对线粒体功能的影响。实验结果显示,Dp44mT@HTH显著降低了细胞内Fe²⁺含量,抑制了呼吸链复合物的活性,导致线粒体钙超载、膜电位崩溃和ATP生成能力下降。
-
自噬抑制与线粒体累积: 通过免疫荧光、Western Blot以及Hoechst 33342染色等技术手段,科学家们发现HCQ有效抑制了自噬体与溶酶体的融合,导致受损线粒体在体内大量累积。这种累积效应进一步加剧了线粒体功能的崩溃,促进了细胞凋亡。Hoechst 33342的染色结果清晰地展示了细胞核在细胞凋亡过程中的形态变化。
-
体内抗肿瘤效果验证: 在4T1乳腺癌小鼠模型中,科学家们验证了Dp44mT@HTH的体内抗肿瘤效果。结果显示,与对照组相比,Dp44mT@HTH处理组的小鼠肿瘤生长受到明显抑制,且未观察到明显的毒副作用。
铁噬效应的深远影响
实验结果显示,“铁噬”纳米粒子通过精准地剥夺癌细胞的铁资源并抑制自噬途径,成功地诱导了不可逆的线粒体损伤。这种损伤不仅限于单一的线粒体功能丧失,还通过自噬抑制导致了受损线粒体的持续累积,形成了一种“恶性循环”,最终促使癌细胞走向凋亡。Hoechst 33342的染色观察为这一过程的验证提供了直观的证据。
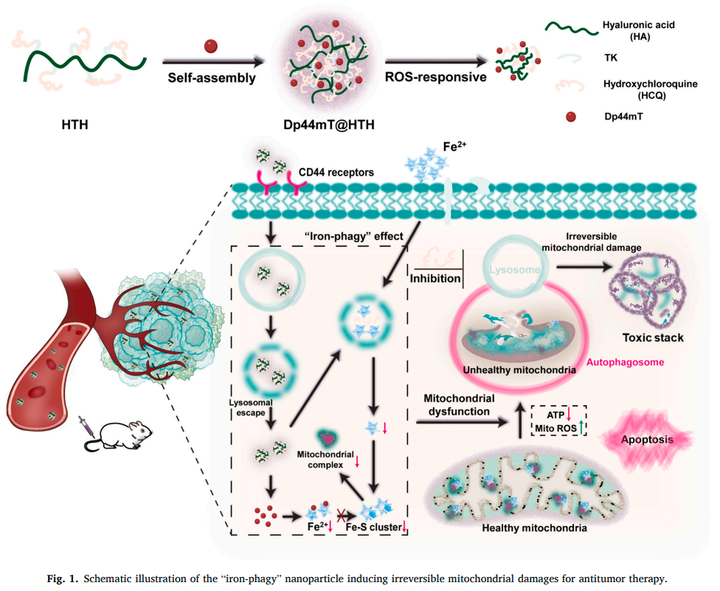
图1生动展示了“铁噬”纳米粒子(Dp44mT@HTH)如何进入癌细胞,诱导线粒体损伤,并最终导致细胞凋亡的过程。整个过程可以分为以下几个关键步骤:
靶向与内化:
“铁噬”纳米粒子(Dp44mT@HTH)表面覆盖有透明质酸(HA),使其能够特异性地识别并结合到癌细胞表面高表达的CD44受体上。
通过受体介导的内吞作用,纳米粒子被癌细胞摄取并内化进入细胞质中。
溶酶体逃逸与药物释放:
进入细胞后,纳米粒子在溶酶体内由于pH值的变化(由于HCQ的质子海绵效应)以及纳米粒子本身的ROS敏感性,导致纳米粒子解体。
解体后,释放出其内部包裹的铁螯合剂Dp44mT和自噬抑制剂羟基氯喹(HCQ)。
线粒体损伤:
Dp44mT进入细胞质后,迅速螯合细胞内的Fe²⁺,导致线粒体中铁硫簇(Fe-S clusters)的生物合成受阻,进而扰乱线粒体呼吸链功能。
线粒体呼吸链功能受损导致ATP生成减少、线粒体膜电位崩溃、线粒体钙超载等一系列线粒体功能障碍。
自噬抑制与线粒体累积:
HCQ不仅减少了细胞对Fe²⁺的摄入,还抑制了自噬体与溶酶体的融合,阻断了细胞通过自噬途径清除受损线粒体的能力。
受损的线粒体在细胞内不断累积,加剧了线粒体功能的崩溃,促进了细胞凋亡。
细胞凋亡与死亡:
随着线粒体功能的持续受损和受损线粒体的不断累积,细胞最终走向凋亡和死亡。
图1以直观的方式展示了“铁噬”纳米粒子抗肿瘤治疗的核心机制,即通过特异性靶向、药物释放、线粒体损伤和自噬抑制等多个环节的协同作用,实现对癌细胞的精准打击。这一机制不仅解释了纳米粒子如何诱导线粒体损伤,还揭示了自噬抑制在促进线粒体累积和细胞凋亡中的关键作用。
尤为值得一提的是,Dp44mT@HTH纳米粒子还展现出了良好的靶向性和生物安全性。这得益于其透明质酸外壳对CD44受体的特异性识别能力,以及纳米粒子在体内的稳定释放特性。这些优点使得“铁噬”纳米粒子在抗癌研究中具有广阔的应用前景。
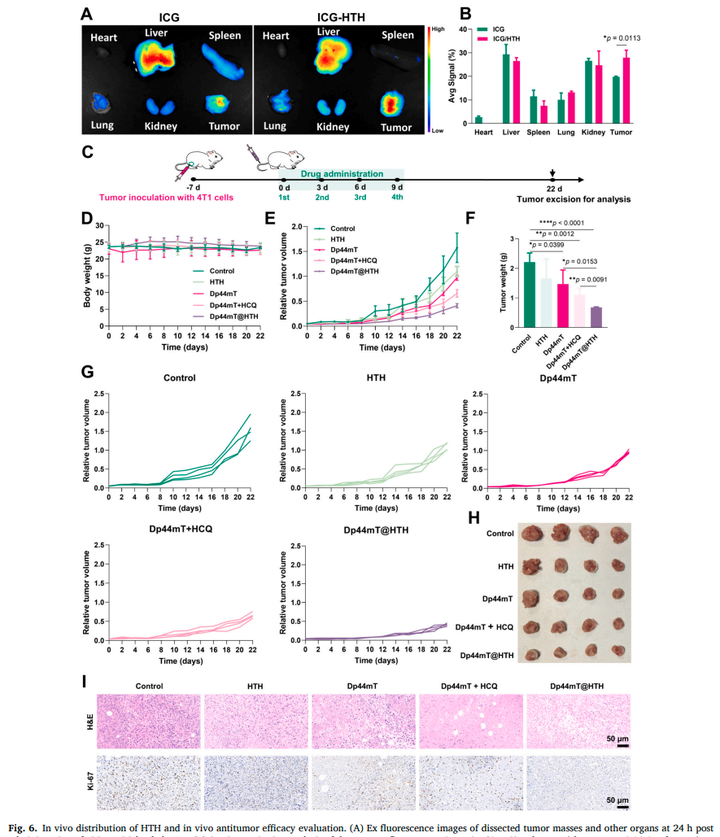
图6包含了多个子图,分别展示了HTH纳米载体的体内分布(A、B)、给药方案(C)、治疗期间小鼠体重变化(D)、肿瘤体积变化(E、G)、肿瘤重量(F)以及肿瘤组织的H&E染色和Ki-67免疫组化染色(I)。
体内分布(A、B):
图A展示了注射ICG标记的HTH纳米载体后24小时内,小鼠各主要器官和肿瘤组织中的荧光分布情况。结果显示,HTH纳米载体在肿瘤组织中的积累显著高于其他器官,表明其具有良好的肿瘤靶向性。
图B进一步通过半定量分析证实了HTH纳米载体在肿瘤组织中的富集程度显著高于游离ICG组,进一步验证了其肿瘤靶向能力。
给药方案(C):
图C简要描述了实验期间对小鼠的给药方案,包括给药次数、给药间隔以及各组小鼠接受的药物或载体类型。
治疗期间小鼠体重变化(D):
图D显示了治疗期间各组小鼠体重的变化情况。结果显示,各组小鼠体重变化趋势相似,未观察到明显差异,表明各治疗方案对小鼠整体健康状况无显著影响。
肿瘤体积变化(E、G):
图E展示了治疗期间各组小鼠肿瘤体积的变化曲线。结果显示,Dp44mT@HTH组小鼠的肿瘤生长受到明显抑制,肿瘤体积显著小于其他组。
图G进一步以相对肿瘤体积的形式展示了各组小鼠肿瘤生长情况,直观展示了Dp44mT@HTH组的抗肿瘤效果。
肿瘤重量(F):
图F展示了治疗结束后各组小鼠肿瘤的重量。结果显示,Dp44mT@HTH组小鼠的肿瘤重量最轻,进一步证实了其抗肿瘤效果。
肿瘤组织的H&E染色和Ki-67免疫组化染色(I):
图I通过H&E染色展示了各组小鼠肿瘤组织的病理学特征。结果显示,Dp44mT@HTH组肿瘤组织中出现大面积坏死区域,表明肿瘤细胞受到严重损伤。
同时,通过Ki-67免疫组化染色评估了肿瘤细胞的增殖活性。结果显示,Dp44mT@HTH组肿瘤细胞增殖活性显著降低,进一步证实了其抗肿瘤效果。
图6通过体内实验全面评估了“铁噬”纳米粒子的抗肿瘤效果。结果表明,该纳米粒子不仅具有良好的肿瘤靶向性,还能显著抑制肿瘤生长并降低肿瘤细胞增殖活性。同时,给药期间小鼠体重无显著变化表明该方案对小鼠整体健康状况无显著影响,进一步证实了其生物安全性。
这项研究不仅为抗癌研究提供了一种新颖的策略,还揭示了线粒体损伤与自噬抑制在抗癌过程中的协同作用机制。通过精准地调控细胞内铁代谢和自噬途径,“铁噬”纳米粒子为开发高效、低毒的抗癌方法开辟了新的道路。
展望未来,科学家们将继续优化“铁噬”纳米粒子的设计,提高其生物利用度和靶向性。同时,他们还将探索该纳米粒子在其他类型癌症中的应用潜力,以期为更多患者带来福音。此外,随着对线粒体功能和自噬机制的深入研究,“铁噬”效应有望在更多领域展现出其独特魅力,为生物医学研究注入新的活力。
总之,“铁噬”纳米粒子的问世,不仅为抗癌研究注入了新的动力,也为我们揭示了生命科学的无限可能。AbMole提供的Hoechst 33342等核酸染料作为实验观察中的重要工具,也将在未来的科学研究中发挥更加重要的作用。





















 1900
1900

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








