鼻咽癌(Nasopharyngeal carcinoma,NPC)作为头颈部恶性肿瘤的一种,其侵袭性和高度转移性导致传统的治疗方案面临重大挑战。患者治疗后无响应甚至复发成为鼻咽癌治疗的重要问题。伴随着对肿瘤微环境的认识,免疫检查点抑制剂联合化疗成为改进鼻咽癌治疗效果的新疗法,这种疗法为癌症的治疗提供了新的可能性。
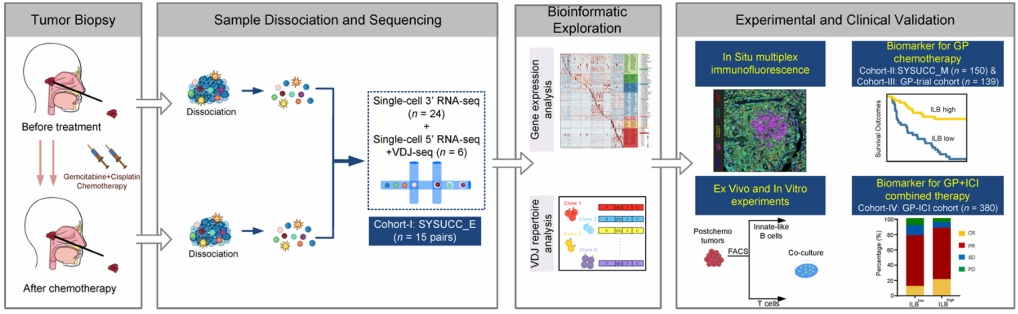
来自中山大学肿瘤防治中心马骏院士领衔的研究团队在《Nature Medicine》发表的一项题为“The tumor immune microenvironment of nasopharyngeal carcinoma after gemcitabine plus cisplatin treatment”的研究采用了单细胞测序、流式细胞术、组织空间分析等多种技术提供了联合治疗后肿瘤免疫微环境的高分辨率图谱,揭示了以先天样B细胞为主导的抗肿瘤机制,为NPC患者临床治疗提供了新思路

01 联合治疗后肿瘤免疫微环境的变化
研究人员首先使用单细胞测序分析了来自15例患者在Gemcitabine联合顺铂化疗(GP化疗)前后匹配的30例肿瘤样本(图1A)。研究人员发现患者的肿瘤细胞在化疗后显示出了抗原呈递分子的表达增加。这种特征与患者的良好预后相关(图1B-C)。因此研究人员进一步分析了GP化疗促进癌细胞抗原呈递的机制。GP化疗后鼻咽癌样本中STING的表达显著增强(图1D),通过基因敲除和体外细胞实验,最终确定了GP化疗通过STING依赖性IFN-Ⅰ途径增强鼻咽癌细胞中MHCⅠ类抗原呈递。癌细胞MHCⅠ类表达的增强促使研究者进一步探究T细胞的变化,结果显示GP化疗后T细胞显示出了较好的变化,主要表现为细胞杀伤因子分泌增加和细胞浸润程度增加(图1E-F)。同时TH1-like细胞和TFH细胞显示出与患者的生存高度相关(图1G)。
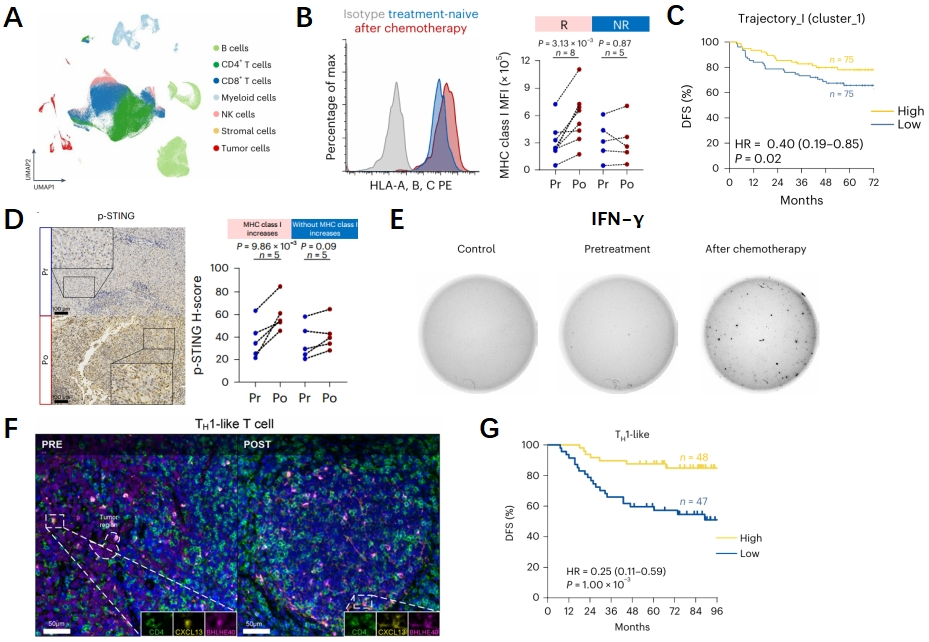
图1 GP放疗后肿瘤免疫微环境的变化
02 ILB细胞可能存在与T细胞的相互作用
研究人员继续探究了鼻咽癌微环境中T细胞激活的因素。GP化疗后髓系细胞的频率显示出了不变甚至降低的趋势,同时与CD4+T细胞的相互作用也并无显著变化(图2A)。但B细胞与TH细胞显示出了较高的相互作用评分,在此研究人员确定了两个在GP化疗后显著增加的B细胞簇(Cluster 5和8)(图2B-C)。这两个细胞簇处于初始状态,但表达了更高的记忆细胞的标志物CD27,这预示着2个B细胞簇具有先天样表型(ILB)(图2D)。ILB细胞与TFH或TH1-like细胞之间的相互作用评分较高,这预示着ILB细胞可能在鼻咽癌微环境中调节TFH细胞和TH1-like细胞(图2E)。
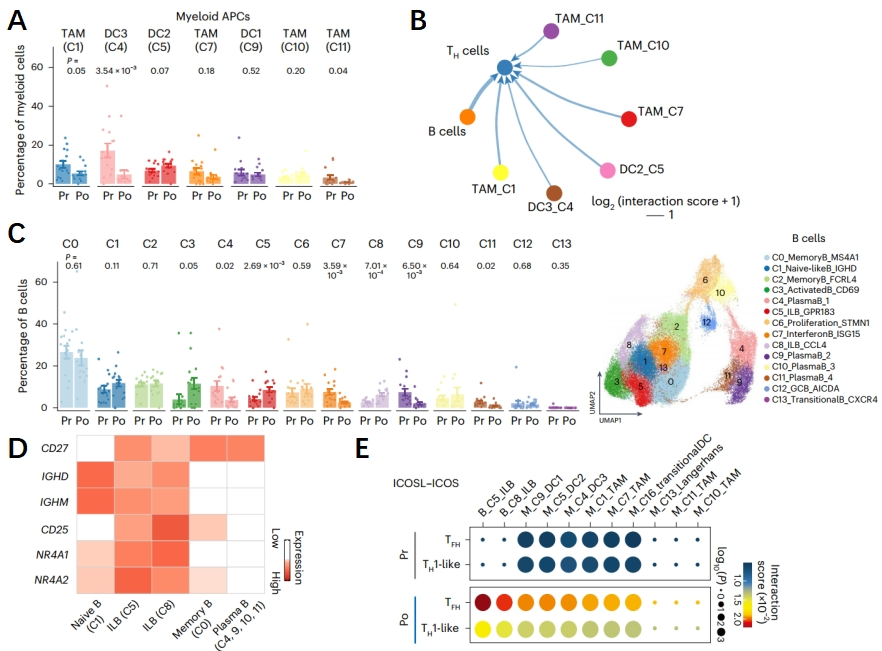
图2 ILB调节鼻咽癌微环境T细胞
03 组织空间分析发现ILB邻近的T细胞亚群
为了进一步探究GP化疗后ILB细胞对鼻咽癌微环境的影响,研究人员对患者样本进行了时空分析,在治疗应答的患者中,化疗后三级淋巴器官(TLO)中出现了明显的ILB细胞聚集。但在无应答患者中基本无变化。同时化疗一周后应答者TLO中ILB细胞频率显著增加,而在无应答者中ILB频率仅有少量的增加(图3A-B)。在关注ILB细胞的同时,研究人员还分析了靠近ILB细胞的T细胞,结果显示靠近ILB细胞的T细胞显示出更高的增殖比例。在该区域中存在更多的TH1、TFH和GZMB+CD8+T细胞,存在较少的Treg和HAVCR2+CD8+T细胞(图3C-D)。在揭示了ILB细胞和T细胞在空间上的高度相关性后,研究人员通过体外共培养实验探究ILB细胞的功能。共培养结果显示ILB细胞介导扩增的T细胞可以增强CD8+T细胞GZMB和perforin的分泌(图3E)。
单细胞数据集显示ICOSL-ICOS轴是ILB细胞和效应TH细胞间排名最高的配受体对之一,通过体外阻断ICOS受体信号,TH1和TFH的扩增被抑制。ICOS信号在mTOR通路中发挥作用,触发糖酵解和后续的效应T细胞增殖。在细胞中加入ICOS激动剂显著激活PI3K-Akt-mTOR通路(图3F-G),以上结果表明ILB细胞通过ICOSL-ICOS轴促进T细胞的扩增。
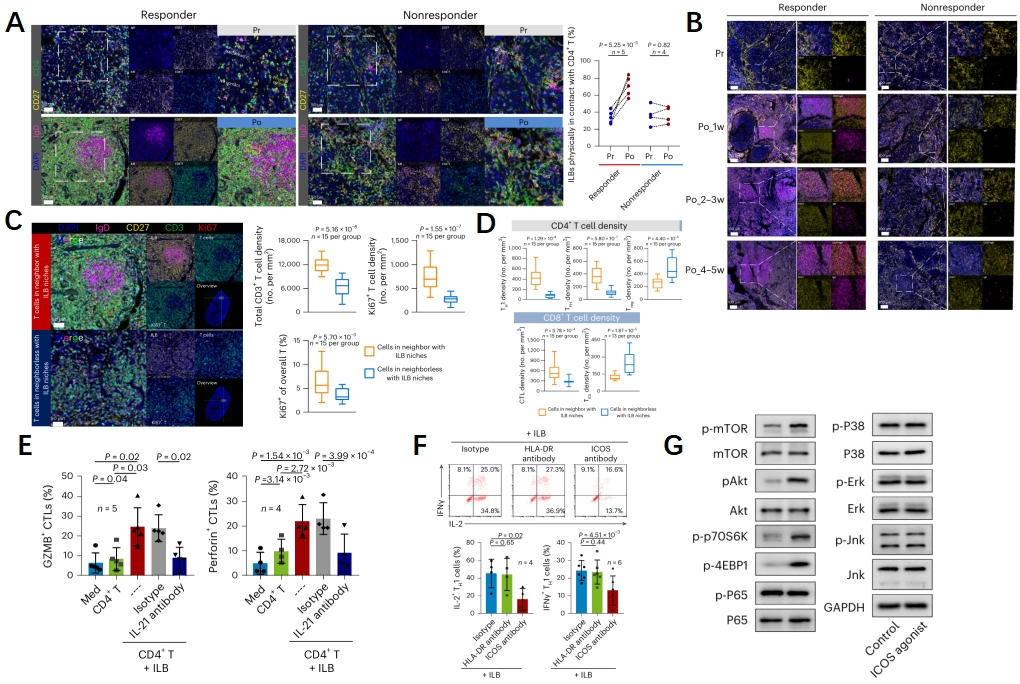
图3 ILB通过ICOSL-ICOS促进T细胞增殖
04 ILB作为生物标志物的临床意义
ILB细胞在鼻咽癌患者GP化疗中显示出了重要作用。研究人员进一步探讨了ILB细胞的临床意义。在GB化疗中ILB细胞频率相比于树突状细胞(DC)或肿瘤相关巨噬细胞(TAM)可以更有效的预测治疗响应和无响应者,同时ILB细胞频率与化疗反应也有着高度的相关性(图4A-C)。研究人员使用多项临床实验样本或数据集进行了分析,发现在多种患者的亚组中(压组包含年龄、性别、是否吸烟等多种因素),肿瘤浸润性ILB细胞的频率增加与患者客观缓解率、良好无病生存期(DFS)和总生存(OS)显著相关。最后研究人员通过多变量Cox回归分析,确定了ILB细胞频率可以作为独立预测因素(图4D-F)。
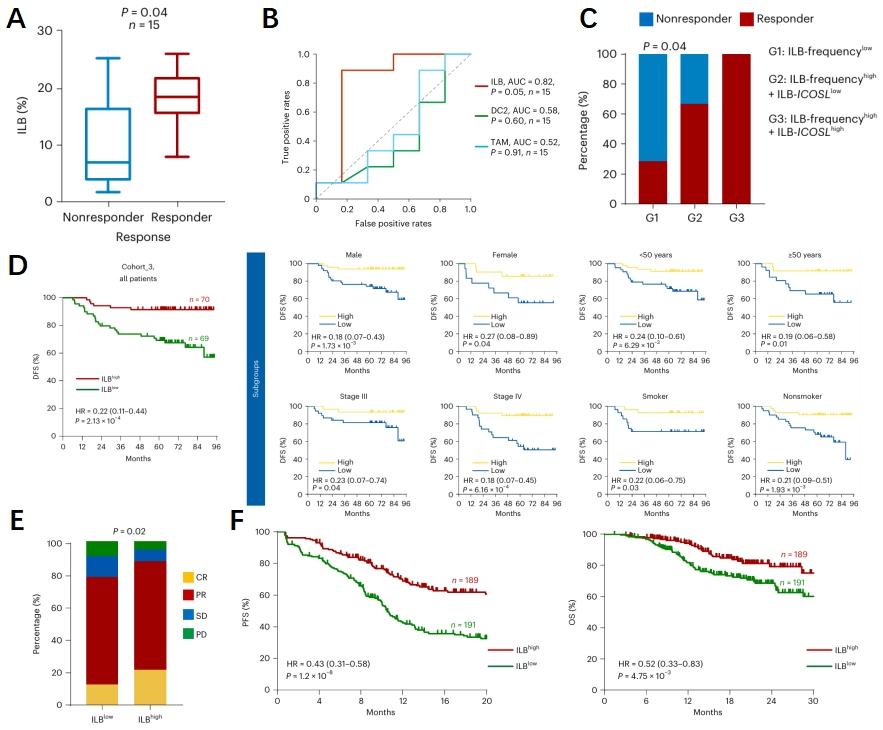
图4 ILB预测患者结局
总结与讨论
本研究揭示了Gemcitabine联合顺铂化疗对鼻咽癌免疫微环境的改变,分析了先天样B细胞(ILB)在GP化疗后促进效应T细胞增殖并增强细胞毒性T细胞功能的机制。最终结合临床数据将ILB细胞确定为独立的疾病预测因素。新疗法开发及临床应用中需要针对患者病灶深入解析,发现其中的关键分子或细胞,从而实现对疾病的全面理解。特别是该研究通过组织空间分析发现了ILB细胞邻近的微环境特征,揭示了ILB细胞互作的细胞亚群,阐明了ILB细胞重要的临床意义背后的内在机制。
| 空间多组学整合方案
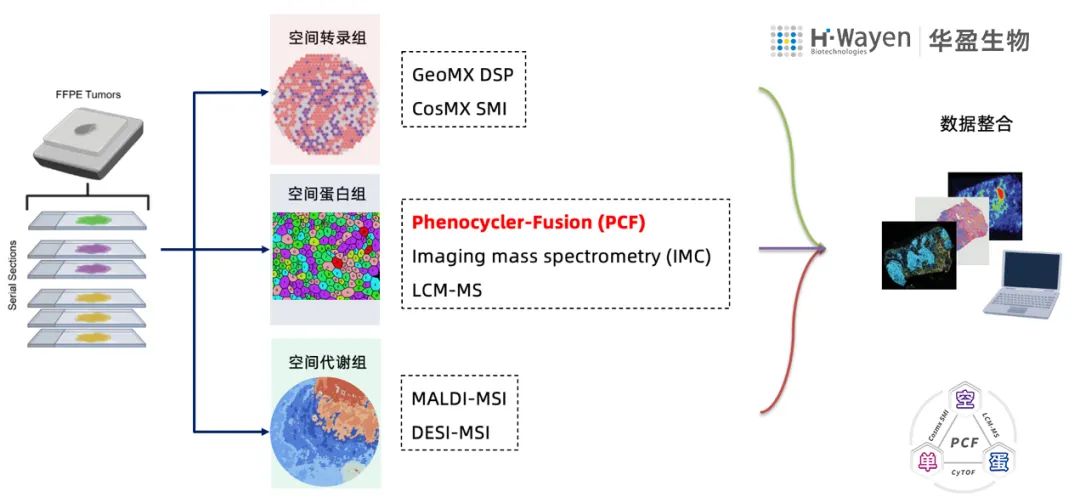
| PCF空间单细胞蛋白组学优势

华盈生物PhenoCycler-Fusion单细胞原位空间蛋白组学技术资格证书

华盈生物是美国Akoya Bioscience公司的PhenoCycler-Fusion空间单细胞蛋白组学技术认证服务商,已经被纳入了该技术的全球CRO服务提供者体系。借助全球领先的PhenoCycler-Fusion空间单细胞蛋白组学技术平台的建立,华盈生物将为中国客户提供更具精准医学特色的服务与合作,推动中国团队在空间生物学领域的研究水平,加快构建符合中国人群的精准医学模式。


业务咨询400-869-2936或17316301592(微信同号)
相关文献
Lv J, Wei Y, Yin JH, et al. The tumor immune microenvironment of nasopharyngeal carcinoma after gemcitabine plus cisplatin treatment. Nat Med. 2023 ;29(6):1424-1436.
![]()
1)Hepatology|中山一院于君/李晓星团队利用空间单细胞蛋白组揭示肝细胞癌的免疫微环境
2)Cancer Discovery | 非小细胞肺癌的空间蛋白组学研究再添新篇章
3) Cancer Cell| 樊嘉院士/张力烨团队解析转移性肝细胞癌的时空演变
4) Nat Commun|直捣黄龙!空间单细胞组学发现外周血靶细胞亚群的组织落脚点
5)Nat Genet|马丁院士团队利用单细胞和空间多组学描绘宫颈鳞癌免疫微环境图谱
6) Cancer Cell | 北大医院李航/张宁/薛瑞栋团队揭示肢端黑色素瘤空间细胞互作关系
7) Cell:如何升华你的单细胞数据——PCF空间单细胞蛋白组联合scRNA-seq解析骨髓微环境
8) Cell长文:肿瘤研究中空间单细胞蛋白组技术如何提升10x 空转数据层次
9) 先睹为快!2024 AACR年会:PCF空间单细胞蛋白组应用案例集锦
| 工作邮箱:market@wayenbiotech.com
| 官网链接:www.wayenbio.com























 1072
1072

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








