肿瘤生物学研究领域中,肿瘤血管生成是一个重要的过程,它不仅为肿瘤组织提供必需的能量和氧气,同时与肿瘤的发展、转移密切相关。因此血管新生是肿瘤从良性转变成恶性的一个关键步骤。尽管血管生成在肿瘤发展中的重要性已被广泛认识,但对其精确的细胞和分子机制的理解仍然有限。传统的研究方法往往难以揭示肿瘤血管系统的全貌,因此如何全面理解肿瘤血管系统是研究者共同面临的难题。
近期来自重庆大学三峡医院的团队在《Nature》(IF=50.5)发表的一项题为“Tumour vasculature at single-cell resolution”的研究采用了单细胞测序、空间转录组、空间单细胞蛋白组等技术揭示了肿瘤血管生成的细胞起源和分化轨迹,识别了与疾病进展、预后和治疗反应相关的特定血管细胞亚群,为抗血管生成的癌症疗法提供了新的标志物和靶点。

01 肿瘤内皮单细胞图谱构建
研究人员对来自372例供体的437个肿瘤样本进行了分析,结果包含了31种癌症类型的200,000个细胞的数据。在肿瘤组织中,内皮细胞可以分为淋巴内皮细胞(LECs)和血管内皮细胞(VECs),而血管内皮细胞可以进一步的分为动脉内皮细胞(ArtECs)、静脉内皮细胞(VenECs)和毛细胞血管样内皮细胞(CapECs)(图1A-C)。接下来研究人员对VECs、LECs和MCs进行无监督聚类分析,将这些细胞共分为29个VEC亚簇、8个LEC亚簇和16个MC亚簇(图1D)。其中多数亚簇表现出泛癌起源,但也存在部分亚簇表现出了癌症特异性,如妇科肿瘤来源的CapECs高表达CXCL1和CXCL3,与子宫内膜癌和卵巢癌的进展相关,皮肤肿瘤来源的CapECs和LECs表达皮肤相关标记物PERP和KRT1413。这些亚群在随后的泛癌分析中被排除。
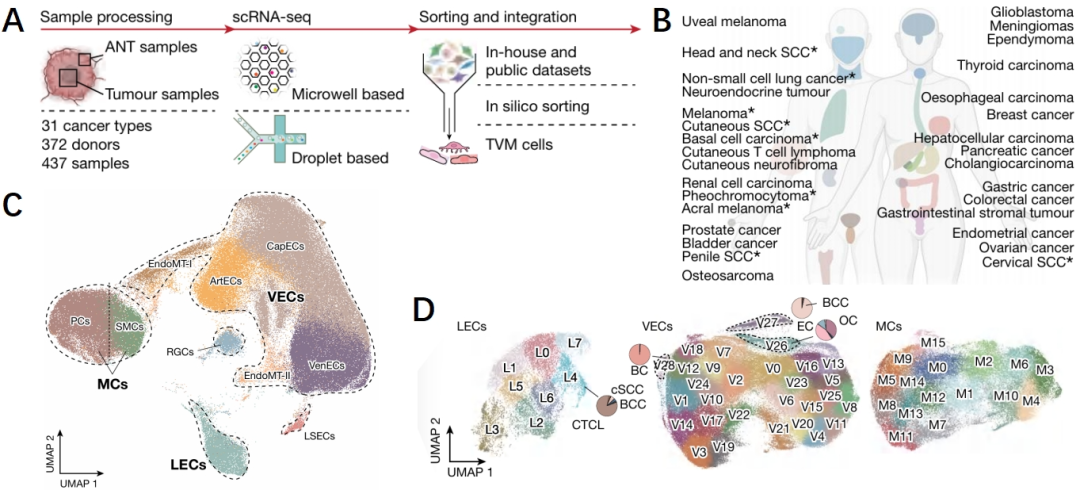
图1 肿瘤内皮细胞精准分型
02 肿瘤血管生成的细胞起源和进化
肿瘤血管的生成可能建立在已有的血管上,为了进一步研究肿瘤血管生成的细胞机制,研究人员对泛癌VECs的数据进行了分析,为了研究肿瘤血管生成的轨迹,研究人员使用了多种分析方法推测出VenECs – CapECs – ArtECs的分化轨迹(图2A-B)。同时研究人员构建了斑马鱼体内肿瘤血管生成模型,肿瘤诱导的新生血管逐渐从肠下静脉向肿瘤部位延伸,这个结果证实了肿瘤血管的分化轨迹(图2C)。同时新生血管表现出毛细血管样特征。血管生成过程中,尖端细胞感知并响应引导信号,茎细胞尾随其后,拉长芽茎形成管腔。研究人员进一步对CapECs的表型进行了分析,鉴定出了尖端样(Tip-like)、茎样(Stalk-like)和过渡态的CapECs,并定义了Tip-like和Stalk-like的发育轨迹,其中Tip-like在早期表达Apelin,并且在肿瘤组织中明显富集,研究人员在此识别了APLN+TipSⅠ细胞,并发现APLN+TipSⅠ细胞与患者生存显著相关(图2D-G)。
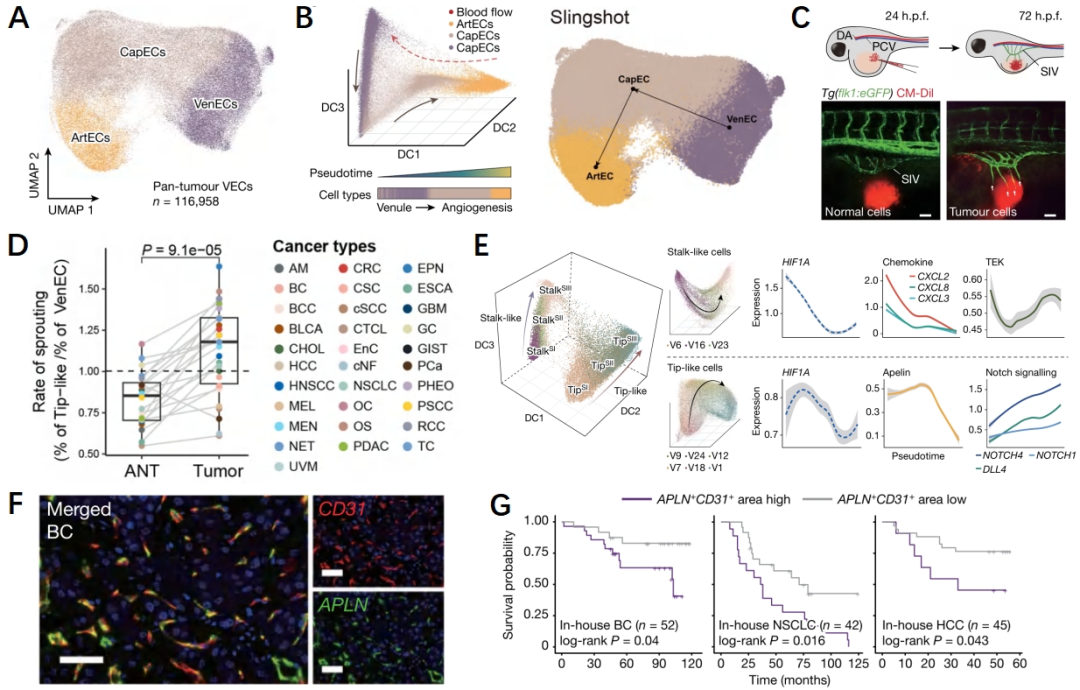
图2 肿瘤血管的起源和进化
03 淋巴内皮细胞异质性
淋巴内皮细胞同样是肿瘤血管生长的重要组分,研究人员分析了泛癌LECs的分化轨迹,发现LECs显示出了两种不同的分化轨迹。其中轨迹T1主要负责淋巴血管生成,而轨迹T2负责抗原呈递。基因分析证实了两种分化轨迹的LECs显示出了对应功能的基因表达,同时HIF1α在T1的表达明显高于T2,这与血管内皮细胞表现出了一致的趋势,证明缺氧可能是肿瘤血管和淋巴管生成的重要因素(图3A-C)。接下来研究人员分析了在Tip/Stalk(T1)和apLECs(T2)两种亚型中的转录因子变化,其中PROX1在T1中的表达明显高于T2,同时PROX1是NFKB1的下游基因,这预示着炎症反应可能与淋巴管生成相关。与T1相反,apLEC(T2)中抗原转录因子TSC22D3特异性表达(图3D-E),已有研究表明TSC22D3可抑制NF-κB核易位和DNA结合。通过空间单细胞蛋白组研究人员确定了apLECs(TSC22D3highNFKB1low)和Tip-likeLECs(TSC22D3lowNFKB1high)的存在。同时可以作为临床结局的预测因素(图3F-G)。
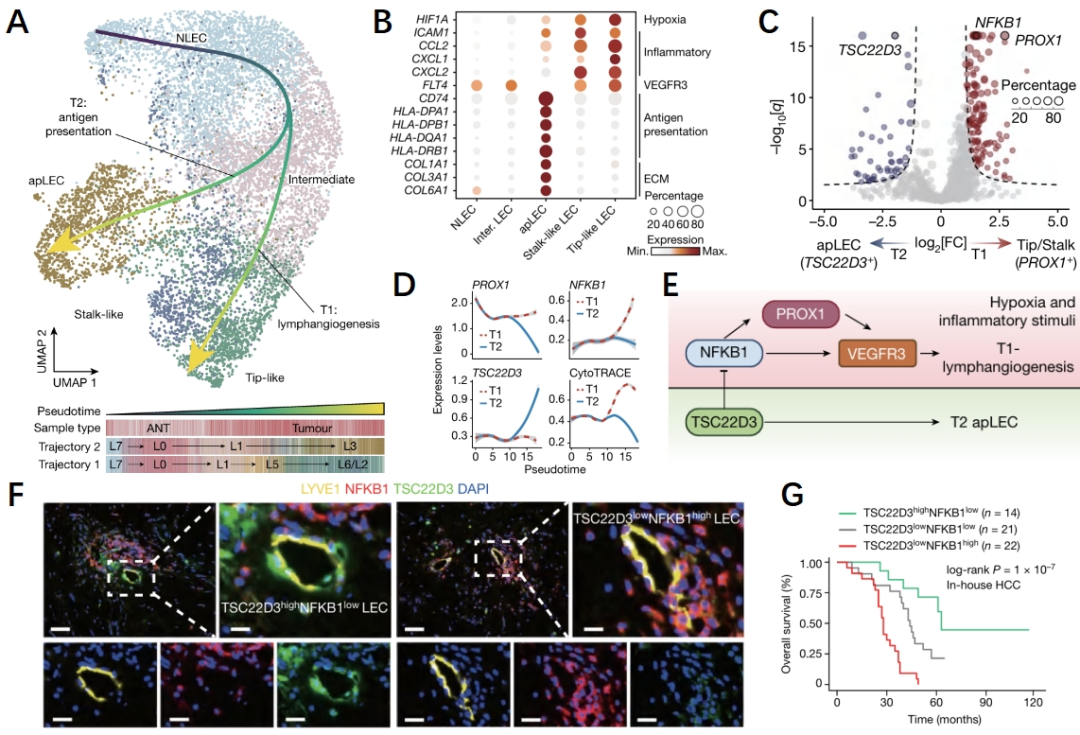
图3 淋巴内皮细胞异质性
04 肿瘤血管与肿瘤微环境的相互作用
为了剖析脉管系统和肿瘤微环境(TME)的相互作用,研究人员对髓系细胞、T细胞、NK细胞、B细胞等多种细胞进行了分型。并将血管细胞和TME细胞进行了相互作用分析。其中髓系细胞和成纤维细胞显示出更多的相互作用,同时研究人员观察到SPP1+ TAM与血管细胞的相互作用频率最高(图4A-B)。研究人员使用空间转录组和空间单细胞蛋白组验证了APLN+ TipSⅠ细胞和SPP1+TAM紧密的空间关系,其中APLN+ TipSⅠ细胞表现出对T细胞的免疫调节潜能(图4C-D)。研究人员进一步发现,APLN+ TipSⅠ可通过CAM1-SPN等多个配受体对诱导T细胞功能障碍和衰竭。这些结果表明APLN+ TipSⅠ有助于形成血管生长的免疫抑制TME(图4E-F)。
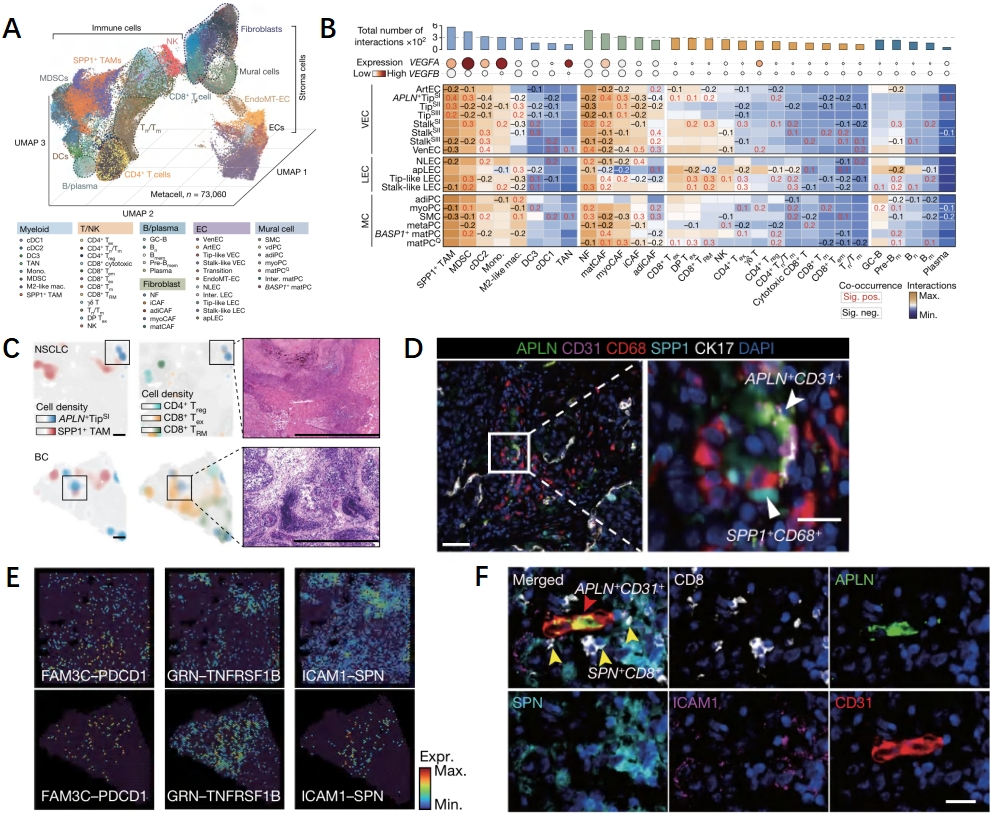
图4 血管细胞和TME细胞的互作关系
总结与讨论
本文通过多组学技术构建了全面的肿瘤血管图谱,不仅指出静脉内皮细胞是肿瘤血管生成的起点,并且发现了与疾病进展和患者不良预后相关的细胞亚群。空间组学帮助研究人员阐明了肿瘤血管生成的分子机制和细胞间的相互作用。贝伐珠单抗作为抗血管生成的代表性抗肿瘤药物,可能出现治疗效果不佳的现象,本文发现的互作细胞为抗血管生成疗法提供了潜在的临床靶点。
如何利用空间组学更好的进行血管研究呢?
血管微环境复杂且关键,血管细胞不仅自身具有极高的异质性,其周围存在的免疫细胞、基质细胞也可能与其发生交互通讯,因此如何全面的看待血管微环境是肿瘤血管、心脑血管等多种疾病研究的重要问题。PhenoCycler-Fusion空间单细胞蛋白组作为空间组学研究的代表技术之一,可以实现组织全片(18x35mm)原位上>100多个抗体的检测,可以帮助我们最大程度还原组织复杂环境,获取更加真实有效的空间信息。以下是应用PhenoCycler-Fusion空间单细胞蛋白组的两个具体案例:
案例一
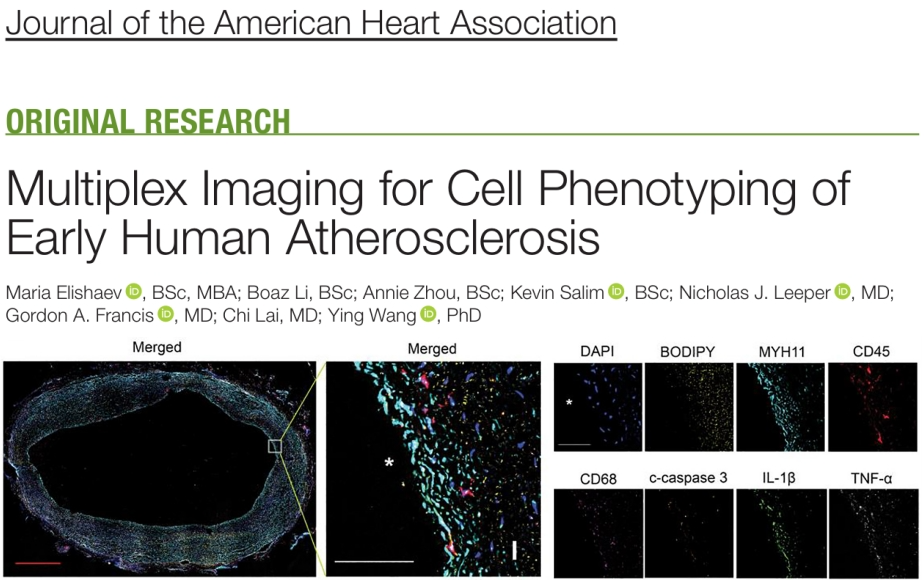
图5 动脉粥样硬化泡沫细胞在血管周围的分布
动脉粥样硬化是多种心脑疾病的诱因,本文研究人员分析了导致动脉硬化的关键细胞—泡沫细胞(Foam Cells)在动脉粥样硬化中的发病机制。通过空间单细胞蛋白组,研究人员发现了以往未知的多个问题。1、人类动脉粥样硬化病变组织中的泡沫细胞主要来源于血管平滑肌细胞而非白细胞。2、泡沫细胞主要富集在早期动脉粥样硬化中脂质积累的深层内膜。3、泡沫细胞与凋亡或促炎细胞的表达关联性不高。
案例二

图6 系统性硬化症的关键血管细胞
系统性硬化症(SSc)作为一种结缔组织疾病,主要表现为血管变化、自身免疫和纤维化重塑。血管细胞的异质性是发现疾病靶点的关键问题。研究人员通过空间单细胞蛋白组识别了7种不同的血管内皮细胞(VEC)亚群,其中CD34+α-SMA+CD31+VECs微环境富含免疫细胞和肌成纤维细胞,这些细胞表达内皮-间质转化(EndMT)的标志物。同时发现该细胞的密度与SSc患者纤维化进展相关。
|空间多组学整合方案
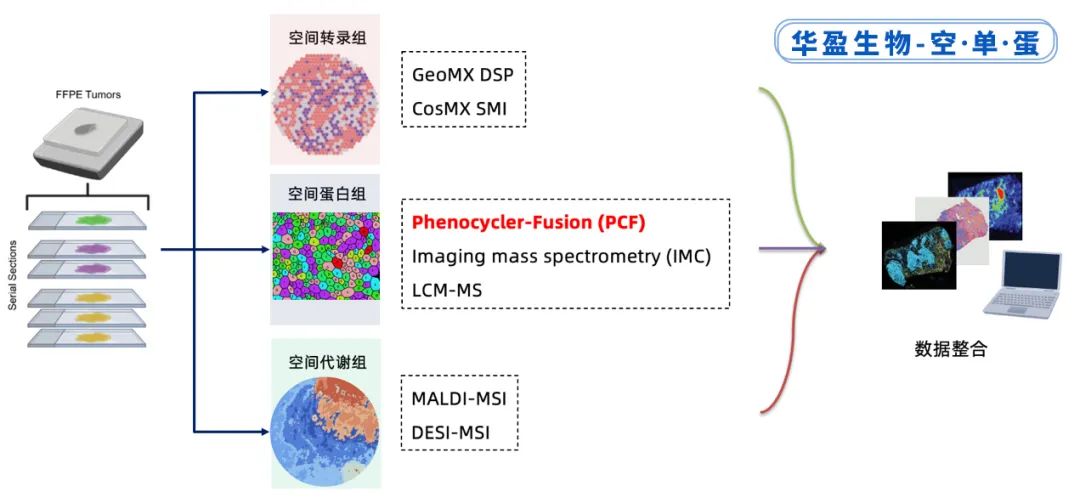
| PCF空间单细胞蛋白组学优势

华盈生物PhenoCycler-Fusion单细胞原位空间蛋白组学技术资格证书

华盈生物是美国Akoya Bioscience公司的PhenoCycler-Fusion空间单细胞蛋白组学技术认证服务商,已经被纳入了该技术的全球CRO服务提供者体系。借助全球领先的PhenoCycler-Fusion空间单细胞蛋白组学技术平台的建立,华盈生物将为中国客户提供更具精准医学特色的服务与合作,推动中国团队在空间生物学领域的研究水平,加快构建符合中国人群的精准医学模式。


业务咨询400-869-2936或17316301592(微信同号)
相关文献
1.Pan X, Li X, Dong L, et al.Tumour vasculature at single-cell resolution. Nature. 2024. Epub ahead of print.
2.Elishaev M, Li B, Zhou A, et al.Multiplex Imaging for Cell Phenotyping of Early Human Atherosclerosis. J Am Heart Assoc. 2024 ;13(12):e034990.
3.Rius Rigau A, Li YN, Matei AE, et al.Characterization of Vascular Niche in Systemic Sclerosis by Spatial Proteomics. Circ Res. 2024 ;134(7):875-891.
![]()
1)Nature Commun|牙周病的全新视角:单细胞与空间技术解析牙龈上皮周围免疫微环境
2)Cancer Cell | 卞修武院士/时雨/平轶芳团队揭示胶质瘤巨噬细胞研究全新视角
3) Nature Medicine | 马骏院士团队解析鼻咽癌联合治疗后的肿瘤免疫微环境
4)Hepatology|中山一院于君/李晓星团队利用空间单细胞蛋白组揭示肝细胞癌的免疫微环境
5)Cancer Discovery | 非小细胞肺癌的空间蛋白组学研究再添新篇章
6) Cancer Cell| 樊嘉院士/张力烨团队解析转移性肝细胞癌的时空演变
7) Nat Commun|直捣黄龙!空间单细胞组学发现外周血靶细胞亚群的组织落脚点
8)Nat Genet|马丁院士团队利用单细胞和空间多组学描绘宫颈鳞癌免疫微环境图谱
9) Cancer Cell | 北大医院李航/张宁/薛瑞栋团队揭示肢端黑色素瘤空间细胞互作关系
10) Cell:如何升华你的单细胞数据——PCF空间单细胞蛋白组联合scRNA-seq解析骨髓微环境
| 工作邮箱:market@wayenbiotech.com
| 官网链接:www.wayenbio.com























 1069
1069

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








