胎儿大脑发育是一个复杂的过程,涉及不同的生长和组织阶段,这对于大脑回路和神经连接的发展至关重要。胎儿脑图谱和标记数据集是研究产前大脑发育的有前景的工具。它们支持识别非典型大脑模式,为潜在的临床条件早期迹象提供洞见。简而言之,产前大脑成像和通过现代工具进行的后处理是一个前沿领域,将显著推进我们对胎儿发育的理解。
在这项工作中,我们首先对特定术语(即"大脑模板"和"大脑图谱")进行术语澄清,突出了文献中术语使用不一致可能导致的误导性解释。我们讨论了表征胎儿大脑发生过程的主要结构和神经发育里程碑。我们的主要贡献是对18个产前大脑图谱和3个数据集进行系统性综述。我们还简要关注了产前神经影像学的临床、研究和伦理含义。本文发表在Neuroimage杂志。
要点:
•对于胎儿大脑发育的研究,术语澄清迫在眉睫。
•描述胎儿大脑发生过程的主要结构具有临床相关性。
•已回顾18个胎儿大脑图谱和3个MR图像数据集。
•需要提供年龄相关分割的多模态时空图谱。
•考虑胎儿神经影像学未来的临床和伦理影响至关重要。
关键词:
胎儿 磁共振成像 大脑图谱 大脑数据集
缩略语:
T2W:T2加权;GA:孕周;MRI:磁共振成像;DL:深度学习;ROI:感兴趣区域
CB:小脑;WM:白质;GM:灰质;CGM:皮质灰质;DGM:深部灰质;LV:侧脑室;BS:脑干;CSF:脑脊液;ECSF:外部脑脊液;VCSF:脑室脑脊液;CP:皮质板;GE:节细胞隆起;CC:胼胝体;HP:海马;LN:豆状核;TH:丘脑;DWI:弥散加权成像;DTI:弥散张量成像;FA:部分异性度;MD:平均扩散率;CFA:彩色编码部分异性度;RD:径向扩散率;AD:轴向扩散率;FOD:纤维方向分布
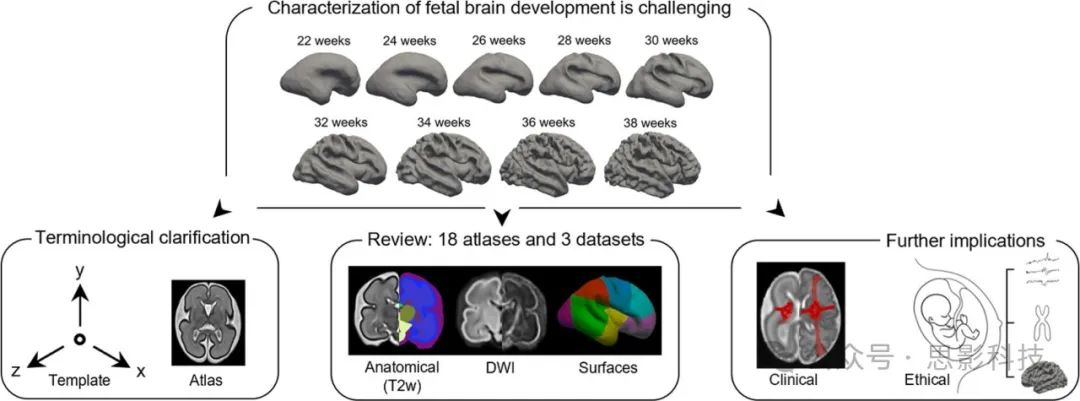
图示摘要
1. 引言
大脑图像的定量分析通常在其流程中包含一些先验信息,以定义标准化坐标系统、识别特定结构并定义正常范围。在磁共振成像(MRI)研究中定义和纳入先验知识的常见方式是定义模板或图谱。在文献中,"大脑模板"和"大脑图谱"经常被部分互换使用,尽管这些构造在研究和临床实践中可能存在细微但相关的差异(Dickie et al., 2017)。因此,对这些术语进行简明的澄清至关重要。"大脑模板"(以下简称"模板")可用于指代用于对齐和分析图像的通用参考空间。相比之下,"大脑图谱"(以下简称"图谱")通常用于指代在参考空间中结构化的数据集合,捕捉人群的解剖(如结构解剖)或生理(如结构和功能连接)特征。图谱也可以在时间域中定义,显示特定数据如何随时间变化和演变。这对于我们理解胎儿神经发育特别相关,因为它可以提供人类大脑架构的洞察。因此,在胎儿场景中,时空图谱是捕捉怀孕期间大脑变化的最有前景的工具。迄今为止,胎儿大脑图谱是基于以周表示的孕周(GA)定义的。
在这项工作中,我们关注包含结构图像和一些相关特征或指标(如结构标签和连接图)的图谱。在文献中,"图谱"用于指代两种不同的图像:图谱参考图像(即大脑的MR图像)和图谱标签图像,后者表示每个大脑体素的解剖结构或组织(另见Makropoulos et al., 2018)。标签允许对大脑体积和形状进行定量分析,并可能促进对大脑功能的更好理解。
在过去几十年里,图谱一直是将先验知识纳入许多最流行的分割算法(如SPM-Dartel(Ashburner, 2007)、FreeSurfer(Fischl et al., 2002)、ANTs(Avants et al., 2011)、FSL-Fast(Zhang et al., 2001))的最先进方法。这是并且仍然是由于它们能够通过最大化参考图像(即图谱参考图像)和受试者MR图像之间相似性的配准过程,将人群图谱的标签匹配到新受试者。此外,图谱是进行聚合大脑发育分析的先决条件,因为它们允许建立受试者之间的对应关系。值得注意的是,就我们的目的而言,图谱仍然是评估产前期大脑发育的可靠工具。
根据上述操作定义,图谱可分为三个主要类别:"单一受试者"图谱、"多受试者"图谱和"概率"图谱。在单一受试者图谱中,图谱参考图像描述单个受试者的解剖结构(Holmes et al., 1998),相关标签通常源自手动过程,为每个体素分配特定标签。为克服依赖单个受试者的局限性,可以使用多个受试者的数据创建图谱。实际上,在"多受试者"图谱中,图谱参考图像被定义为多个受试者的解剖图像集合,而图谱标签图像指的是为每个受试者计算的标签集合。以下我们也将这种"多受试者"图谱称为"数据集"。相比之下,概率图谱通过合并多个受试者的图像来得出其图谱参考图像,从而反映人群解剖结构的变异性(Mazziotta et al., 2001; Irfanoglu et al., 2022)。在这种情况下,通常使用自动分割方法为每个体素分配给定标签的概率。
与产后图谱相比,胎儿MRI大脑图谱的构建面临两个主要挑战。首先,胎儿MRI本身就是一项具有挑战性的任务,因为大脑的大小、扫描仪中母亲的身体(有时还有兄弟姐妹)以及胎儿的运动(Uus et al., 2023b)。胎儿MRI最常见的采集方案涉及快速2D序列的采集,包括具有高平面分辨率但也有较大厚度的几个切片(Ciceri et al., 2023)。获得的图像可能存在运动引起的伪影(例如,连续切片之间的不一致)和与标准平面(即轴向、冠状、矢状)不同的采集平面。其次,在产前期,大脑极其可塑并经历惊人的生长(Garcia et al., 2018a)。因此,有必要为非常狭窄的时间窗口(即以周为范围)使用特定的大脑图谱(Evans et al. 2012)。
据我们所知,聚焦于产前场景,只有两项工作对大脑图谱进行了严格的综述(Makropoulos et al., 2018; Oishi et al., 2019)。尽管Makropoulos及其同事主要旨在提供产前和新生儿期自动大脑分割技术的全面综述,但他们也筛选了可用的图谱,并发现了胎儿领域的两个概率图谱。次年,Oishi及其同事进行了类似的研究,也包括产后直到72个月。因此,报告了产前期的三个概率图谱。自那时起,几项已发表的研究解决了为胎儿MRI定义模板和图谱的问题。
在当前工作中,我们旨在提供这一具有挑战性研究领域最新发现的全面综述。我们特别关注产前期,并筛选了最近引入的MRI图谱,因为科学和临床兴趣正在增加,神经影像学技术(如弥散MRI,Karimi et al., 2021)在探索胎儿发育方面取得了进展。我们还报告了公开可用的链接,因为数据可用性对于开发能够解决胎儿大脑变化和疾病相关解剖改变广泛范围的人工智能(AI)算法至关重要。用于胎儿神经影像学的AI工具可能是该领域最活跃和最有前景的挑战。这些以及胎儿成像的其他进展可能成为未来研究和临床应用的潜在游戏规则改变者,但这种方法可能带来重大的伦理关切。
1.1. 产前大脑发育框架
在妊娠期间,胎儿大脑经历其多个脑结构的显著发育,特征为细胞增殖、迁移和网络形成(Serati et al., 2019)。胎儿大脑MRI有潜力监测不同脑区大小和形态的变化。一些区域可能/应该随时间消失。例如,一个有趣的暂时性结构是节细胞隆起(GE)(图1)。它是胎儿大脑腹侧端脑的增殖结构,在受孕后第5周出现,在妊娠第35周内消失(Boitor-Borza et al., 2021),它包含基底神经节、丘脑、杏仁核和大脑皮质中间神经元的前体神经元(Righini et al., 2013)。
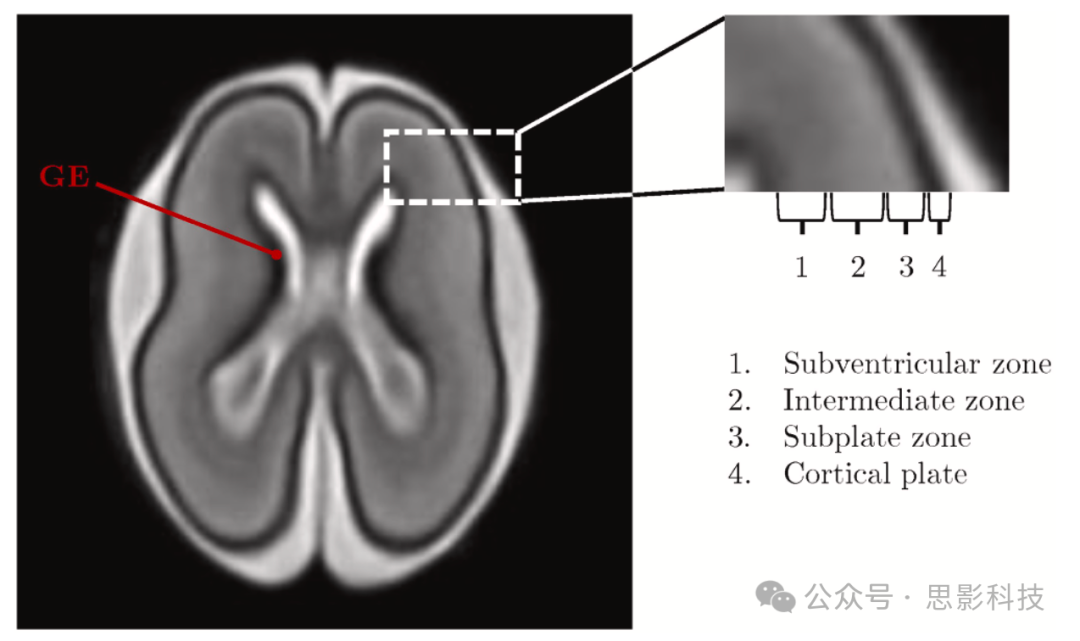
图1 21周胎儿的T2加权图像,显示大脑结构。图像放大部分描绘了胎儿端脑壁及其亚结构:室下区、中间区、皮质下带和皮质板。GE:节细胞隆起。
特别值得注意的是胎儿端脑壁及其亚结构。它具有分层结构,从内到外特征为脑室区和室下区、中间区、皮质下带和皮质板(CP,Huang et al., 2010)(图1)。从脑室区和室下区,神经元增殖并径向迁移到大脑表面,形成几个脑层,如CP和皮质下带,最终将成熟为新皮质(Barkovich et al., 2012)。皮质下带是一个暂时的大脑壁隔室,其中祖细胞和丘脑及大脑区域的传入神经纤维分离和生长。它是人类大脑皮质中最先发育的区域之一。皮质下带被描述为协调皮质活动的皮质放大器。敏感的生长和迁移窗口对认知功能有重要影响(Serati et al., 2019)。有假设认为,由于基因负荷导致的早期皮质下带突触回路改变可能参与精神病和神经发育障碍(如精神分裂症和自闭症)的病理生理学(Harkin et al., 2017)。CP(皮质板)经历其表面逐步折叠的过程,在胎儿期,特别是在第二和第三孕期,形成多个沟回,随着孕周增加呈线性增加(Garcia et al., 2018; Xu et al., 2022)。随着脑回形成的进展,表面积逐渐扩大,随孕周增加呈指数增长。相反,皮质厚度遵循双相进展,先增加后随孕周减少(Xu et al., 2022)。
妊娠期间发生的几种损伤可能改变这种复杂的大脑细胞组织机制,导致脑损伤。因此,上述结构的定量特征是评估胎儿大脑生长的一个有用的代理指标,有望及时检测到正常发育路径的早期偏差。在这种情况下,胎儿大脑的时空图谱是评估产前神经发育轨迹潜在偏离或异常的有用工具,并为基于人群的分析提供必要的参考空间。
2. 方法
第一作者(TC)于2023年9月进行了文献搜索,并于2024年1月重复了搜索。在PubMed文献数据库中使用与"胎儿"、"大脑"、"MRI"以及"图谱"或"模板"或"数据集"相关的适当搜索词(见补充材料1)。此外,还使用Google搜索引擎进行了手动搜索,以识别与我们研究问题相关的所有证据。所有包含的文章均为英文同行评议,没有预定义的日期限制或样本大小限制。
本次综述对检索到的文章应用的排除标准为:
• 不包括活体胎儿参与者的研究;
• 非MRI相关的样本数据(如超声成像);
• 非脑相关的样本数据;
• 不包含我们所指的图谱参考图像或图谱标签图像的文章。
病例报告、综述文章和观点文章被排除在结果之外,尽管手动评估了它们的参考文献列表以寻找重要的额外参考。在下一节中,我们根据以下特定二分法呈现我们的综述发现:胎儿大脑MRI概率图谱和胎儿大脑MRI数据集。
3. 结果
我们的数据库搜索策略产生了144项研究。在检查重复项并筛选标题和摘要后,我们确定了87篇潜在文章,其中9篇来自使用Google搜索引擎进行的更广泛的手动搜索。根据纳入和排除标准,19项研究被纳入本综述。研究选择过程如图2所示。
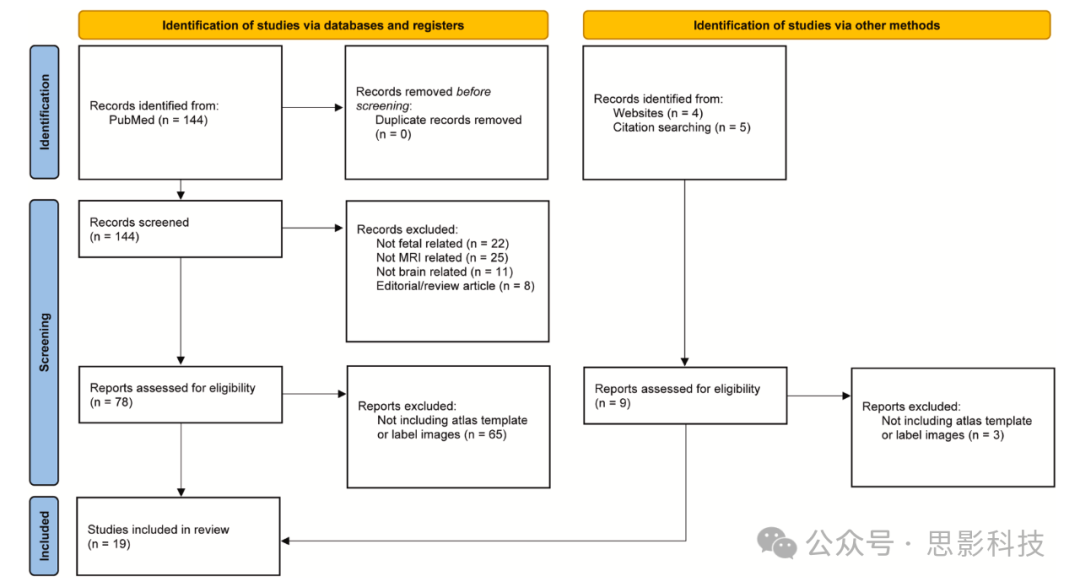
图2 PRISMA流程图。报告了本综述中使用的研究选择过程。
我们确定了21个图谱(图3),其中15个可在线访问。值得注意的是,18个大脑图谱被归类为概率图谱,而其余3个图谱被归类为数据集(即多受试者图谱)。此外,一项研究同时提供了概率图谱和数据集(Urru et al., 2023)。
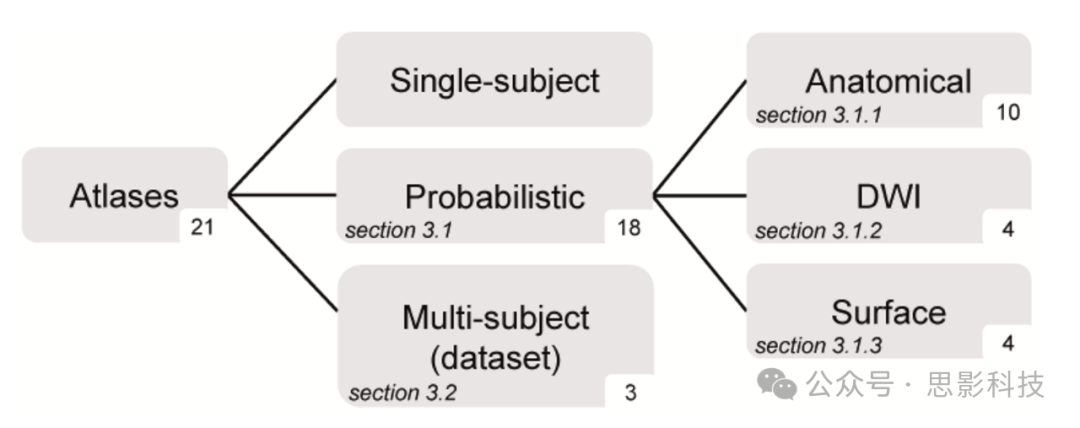
图3 图谱分类。每个类别的图谱数量报告在每个框的右下角。未识别到单一受试者图谱。概率图谱基于用于表征大脑解剖的参考图像(即解剖、扩散和表面图像)进行分类。DWI:弥散加权成像。
在处理胎儿图谱时需要考虑的一个关键方面是其孕周域,即图谱覆盖的孕周范围。具有宽孕周域的胎儿图谱通常包含覆盖整体域小部分的各种子图谱。在图4中,我们报告了公开可用的胎儿MRI图谱和数据集所覆盖的孕周(以周为单位)。
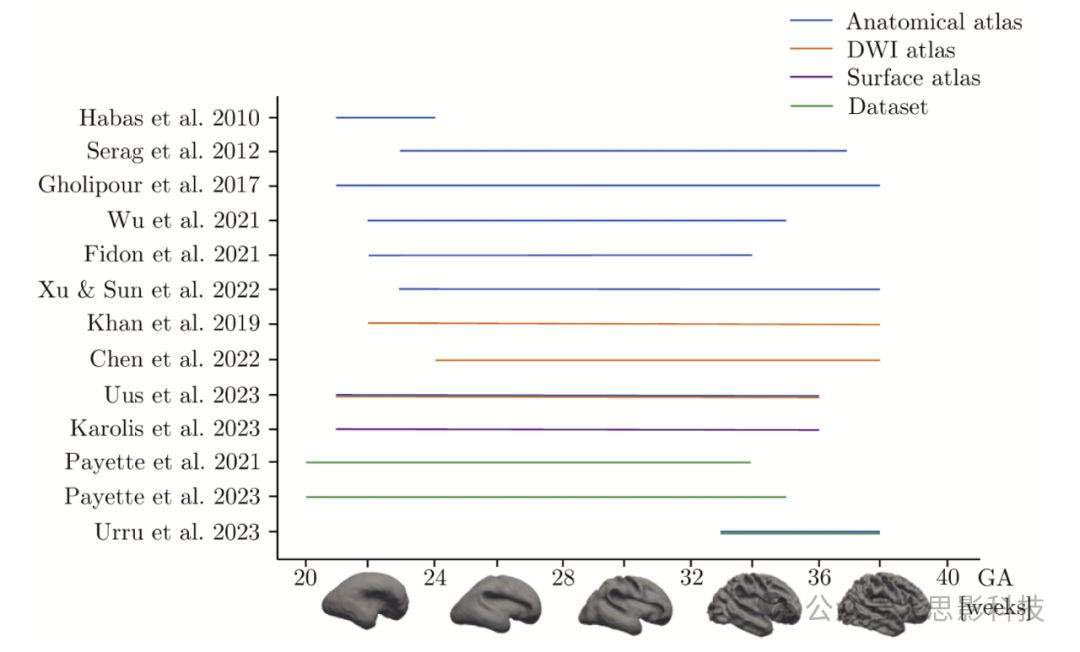
图4 公开可用的胎儿MRI图谱或数据集的孕周域。图表描述了本综述中包含的每个胎儿MRI图谱或数据集所覆盖的孕周(以周为单位)。沿x轴报告了不同孕周正常胎儿皮质表面的示例。
图谱和数据集中包含的MRI模板图像是胎儿大脑的3D高分辨率重建。如前所述,标准胎儿大脑采集协议包括超快速2D序列,因为它们对胎儿运动的敏感性较低且信噪比较高(Glenn, 2010; Gholipour et al., 2014),resulting in voxels with an anisotropic size ratio. 然而,得益于先进的超分辨率重建算法,如NiftyMIC、MIALSRTK、SVRTK和NeSVoR,这些多个2D胎儿扫描可以被组合以生成具有等向体素大小的高分辨率胎儿大脑重建。值得注意的是,数据集通常仅提供每个受试者的3D高分辨率重建图像作为图谱参考图像。相比之下,概率图谱根据其预期用途和模态,包括不同类型的高分辨率3D重建作为图谱参考图像:解剖图像、弥散图像和表面(图5)。
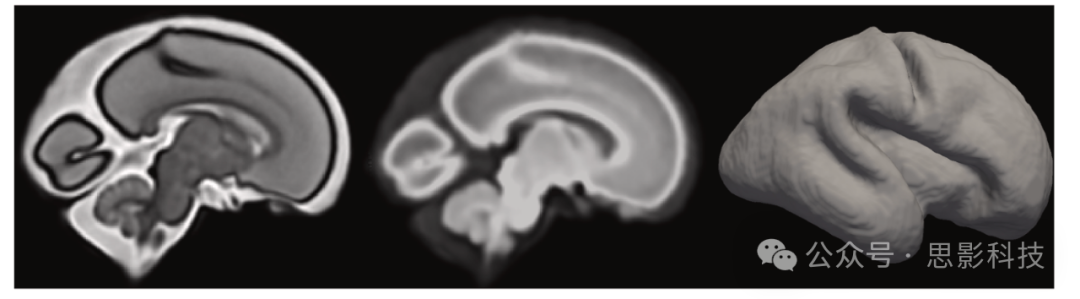
图5 胎儿大脑图谱中不同图谱参考图像的示例。从左到右:28周胎儿的结构解剖、结构弥散和表面图像。结构解剖和结构弥散图谱参考图像来自Uus et al.(2023)公开可用的图谱。所描绘的表面图谱的图谱参考图像显示了皮质板,通过MATLAB从前述Uus et al.(2023)公开可用的图谱生成。
3.1. 胎儿大脑的概率MRI图谱
在不同的胎儿大脑MRI概率图谱中,我们可以根据图谱参考图像的结构或采集模态识别三种不同的图谱:解剖图谱、弥散加权成像(DWI)图谱和表面图谱。
我们确定了18个胎儿大脑的概率图谱,其中12个是公开可用的。大多数公开可用的图谱(N = 8)提供T2加权(T2w)体积高分辨率图像作为图谱参考图像(图6),该图像与定义一些感兴趣结构的图谱标签图像相关联。它们通常用于识别新受试者的结构。其他公开可用的图谱(N = 3)基于DWI图像,提供几个重建的参数图作为图谱参考图像,这些参数图源自广泛使用的弥散张量成像(DTI)模型,如部分异性度(FA)、彩色编码FA(cFA)、平均扩散率(MD)、径向扩散率(RD)、轴向扩散率(AD)和纤维方向分布(FOD)(图7)。这些参数图使用水分子的微观运动来研究大脑发育中复杂纤维结构的排列(De Luca et al., 2021),因此可以直接与新受试者进行比较。其中一个还提供图谱标签图像。第三类图谱(即表面图谱)提供表示胎儿大脑结构表面的网格作为图谱参考图像(图8)。这些通常从高分辨率T2w体积图像派生,通常用于更好地研究高度卷曲的大脑皮质的年龄相关变异性。可以从大脑皮质表面导出几个生物测量指标(如表面积、皮质厚度和皮质折叠/脑回形成),以全面提供跨孕周的大脑皮质特征的各种详细方面(Li et al., 2015)。此外,表面图谱可用于对齐或映射从不同MRI扫描获得的复杂或不规则解剖结构的表面,提供更准确的匹配(Cachia et al., 2003)。
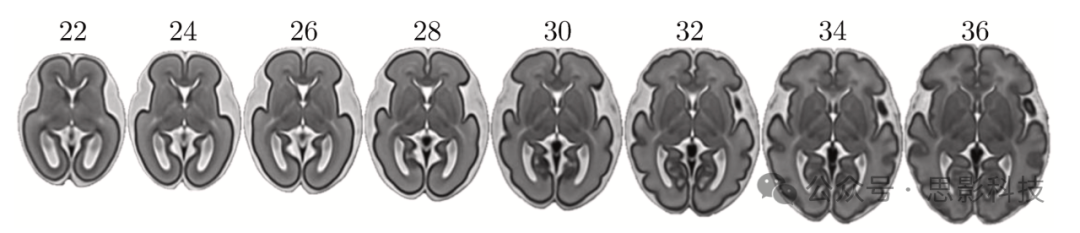
图6. 覆盖22至36周的胎儿大脑T2加权图像。这些图是根据Uus et al. (2023)公开可用的图谱生成的。

图7. 覆盖22至36周的胎儿大脑纤维方向分布(FOD)图。这些图是根据Uus et al. (2023)公开可用的图谱生成的。
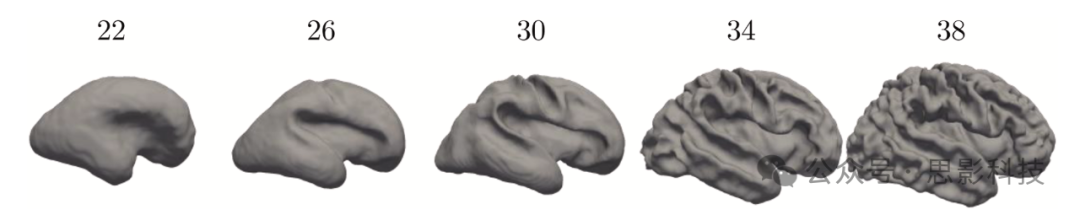
图8. 覆盖22至38周的胎儿大脑皮质表面。图中描绘的表面是根据Gholipour et al. (2017)公开可用的图谱生成的。
表1显示了按预期用途和模态分组的公开可用胎儿大脑MRI图谱概览。
表1. 来自MR图像的公开可用胎儿大脑图谱
3.1.1. 解剖图谱
Habas et al. (2010) 构建了第一个胎儿大脑时空图谱,使用20个重建的(体素大小为0.5 mm等向)正常外观大脑。该胎儿图谱为21-24孕周范围内的每一周定义,包括特定年龄的T2w图谱参考图像和发育中皮质灰质(cGM)、发育中白质(WM)、生发基质(germinal matrix)和侧脑室(LV)的组织概率标签图像。为创建图谱,他们对从固定手动分割提取的受试者间组织标签图进行了组间配准,然后用二次多项式模型化了MR强度、组织概率和胎儿大脑形状的变化。这个图谱是提供标准化框架以比较和分析胎儿大脑MR图像的首次尝试。它不能直接访问,但可以通过作者应要求并通过数据共享协议获得。
Serag et al. (2012) 从80个重建的(体素大小为1.18 mm等向)正常外观大脑的胎儿衍生出一个时空大脑图谱。该胎儿图谱为23-37孕周范围内的每一周定义,包括特定年龄的T2w图谱参考图像和皮质、大脑半球、脑脊液(CSF)和侧脑室(LV)的组织概率标签图像。组织概率图像是通过对每个受试者进行手动分割生成的。用于时空图谱构建的方法依赖于非刚性配准方法来消除所有图像对之间的偏差,然后使用自适应核回归算法(Nadaraya et al., 1964)为每周生成解剖模板图像。值得注意的是,使用时变核宽度可以克服不同年龄受试者分布的变化。这种方法是该图谱的主要特性,考虑到它在每个时间点保持一致的细节水平。
Dittrich et al. (2014) 从32个重建的(体素大小在0.78 mm等向和0.9 mm等向之间)健康妊娠胎儿引入了胎儿大脑的时空潜在图谱。该胎儿图谱为20-30孕周范围内的每一周定义,包括特定年龄的T2w图谱参考图像,配备LV结构的标签图。然而,这项研究的主要新颖性在于半监督方法,允许从部分标注的受试者中分割大脑,从而减少手动标注所需的时间。由于论文的核心是图谱构建方法,图谱本身不公开可用。
Gholipour et al. (2017) 从81个重建的(体素分辨率为1 mm等向)健康妊娠胎儿衍生出胎儿大脑的时空图谱。该胎儿图谱的更新版本于2018年2月发布,为21-38孕周范围内的每一周定义,包括特定年龄的T2w模板和124个大脑结构的标签图像(从ALBERTS图谱手动精炼并从较高孕周传播到较低孕周),包括cGM(皮质灰质)、WM(白质)、深部GM(dGM)、CSF(脑脊液)、LV(侧脑室)、脑干(BS)、小脑(CB)等。此外,覆盖21-30孕周的图谱包括发育中WM层(如皮质下带、中间带和脑室带)的标签。与之前的工作不同,Gholipour及同事专注于构建一个清晰的可变形时空图谱,以便于使用概率标签融合方法进行图谱标记和分割。他们将考虑孕周的核回归与对称微分同胚可变形空间配准相结合,构建了一个详细的图谱,是所有关键孕周解剖结构的无偏平均代表。该图谱标志着大脑研究和临床评估的重大进展,因为它被包含在几个超分辨率重建算法中。它被用于为新受试者的高分辨率等向图像重建定义标准放射学解剖空间。
Li et al. (2021) 从35个重建的(体素分辨率为0.8 mm等向)来自中国人群的健康妊娠胎儿引入了胎儿大脑的时空图谱。该胎儿图谱在23-36孕周范围内以2周间隔定义,包括特定年龄的T2w模板,以及基于分割工具定义的大脑组织掩模(即不包括CSF),随后进行手动校正。图谱参考图像是使用迭代可变形配准方法生成的。该算法选择以目标孕周为中心的2周时间间隔内的五个胎儿大脑,并执行多阶段配准(仿射、仿射+非线性)以计算与目标孕周相关的单一模板。与其他模板不同,作者没有定义任何ROI,而是进行了基于体素的分析。这个图谱是首次尝试关注特定人群(即中国人群)。然而,该图谱不能直接访问,尽管可以通过作者应要求并通过数据共享协议获得。
Wu et al. (2021) 从89个重建的(体素分辨率为0.8 mm等向)来自中国人群的健康妊娠胎儿衍生出胎儿大脑的时空图谱。该图谱为21-35孕周范围内的每一周定义,包括特定年龄的T2w图谱参考图像和124个大脑结构的标签图像,如Gholipour et al. (2017)所介绍的。这些特定年龄的体积胎儿大脑模板是使用ANTs无偏组间配准算法生成的,其标签是通过从Gholipour et al. (2017)图谱的传播方法衍生,随后进行手动精炼。与原始手稿不同,可用的模板范围从22到35孕周。这个图谱是首次公开尝试表征中国人群的产前大脑发育。
Fidon et al. (2022) 衍生出首个来自37个重建的(体素分辨率为0.8 mm等向)开放性脊柱裂(SBA)胎儿的胎儿大脑时空图谱。该胎儿图谱为21-34孕周范围内的每一周定义,包括:
• 重建的T2w模板图像及其大脑掩模标签图像;
• WM、脑室系统、CB、脑外CSF、cGM、dGM、脑干(BS)和胼胝体(CC)的组织标签图像;
• 七个解剖标志的标注,包括LV的前角、后板、CB和脑干(BS)之间的连接处,以及Monro孔处的dGM边界。
图谱构建所遵循的流程依赖于一个基于加权广义普鲁克分析(Gower et al., 1975)方法的初始化步骤,该方法仅使用解剖学标志注释来线性对齐体积,随后进行时间加权体积平均;一个精细化步骤,通过将所有胎儿大脑重建非线性配准(Modat et al., 2014)到中间体积并计算新的加权体积平均,来改善中间图谱的图像清晰度;最后是一个后处理步骤,手动修正获得的图谱分割。提出的图谱是临床人群图谱(即开放性脊柱裂胎儿)的一个例子,旨在支持临床实践(即开放性脊柱裂围手术期阶段)。此外,它为开发特定的基于深度学习的分割方法提供了定制的先验知识。
Xu & Sun et al. (2022) 从90个重建的(体素分辨率为0.8 mm等向)来自中国人群的健康妊娠胎儿衍生出胎儿大脑的时空图谱。该图谱为23-38孕周范围内的每一周定义,包括特定年龄的T2w模板图像和85个大脑结构的标签图像,包括皮质和深部灰质、白质、脑脊液、侧脑室、脑干、小脑、海马和杏仁核。图谱使用自适应核回归方法根据孕周重新分组受试者,然后使用成对初始化的组间配准流程生成特定年龄的图谱。与之前关注中国人群的图谱相比,这项研究引入了几个新颖之处以增强与其他现有图谱的可比性,包括使用3T扫描仪而非1.5T,更高分辨率的图像(即切片厚度<2 mm),以及更宽的孕周范围。
Urru et al. (2023) 及同事利用Gholipour et al. (2017) 的可用数据构建了该图谱的新版本。这个新图谱通过将特定年龄的T2w模板图像及其标签图像配准到Serag et al. (2012) 相应的新生儿时间图像生成。对每个时间点执行配准后,通过分配最频繁或最可能的类别来执行标签对应。因此,Gholipour et al. (2017) 定义的124个结构标签在整个孕周范围(21-38孕周)内被标准化为9个恒定组织标签,其中还包括定义不同白质层的标签。他们将这个新版本的图谱纳入一个统一的框架中,同时对胎儿和新生儿大脑图像进行分割。这种方法解决了缺乏单一工具进行围产期大脑发育分析的问题。此外,他们还引入了一个公开可用的数据集,专门设计用于辅助分割过程(详细描述见3.2节)。
3.1.2. DWI图谱
Khan et al. (2019) 基于67例健康妊娠胎儿的弥散张量图像(DTI)衍生出首个胎儿大脑图谱。与T2w图像采用相同方法,DWI数据被重建为更高分辨率,最终体素大小为0.75 mm等向。该胎儿图谱为22-38孕周范围内的每一周定义,是Gholipour et al. (2017)图谱的扩展。它包括特定年龄的DTI模板图像(估计自最多2个b=0 s/mm2和12个b=500 s/mm2的体积)及其估计的FA、cFA和MD标签图像。如同Gholipour et al. (2017),时空dMRI图谱基于核回归策略开发,使用基于张量的配准以准确对齐WM结构,在任何给定年龄点产生无偏的年龄回归模板。这个DTI图谱使研究人员能够探索胎儿大脑成像分析的新前沿,检测主要神经纤维束通路,并表征子宫内发生的胎儿大脑重组。2022年,Calixto et al. 手动扩展了这个图谱,为23-30孕周范围内的每一周标记了14个感兴趣区域。这套新标签用于表征DWI图像中的不同结构,但不公开可用。
Chen et al. (2022) 从89个重建的(体素分辨率为1.2 mm等向)健康妊娠胎儿衍生出胎儿大脑的时空DTI图谱。该胎儿图谱为24-38孕周范围内的每一周定义,包括从特定年龄DTI模板图像(从30个b=600 s/mm2的体积获得)估计的FA、cFA、MD、RD和AD的标签图像。此外,标签图像包括24-26孕周范围内每周的体素内FOD图。与Khan et al. (2019)不同,时空DTI图谱是通过核回归策略开发的,使用基于FOD的配准而非基于张量的配准,以更准确地对齐结构,在任何给定年龄点产生无偏的年龄回归模板。作者在图谱生成的初始化中使用成对配准和形状更新,而不是在刚性对齐受试者图像后直接平均,以避免个体大脑的偏差。这个图谱呈现的重建图像分辨率更高(1.2 mm等向),相比Khan et al. (2019)的重建(0.75 mm等向),并在较窄的孕周范围(24-38周)内定义。
Uus et al. (2023) 作为发展中人类连接组计划(dHCP项目)的一部分,引入了正常胎儿大脑发育的多通道时空MRI图谱。用于图谱构建的队列包括187名无报告异常且MR图像质量良好的胎儿。具体而言,胎儿大脑以0.5 mm等向的体素分辨率重建。该图谱为21-36孕周范围内的每一周定义,包括4个通道:结构(T2w, T1w)和弥散(FA, MD, RD, 平均DWI b=1000s/mm2, FOD) MRI通道、组织分割和标签描述通道。时空图谱使用MIRTK工具箱构建,类似于基于Schuh et al. (2018)的dHCP新生儿图谱,采用多通道(T2w+皮质)引导配准。多标签脑组织分割包括19个ROI,基于胎儿大脑组织学图谱(Bayer and Altman, 2003 & 2005)的单独左/右结构;分割图是使用优化的dHCP Draw-EM新生儿流程分割(Makropoulos et al., 2018b)的半手动精炼和图谱时间点之间的配准相结合创建的。考虑到它基于多通道方法中最多数量的胎儿(187),这是一个特别全面的胎儿大脑发育映射。此外,重建图像显示高分辨率水平(0.5 mm等向)。然而,与其他图谱相比,它定义的孕周范围较窄。
3.1.3. 表面图谱
Clouchoux et al. (2012) 从12个重建的(等向体素分辨率为1 mm)健康妊娠胎儿构建了皮质板的时空表面图谱。该图谱在四个孕周范围内定义:25-28、28-30、30-32和32-35周,包括皮质板表面以及每个周范围内沟回位置的概率模板图像(岛叶、中央沟、下额沟、上颞沟、后中央沟、上额沟、顶内裂、前中央沟和下颞沟)。其构建依赖于皮质板表面的迭代配准,如Lyttelton et al. (2007)所述,随后计算平均表面。结果图谱用于描述妊娠期间的胎儿折叠模式和脑回形成过程。该图谱未公开可用。
Wright et al. (2015) 从80个重建的(体素分辨率为1 mm等向)健康妊娠胎儿构建了发育中大脑皮质的时空表面图谱。该时空表面图谱为23-37孕周范围内的每一周定义,包括皮质灰质/白质表面模板图像及其19个从新生儿图谱集(Gousias et al., 2012和2013)传播的分割图像。皮质表面图谱通过在谱域应用核回归算法(Nadaraya et al., 1964)构建。表面图谱允许使用联合谱分析来更准确地识别受试者间皮质对应关系,比应用于基于体素图像的常见球面恶魔方法更准确。然而,开发的图谱未公开可用。
Xia et al. (2019) 从25个重建的健康妊娠胎儿构建了特定年龄的胎儿皮质表面图谱。该图谱为26-29孕周范围内的每一周定义,包括特定年龄的T2w模板图像,配备基于顶点间皮质生长模式的生物学意义分割图。具体来说,为全面捕捉顶点间生长模式的相似性,他们首先构建了两个互补的相似性矩阵(一个基于顶点的生长轨迹,另一个基于顶点生长轨迹与一组参考点的相关性剖面),并融合(Wang et al., 2014a)它们以捕捉其共同和互补信息。最后,对融合的相似性矩阵进行谱聚类(Ng et al., 2002),将时空胎儿皮质表面图谱划分为10个不同区域群集:感觉运动、后顶叶、背外侧前额叶、扣带回和内侧额叶、腹外侧前额叶和前岛叶、眶额叶和前扣带回、内侧颞叶、后颞叶、前颞叶和后岛叶、枕叶和楔前叶。最终图谱被用来提出一种基于皮质表面动态变化的新分区方法。该图谱未公开可用。
Karolis et al. (2023) 从dHCP项目招募的242个正常胎儿大脑引入了时空表面图谱。该图谱为21-36孕周范围内的每一周定义,提供软脑膜、中-厚度、白质和高度膨胀的表面。此外,它还提供了一些皮质形态变化(厚度、曲率和沟深度)的派生图和球面配准到模板的结果。该图谱通过调整Bozek et al. (2018)为新生儿表面图谱引入的程序生成,基于球面配准方法(多模态表面匹配)。其生成涉及三个主要步骤:首先,通过基于沟深度的仿射配准到第36周的dHCP新生儿模板初始化共同参考空间;其次,使用基于沟深度的非线性对齐粗略精炼模板;第三,使用基于曲率的对齐进一步精炼模板。这个新颖的时空图谱是首个公开可用的表面图谱,为探索胎儿大脑脑回形成过程开辟了新机会。
3.2. 胎儿大脑MRI数据集
胎儿大脑MRI数据集,或多受试者图谱,包括一组受试者的个体3D重建作为模板图像(通常源自T2w序列)以及它们的个体分割作为标签图像。数据集可以作为多受试者图谱使用,通过一系列受试者间配准和标签融合程序,能够将图谱的标签传播到新的受试者。此外,数据集是宝贵的资源,可以用于开发和评估新方法,这些方法能够通过学习不同大脑结构之间的复杂关系和受试者间变异性来自动化胎儿大脑的标记过程。
表2 提供了公开可用的胎儿大脑MRI数据集概览
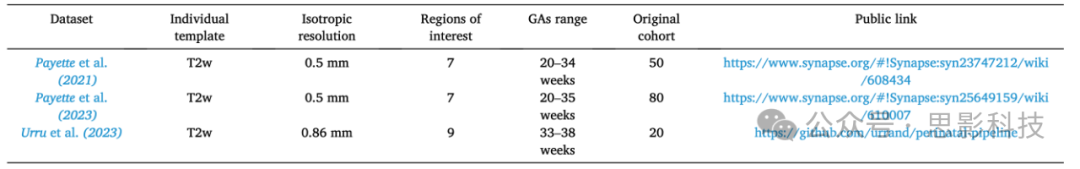
Payette et al. (2021) 提供了首个公开可用的数据集(FeTA - 胎儿组织标注和分割数据集),包含50个病理性(N = 32)和神经典型(N = 18)MRI胎儿大脑,年龄范围从20到33孕周。病理受试者包括接受脊柱裂修复手术前后MRI检查的胎儿。该数据集包括50个T2w胎儿大脑重建(体素大小为0.5 mm等向),每个都有一个标签图像,报告7种不同组织/标签的手动分割:外部脑脊液(eCSF)、灰质、白质、侧脑室、小脑、深部灰质和脑干(图9)。这个数据集首次在FeTA Challenge 2020中引入,这是一个多类别和多中心图像分割挑战,旨在开发可泛化的自动多类别分割方法,用于发育中人类大脑组织。
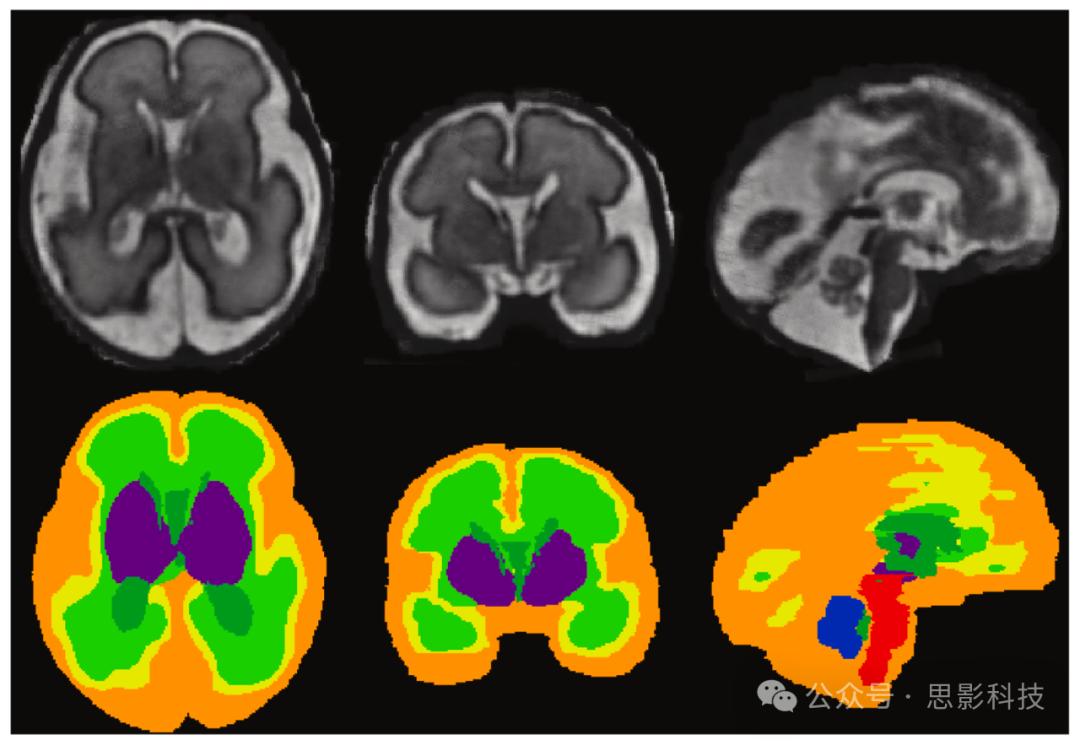
图9 28.7周胎儿的手动分割示例(橙色:外部脑脊液;黄色:灰质;亮绿色:白质;深绿色:脑室;蓝色:小脑;紫色:深部灰质;红色:脑干/脊髓)。图片改编自Payette et al. (2023)公开可用数据集。
FeTA Challenge 2021和2022分别发布了这个数据集的新版本。更新后的开源可用数据集包括80个受试者(49个病理性和31个神经典型),范围在20-35孕周(Payette et al., 2023)。同样,每个受试者都发布了一个T2w胎儿大脑重建(使用NiftyMIC、MIALSRTK或SVRTK重建)和相应的七个标签图像(图9)。
Urru et al. (2023) 引入了一个公开可用的胎儿数据集和一个概率图谱(见3.1.1节)。该数据集范围从33到38孕周,专门设计用于辅助分割过程,利用反向投影和标签融合方法。数据集包括20个T2w胎儿大脑重建(体素大小为0.86 mm等向),每个都有一个标签图像,报告9种不同组织/标签的手动分割,这些标签是从Gholipour et al. (2017)图谱的增强版本获得的:脑脊液、皮质灰质、白质、侧脑室、小脑和脑干、深部灰质、高强度白质、低强度白质。
4. 讨论
胎儿MRI是表征胎儿中枢神经系统的第三级诊断工具,通常在常规超声检查结果不确定时使用(Pollatou et al., 2022)。自从在临床实践中应用以来,胎儿MRI促进了大脑发育新研究课题的发展。它提供了大脑解剖和功能的宝贵特征(Oishi et al., 2019),导致对可作为参考的标准图谱需求增加。如今,技术进步、新型成像技术和基于AI的算法显著促进了精细胎儿大脑图谱的生成。3T扫描仪推动了胎儿MRI研究的重大进展,特别是支持获取更高质量的图像。从1.5T到3T的过渡中存在几个担忧,包括特定吸收率(SAR)可能增加、对胎儿生长的潜在影响,或由于3T磁体的高噪声水平对胎儿听觉系统发育的影响(Colleran et al., 2022)。在最近的工作中,Manganaro et al. (2023) 声称没有实验证据表明3T记录对胎儿有负面影响。出于显而易见的原因,胎儿和母亲的安全应被视为优先考虑。因此,进一步的研究应继续调查并最终澄清这一点。
新型成像技术,特别是DWI模型如体素内不相干运动(IVIM)模型(Yuan et al., 2019; Jakab et al., 2018; Ercolani et al., 2021)和静息态fMRI(van den Heuvel et al., 2016; Vasung et al., 2019),对于更好地表征胎儿大脑解剖和连接性变得至关重要。基于AI的算法为节省时间和精确采集(如Singh et al., 2020)以及可靠的处理工具(如Sobotka et al., 2022; Karimi et al., 2023)提供了宝贵的解决方案。此外,基于AI的算法已经显示了结合不同成像模态(如扩散和结构MRI)的潜力(Ball et al., 2017)。因此,生成多模态时空胎儿大脑图谱,在尽可能广泛的孕周范围内组合同一解剖空间中的多个MRI衍生图,是胎儿大脑研究未来的一个具有挑战性的趋势。对多模态图谱需要额外考虑。
与成人人群研究类似,功能和解剖成像方法的结合似乎是胎儿领域未来的一个关键方向,以更好地表征大脑结构和功能之间的密切关系(De Vareilles et al., 2023)。然而,几个因素阻碍了多模态图谱的生成。一个主要因素是获取和处理这些类型数据所涉及的技术挑战。例如,DTI方法需要更长的采集时间,使其非常容易受到受试者运动的影响(Khan et al., 2019);fMRI方法在平面内和平面间方向都产生较差的图像分辨率,这使得连接性分析的可重复性困难(Sobotka et al., 2022)。此外,与结构成像方法相比,涉及更新技术(如扩散和功能MRI)的处理方法数量有限(如Uus et al., 2023c)。综合这些考虑因素有助于理解为什么使用多模态图谱具有挑战性。一个需要考虑的关键附加点是:多模态图谱不应仅从结构和功能方法之间的协同作用角度来考虑。例如,通过结合不同的解剖采集序列,临床医生可能从不同对比度的使用中显著受益。因此,多模态应该从结构和功能数据之间的协同作用以及结构图像的不同对比度两个方面来考虑。
在这项研究中,我们回顾了10个结构解剖图谱、4个结构扩散图谱、4个表面图谱和3个数据集(或多受试者图谱)。除了图谱参考图像外,每个公开可用的解剖图谱都包含一个有用的图谱标签图像,用于识别和研究特定的脑结构(表1)。从这个角度来看,我们可以识别两种不同的分割任务方法。第一种方法只描述主要脑结构(<10个),如皮质灰质或脑室。其他图谱提供每个脑结构的精细分割,为每个主要脑结构识别数十个区域(>30个)(Gholipour et al., 2017; Wu et al., 2021; Xu and Sun et al., 2022)。第二种方法可能引起一些与胎儿大脑大小和获取图像分辨率相关的担忧。常见的采集协议包括快速2D T2w序列,体素大小具有0.4-1 mm的高平面内分辨率,但切片厚度较大,为2-4 mm(Ciceri et al., 2023b),而平均胎儿大脑体积在22-24周时约为103 cm3(大致为直径6.4 cm的球体),32-34周时约为319 cm3(Tran et al., 2023)(大致为半径9.2 cm的球体)。因此,在定义分割方案时,保持分辨率、可靠性和可重复性之间的良好平衡至关重要。
处理胎儿大脑图谱时需要考虑的一个关键方面是,大脑在孕期经历快速而广泛的变化。因此,一些结构在不同孕周期可能有不同的形状,有些可能只是暂时的(即只在特定孕周范围内可检测到)。因此,在构建概率模板图像时,必须谨慎地结合来自不同孕周的图像。一种常见方法是根据孕周将原始人群划分为子集,并构建一组图谱参考图像,每个图像描述一个短的孕周期(Habas et al., 2010; Clouchoux et al., 2012; Xia et al., 2019; Urru et al., 2023)。尽管这种方法在概念上简单有效,但它的限制是每个图谱参考图像可能只基于少数受试者,而且连续孕周期的图像可能差异很大。更复杂的方法包括考虑图谱参考图像时间演变的项(如核回归算法)(Serag et al., 2012; Dittrich et al., 2014; Wright et al., 2015; Khan et al., 2019; Gholipour et al., 2017; Xu and Sun et al., 2022; Chen et al., 2022),从而将所有受试者包括在图谱构建过程中,并确保结果图像之间的时间一致性。进一步的结果是,区域定义和分割协议应针对孕周范围进行优化,随着孕周域之间距离的增加,可靠的生理分割可能会有很大的不同。例如,在Gholipour et al. (2017)中,为21-30孕周和31-38孕周范围提供了不同的白质分割。
总的来说,基于胎儿图谱的图像分析有一定数量的局限性,这可能在后续分析步骤中产生不准确性。特别是,受试者-图谱配准错误可能导致解剖结构重建的改变(主要在高解剖复杂性区域)。基于单一受试者图谱的分析可能无法准确表示个体发育、受试者间变异性或人群队列的解剖结构。此外,图谱可能无法准确表示非典型大脑发育的改变解剖结构。分析低分辨率图像可能导致精细解剖细节的丢失或模糊的组织边界。因此,为了缓解这些缺陷,研究人员应考虑适当的预处理流程和特定队列的图谱。结合使用不同的概率图谱可能是评估结果准确性和可靠性的有价值解决方案。还探索了其他方法,如数据驱动方法(Payette et al., 2023; Fidon et al., 2024)。在这种情况下,深度学习(DL)方法正在迅速获得认可。DL方法试图通过直接从受试者训练数据学习不同脑结构之间的复杂关系来避免这些缺陷,而不是从图谱推断。然而,DL方法需要大量数据集进行训练,因此在某些情况下,基于图谱的方法仍被认为是重要的,例如当有明确的解剖先验或专门知识可用时,或者在小数据集的情况下。因此,鉴于当前复杂的情况,结合DL和基于图谱的方法可能是利用两种方法优势的务实方式(Litjens et al., 2017; Fidon et al., 2024)。
在胎儿环境中回顾的图谱中,71.4%是公开可用的。考虑到数据隐私要求以及与这个特殊人群相关的一般担忧,这是一个巨大的成就。公开图谱和数据集在推进可复制研究、改进临床应用以及更广泛地促进医学成像领域方面发挥着关键作用。国际项目(如dHCP)和挑战(如FeTA Challenge)等倡议旨在促进医学成像数据的共享用于研究目的,并为开发和评估新的分析方法和算法提供宝贵资源。尽管这在开放科学方面是一个显著的成就,但对于临床病例来说,情况更为复杂。只有一个临床图谱(Fidon et al., 2022)和一个临床数据集(Payette et al., 2023)是公开可用的(两者都与SBA条件相关)。胎儿大脑疾病特异性图谱和数据集的主要担忧之一与疾病相对于一般人群的较低发病率有关。临床表现的异质性和疾病相关特征注释的复杂性是进一步的担忧。最后但同样重要的是,临床人群的数据隐私法规出于显而易见的原因通常更为严格。
4.1. 临床、研究和伦理影响
人类产前大脑成像是一个令人着迷但极其复杂的挑战。胎儿大脑图谱和数据集支持监测大脑发育里程碑、识别异常,进而为潜在(未来)临床状况的前驱征兆提供新的关键洞见。首先,人脑的特征是复杂的脑回和沟裂模式。尽管在这一领域做出了相当大的努力,但导致脑回形成的神经生物学机制仍远未被完全理解。考虑到产前发育中非典型的脑回形成轨迹已与许多神经系统、神经认知和行为障碍相关联,这一点不容忽视。胎儿成像中的先进多模态MRI技术正在提供以前未探索的关于产前大脑形态结构和功能连接的信息(De Asis-Cruz and Limperopoulos, 2023)。产前成像是一种新的强大工具,有助于定义胎儿大脑发育的规范模式,可能支持识别高风险胎儿(Xu et al. 2020; Machado-Rivas et al. 2022; Kim et al. 2023)。反过来,先进产前MRI大脑发现与长期神经发育结果之间的潜在关联可能在促进(非常)早期产后康复/康复干预方面发挥重要作用,这可能限制成年期潜在的负面后果。
在当前的工作中,小脑等结构值得简要提及。如今,大量研究一致认为小脑对运动和非运动功能都起着关键作用(Buckner et al., 2013; Marek et al., 2018; Diedrichsen et al., 2019)。此外,有假设认为小脑的原发性损伤可能导致功能相连的大脑区域的继发性功能障碍(Wang et al., 2014; Casartelli et al. 2018)。有趣的是,人类小脑与新皮质结构相比具有延长的发育轨迹(Wang et al. 2001; Sathyanesan et al. 2019)。因此,它也有一个较长的关键易受伤害时间窗口(De Asis-Cruz and Limperopoulos, 2023),产前成像的进展可能为临床监测这些方面提供有前景的视角。值得注意的是,过去5年发表的所有解剖图谱和数据集都考虑了小脑;这间接支持了对这一特定解剖结构日益增长的兴趣。
毫无疑问,当前产前神经成像技术的进展将为胎儿大脑研究提供重要见解,也可能为某些临床实践如产前发育监测提供重要支持(例如,Zoetmulder et al. 2023; Stuempflen et al. 2023)。尽管将产前神经成像应用于常规临床实践存在明显困难,但这一观点仍可以得到认同。与生物医学领域的许多其他尖端和开创性技术(如脑机接口、神经假体等)一样,产前神经成像仅限于实施适当安全程序和数据收集、处理和解释的临床中心。相比之下,产前成像进展的伦理影响似乎经常被低估。我们意识到这些伦理问题的重要性和紧迫性,但对它们的评估可能超出了我们在本工作中的具体目标。我们敦促基础研究人员、临床医生、护理人员、公共卫生决策者,尤其是普通民众考虑该领域科学进步的伦理影响。忽视"新"的和实质上未经探索的伦理问题的风险不仅限于产前神经成像的进展。它正成为所有涉及AI的人的一个根本关切,无论具体的(子)领域如何。例如,当涉及临床医生可以要求其他更具侵入性的子宫内检查的可能性时,产前大脑成像中基于AI的方法变得极其(且可能戏剧性地)重要。
我们应该回到将技术进步视为人类进步的工具,而不是误导性地将其视为人类进步的目标。因此,伦理关切将重新获得其在科学努力中的中心地位。这不会自动解决问题,但至少会促进一种更具批判性的方法。
5. 结论
产前大脑是个体发展的关键窗口。科学界应将早期发展阶段的研究视为优先事项,以最大化我们对发育中大脑的理解。在这项工作中,我们对胎儿大脑图谱和数据集进行了系统性回顾。我们对文献中经常不一致使用的特定术语进行了术语澄清,然后特别关注了产前期,分析了18个胎儿大脑图谱和3个数据集。基于图谱的方法仍在作为跨孕周胎儿大脑结构知识库方面发挥着至关重要的作用。然而,数据集无疑是该领域一个有前景的领域,支持尖端的基于人工智能的方法。
越来越多关注产前大脑发育的研究证实了本工作中回顾的图谱和数据集对临床和研究目标可能承担的关键作用。除此之外,我们强调需要继续监测与胎儿大脑研究相关的安全性、可行性、可靠性和伦理问题。























 177
177

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








