探索尿路上皮癌的分子异质性与免疫治疗潜力:解读《Molecular heterogeneity in urothelial carcinoma and determinants of clinical benefit to PD-L1 blockade》
尿路上皮癌(Urothelial Carcinoma,UC)是一种常见且复杂的癌症。近日,发表在《Cancer Cell》上的一篇重磅文章,详细分析了PD-L1抑制剂atezolizumab在UC治疗中的分子机制和临床意义。作为研究者或免疫治疗领域的关注者,这篇文章无疑提供了许多值得学习的内容。本文将从研究背景、主要参与机构、研究发现及局限性等方面为您解读这篇文献。
1. 为什么开展这项研究?背景与意义
近年来,免疫检查点抑制剂(如PD-1/PD-L1抑制剂)在癌症治疗中取得了突破性进展。Atezolizumab,作为一款PD-L1抑制剂,已被批准用于治疗包括尿路上皮癌在内的多种癌症。然而,尽管部分患者从中获益,但治疗的整体反应率并不高,且具体的分子机制和影响因素尚未完全阐明。
这篇文献整合了IMvigor系列临床试验的数据,希望通过大规模分子分型和免疫微环境分析,回答以下关键问题:
- 哪些患者能够从atezolizumab治疗中获益?
- 肿瘤微环境如何影响免疫治疗效果?
- 是否可以通过分子标志物优化治疗策略?
为此,研究团队整合了四项关键临床试验(IMvigor210、211、130和010),共计2803名患者的数据,进行了前所未有的多组学分析。
2. 背后的研究机构:谁在推动这项工作?
首先需要介绍主导这一研究的团队和机构。这项研究的核心数据整合和分析由Genentech公司完成。Genentech是一家总部位于加州南旧金山的生物技术公司,作为atezolizumab的开发商,它既负责药物研发,也主导了这些临床试验的数据分析。
不过,IMvigor系列试验的执行并非仅由Genentech完成,而是一个国际多中心合作项目,以下是一些重要参与机构:
- Dana-Farber Cancer Institute(波士顿,美国):在癌症免疫疗法研究中处于全球领先地位。
- Memorial Sloan Kettering Cancer Center(纽约,美国):专注于精准医学和复杂癌症治疗。
- Netherlands Cancer Institute(荷兰):以其在分子肿瘤学方面的贡献著称。
- Gustave Roussy Cancer Institute(法国):欧洲最大的癌症治疗中心之一。
这场"科学接力赛"最终在Genentech的分析团队手中完成了数据的整合和文章的撰写。
3. 文章的主要发现和结论
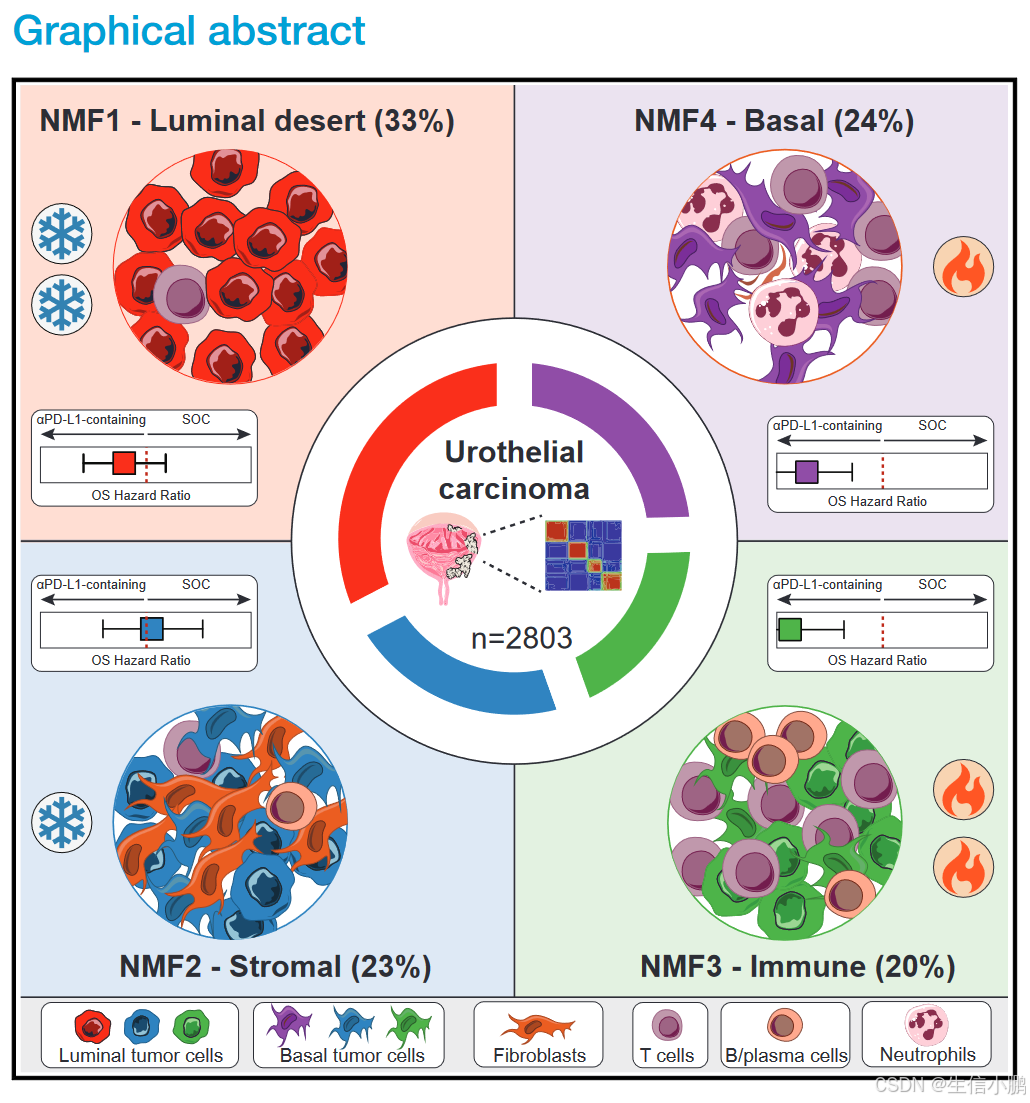
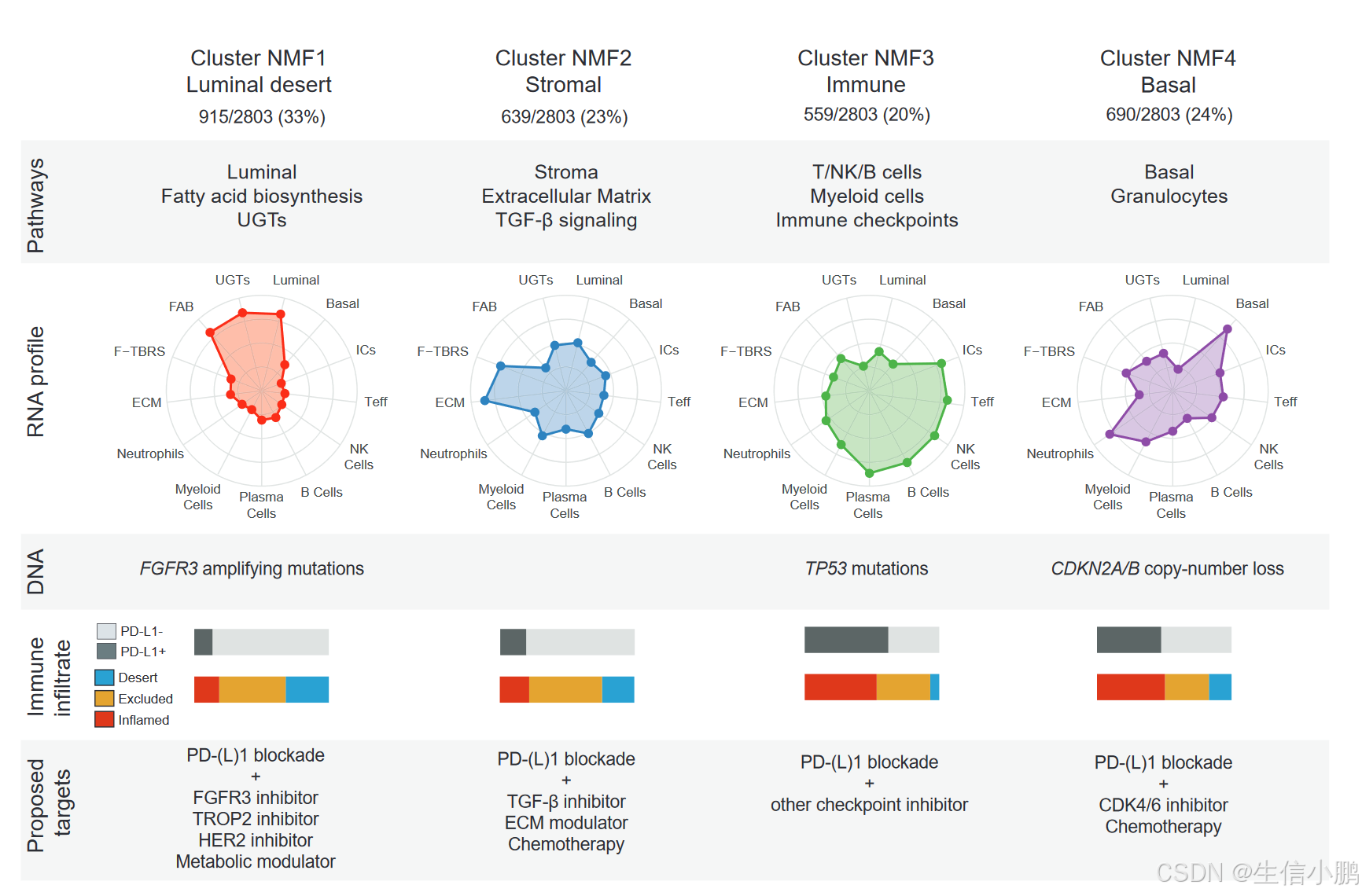
通过非负矩阵分解(NMF)算法,研究团队揭示了尿路上皮癌的四种分子亚型,每种亚型均表现出不同的肿瘤微环境特征和治疗响应:
-
Luminal Desert(33%):
- 特点:免疫活性低,PD-L1表达少。
- 临床表现:对atezolizumab反应差,生存率较低。
-
Stromal(23%):
- 特点:富含基质细胞,免疫抑制信号显著。
- 临床表现:治疗效果较差。
-
Immune(20%):
- 特点:浸润性免疫细胞多,如CD8+ T细胞和B细胞。
- 临床表现:显著获益于atezolizumab(中位总生存期达到17.5个月)。
-
Basal(24%):
- 特点:表现出浸润性基底细胞特征,伴随一定的免疫活性。
- 临床表现:对免疫治疗的响应良好。
此外,研究还发现:
- **高PD-L1表达(IC2/3)**患者对atezolizumab的响应更好。
- 基于H&E病理切片的数字病理学技术可以预测分子亚型,为精准治疗提供了潜在工具。
4. 文章的局限性
尽管本研究数据量庞大,分析精细,但仍存在一些局限性:
- 回顾性分析为主:
- 数据来源于既往的临床试验,可能存在选择偏倚。
- 分子亚型的适用性:
- 这些亚型需要在更广泛的人群中进一步验证,尤其是对于非转移性患者。
- 治疗组合策略未深入探讨:
- 虽然文章揭示了免疫治疗的分子机制,但未深入研究免疫治疗与化疗或靶向治疗的协同作用。
- 分析流程的代码未公开:
- 虽然所用的分析方法较为常规,但未提供详细代码。
5. 我们可以学习利用的方面
这篇文章的研究内容对于免疫治疗研究和应用有很多启发:
- 多组学数据整合:
- 通过RNA测序和机器学习进行分子分型,提供了探索肿瘤异质性的有效途径。
- 免疫微环境分析:
- 了解肿瘤微环境的不同特征,可以更精准地预测患者的治疗响应。
- 数字病理学的应用:
- H&E切片与人工智能结合的潜力巨大,未来有望加速肿瘤分型和个性化治疗。
- 精准医学策略:
- 将分子亚型纳入临床决策,可以提高治疗效率,避免不必要的副作用。
总结
通过整合IMvigor系列试验的数据,这篇文献揭示了尿路上皮癌的分子异质性及其对PD-L1抑制剂的影响。无论是研究设计、分析方法,还是得出的临床意义,都为免疫治疗领域的研究者提供了丰富的启示。未来,如何将这些分子分型应用于实际临床场景,仍是一个值得探索的重要方向。

























 884
884

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










