大学物理实验——锂离子电池3-电池测试
1. 实验目的
1、了解可充锂离子电池的工作原理
2、了解电解质溶液的导电机理
3、掌握纽扣锂离子电池的电极材料、电极的制备工艺及纽扣锂离子电池的装配
4、掌握锂离子电池电性能测试方法
2. 实验器材
新威八通道电池充放电测试仪
3. 实验原理
可充锂离子电池工作原理:充电时锂从氧化物正极晶格间脱出,锂离子迁移通过有机电解液,嵌入到碳材料负极中,同时电子补偿电荷从外电路供给到碳负极,保证负极的电
荷平衡;放电时则相反,锂从负极碳材料中脱出回到氧化物正极中。锂离子电池的充放电反应通常可简单表示为(正向反应为充电过程,逆向反应为放电过程,其中 Me 为过渡金
属,如 Co、Mn、Ni 等):
Li x MeO 2 + 6C →MeO 2 +LixC 6
在充放电过程中, Li+ 在正负极间嵌入脱出往复运动犹如来回摆动的摇椅,因此这种电池又被称 “Rocking -chair batteries ” ,即摇椅式电池。锂离子充放电的原理与结构示意图:
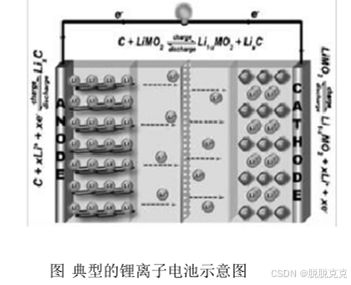
下面以尖晶石型 LiMn 2 O 4 为正极材料、富锂层状石墨为负极,叙述锂离子电池充放电过程:
(1) 正极
放电时,正极从外部电路获得电子,锂离子嵌入正极材料,部分 Mn4+ 被还原为Mn3+ ;充电时,正极把电子释放给外部电路,锂离子从正极材料中脱嵌进入电解液,电极反应为
Lix Mn 2O4 +yLi ++ye-+Mn O== Lix+yMn 2O4
(2) 负极
放电时,负极石墨层间的锂离子脱嵌进入电解液,电子通过外电路释放,充电时,负极从外部电路获取电子,锂离子嵌入石墨层间,相应的电极反应为:
Liz C+ == yLi ++ye-+Liz-yC
对于磷酸钛锂的充放电反应是在 LiTi 2 (PO 4 ) 3 和 Li 3 Ti 2 (PO 4 ) 3 两相间进行的,充电时 Li+ 嵌入LiTi 2 (PO 4 ) 3 中转化为结构相似的 Li 3 Ti 2 (PO 4 ) 3 ,放电时 Li + 从 Li 3 Ti 2 (PO 4 ) 3 中脱出形成LiTi 2 (PO 4 ) 3 :

锂离子插入和脱出磷酸钛锂结构的过程中,电压维持在。
锂离子在电解液中通过微孔薄膜往返迁移,然后嵌入到电极中。电子通过外电路转移释放或者消耗能量。从锂离子电池的充放电过程,可以看到锂的化合态始终为 +1价,无0价(金属锂)转变,所以这种二次电池称为 “锂离子电池 ”。
电解质体系
1) 非水电解质:非水锂离子电池的电压在 3 V 以上,金属锂非常活泼,需要使用有机电解液体系。通常在有机溶剂中溶解含有锂离子的电解质。例如溶解有 1 mol/L
LiPF 4 的 EC+DMC(体积比 1:1)有机电解质溶液。
2) 水相电解质:与水可发生剧烈反应,传统的水溶液体系不能适应锂电池,隔膜:电池中隔膜的主要作用是离子的导体,并且将电池的正负极隔离以防止电池短
路。非水有机锂离子电池一般采用高强度薄膜化的聚烯烃多孔膜,例如 Celgard2325 型隔膜。水相锂离子电池体系通常采用亲水性多孔的隔膜,可以是聚合物多孔膜或无机
纤维膜等。
4. 实验内容与步骤
- 称重:将实验中称重电极片,并计算所涂实际正极活性物质量( 80%)。
- 配置电解液 1 M Li 2 SO 4 (或 LiNO 3 )溶液。
- 冲制玻璃纤维隔膜片,在切片机上切出直径为 16 mm 的纤维片;
- 冲制 LiMn 2 O 4 电极片,在切片机上冲出直径为 16 mm 的电极片;并计算电极片的活性物质的质量
- 组装电池:取正极壳口(正极壳一般较大,切朝外一面上面有 +号)朝上,放入正极电极片,保证活性物质的面向上(一般黑色面为电极面);然后放入玻璃纤维隔膜片 1 片;滴加数滴电解质溶液保证能够润湿电极片和隔膜;然后将负极电极片放入(保证活性物质面向下);(根据电池壳的尺寸决定是否放入垫片和弹簧片);盖上负极壳。
- 封口:用塑料镊子将电池壳小心放到封口机上,保证电池的正极壳在下面、负极壳朝上(负极一般上面为粗糙一面);调整至中心;关上封口机的油压阀门;反复压下手柄直至压力到 5 Mp 以上,将电池壳封住。
- 取下电池,用纸巾将溢出的电解质擦干净;
- 用万用表测试电池的开路电压(可能有偏差,但不应等于零)、测试电池的电阻(不应等于零)。经过老化处理数小时。
- 将密封好的电池连接到新威电池测试系统上,在室温下及 V 间测试电池性能。预先编好充放电程序,输入活性物质量。
例如充电:设定电流如 50 mA/g,充电结束电压为 V放电:设定电流如 50 mA/g,放电结束电压为 V循环次数: 50 圈
5. 实验记录


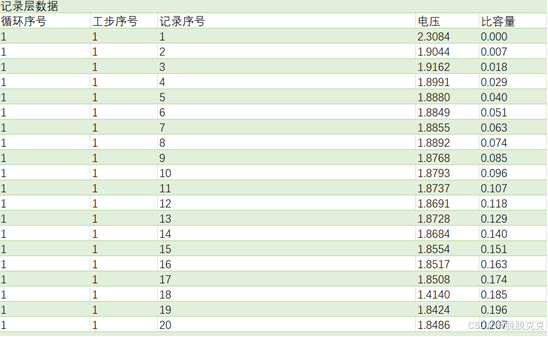
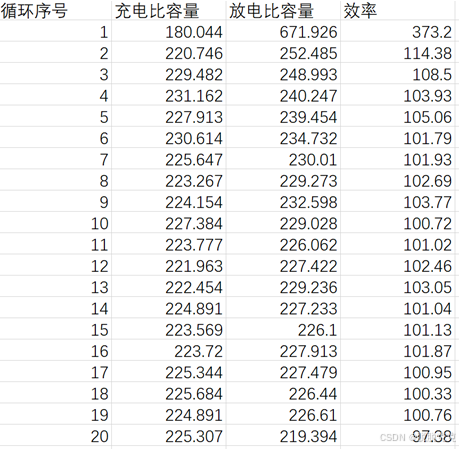
6. 数据处理和误差分析
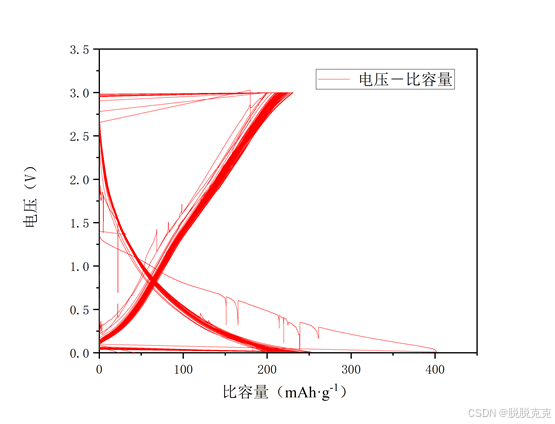
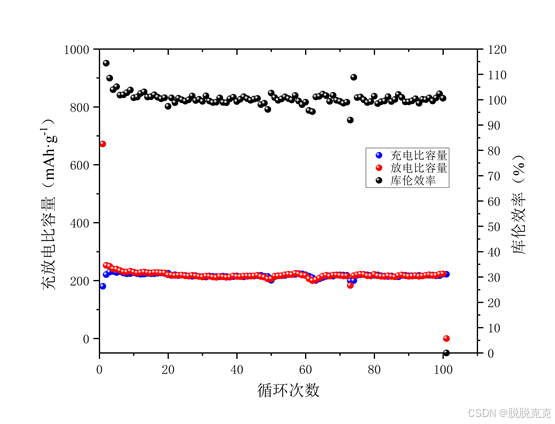
由图可知:
该电池在经过100次循环后有着近100%的优异库仑效率,充放电比容量为250 mAh·g-1左右,在充放电过程中表现出高度的可逆电化学反应,
误差分析:
1.电池测试过程中出现短路
2.用手直接触摸电极片,导致电压测量不准
电池性能测试结果分析
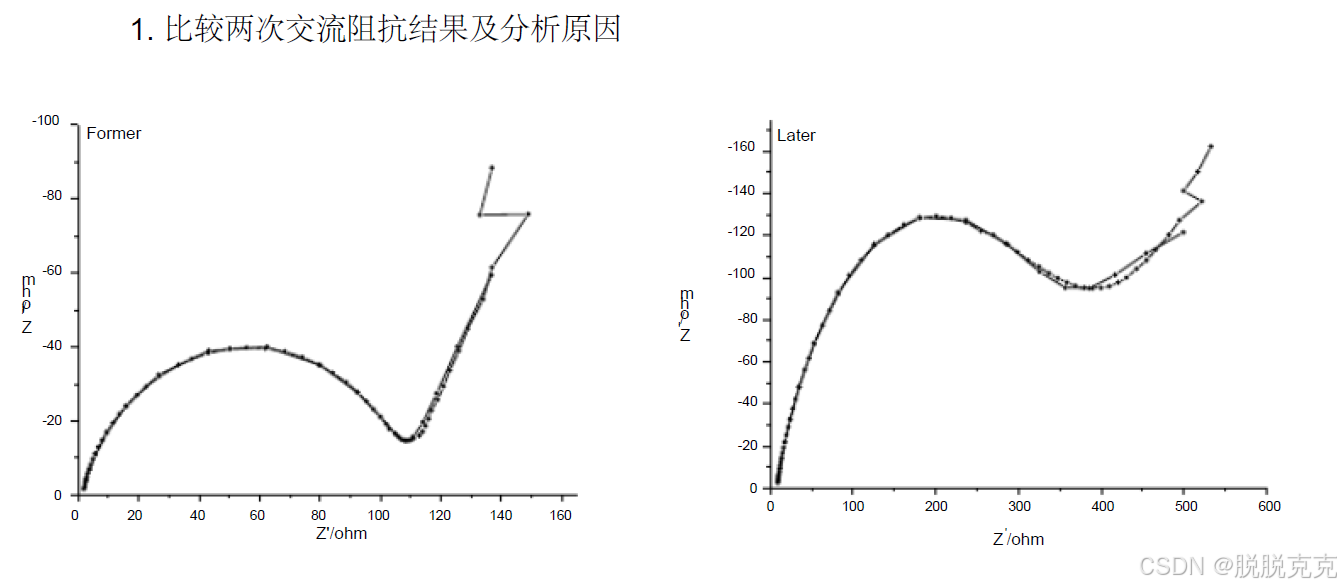
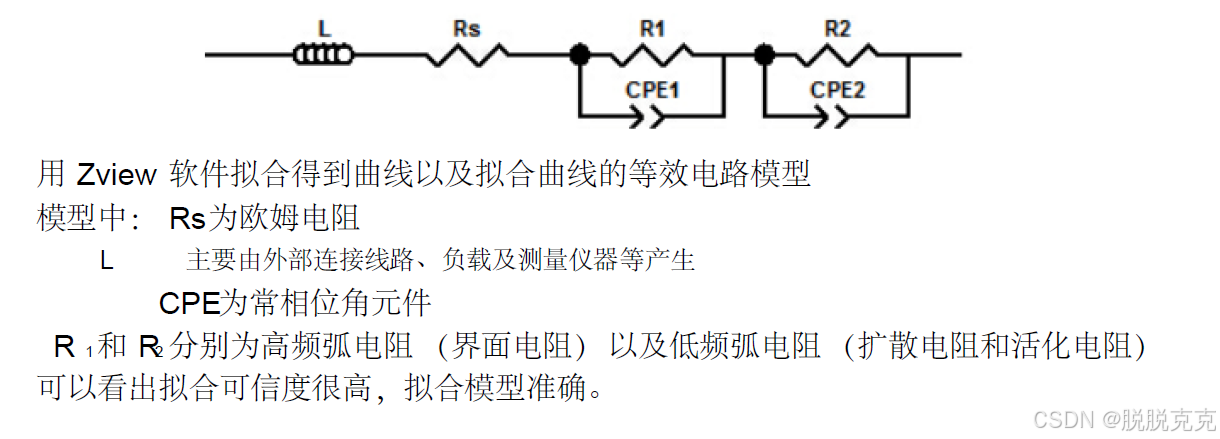
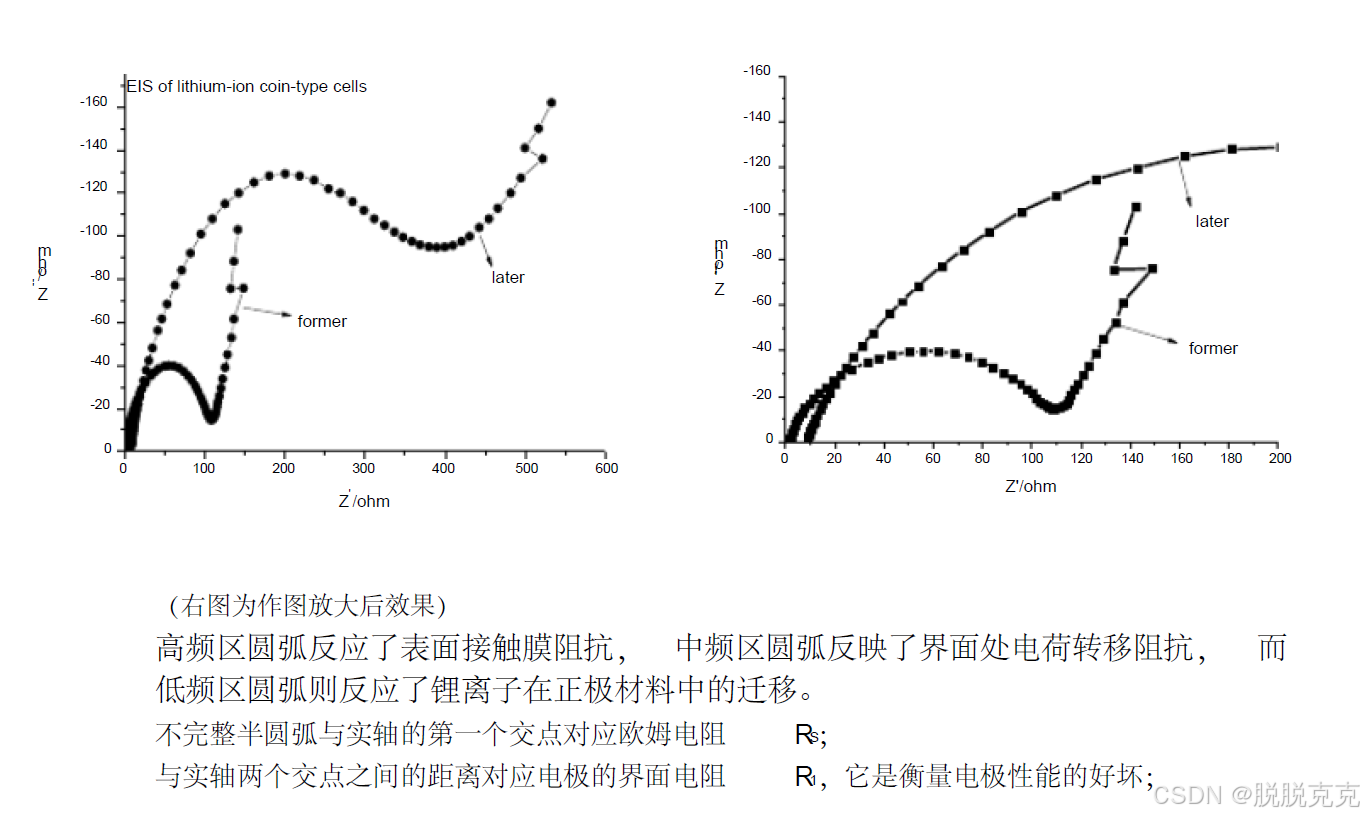
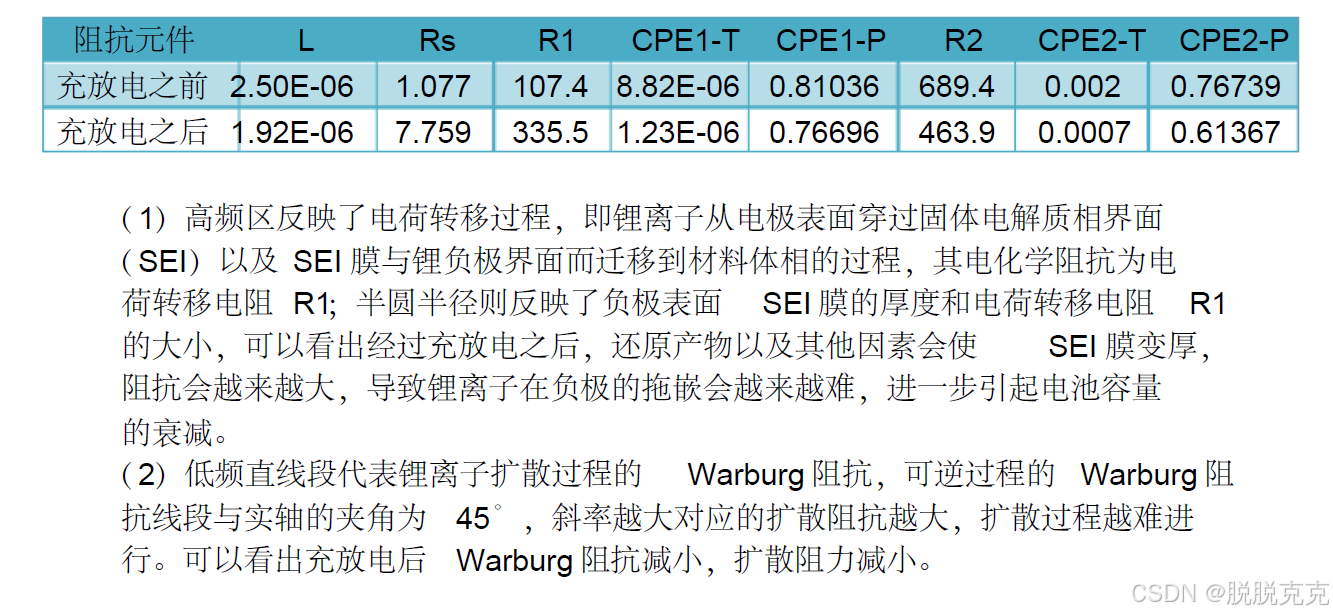
1. 比较两次交流阻抗结果及分析原因
2. 运用origin 做出首次充放电曲线以及循环倍率曲线
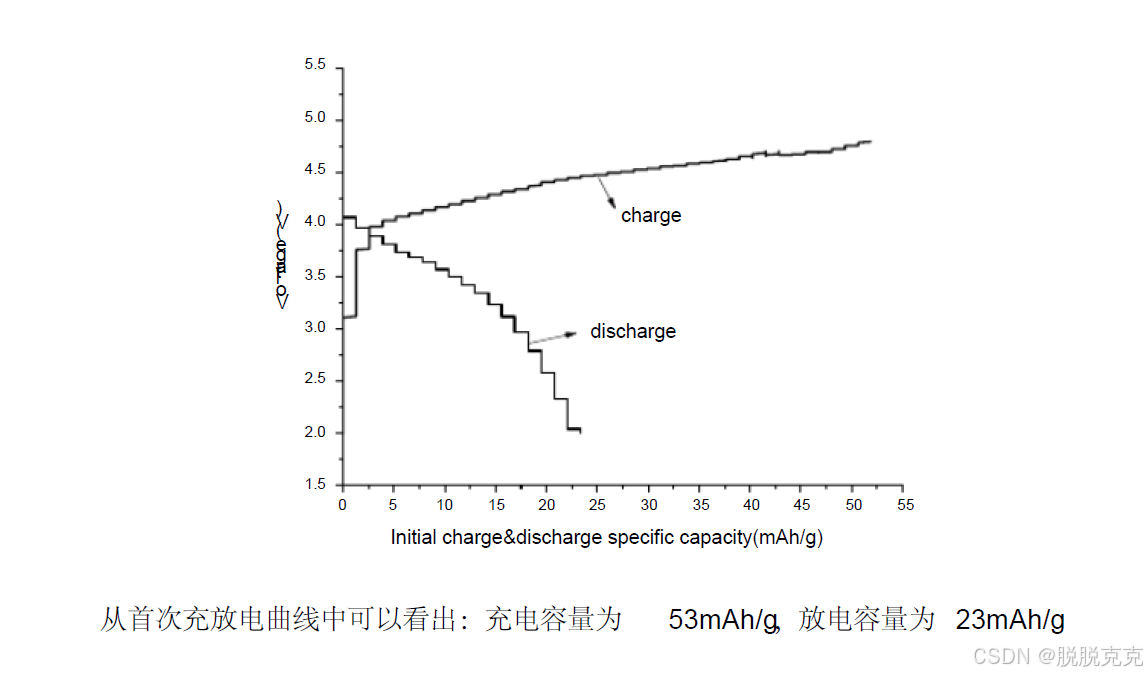
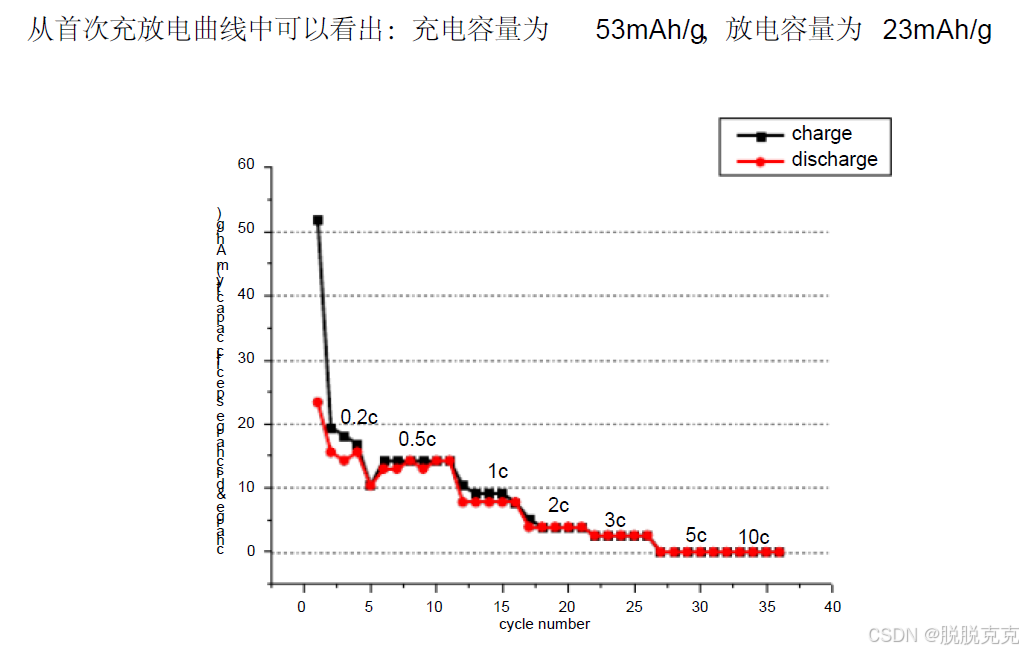
上图为电池在不同倍率条件下的放电容量循环图。测试扣式电池在2.5V-4.8V 电压范围下0.2C 首次充放电、0.5C 10 次循环和1C 2C 3C 5C 10C每个倍率下5 次倍率性能测试。图中显示随着电流密度的增大, 材料的放电充电容量呈下降趋势,在第27 次循环时,电池的容量已变为0.但分析数据可知, 电池容量太低, 性能不是很好, 原因是正极极片制作过程出问题,而且与电池装配和封口工艺有很大的关系。
3. 分析CV曲线中氧化还原峰形成的原因, 以及两次循环中峰位置和形状的变化?
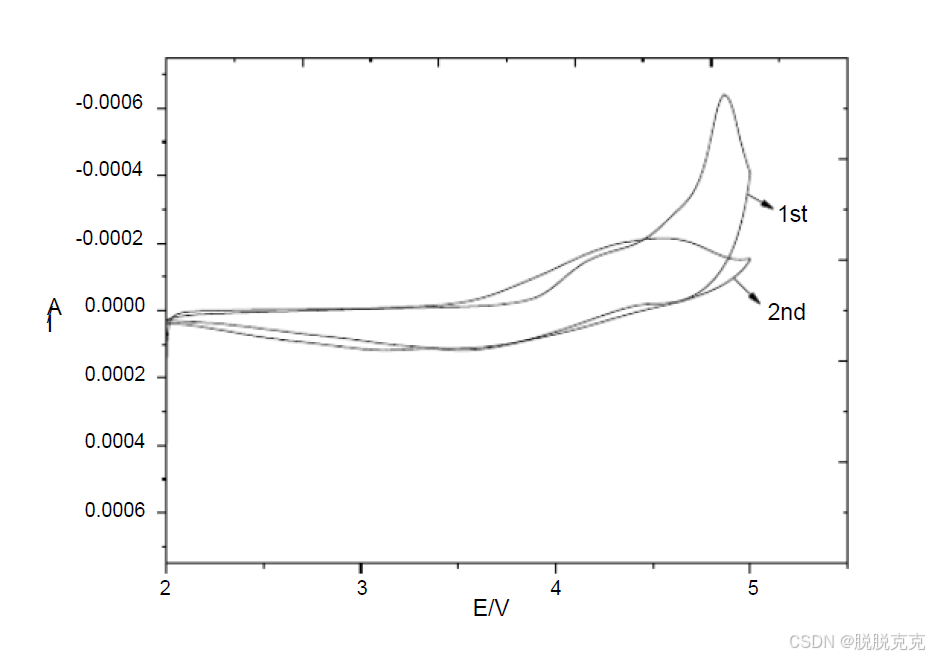
7. 思考题及实验小结
1、锂离子电池负极材料的充放电测试时,常采用恒流测试。在恒流测试中,电池以恒定的电流进行充电或放电,这有助于评估电池在不同电流条件下的性能,并获取电压随时间的曲线。恒流测试是常用的电池性能评估方法,能够揭示电池的循环稳定性、容量衰减等信息。
2、原因:
实际应用需求: 锂离子电池在实际应用中可能会面临不同的电流需求,例如电动汽车或储能系统中的高功率放电。倍率性能测试可模拟不同倍率的放电条件,评估电池在不同工作条件下的性能表现。
循环寿命: 高倍率放电通常会引起电池内部的化学反应和热效应,因此倍率性能测试还可以用于评估电池在高倍率工况下的循环寿命和稳定性。
现实意义:
电池设计优化: 通过倍率性能测试,可以优化电池的设计,使其能够适应高倍率放电的应用场景,提高电池的功率密度。
安全性评估: 高倍率放电可能导致电池内部温升,倍率性能测试有助于评估电池在高倍率下的热管理和安全性能。
市场竞争力: 在某些应用中,如电动汽车领域,高倍率性能是提高电池竞争力的关键因素,因此进行倍率性能测试有助于电池制造商在市场上取得优势。
【参考文献】
[1] 锂离子电池材料配制及电化学性能研究,李昱树,电子科技大学 2103 年硕士论文
[2] 扣式锂离子电池的制备工艺研究,张勇,武行兵,电池工业第13 卷第2 期 2008 年4 月
[3] 锂离子电池三元复合正极材料的合成及其电化学性能研究,牛晓波,重庆大学2006 年硕士论文
























 46
46

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








