作者,Evil Genius
初四了,新年了,在医院熬了一宿,刚起来,北京的一个课题组在分析外显子和单细胞空间数据的时候问了我一个问题,那就是单细胞空间的临床运用在哪里?其实结合工作经历而言,我认为单细胞的临床运用可能还遥遥无期,但是空间的运用已初见端倪,我们简单来看一下。
我们都知道在特检领域有三大系统,分别是肿瘤基因检测系统(WES)、遗传基因检测系统、感染性疾病基因检测系统(mNGS和tNGS),其中关于肿瘤基因检测系统介绍的最多,遗传次之,tNGS目前介绍的少一点。那么如果我们对单细胞空间和临床检测相当了解的话,那么很容易看到其中的结合部,那就是VDJ和宏基因组检测。
其中单细胞也可以做宏基因组和VDJ,但是单细胞由于采用drop-seq的方式,而且一块组织经过处理已经丢失了大部分的信息,每个样本仅剩下1万左右的细胞供下游分析,而且方法在应用层面存在诸多缺陷,临床运用任重道远。
但是空间就不同了,关于空间宏基因组的检测之间都介绍过,文章在
GATK的人类宿主的微生物检测流程PathSeq和在空转上的运用
单细胞空间宏基因组揭秘微生物群对癌症空间和细胞异质性的作用
单细胞空间宏基因组揭秘微生物群对癌症空间和细胞异质性的作用2
且空间转录组检测病原微生物的方法已经成熟,那么在应用层面检测到的病原微生物与其在组织部位的具体位置,将会为医疗领域的运用提供极大的帮助。

另一个结合点在VDJ,单细胞VDJ已经存在了很多年了,但是一直无法解决我们实际上的问题,最根本的原因在于还是无法找到真针对特定肿瘤的靶向VDJ序列。
在临床运用上,比如目前最火的CAT-T疗法,在临床上,CAR-T细胞的治疗首先需要收集患者的外周血并分选出T细胞,T细胞在体外进行刺激扩增并通过病毒载体转入特定的CAR基因,被称为CAR-T,随后再将扩增后的CAR-T回输给患者,在患者体内行使其被设定的肿瘤杀伤作用。
CAR的基本结构如下图所示

CAR分子包括三个主要部分:胞外域、跨膜域和胞内域。胞外域中的抗原结合域通常是一个抗体来源的单链片段scFv分子,主要由抗体的可变轻链(VL)和可变重链(VH)及中间的Linker区连接组成,再通过铰链区(Hinge)连接到跨膜结构域,负责识别抗原。跨膜域的主要功能在于将CAR分子锚定在细胞膜上,其对CAR分子表达的稳定性具有重要作用。胞内域则包括共刺激结构域和信号转导结构域,二者合力负责T细胞的完全活化。其中,通过在一代CAR CD3ζ胞内信号转导区上增加共刺激结构域,已逐渐衍生出二代、三代甚至四代CAR,目前临床上使用较多的依旧为二代CAR。
T细胞表面表达T细胞抗原受体(T cell receptor,TCR) TCR为所有T细胞表面的特征性标志,以非共价键与CD3结合,形成TCR—CD3复合物,TCR的作用是识别抗原。T细胞的激活需要两个信号,第一信号是上述的TCR和多肽-MHC分子的结合形成的TCR信号,但是这条信号不足以激活静止状态的T细胞。只有在CD28和其受体提供的第二条共刺激信号的情况下,T细胞激活相关的RNA及蛋白才会被合成,关键细胞因子IL-2才会被分泌,细胞也会从G0期进入到G1期。因此,是共刺激信号和TCR信号一起完成T细胞的激活。
其实看到这里,我们基本上就明白了,核心就在在于抗原的识别,其中一位哈佛的博士跟我交流,问我能不能通过分析肿瘤单细胞的VDJ找到特定靶向的TCR/BCR,只要能找到,剩下的免疫疗法部分他完全可以搞定,并且几年内就可以产生针对肿瘤组织的高效免疫疗法,并且让我可不可以出一个方案,说实话,说的我很心动,但是结合多年的单细胞分析经验,这个道路不太好走,不过空间VDJ 的研究似乎更有价值一点。
关于空间VDJ的内容,我也写过很多,列在下面
全球首篇FFPE空间转录组分析揭示了肾细胞癌中三级淋巴结构抗肿瘤机制

10X空间转录组技术创新之同时测RNA和TCR(BCR)

10X空间转录组之免疫组库分析
Science|Spatial VDJ可实现B细胞和T细胞的空间转录组学研究
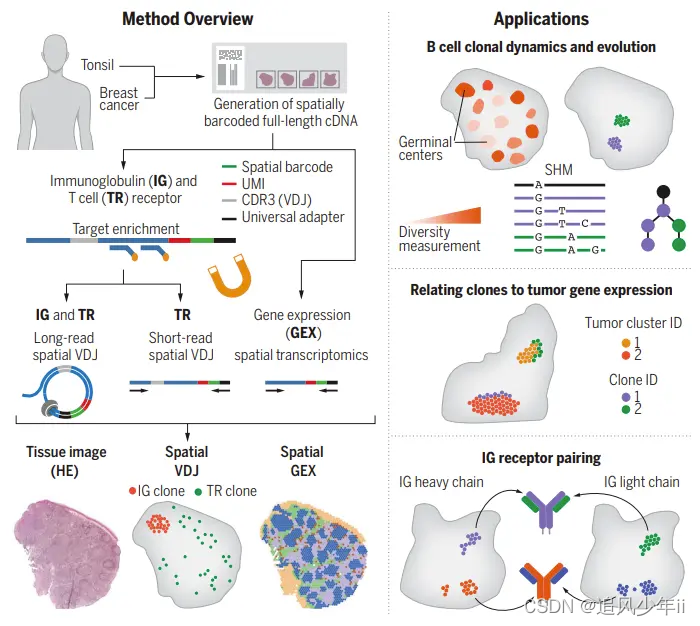
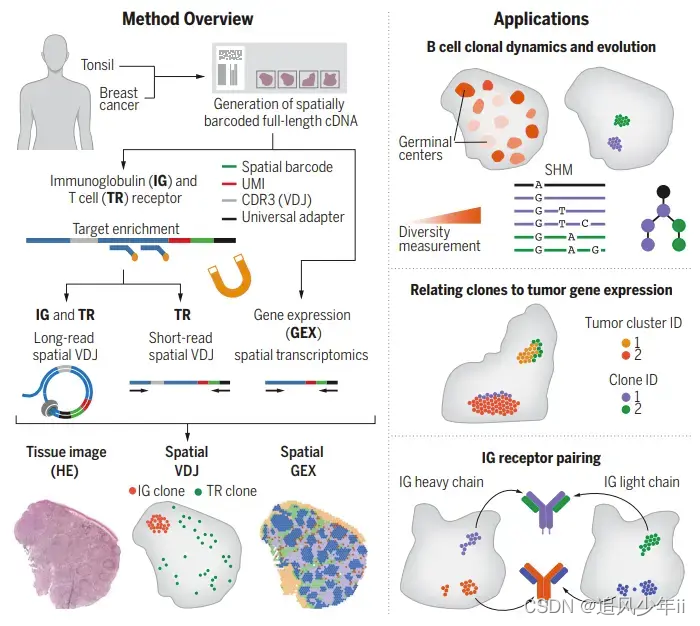
其中空间VDJ能够解决为问题最为关键,一方面不仅是寻找能够浸润肿瘤组织的TCR或者BCR序列,一方面是识别肿瘤组织内部的异质性并且各个异质性区域特有的VDJ序列,这其实为完全攻克肿瘤提供了良好的契机。
或者更进一步,同时获取不同肿瘤异质性区域的突变信息和VDJ信息,那么对于后续的免疫疗法的运用将是极大的促进。
这里我们来看一下最新的这一篇science,Spatial transcriptomics of B cell and T cell receptors reveals lymphocyte clonal dynamics
Spatial transcriptomics of B cell and T cell receptors reveals lymphocyte clonal dynamics
期刊:Science
影响因子:56.9
发表时间:2023年12月
淋巴细胞克隆在组织内的空间分布对其发育、选择和扩增至关重要。文章提出了一种空间VDJ技术(Spatial VDJ),能够在空间上解析B细胞受体和T细胞受体。该方法有两个版本:一个是用于研究全长免疫球蛋白(immunoglobulin,IG)和T细胞(TR)转录本,使用三代长读长测序(long-read,LR),即LR Spatial VDJ;另一个是仅用于研究TR的二代短读长测序(short-read,SR),即SR Spatial VDJ。两个版本都使用了针对IG和TR基因恒定区的杂交捕获技术。
背景知识
B细胞和T细胞对感染和炎症做出反应,调节组织稳态,并保持免疫记忆。B细胞和T细胞的靶向反应性由其克隆可遗传的抗原受体决定。单细胞技术允许在细胞水平上研究抗原受体,但缺乏空间分辨率。目前的空间转录组学(ST)方法不能保留全长抗原受体转录本,因为文库准备步骤会将定义淋巴细胞克隆性所需的互补决定区3(CDR3)分段。淋巴细胞克隆性的空间分析可能将特异性抗原受体与肿瘤相关、自身或外来抗原联系起来,这可能有助于识别和利用抗原特异性克隆进行治疗。已经开发出几种技术来空间分辨人类组织中的抗原受体序列。这些包括基于聚合酶链反应(PCR)的T细胞受体(TCRs)的ST或Slide-seq文库扩增,激光引导微解剖与测序相结合,以及通过对ST文库中残留的CDR3区域序列的罕见的更长免疫球蛋白(IG)转录本进行深度测序捕获。然而,目前缺乏以高通量、用户友好的方式全面绘制全长B细胞受体(BCR)和TCR序列及其在组织中的谱系关系的方法。
在这项工作中,开发了可变、多样性和连接(VDJ)序列的空间转录组学(Spatial VDJ),该技术可绘制人类组织中的全长BCR和TCR转录本。Spatial VDJ是新鲜冷冻组织的Visium空间基因表达(Spatial GEX)的扩展,该技术依赖于组织切片中聚腺苷酸RNA的3'-靶向条形码。来自人类扁桃体组织的空间GEX文库显示了丰富的BCR和TCR恒定基因表达。尽管如此,它们仍然只占总文库的一小部分。在进行片段化之前,CDR3区域序列可以从空间条形码全长Visium cDNA中进行PCR扩增。 因此,测序CDR3区域和空间条形码从Spatial GEX cDNA文库应该是确定克隆性和抗原受体转录本位置的可行方法。


Outline of the PCR approach targeting the V and C genes of each receptor chain (TRB, IGHG, or IGHM) from full-length Spatial GEX cDNA libraries (top).
作者开发了两个空间VDJ版本:(i)长读(LR)空间VDJ,它生成全长IG和T细胞(TR)抗原受体转录物的空间条形码文库;(ii)短读(SR)空间VDJ仅用于TR序列,它使用基于cdr3相邻V引物的两步半嵌套pcr方法。对于这两种方法,使用针对TR和IG恒定区的杂交捕获探针来富集抗原受体转录本,同时保留空间条形码、唯一分子标识符(UMI)和全长受体序列。与未富集的空间GEX库相比,杂交捕获显著增加了TR和IG的UMI和空间条形码计数,并保留了IG和TR的转录本分布。

Hybridization target capture of IG and TR constant regions increases the IG and TR gene counts in spatial transcriptomics libraries
总结一下:Spatial VDJ是10x Visium空间基因表达(Spatial GEX)技术的扩展,Spatial GEX依赖于组织切片中3’polyA序列进行靶向捕获,在片段化步骤之前,CDR3区域序列可以从空间条形码全长Visium cDNA中进行PCR扩增(图2A),因此,能够通过该技术得到CDR3区域和空间GEX cDNA文库的barcode序列,可同时得到抗原受体转录本表达量和位置信息。其中:(i)Long-read (LR) Spatial VDJ技术,可构建空间的全长IG和TR受体转录组文库;(ii)Short-read (SR) Spatial VDJ技术,只构建TR受体序列文库。对于这两种方法,都使用了针对TR和IG恒定区的杂交捕获探针来富集抗原受体转录本,同时保留了空间条形码、唯一分子标识符(UMI)和全长受体序列。与未富集的空间GEX文库相比,杂交捕获显著增加了TR和IG的UMI和空间条形码计数,并保留了IG和TR转录本分布。
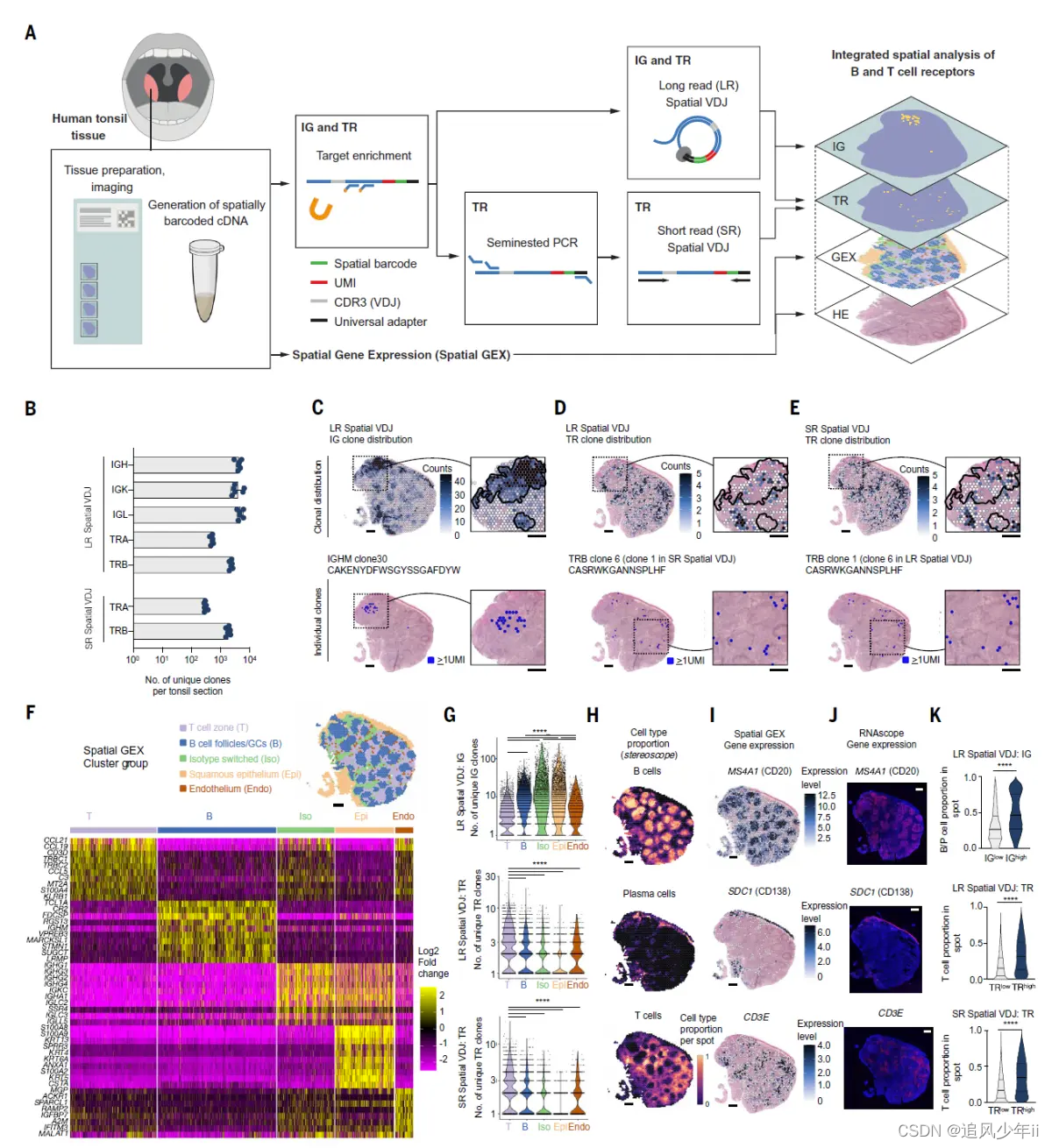
Spatial VDJ技术原理图及分析结果图
文章中将这种技术运用到了一些案例中,比如我们最关注的Spatial VDJ captures B and T cell clones in human tumors
绘制肿瘤内的B细胞和T细胞克隆可能有助于识别和治疗利用单个或群体克隆来增强肿瘤相关免疫。文章从两个未经治疗的HER2阳性乳腺肿瘤(P1和P2)中生成了Spatial GEX和VDJ文库。为了更好地捕捉患者内部异质性,将活检分为多个区域,标记为区域A (RegA)至区域RegE,每个区域包含肿瘤、肿瘤边界和邻近的非肿瘤组织。在每个患者和切片中鉴定出数千个独特的IG克隆序列和数百个独特的克隆TR序列,在肿瘤区域外发现的独特克隆数量最多。在细胞质母细胞和表达apoe的巨噬细胞富集的位点上,IG克隆型计数最高,这表明肿瘤浸润性巨噬细胞和浆细胞之间存在关联。具有最高TR受体计数的spot富含髓细胞和T细胞相关基因和细胞亚群,在P2中类似于成熟的三级淋巴结构(TLS),但在P1中没有。一些IGH克隆在TLS样区和富含质母细胞区之间共享,这表明至少有一些肿瘤相关的质母细胞可能来自TLS激活的B细胞。
通过对相同肿瘤的匹配单细胞RNA测序(RNAseq) VDJ (scVDJ)分析,证实了大约一半的空间VDJ定义的TR受体链,类似于基于空间pcr的TRB扩增方案。对于IG克隆,仅通过scVDJ确认了LRSpatial VDJ数据集的3.0和2.9%。通过scVDJ检测到的TR大约是IG克隆的10倍,而在Spatial VDJ中则相反。分析表明,Spatial VDJ(与scVDJ相比)更容易捕获浆细胞克隆,这可能是由于每个浆细胞中丰富的IG转录物表达以及浆细胞对单细胞解离方案的敏感性`。相反,Spatial VDJ对TR克隆的检测减少可能是由于数据上罕见转录本的捕获效率低下(由于每个细胞和/或每个克隆的TR表达量低)。这些限制可能也适用于罕见的B细胞克隆,因为与浆细胞相比,B细胞表达IG转录物的水平较低。支持Spatial VDJ捕获更多扩展克隆的概念,与Spatial VDJ共享的scVDJ TR克隆每个克隆具有更多细胞,并且在多个肿瘤区域检测到的scVDJ克隆更频繁地被Spatial VDJ捕获。
扩大肿瘤浸润的B细胞和T细胞克隆可能表明局部抗原特异性相互作用与肿瘤调节潜能。肿瘤包含表型多样的淋巴细胞,但确定哪些B或T细胞克隆和亚群直接与肿瘤相互作用是具有挑战性的。在匹配的肿瘤活检中,空间VDJ与scVDJ联用显示扩增的T细胞克隆在肿瘤边界相对于非肿瘤区域或肿瘤内富集。这些克隆表现出从CD4或CD8效应细胞到调节性T细胞的表型。因此,Spatial VDJ提供了一个平台,根据空间分布和细胞状态来定义假定的肿瘤反应性克隆型,这在分析游离组织时是不可能的。分析发现这与扩增的B细胞克隆特别相关。在P2中,发现了四个不同的肿瘤cluster。不同的IG克隆在单个肿瘤cluster的边界上有明显的富集,其中两个(IGL克隆6和IG克隆39)与切换类B细胞(分别为IGHA1和IGHG1)匹配。大多数克隆在肿瘤边界的有限部分富集,表明局部抗原结合反应(例如,IG克隆与表达不同抗原的不同肿瘤亚克隆共定位)。所有肿瘤簇都富集了癌细胞,但表现出不同的富集基因。这种肿瘤内的异质性可能导致同一肿瘤内不同的肿瘤生长和治疗反应[例如,不同的IG克隆在不同的肿瘤位置驱动抗体依赖性肿瘤细胞杀伤]。因此,将无监督方法与空间VDJ相结合可以识别在特定肿瘤区域富集的潜在肿瘤反应性抗原受体。
配对的BCR或TCR序列决定抗原结合。空间VDJ捕获单个抗原受体转录本,因此不能自行定义受体对。然而,成对的受体链应该在组织中共定位。使用匹配的单细胞VDJ数据集来验证配对受体的使用,分析观察到大多数IG对在活检区域具有很高的空间相关性。为了仅根据Spatial VDJ数据预测抗原受体配对,开发了一个称为“修复”的计算框架。因此,使用Spatial VDJ进行“修复”可能潜在地用于预测人体组织中成对的IG受体的新生,以进行进一步的抗体研究。

Spatial VDJ uncovers B cell spatial evolution
空间VDJ还揭示了不同B细胞卵泡内和卵泡之间的B细胞克隆家族多样性(包含生发中心),这是B细胞克隆扩增和成熟的关键位点。B细胞的空间系统发育分析表明,B细胞无性系的分支和地理分布是同步的。























 798
798

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








