基本概念
- 原子实+核外电子模型
- 化学键:其实是电子几率的重新分布
- 电离能(I):失去一个电子需要获得的能量
- 亲和能(A):获得一个电子失去的能量
- 电负性: Km∗(I+A)
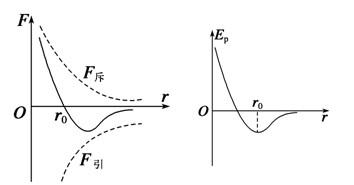
- 吸引势和排斥势的平衡
U(r)=−Arm+Brnf(r)=−∂U∂r - 排斥力是短程力,吸引力是长程力
(图片来自百度)
基本类型
离子结合
结合能:原子结合成晶体释放的能量
W=UN−U(r0)
包括库仑吸引力和排斥力两个方面。
库仑势
一个正离子的平均库仑能
12∑n1,n2,n3q2(−1)n1+n2+n34πε0n21r2+n22r2+n23r2−−−−−−−−−−−−−−−√
一个原胞的平均库仑能为
q24πε0r∑n1,n2,n3(−1)n1+n2+n3n21+n22+n23−−−−−−−−−−−√=−αq24πε0r
其中和式 α 称为马德隆常数,取决于晶体结构。
排斥势
两个相邻原子之间的排斥势设为 brn ,(以NaCl晶体为例),每个原子有6个最近邻原子,所以每个离子的排斥势为
12⋅6brn
每个原胞的排斥势为
6brn
将上面两个结果相加,一个原胞中
U=N[−αq24πε0r+6brn]=N[−Ar+6Brn]
由平衡条件 (dUdr)r0=0 ,得
U(r0)=−Nαq24πε0r0(1−1n)
W=−U(r0)=Nαq24πε0r0(1−1n)
共价结合
- 共价键具有饱和性和方向性。
- 现代的共价理论以氢分子的量子理论为基础
氢分子的量子理论
(−ℏ22m∇21+VA1+VB1)ψ1=ε1ψ1(−ℏ22m∇22+VA2+VB2)ψ2=ε2ψ2
其中 ε1=ε2=ε0
采用线性组合方法,设
ψ1=C+(φA+φB)ψ2=C−(φA−φB)
得
ε+=2C2+(Haa+Hab)≈2C2+(ε0+Hab)ε−≈2C2−(ε0−Hab)
Hab<0 为负电子云与原子核之间的库仑作用。
异类原子之间的共价结合
薛定谔方程类似,线性组合为
ψ=C(φA+λφB)
引入
⎧⎩⎨V2=−HabV3=εB−εA2
最终解为
⎧⎩⎨⎪⎪ε+=εA+εB2−V22+V23−−−−−−−√ε−=εA+εB2+V22+V23−−−−−−−√
⎧⎩⎨⎪⎪⎪⎪⎪⎪⎪⎪⎪⎪⎪⎪λ+=V22+V23−−−−−−−√−V3V2λ−=V22+V23−−−−−−−√+V3V2
杂化轨道理论
金属性结合
特点:
- 电子“共有化”
- 没有方向性和饱和性,通常为密排结构
- 导电性、导热性、范性良好
范德瓦尔斯结合
- 稀有气体元素
- 饱和
- 瞬时电偶极矩作用
- 色散力,随机
- 静电力,分子固有的极矩
- 诱导力,分子间的极化
- 结合能低,熔点低
- 势能形式
u(r)=−Ar6+Br12
可以写成Lennard-Jones势的形式
4ε[(σr)12−(σr)6]
混合成键
实际中固体的结合往往不是单一的方式,而是和多种结合形式相关。
混合成键
例:石墨。
- 层内 sp2 杂化,为共价键;
- 层间Van der Waals结合
- 电子气,金属性结合
键的过渡形式
电离度:描述共价结合中离子键的成分,有3种不同的标度方式:卡尔森,泡利,菲利普。
卡尔森电离度理论
ψ=c(φa+λφb)
λ=1 时完全共价结合, λ=0 时完全离子结合






















 1440
1440

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








