大家好!今天跟大家分享的是2020年4月发表在EBioMedicine(IF = 5.736)上的文章。文章利用从临床搜集的胰腺导管腺癌(PDAC)病人样本,通过LASSO算法及Cox回归分析,构建5分子预后模型,同时利用生存曲线、ROC曲线和多变量Cox回归分析验证了该模型的预后价值,并评估该模型预测术后ACT治疗预后的价值。
题目:Prognostic and predictive value of a five-molecule panel in resected pancreatic ductal adenocarcinoma: A multicentre study
5分子预测模型在胰腺导管腺癌术后中的预后预测价值:一项多中心的研究
摘要
胰腺导管腺癌(PDAC)的预后极差。现有的临床病理参数和分子标志物作为预后标志物预测能力有限。首先,文章设计了一种新的计算策略,该方法基于生物信息学预测(CIPHER)整合了来自组学和文献的预后证据,以生成网络,旨在系统地识别与PDAC相关的潜在高置信度预后候选物。回顾性收集了605例经切除的PDAC患者的标本后,在癌症组织中使用芯片测序和免疫组化检测了23名候选基因,构建了一个包括5个基因的预测模型。在训练集数据中,高风险患者的疾病特异性生存率(DSS)显著低于低风险患者。在两个不同的验证数据数据集中,高风险组和低风险组之间也观察到相似的显著差异。在多变量分析中,5分子预测模型是唯一重要的预后指标。此外,该预测模型与传统的临床病理变量相结合,可以大大提高其长期生存的预测能力。无论是单因素或者是多因素分析,在所有数据集中的高风险患者的辅助化疗(ACT)与更好的DSS相关。新型预后预测模型在预测PDAC患者术后存活率方面具有强大的能力。
流程图

1. 病人样本的获取
从北京协和医院(PUMCH)获取了381个病人样本,作为模型的训练数据集;从仁济医院(RJH)获取了169个病人样本;从哈尔滨医科大学附属第一医院(HMH)获取了116个病人样本,作为模型的两个不同的验证数据集。
2. 5分子预测模型的构建
本文最初采用了基于生物信息学的无偏整合策略,初步鉴定了368个PDAC相关基因。在这些基因中,通过手工文献检索发现了12个被报告为高可信度的预后标志物,另外根据3个类型的预后证据及其对于生物学通路的代表性,推测出了11个PDAC相关的新预后标志物,总共确定了23个PDAC相关预后候选标志物(图1a)。根据积分正比和染色强度的分数,使用Cox回归模型评估训练数据集中23种标记物与DSS之间的关联。
使用LASSO算法,选择了五个标记物CAPN2、DVL1、FLNA、GLI1和SHH(图1b,c)。使用模型的系数导出一个公式来评估每位患者的DSS的风险评分,形成一个5分子预测模型。
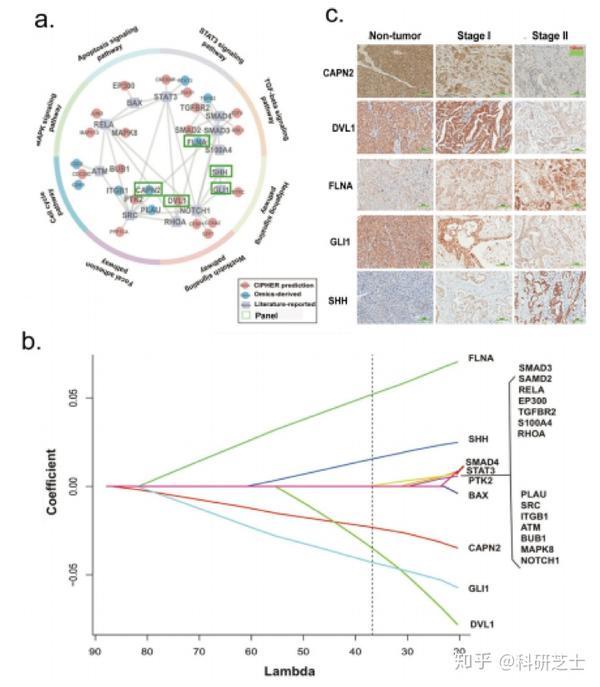
3. 5分子预测模型的生存曲线及ROC曲线分析
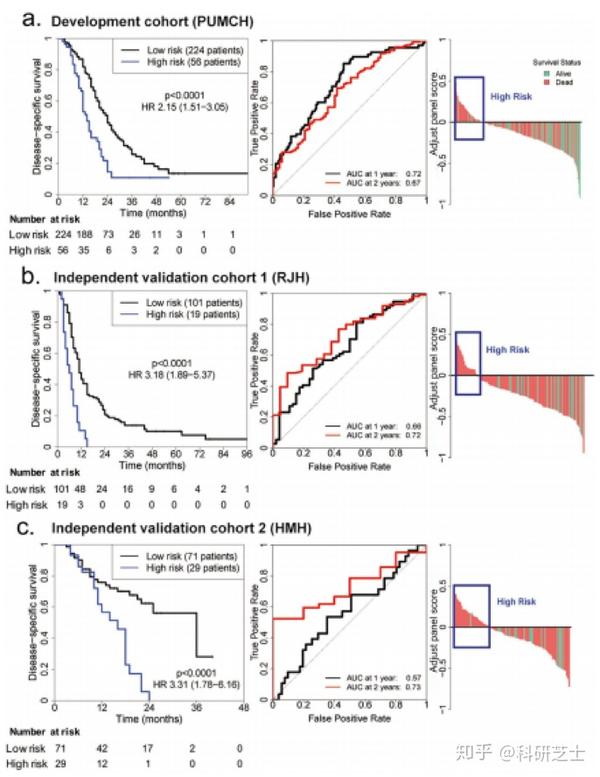
根据每位患者各自的5个标记物表达水平以及通过X-tile图确定的最佳临界值,将患者分类为高风险(风险评分≥0.014)和低风险(风险得分<0.014)。在训练数据集中,高风险患者的DSS明显低于低风险患者。1年和2年时ROC曲线的AUC分别为0.72和0.67。术后2年,高风险组的大多数患者死亡(2年生存率:15.0%,低风险组为46.0%)(图2a)。
将相同的临界值应用于RJH验证数据集时,高风险组的DSS也显著低于低风险组。ROC曲线在1年和2年时的AUC分别为0.66和0.72。手术后2年,高风险组中没有患者存活(2年生存率:0.0%,低风险组为21.0%)(图2b)。同样,在HMH验证数据集中,低风险组的DSS明显高于高风险组。ROC曲线在1年和2年时的AUC分别为0.56和0.68。术后2年,高风险组中只有一名患者还活着(2年生存率:6.0%,低风险组为62.0%)(图2c)。
4. 5分子预测模型的预后价值
在训练数据集中,利用多元Cox回归分析调整了年龄,性别,肿瘤位置,CA19-9水平,肿瘤分化,T期,淋巴结转移和辅助化疗因素,发现5分子预测模型为PDAC的独立预后因素。RJH验证数据集以及整个数据集的500名患者的结果与训练数据集相似。此外,与临床病理特征不同,该5分子预测模型是唯一的在3类数据中均为独立预后因素的因素(表1)。
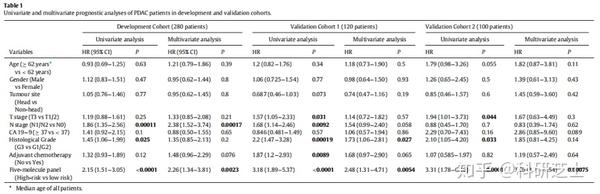
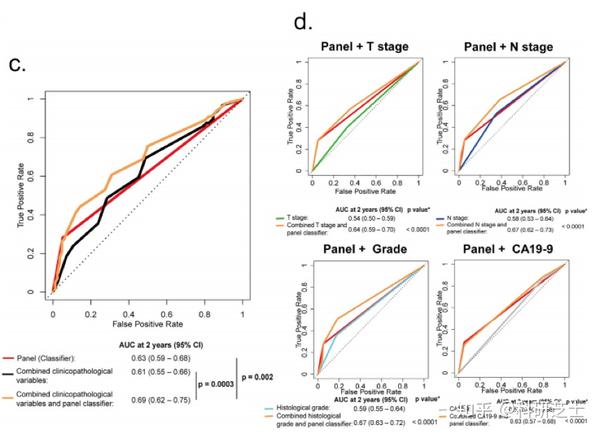
在根据上述临床病理参数分层的大多数癌症亚组中,5分子预测模型也可有效区分不同的DSS(图3)。5分子预测模型显示出更强的预测能力,与单个基因预测相比,AUC和HR高得多(图4a、b)。与主要的临床病理因素相比,该预测模型似乎在某些方面具有优势,尽管这并不明显优于N期和组织学分级。这些数据表明,该预测模型在区分PDAC根治性切除术后的长期预后方面优于其组成部分,但优于主要而非全部主要临床病理因素。本文发现,在所有患者和训练以及验证数据集中,预测模型和临床病理因素的组合比单独预测的因素具有更高的预后预测效率(图4c)。此外,与单独的临床病理因素相比,单独的临床病理变量和该预测模型的组合显示出更好的预测能力(图4d)。因此,本文推测5分子预测模型可以为临床病理特征增加明显的预后价值。
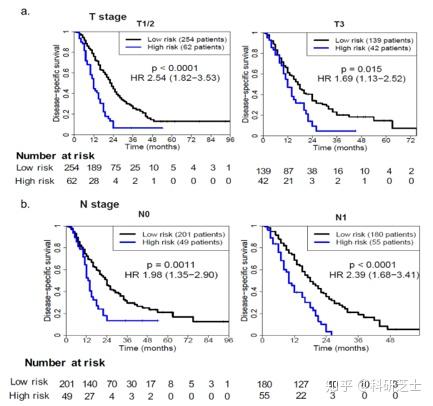


5. 5分子预测模型预测ACT治疗患者预后
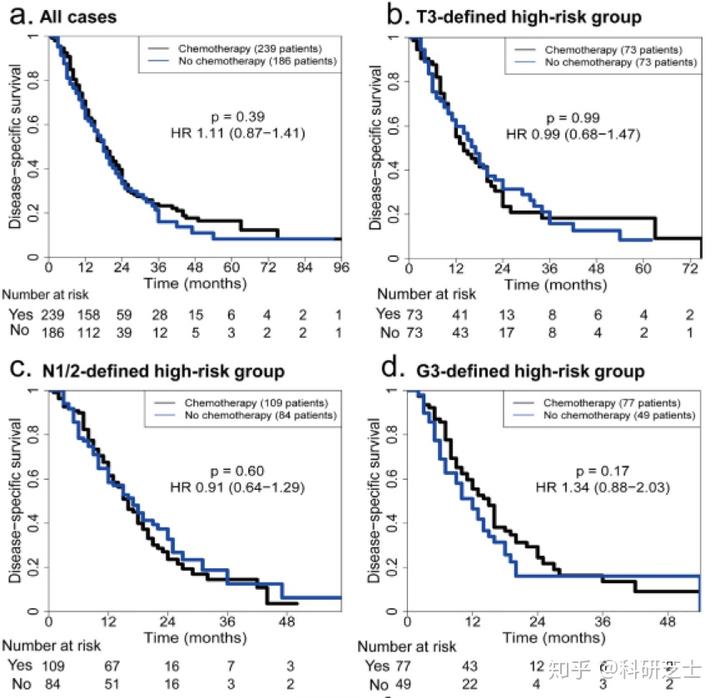
在所有三个数据集(整个数据集,训练数据集和验证数据集)中,接受术后ACT治疗的患者的预后均未比未接受术后ACT的患者好。在高风险因素中,只有5分子预测模型能够识别出从术后ACT中获益最大的患者,癌症不同阶段、T和N期这些因素都无法识别。在所有3个数据集的低风险组中,有或没有术后ACT对患者生存率均无显著影响,但是低风险组中没有术后ACT的患者生存率则显著低于高风险组中进行术后ACT的患者。此外,在根据高风险患者的临床病理特征进行了多因素分析Cox回归分析中,ACT仍然是重要因素。本文在针对癌症不同阶段、T和N期进行了调整的多元Cox回归分析中,进行了ACT与临床病理表型和预测模型之间的交互作用检验。在整个数据集中,ACT与预测模型之间存在显著的交互作用。该结果与生存曲线一致(图4)。ACT和预测模型之间的显著交互作用也出现在训练和验证数据集中。此外,癌症不同阶段、T和N类均未显示与ACT有显著的交互作用。这些结果表明,5分子预测模型可能有助于区分可从ACT中获益更多的患者。

结语
本研究利用临床收集的病例样本,旨在构建一个多分子生物标志物预测模型,以更准确地预测PDAC术后患者的预后。文章内容详实,思路清晰,各种分析全面,结合了胰腺导管腺癌各种临床因素进行生物信息学分析,尤其是在分析过程中找到了5分子预测模型与PDAC患者是否适用于接受ACT治疗的联系,为本文的一大亮点。该文章的问题还是在于停留在了基因表达水平上的研究,关于这个预测模型的生物学机制研究还需要进一步探索。




















 4925
4925

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








