背景:
精神疾病在症状、遗传学以及涉及的脑区和神经回路方面表现出重叠。研究发现,脑结构的改变与脑转录组水平上风险基因的表达谱平行变化,这可能表明大脑对疾病过程存在潜在的跨诊断脆弱性。
方法:
我们基于来自精神疾病患者(n = 390)和匹配的对照参与者(n = 293)的汇总数据,对四种主要精神疾病中大脑皮层的转录组脆弱性进行了表征。我们比较了与精神分裂症、双相情感障碍、自闭症谱系障碍和重度抑郁症相关联的风险基因的常态表达谱,以检验大脑皮层跨疾病的空间表达谱重叠情况及其与基于磁共振成像获得的跨疾病脑结构改变谱的一致性。
结果:
我们发现精神疾病风险基因在边缘系统、腹侧注意网络和默认模式网络的多模态皮层区域中表达较高,而在初级躯体感觉网络中的表达较低。风险基因在与磁共振成像跨疾病谱相关的基因中呈现富集,这表明脑解剖结构与精神疾病转录组之间存在共同联系。对这一跨疾病结构改变图谱的进一步表征显示,星形胶质细胞、微胶质细胞以及皮层上层的基因标记均存在富集。
结论:
我们的研究结果表明,疾病风险基因的常态表达谱赋予大脑皮层在多种精神疾病中存在共享且具有空间特征的脆弱性。转录组风险的跨诊断重叠提示了精神疾病脑功能障碍的共同生物学机制。本文发表在Biological Psychiatry: Cognitive Neuroscience and Neuroimaging杂志。
本文回答的问题
-
哪些皮层区域在精神疾病中表现出差异表达基因 (DEGs) 的最高和最低表达?
-
表达谱的空间重叠表明精神疾病潜在的生物机制是什么?
-
在基于神经影像的跨疾病涉及图谱中,富集了哪些类型的基因标记?
-
疾病风险基因的表达水平如何与参与多模态认知功能的皮层区域相关联?
-
哪些疾病对显示出最高程度的共享差异表达基因 (DEGs)?
关键词:皮层;跨疾病;基因表达;微阵列;MRI;精神病学
正文:
精神疾病是一类常见的、多因素的疾病,其伴随着大脑功能的多种变化。精神疾病具有中到高的遗传性,这表明在疾病病因中遗传因素起着重要作用。因此,理解精神疾病的一大挑战在于确定遗传和分子因素如何影响大脑中疾病风险。大多数遗传风险位于基因组的调控区域,这提示了基因表达异常在精神疾病神经生物学中的关键作用。
大规模合作已经在鉴定大脑层面基因表达的精神疾病特征方面取得了重要进展 。已知各皮层区域的基因表达水平存在很大差异,与精神疾病相关的基因功能紊乱可能会影响不同的大脑区域,这取决于风险基因的表达水平。最近,将转录组研究结果与神经影像学获得的疾病相关脑结构改变指标相结合的研究报道了结构差异,这些差异与皮层上风险基因的常态(健康)表达的区域变异相吻合。例如,风险基因的常态表达谱被发现与一系列精神疾病中的结构改变相关联——如连接性、皮层厚度和大脑形态测量的变化——这些疾病包括精神分裂症 (SCZ) 、自闭症谱系障碍 (ASD) 和重度抑郁症 (MDD,即重度抑郁症)。
遗传、行为和神经影像学研究已强调精神疾病表型之间存在高度重叠:不同疾病共享症状、表现为共病、在大脑结构和神经回路上显示出共同的病理性改变,并且可表现出较强的遗传相关性。尤其是在死后大脑组织的转录组研究中,通过比较患者与对照组之间的差异表达基因 (DGE),报告了相似基因在多种疾病中表达异常的高度重叠。此外,共享的转录调控异常程度与疾病之间的多基因重叠量相关。这种跨诊断的转录组调控异常重叠——加上皮层上基因表达的空间变异性——提示在大脑转录组水平上可能存在一种共享的疾病脆弱性。
在本研究中,我们结合并整合了精神疾病差异表达基因 (DGE) 研究的数据与来自Allen人脑图谱 (AHBA)的神经典型个体区域性基因表达数据,以评估4种主要精神疾病中风险基因在皮层上的空间表达谱。我们研究了在精神疾病中差异表达的基因的常态表达在多大程度上趋同为一种跨皮层共享的空间表达谱——以及这些大脑区域是否在多种精神疾病中尤其容易受到疾病影响。我们的结果显示,差异表达基因 (DEGs) 呈现出高度相似的常态表达模式,并在参与多模态认知网络的大脑区域中表达尤为丰富。风险基因在与跨疾病共享结构改变的空间谱相关的基因中呈现富集,而这种结构模式进一步在星形胶质细胞、微胶质细胞以及皮层第1、2和5层的基因标记中得到富集。我们的研究结果表明,反映在大脑转录组中的精神疾病脆弱性呈现出一种趋同的模式。
方法与材料
研究方法
我们分析了4种主要精神疾病——精神分裂症 (SCZ)、双相情感障碍 (BD)、自闭症谱系障碍 (ASD) 和重度抑郁症 (MDD,即重度抑郁症)——中差异表达基因 (DEGs) 的皮层常态表达谱。这些表型之所以被选中,是因为它们已通过DGE研究得到了广泛表征。此外,还将神经系统疾病(包括阿尔茨海默病 (AD)、帕金森病 (PD) 和亨廷顿病 (HD))的DGE数据作为非精神疾病对照组纳入研究。我们聚焦于DEGs,因为这些基因在精神疾病中广泛报道,并且其表达可以在死后大脑中直接测量。我们分析了精神疾病之间表达模式的跨诊断重叠程度,将这些模式与神经影像学获得的功能网络和跨疾病结构改变的空间谱进行比较,并探索了大脑中细胞类型和层标记的富集情况(见补充方法)。常态基因表达与差异表达基因 (DGE) 的数据均来自公开数据库及先前已发表的研究,详见下文说明。
基因表达数据
差异表达基因 (DEGs)
DEGs 的定义基于对死后皮层样本进行的DGE微阵列研究。纳入了4种主要精神疾病(SCZ、BD、ASD和MDD,即重度抑郁症)以及1种非神经表型(炎症性肠病)的DGE数据。这项综合性研究收集并重新处理了已发表研究中来自皮层样本的微阵列数据,涉及精神分裂症患者 (n = 159)、双相情感障碍患者 (n = 94)、自闭症谱系障碍患者 (n = 50)、重度抑郁症患者 (n = 87) 以及炎症性肠病患者 (n = 197) 和匹配的对照参与者 (n = 293)(详见表1中采样的皮层区域)。原始论文中详细描述了质量控制和归一化程序。针对每种疾病,提取了每个基因的log₂折叠变化值及其对应的P值。在所有与健康对照组相比显示出显著差异表达的基因中,平均有87%(范围为65%–95%,具体取决于疾病)在AHBA中具有常态表达数据(详见表1)。
表1. 纳入的精神疾病的差异表达基因数据
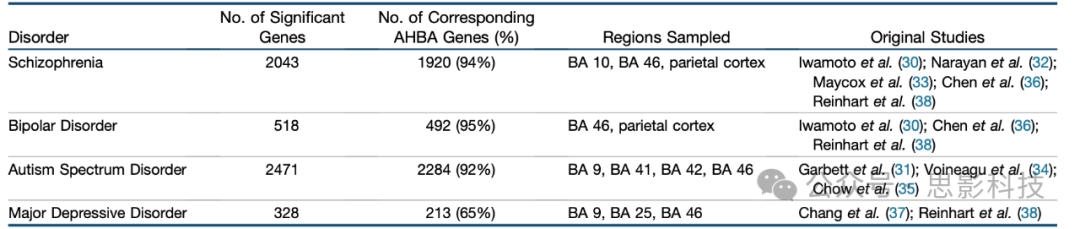
来自 Gandal 等人的荟萃分析数据,他们纳入了来自多项研究的微阵列实验数据(见“原始研究”栏目)。
AHBA,Allen 人脑图谱;BA,Brodmann 区。
疾病特异性
另外,将 3 种神经疾病(AD、PD 和 HD)的差异表达基因(DGE)微阵列数据作为非精神疾病对照组纳入。AD 的基因表达数据来自 Brodmann 区 22,涉及 55 名患者和 22 名对照参与者 (39);PD 的基因表达数据来自皮层样本,涉及 16 名患者和 20 名对照参与者 (40);HD 的基因表达数据则来自 Brodmann 区 4 以及尾状核,涉及 37 名患者和 29 名对照参与者。我们进一步通过纳入一份在 600 多项大脑及其他组织的 DGE 研究中发现的非特异性差异表达基因列表来评估疾病特异性,因为与疾病相关的 DGE 可能既反映疾病特异性效应,也反映基因表达中一般性的非特异差异。该非特异性基因列表(称为差异表达“先验”)包含 19,172 个基因,并列出了每个基因在任一特定微阵列研究中差异表达的概率,从而捕捉 DGE 研究中的非特异性命中。
常态基因表达
通过使用来自 AHBA的常态基因表达数据,考察了大脑各区域的空间基因表达模式。这些数据描述了来自 6 个神经典型捐赠者(死后大脑)的丰富微阵列研究 (http://help.brain-map.org/display/humanbrain/Documentation)。数据按照先前介绍的流程进行预处理,最终得到一个 57 × 20,949(大脑区域 × 基因)的矩阵(补充方法)。
Allen 人脑图谱
Allen 人脑图谱 (AHBA) 被用于检验大脑皮层的常态基因表达模式。AHBA 描述了来自六个神经典型捐赠者死后大脑的丰富微阵列研究。从六位捐赠者(H0351.1009、H0351.1012、H0351.1015、H0351.1016、H0351.2001 和 H0351.2002)中分析了覆盖 58,692 个探针的左半球组织样本 (2–4)。这些探针被注释为 HUGO Gene Nomenclature Committee (HGNC) 符号 (http://biomart.genenames.org),最终纳入了 20,949 个基因。表达值经过 log₂ 转换,并将样本空间映射到 Desikan-Killiany 图谱 (DK114) 左半球的 57 个皮层区域。属于同一大脑区域的组织样本的基因表达谱被取平均,在每位捐赠者内部按皮层区域归一化为 z 分数,最终在六位捐赠者之间取平均,生成了一个 57 × 20,949(大脑区域 × 基因)矩阵,详见 Wei 等人的详细描述。
与疾病相关的 DEGs 的常态表达
对于每种 DGE 表型,纳入了在 AHBA 中具有可用表达数据且在原始数据集中被报道为显著差异表达的基因。根据绝对 log₂ 折叠变化,提取了前 100 个 DEGs 作为每种表型的感兴趣基因集(对于 HD,由于没有 log₂ 折叠变化数据,采用了 Student t 统计量)(图 1A)。此外,还另外选取了前 50 和前 200 个 DEGs 作为验证分析(见补充材料)。通过对感兴趣基因在 AHBA 中的常态表达数据取平均,获得了每个基因集在皮层上的空间表达模式(图 1B)。随后将这些空间表达模式相互关联,以评估各疾病间的重叠情况(图 1C),其中还包含了检验空间及基因特异性的零模型(见统计分析)。
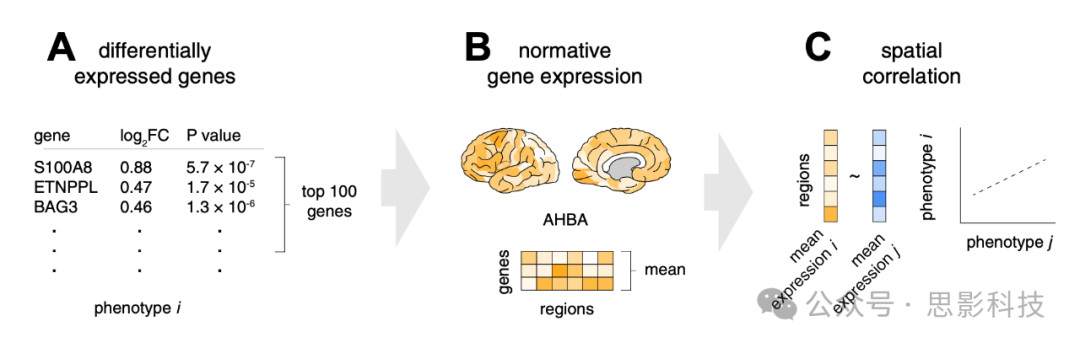
图 1. 研究方法。
(A) 从文献中获得差异表达基因,按差异表达程度排序,并提取前 100 个作为每种表型的感兴趣基因集。
(B) 通过 Allen 人脑图谱 (AHBA) 获得皮层上的常态基因表达谱,并计算出每个感兴趣基因集的平均表达模式。
(C) 将各疾病的平均常态表达谱进行比较,以评估空间重叠。
FC,fold change。
神经影像学数据
静息态功能网络
静息态功能网络数据来源于 Yeo-7 图谱,该图谱描述了 7 个不同的静息态功能网络,包括视觉、躯体运动、背侧注意、腹侧注意/突显、边缘、前顶叶/中央执行和默认模式网络。
功能网络图谱通过多数投票法映射到 DK114 图谱:对于 DK114 图谱中的每个皮层区域,统计了属于各个静息态网络的顶点数,并将顶点数最多的静息态网络分配给该 DK114 区域。
跨疾病涉及图谱
基于体素的形态测量数据来自 BrainMap (http://www.brainmap.org),这是一个涵盖多种脑疾病神经影像实验数据的广泛数据库。检索了评估皮层体积变化的磁共振成像研究,涉及精神分裂症、双相情感障碍、自闭症谱系障碍和重度抑郁症,并对每种疾病内的所有实验进行了基于激活可能性估计的荟萃分析。跨疾病涉及图谱通过对皮层区域内所有体素的激活可能性估计取平均计算得出(更多信息见补充方法)。
统计分析
通过将每个皮层区域的表达水平与由等大小随机基因集合得到的表达水平零分布进行归一化,来测试表达模式的基因特异性。归一化表达模式的计算方法为:取感兴趣基因集在全皮层的平均表达谱,减去随机选取的 1000 个等大小基因集合的平均表达谱,再除以这 1000 个随机基因集合的标准差,从而得到表达的 z 分数。在主要分析中,考虑了 AHBA 中所有基因,以纳入尽可能多的 DEGs 的常态表达数据;另外,使用更特定背景基因集合(例如在大脑中表达的基因和在大脑中富集的基因)的分析也在补充材料中描述。
空间自相关是大脑模式(包括基因表达模式)的常见特征,因此我们进一步使用检验空间特异性的零旋转模型 (null-spin models) 来评估转录组学关联。使用 WebGestalt (webgestalt.org) 进行了基因集合富集分析,以检验与跨疾病涉及图谱相关的基因是否在感兴趣的基因集合中(包括疾病风险基因)表现出富集。WebGestalt 产生的归一化富集得分 (NES) 被用作校正基因集合大小后的富集度指标,正分数表示富集,负分数表示耗竭。
采用偏最小二乘回归来获得 AHBA 中每个基因的偏最小二乘权重,作为其与跨疾病涉及图谱关联程度的指标。
与第一个偏最小二乘分量对应的权重(共 20,949 个基因)被用作基因集合富集分析的参考,以检验与跨疾病涉及图谱具有类似空间表达模式的基因是否在感兴趣的基因集合中富集。
在适当情况下,使用 Benjamini 和 Hochberg 假发现率 (FDR) 校正方法进行多重检验校正,q 值设为 0.05。
结果
精神疾病基因显示出趋同的皮层表达谱
我们首先研究了4种主要精神疾病(精神分裂症 [SCZ]、双相情感障碍 [BD]、自闭症谱系障碍 [ASD] 和重度抑郁症 [MDD])中差异表达基因 (DEGs) 的跨诊断重叠情况。前100个 DEGs(图2A;表 S1)在各疾病之间显示出高度重叠:在所有 4 种疾病的前 100 个 DEGs 中共包含 331 个独特基因,其中有 62 个基因在 2 种或更多疾病中共享,6 个基因在 3 种或更多疾病中共享(图2B);(从分析中剔除这些共享基因后,结果依然一致,详见补充结果)。重叠程度在 SCZ 与 BD 之间最高(共享 46 个基因),其次是 SCZ 与 ASD 之间(共享 17 个基因),两者均显著超过随机选取基因集预期的共享基因数(均 p < .001,1000 次置换)。而 SCZ-MDD、BD-ASD、BD-MDD 和 ASD-MDD 之间共享基因的程度则不显著(p > .05)。
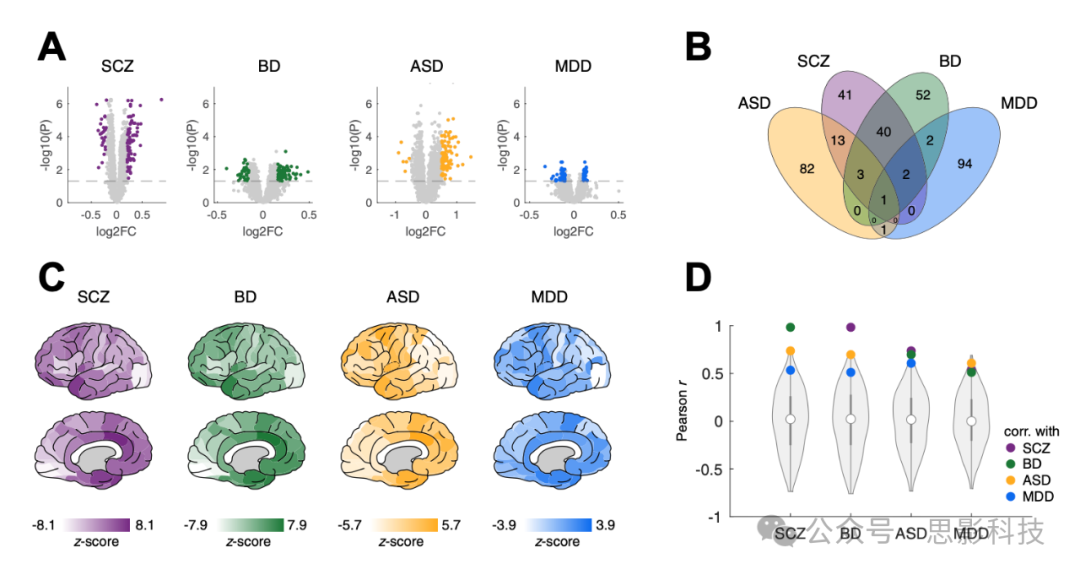
图 2. 四种主要精神疾病中差异表达基因 (DEGs) 的常态表达谱。
(A) 精神分裂症 (SCZ)、双相情感障碍 (BD)、自闭症谱系障碍 (ASD) 和重度抑郁症 (MDD) 的差异表达火山图。彩色点代表各疾病感兴趣基因集中前 100 个 DEGs;虚线表示显著性阈值 (p < .05,经假发现率校正)。
(B) 各疾病之间共享 DEGs 数量的维恩图。
(C) SCZ、BD、ASD 和 MDD 前 100 个 DEGs 的常态表达模式(表达归一化为随机基因集的平均表达谱,1000 次置换)。
(D) 每种疾病的皮层表达谱(水平轴)与其他疾病的表达谱之间的相关性(彩色点表示)。每种疾病与 1000 个随机基因集的相关系数的零分布以灰色显示。corr.,相关性;FC,fold change。
各疾病中前 100 个 DEGs 的常态表达谱反映了这些基因在神经典型大脑皮层上的表达程度。与随机基因集相比,这些基因在额上皮层区域、颞叶区域(颞极和内嗅皮层)以及前扣带皮层中表达较高(图2C;表 S2);而在外侧枕叶、顶上叶和中央后回区域的表达则相对较低(表 S2)。这些表达模式在各疾病之间显示出高度重叠,其中颞极和内嗅皮层在所有 4 种精神疾病中均表现出高表达(双尾 z 检验,z 分数 > 2.3,p < .05,经 FDR 校正),而外侧枕叶皮层和中央后回则显示出较低的风险基因常态表达(z 分数 < −2.9,p < .05,经 FDR 校正)。
表达谱的空间重叠可能反映了共享的基础生物机制的特定贡献,也可能反映了皮层上非特异性的转录梯度。我们将各疾病对之间的空间相关性与不同零模型进行了比较,以评估所观察到的跨疾病重叠的基因集合的空间特异性。结果显示,SCZ-BD、SCZ-ASD、BD-ASD 和 ASD-MDD 之间的空间相关性均超过了各疾病与随机基因集之间相关系数的零分布(p < .05,经 FDR 校正,每种疾病 1000 次置换),这确实表明这些疾病的基因表达模式存在特定的空间相关性(图2D)。而 MDD 与 SCZ 及 BD 之间的相关性则未能超过该零条件(p > .05,经 FDR 校正,每种疾病 1000 次置换)。进一步利用零旋转模型检测表达谱的空间特异性显示,每对疾病之间的空间相关性均超过了旋转零分布(p < .001,经 FDR 校正,每种疾病 1000 次置换)。
我们还探讨了皮层表达谱是否特异于所纳入的精神疾病,或是否反映了大脑更普遍的脆弱性。为此,该分析扩展至 3 种神经疾病(阿尔茨海默病 [AD]、亨廷顿病 [HD] 和 帕金森病 [PD])前 100 个 DEGs 的常态表达模式(图3A)。结果显示,各常态表达模式之间的空间相关性(图3B)在精神疾病之间(均值 = 0.68,标准差 = 0.17)明显高于精神疾病与神经疾病之间(均值 = 0.21,标准差 = 0.18)的相关性(t₁₆ = 5.20,p = 8.78 × 10⁻⁵),表明观察到的转录组重叠在精神疾病中具有一定的特异性(图3C)。
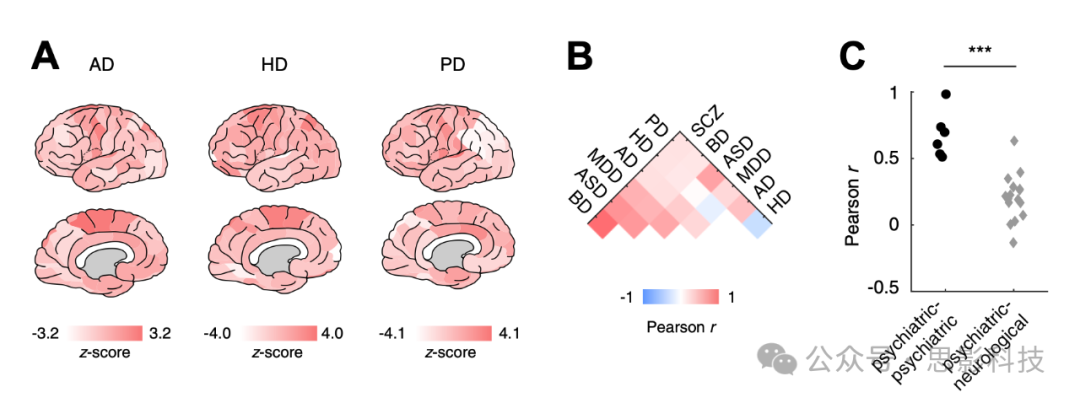
图 3. 与神经疾病常态表达谱的比较。
(A) 阿尔茨海默病 (AD)、亨廷顿病 (HD) 和 帕金森病 (PD) 前 100 个差异表达基因的常态表达谱(表达归一化为随机基因集的平均表达谱,1000 次置换)。
(B) 精神疾病与神经疾病在皮层区域上的空间相关性。
(C) 精神疾病常态表达重叠的特异性。精神疾病之间的空间相关性(黑色圆点)高于精神疾病与神经疾病之间的相关性(灰色菱形)。
ASD,自闭症谱系障碍;BD,双相情感障碍;MDD,重度抑郁症;SCZ,精神分裂症。
风险基因在多模态认知网络中表现出高表达
我们继续探讨精神疾病相关基因是否在支持多模态认知功能的皮层区域中具有高表达,而这些区域被认为在精神疾病中受到特别影响。将常态表达值划分到7个经典的静息态功能网络中(图4A),结果发现这些疾病风险基因在支持多模态认知网络的皮层区域中的表达确实高于属于初级躯体感觉网络的区域(图4B)。对于精神分裂症、双相情感障碍、自闭症谱系障碍和重度抑郁症的风险基因来说,其在边缘网络中的表达显著高于在初级网络中的表达 (p < .05,经 FDR 校正)(见表2)。腹侧注意网络在这4种疾病中也表现出比初级网络更高的风险基因表达 (p < .05)(表2)。在精神分裂症、双相情感障碍和自闭症谱系障碍中,默认模式网络的表达还显著高于视觉和躯体运动网络,但在重度抑郁症中则不然 (表2)(所有比较均采用双尾检验并在功能网络和疾病间经FDR校正)。
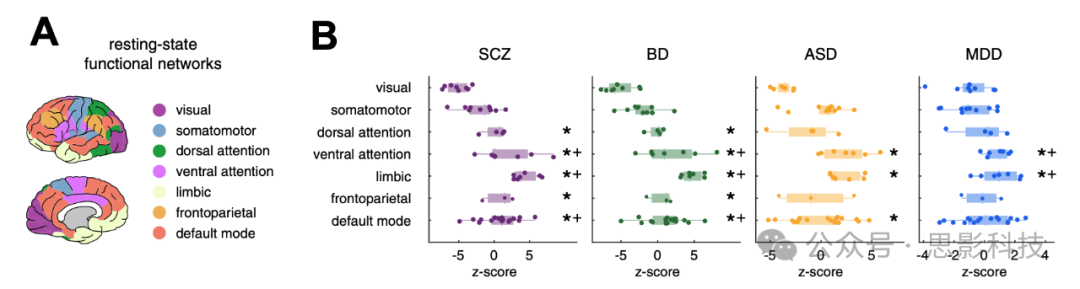
图 4. 精神疾病风险基因在静息态功能网络中的表达情况。
(A) 基于静息态功能磁共振成像 (45) 将7个功能网络划分到 DK114 图谱上。
(B) 精神分裂症 (SCZ)、双相情感障碍 (BD)、自闭症谱系障碍 (ASD) 和重度抑郁症 (MDD) 风险基因在各7个功能网络所属皮层区域的常态表达(表达值归一化为随机基因集的平均表达,1000次置换)。星号表示某网络相对于视觉网络表达显著更高,+号表示某网络相对于躯体运动网络表达显著更高(在所有网络和疾病之间经假发现率校正)。
表 2. 支持多模态过程与初级感觉过程的静息态功能网络中风险基因表达的比较
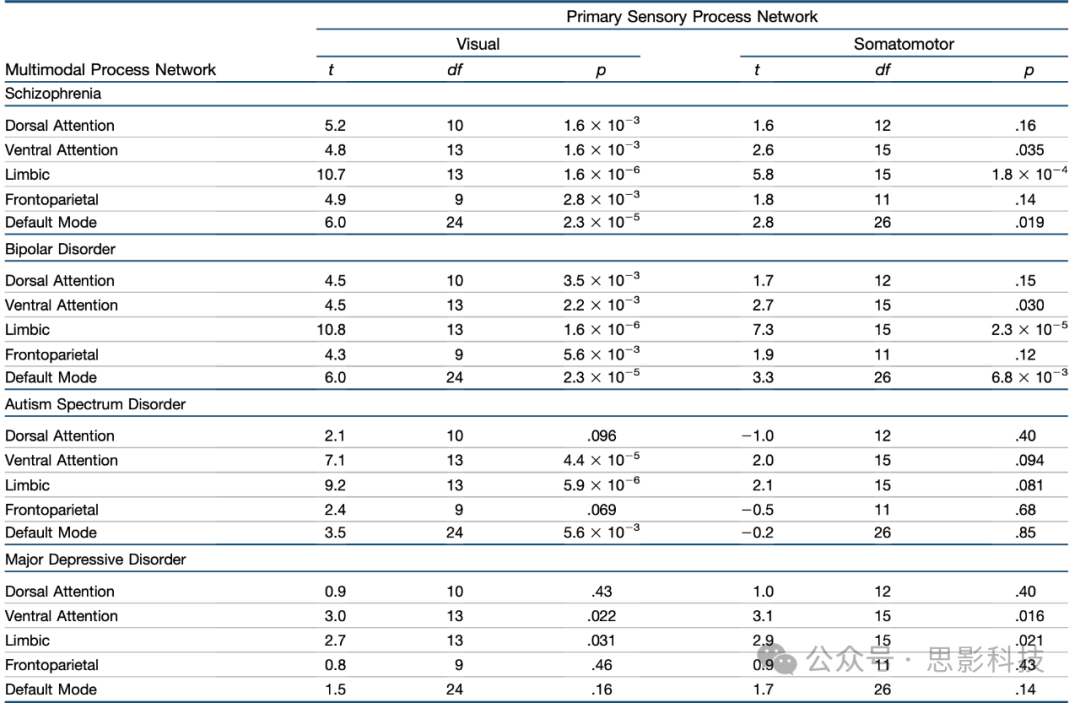
统计数据代表对静息态功能网络中相应皮层区域表达水平之间进行的 t 检验(双尾检验,并在各网络和疾病间采用假发现率校正)。
常态表达反映跨疾病皮层受累情况
接下来,我们探讨了疾病差异表达基因 (DEGs) 在皮层上的表达模式是否反映了大脑对精神疾病的一般性脆弱性。我们将来自 BrainMap 数据库的基于体素形态测量 (VBM) 研究得到的皮层疾病受累图谱整合到一起,针对精神分裂症 (SCZ)、双相情感障碍 (BD)、自闭症谱系障碍 (ASD) 以及重度抑郁症 (MDD) 构建了一个平均的精神疾病跨疾病受累图谱,以反映各精神疾病之间共享受累的程度(图5A)。
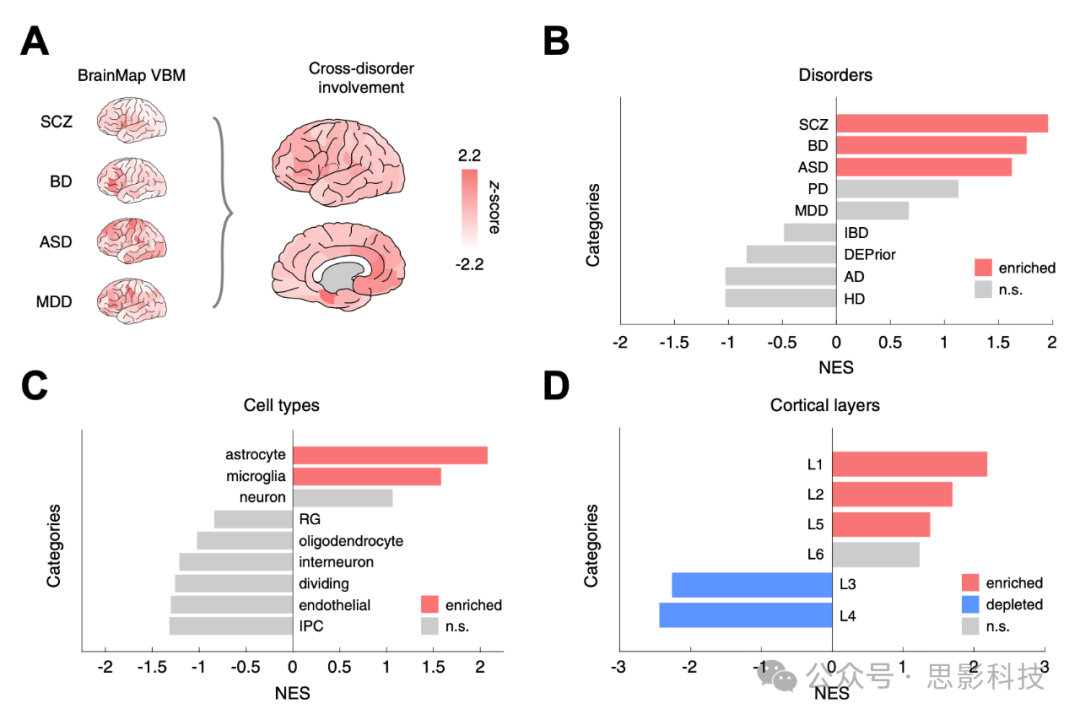
图 5. 基因表达谱与跨疾病脑结构改变之间的关联。
(A) 基于 BrainMap 数据库中体素形态测量 (VBM) 荟萃分析得到的各疾病受累图谱被整合为一个跨疾病受累图谱,代表精神分裂症 (SCZ)、双相情感障碍 (BD)、自闭症谱系障碍 (ASD) 和重度抑郁症 (MDD) 中的脑结构改变。正的 z 分数表示较高的区域性疾病受累。
(B) 与跨疾病受累图谱相关的基因在 SCZ、BD 和 ASD 中差异表达基因中表现出富集,而在非精神疾病表型中则未见富集。
(C) 与跨疾病受累图谱相关的基因在星形胶质细胞和微胶质细胞的标记基因中表现出细胞类型富集。
(D) 与跨疾病受累图谱相关的基因在皮层第1层 (L1)、第2层 (L2) 和第5层 (L5) 的标记基因中表现出层特异性富集,而在第3层和第4层的标记基因中则表现为减少。
AD,阿尔茨海默病;DEPrior,差异表达先验;HD,亨廷顿病;IBD,炎症性肠病;IPC,中间前体细胞;NES,归一化富集得分;n.s.,不显著;PD,帕金森病;RG,放射状胶质细胞。
基因集合富集分析显示,与跨疾病受累图谱相关的基因(表 S3)在 SCZ 的前 100 个 DEGs 中表现出富集(NES = 1.98, p < .001)、在 BD 中表现出富集(NES = 1.77, p = 5.2 × 10⁻³)以及在 ASD 中表现出富集(NES = 1.61, p = .02),但在 MDD 中则未见富集(NES = 0.67, p = .95,经 FDR 校正)(图5B)。这表明精神疾病具有潜在的特异性,因为对于神经疾病(包括 AD、HD 和 PD)的 DEGs、对于非大脑表型 IBD 的 DEGs 以及对于文献中常见的差异表达基因集合(差异表达先验),均未发现富集(所有 p > .4,经 FDR 校正)(图5B)。进一步对这些结果的基因特异性进行测试显示,观察到的 SCZ、BD 和 ASD 基因在跨疾病受累模式中的富集程度也超过了相同大小随机基因集合的富集零分布(SCZ p < .001,BD p < .001,ASD p = .009,经 FDR 校正,1000 次置换)。有关敏感性分析,见补充结果。
我们进一步通过探讨与跨疾病受累图谱相关基因在大脑细胞类型和皮层层次标记中的富集情况,对基于神经影像的跨疾病受累图谱进行了表征(详情见补充方法)。结果显示,与跨疾病图谱相关的基因在星形胶质细胞标记基因中表现出富集(NES = 2.07, p < .001),在微胶质细胞标记基因中也表现出富集(NES = 1.58, p = 9.2 × 10⁻³,经 FDR 校正)(图5C)。此外,我们观察到在跨疾病图谱中,第1层皮层标记基因表现出富集(NES = 2.18, p < .001)、第2层表现出富集(NES = 1.69, p < .001)以及第5层表现出富集(NES = 1.38, p = .035),而第3层(NES = −2.26, p < .001)和第4层(NES = −2.44, p < .001,经 FDR 校正)的标记基因则表现为减少(图5D)。
讨论
我们表明,4种主要精神疾病(精神分裂症 [SCZ]、双相情感障碍 [BD]、自闭症谱系障碍 [ASD] 和重度抑郁症 [MDD])的风险基因的常态表达谱趋同于相同的皮层区域。所观察到的空间重叠表明,大脑皮层对跨精神疾病的转录调控异常存在共同的脆弱性。共享疾病风险基因的表达在支持整合性大脑网络的皮层区域中尤为高,例如边缘、腹侧注意和默认模式网络。我们发现,精神疾病风险基因在那些其表达谱与基于磁共振成像得到的疾病受累图谱相吻合的基因中呈现出富集,这表明转录组风险与神经影像学获得的皮层体积改变在精神疾病中存在空间上的趋同。
观察到精神疾病风险基因的跨诊断空间表达谱与这样一个观点相契合:精神疾病在遗传水平上共享重要的病理机制。大量遗传风险位于非编码和调控位点,强调了基因表达调控异常在精神疾病中的重要性。我们的研究结果表明,风险基因的表达谱反映了与疾病相关的大脑皮层改变。因此,那些在基线状态下风险基因表达较高的脑区可能对精神疾病中的转录调控异常尤为脆弱。
我们的跨疾病分析表明,疾病风险基因在支持整合性认知网络的多模态皮层区域中表达尤为丰富,这些区域构成了如默认模式、边缘和腹侧注意网络。这些区域的病理性改变可能会对大脑功能产生深远影响,因为多模态区域和网络在大脑中具有核心作用。转录组调控异常可能特别影响像默认模式网络这样依赖高度互联网络枢纽的整合性网络,这些枢纽具有较高的脑可塑性和快速代谢,这被认为使它们更容易受到病理干扰。事实上,默认模式网络以及腹侧注意和边缘网络的区域通常在精神疾病的病理和遗传学中被频繁涉及。
在与跨疾病受累图谱相关的基因中,富集了星形胶质细胞和微胶质细胞的遗传标记,这提示这些细胞类型在大脑皮层对精神疾病脆弱性中发挥着重要作用。实际上,星形胶质细胞相关基因在 SCZ、BD 和 ASD 中普遍上调,而在 ASD 中微胶质细胞相关基因亦呈上调状态。先前的研究也发现,星形胶质细胞和微胶质细胞的特异性表达谱与抑郁症的脑形态变化以及多种精神疾病表型中的皮层厚度差异相关,这表明这些过程在精神疾病病因中可能具有共同作用。
与跨疾病受累图谱相关的基因在皮层第1层、第2层和第5层中的富集表明,这些皮层层次在精神疾病的共同神经生物学中可能具有潜在的相关性。确实,有研究表明,SCZ 中超颗粒层的异常层状组织和变薄,以及关于 SCZ 在第5层兴奋性和抑制性神经元中遗传率富集的报道;然而,其他研究显示,第3层锥体细胞的形态异常及脊突密度下降,这与 SCZ 中宏观连接性中断相关,但在第5层和第6层(亚颗粒层)中则不明显。需要指出的是,我们关于富集的发现是基于那些与基于神经影像学获得的跨疾病受累图谱相关的基因的表达模式,这虽然反映了精神疾病中大脑改变的共享方面,但不一定捕捉到图谱中各疾病的具体病理机制。因此,未来需要开展将大尺度脑部改变与微尺度转录组及遗传扰动联系起来的特定疾病研究,以支持关于各层在不同精神疾病中参与程度及特异性的结论。
在解读本研究结果时,需要考虑一些方法学因素。Allen 人脑图谱 (AHBA) 是目前最全面、空间细节最丰富的基因表达数据库之一,但其数据仅限于6个供体大脑的死后微阵列实验。AHBA 不完全适用于解析时间动态和个体差异对大脑转录模式的潜在相关贡献。此外,本研究中使用的差异表达数据通常来源于一处或少数几个大脑区域。尽管这为各疾病中 DEGs 的区域间差异留下了可能,但一项关于 ASD 的最新研究在整个皮层采样了差异表达,并报告了各区域之间良好的一致性,这表明采样有限区域是一种合理的方法。或者,也可以使用全基因组关联研究来定义疾病风险基因,这些风险基因也已成功与神经影像学发现相联系。在本研究中,我们选择基于差异表达来定义风险基因,因为这种方法在大脑中直接测量,并且可能与疾病表型更为接近。
我们没有发现与跨疾病受累图谱相关的基因在 MDD 的 DEGs 中表现出特别的富集。可能是因为跨疾病受累图谱对 MDD 相关大脑改变的反映较弱。这可能由于在计算跨疾病受累图谱时,MDD 的磁共振成像实验较其他疾病较少,或者因为 MDD 通常表现出较轻的灰质减少。
一个突出的问题是,观察到的不同疾病间大脑改变空间模式的相似性究竟在多大程度上来源于风险基因基线表达水平的相似性,又在多大程度上源于精神疾病对相同皮层区域的选择性攻击,进而导致这些区域中表达水平最高的基因出现转录调控异常,并在疾病中表现为差异表达。功能性后续研究对于进一步解析这些效应的因果方向是必要的。此外,探究观察到的转录组重叠是否扩展到更大范围的大脑疾病(例如其他发育性、情绪和人格障碍),这些疾病也被报道在大脑结构上存在共享的改变 ,将会非常有趣。与更广泛的神经疾病的比较将进一步帮助确定我们的发现在多大程度上可能特异于精神疾病。星形胶质细胞和微胶质细胞在神经疾病(例如多发性硬化症)中也发挥着重要作用,这需要更详细地研究这些细胞在不同大脑疾病中参与的具体途径和功能。我们的研究结果表明,在4种主要精神疾病中,大脑转录组和神经影像学模式之间存在空间重叠的证据。整合其他生物学资源,如组织学或神经递质图谱,将有助于进一步细化精神疾病病理生理过程的细胞和分子特征。
总结
我们报道了4种主要精神疾病中的差异表达基因,显示出皮层常态表达谱的高度空间重叠。这些表达谱趋同于参与多模态认知处理的皮层区域,并与大脑的跨疾病结构改变相关联。我们的研究结果指向在转录组水平上,大脑对精神疾病存在一种共享的内在脆弱性。























 1544
1544

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








