MedCoT:多专家层次化推理+自反思思维链+稀疏MoE,让医学图像问答兼具准确率与可解释性
- 论文大纲
- 数据
- 全流程
- 一、拆解【解法】
- 二、将整个解法拆解为更加具体的子解法,直到不可拆解
- 三、这些子解法的逻辑链形式(决策树)
- 四、是否存在隐性方法?(分析关键步骤的逐行对比)
- 五、方法的潜在局限性
- 提问
- 1. 关于多专家模式
- 2. 自反思流程的细节
- 3. 有无对比其他多专家方法
- 4. 连续复合问题处理
- 5. 输入不完整或噪音过多怎么办
- 6. 跟进专家是否冗余
- 7. 稀疏激活如何选择专家
- 8. 与纯 GPT-4 诊断对比
- 9. 训练成本是否过高
- 10. 如何确保推理链具备医学合规性
- 11. 如果需要病理级别判断
- 12. 评估可解释性的方法
- 13. 改写初始推理时的信息遗失
- 14. 与传统影像分析算法对比
- 15. 如果初始问题本身模糊
- 16. 扩展到多语种
- 17. 多模态与结构化病历数据
- 18. 使用 MoE 的可扩展性
- 19. 如何避免不恰当的“平票”
- 20. 当前方案是否能直接投入临床使用?
论文:MedCoT: Medical Chain of Thought via Hierarchical Expert
代码:https://github.com/JXLiu-AI/MedCoT
论文大纲
└── 1 简介【论文背景与研究动机】
├── 1.1 医学影像问答(Med-VQA)的重要性【研究背景】
│ ├── 帮助医生快速解读医疗图像【应用价值】
│ └── 满足患者个性化咨询需求【应用价值】
├── 1.2 当前Med-VQA研究现状【研究现状】
│ ├── 大多侧重“答案准确率”【现有不足】
│ └── 缺乏对推理路径的关注【现有不足】
└── 1.3 存在的主要挑战【问题描述】
├── 单一模型易出现偏差【具体挑战】
├── 解释性与可追溯性不足【具体挑战】
└── 实际诊断往往需要多专家参与【具体挑战】
└── 2 相关工作【前期研究】
├── 2.1 医学视觉问答传统方法【技术脉络】
│ ├── MEVF、MMBERT 等方法【代表模型】
│ └── 主要依赖深度学习特征融合【技术手段】
├── 2.2 多模态大模型与CoT技术【技术脉络】
│ ├── CoT在通用场景下的成功【背景支持】
│ └── 多模态CoT在医学领域的可行性【研究趋势】
└── 2.3 混合专家模型(MoE)【技术脉络】
├── 采用稀疏激活机制【工作原理】
└── 可提高模型对复杂输入的适应性【优点】
└── 3 方法:MedCoT【核心贡献】
├── 3.1 设计思路【理论基础】
│ ├── 借鉴真实医疗诊断流程【灵感来源】
│ └── 引入多专家验证的层级式推理【创新点】
├── 3.2 三层专家结构【主要模块】
│ ├── (1) Initial Specialist【初步诊断】
│ │ ├── 生成初步推理路径(Rationale)【功能】
│ │ └── 可能包含错误与不完整信息【局限】
│ ├── (2) Follow-up Specialist【跟进核查】
│ │ ├── 自反思校正初步推理【功能】
│ │ └── 输出有效且精炼的合理性说明【功能】
│ └── (3) Diagnostic Specialist【最终诊断】
│ ├── 融合上下文信息【功能】
│ └── 由稀疏MoE投票得出最终答案【决策方式】
├── 3.3 稀疏MoE机制【关键模块】
│ ├── 只激活少数专家进行推理【原理】
│ ├── 减少计算量、提升可扩展性【优点】
│ └── 不同专家专注处理不同类别问题【特性】
└── 3.4 整体工作流程【过程概述】
├── 输入:医疗图像 + 文本问题【输入】
├── Initial Specialist 产生初步思路【第一步】
├── Follow-up Specialist 纠正并确认推理【第二步】
└── Diagnostic Specialist 做最终诊断并输出答案【第三步】
└── 4 实验与结果【性能评估】
├── 4.1 数据集与实验设置【实验配置】
│ ├── VQA-RAD、SLAKE-EN 等标准数据集【使用数据】
│ └── 训练参数与实现细节【实验细节】
├── 4.2 主要结果【实验结论】
│ ├── 相比主流方法精度提升显著【定量指标】
│ └── 解释性优势:可输出推理路径【定性指标】
└── 4.3 消融与讨论【结果分析】
├── 去除Follow-up Specialist会显著降低性能【现象】
├── 不使用MoE时的准确率亦有下滑【现象】
└── 多专家投票可更好应对器官特异性问题【发现】
└── 5 结论【研究总结】
├── 5.1 主要贡献【创新点】
│ ├── 引入分层验证的诊断专家机制【方法创新】
│ └── 提供可解释的推理路径【应用价值】
└── 5.2 展望与未来工作【进一步研究方向】
├── 减少大模型幻觉(hallucination)仍需深入研究【挑战】
├── 扩展至更大规模医疗图像领域【应用前景】
└── 探索隐私保护和专有数据结合【应用前景】
└── 6 局限性【不足与思考】
├── 6.1 仍依赖LLMs生成推理路径的准确性【局限】
├── 6.2 多专家结构在推理速度上较单模型更慢【折衷】
└── 6.3 对幻觉的完全抑制尚未解决【难点】
└── 7 致谢【研究支持】
├── 7.1 资助来源【资金支持】
└── 7.2 合作伙伴【合作支持】
核心方法:
└── 3 核心方法【从输入到输出的多专家层次化推理框架】
├── 3.1 前提与任务定义【方法基础】
│ ├── 输入:图像 I 与问题 Q【模型所需信息】
│ │ └── I:医疗影像(如X光片、CT等),Q:自然语言问题【数据类型】
│ ├── 输出:R 与 A【阶段性与最终结果】
│ │ ├── R:推理过程(rationale),即模型的中间思路【可解释性】
│ │ └── A:最终答案(answer),即对医学问题的解答【诊断结果】
│ └── 任务表征:f 与 g【函数映射】
├── f:根据(I, Q)生成推理 R【初步/跟进专家的输出】
└── g:利用 R 最终生成答案 A【诊断专家的输出】
├── 3.2 初始专家(Initial Specialist)【生成初步推理R】
│ ├── 输入:图像 I 与文本 Q【从外部获取】
│ ├── 方法:大型语言模型(LLMs) + 提示(Prompt)【技术手段】
│ │ ├── 提示示例:“请分步骤进行分析,并给出推理”【让模型输出步骤化思考】
│ │ └── 利用LLM的推理能力,产生第一版R【思路草稿】
│ └── 输出:初步R【可能含有不完整或错误的推理】
├── 3.3 跟进专家(Follow-up Specialist)【检验并修正R】
│ ├── 输入:初始R【来自Initial Specialist】
│ │ └── 仍可访问同一图像 I + 问题 Q(以核查一致性)【保证上下文完整】
│ ├── 处理过程:自我反思(Self-Reflection) + 验证策略【方法关键点】
│ │ ├── 判断R是否有效【有效则保留】
│ │ └── 无效则重新推理或修正【校正错误】
│ ├── 额外生成:图像描述(Caption)【知识补充】
│ │ └── 缩小视觉与文本的模态差异【降低理解偏差】
│ └── 输出:改进后的R【更准确、更精炼的推理】
├── 3.4 诊断专家(Diagnostic Specialist)【本地化多模态语言模型】
│ ├── 输入:改进R + 图像描述 + 原始问题与图像【完整上下文】
│ ├── 多模态T5架构【基础网络】
│ │ ├── TextualEncoder:把文本转为特征向量F_t【文本表示】
│ │ ├── VisualEncoder:将图像转为特征向量F_v【视觉表示】
│ │ └── Cross-Attention Network:融合F_t与F_v【多模态交互】
│ ├── 稀疏混合专家(Sparse MoE)【关键模块】
│ │ ├── 由 N 个子专家组成【结构】
│ │ ├── 仅激活 top-k 个子专家进行推理【稀疏激活】
│ │ ├── 不同专家擅长不同器官/特征处理【专业化分工】
│ │ └── 投票机制:在特征层面做加权或多数表决【形成融合输出】
│ ├── TextualDecoder:将融合后特征映射回文本【答案生成】
│ │ └── 优化目标:最小化负对数似然、提升答案与真值匹配度【损失函数】
│ └── 输出:最终答案 A【回答问题】
└── 3.x 整体流程【方法衔接与输出】
├── Step1: 初始专家接收(I, Q),生成初步R【第一阶段】
├── Step2: 跟进专家对R进行自我反思与修订,并补充图像Caption【第二阶段】
├── Step3: 诊断专家整合修订R、Caption、(I, Q)等信息,用多模态T5 + MoE输出A【第三阶段】
└── 最终得到可解释的推理R与答案A【全流程目标】
临床诊断中,医生需要清晰了解推理过程,以确保诊断结论可靠、可追溯。然而,多数传统医学图像问答方法偏重准确率,忽视了诊断推理的可解释性,易导致医患双方对模型的信任不足。
现实临床中通常采用“多位医生会诊”的模式(初始推理—跟进校正—最终诊断);但常见的AI模型往往由单一网络完成推理,无法充分应对多器官、多疾病的复杂度,也缺乏必要的纠错机制。
MedCoT(Medical Chain-of-Thought):一种面向医学图像问答的分层多专家推理框架,融合了初始推理、跟进校正以及稀疏混合专家投票三大环节,旨在提供更高的诊断准确度与可解释性。
(1)要解决的类别问题:
- 该论文聚焦在“医学图像问答(Med-VQA)”这一类别问题上。它属于多模态任务,需要同时理解医疗影像与相应的自然语言问题。
(2)要解决的具体问题:
- 可解释性不足:以往的医学图像问答方法多关注答案准确率,缺少清晰的推理过程,医生和患者难以信任或追溯模型的结论。
- 单专家模型易出现偏差:传统方案通常只用单一模型,难以在复杂多样的医学场景中保证稳定、可靠的诊断决策。
- 对多专家会诊的需求:真实世界中常需要多位医生会诊,才能获得更准确的诊断;而现有方法很少模拟这一“多专家验证”的思路。
因此,MedCoT正是为了在医学图像问答中同时实现可解释、多专家协同决策、以及更高准确度而提出的。
创新点:
-
创新点 1:层级化多专家验证
- 在医学场景下,“初始—跟进—最终诊断”的结构,有效减少了单模型带来的误判与不透明。
-
创新点 2:自我反思 + 稀疏MoE结合
- 通过自动生成的推理链与专家间的相互校验,提高可解释性与诊断准确度。
-
创新点 3:无需人工标注推理过程
- 以往许多多模态 CoT 需要人为注释“正确推理路径”,该方法显著减少人工成本,且可自动修正错误推理。
-
总体意义:
提供了一个能让医学图像问答“知其然也知其所以然”的解决方案,在实际临床应用中更具可行性与可追溯性。 -
理论贡献
- 将Chain-of-Thought机制扩展到医学多模态场景,提出层级化多专家验证的新范式,为后续研究在“可解释医疗AI”上提供了新的方法论参考。
- 结合稀疏MoE,使多专家在推理时“按需激活”,拓展了多模态CoT与可扩展性模型的融合思路。
-
实践意义
- 临床可落地性:可解释且多专家校正的模型结果更易被医患信任,有助于辅助真实医疗决策,减少误诊风险。
- 可复用性:该多专家架构可适配不同类型的医学影像问答任务,如X光、CT、MRI等多种成像方式,具备较强的可扩展性。
可能的反驳及应对
- 反驳:引入多专家可能导致推理时间加长,且大模型存在幻觉(hallucination)风险。
- 应对:医疗诊断更注重准确与可追溯,适度增加推理环节在临床上是可接受的;论文也通过自我反思流程减少大模型幻觉的影响,并逐步探索进一步抑制方法。
实验现象:去除多专家或自我反思机制会导致性能下降
- 观察:作者在消融实验里发现,一旦去掉“跟进专家”或移除“稀疏MoE”,在VQA-RAD等数据集的准确率显著下降。
- 思维模型:多专家协同机制在医学场景确实有效;与临床经验吻合——几个专家共同讨论往往比单人判断更为稳妥。
数据
-
数据来源:
论文选用了四个主流的医学图像问答数据集,包括:- VQA-RAD (Lau et al., 2018)
- SLAKE-EN (Liu et al., 2021)
- Med-VQA-2019 (Ben Abacha et al., 2019)
- PathVQA (He et al., 2020)
-
数据规模(示例性数据量):
不同论文对各数据集的统计略有差异,这里仅列出常见已公开的部分规模(论文正文或附录中通常会具体说明):- VQA-RAD:含约 315 张医学影像,约 3,515 道问答对。
- SLAKE(英文版 SLAKE-EN):含多种类型医学影像,总问答对量约 6,465,图像数量 200+。
- Med-VQA-2019:约包含数千道医学问答对,覆盖不同医疗场景与影像类型。
- PathVQA:专注于病理学影像领域,问题量较大,涵盖不同病理切片、器官类别等。
全流程
- 共用特征:
- “需要多专家会诊” → 对应子解法:稀疏MoE
- “需要可解释推理链” → 对应子解法:初始专家 + 跟进专家
- 何时使用?
- 当题目是类似的“是否存在某种病灶”“影像中是否有异常阴影”等;这些问题都可套用“多专家 + 自反思 + MoE投票”这一解法。

- 当题目是类似的“是否存在某种病灶”“影像中是否有异常阴影”等;这些问题都可套用“多专家 + 自反思 + MoE投票”这一解法。
-
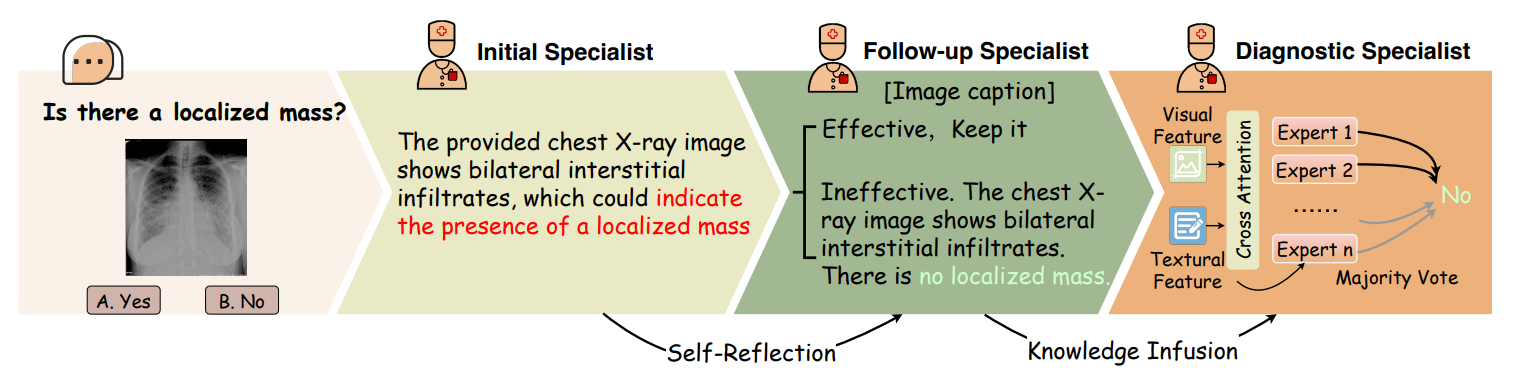
问题: “Is the anatomy of the brain gyri affected?”(脑回结构是否受影响?)
- 选项:“A. Yes”、“B. No”。
- 图中显示大脑 MRI 影像。
-
Initial Specialist:
- 给出第一版推理链,可能提到“脑回有多种病因可导致异常,如脑积水导致过多脑脊液……”并初步判定“可能Yes”。
- 但存在不精确之处(如红字部分“脑内过多积液”),并未真正从图像上看到明确异常。
-
Follow-up Specialist:
- 纠正初始推理中过度推断的部分:实际并未观察到明显异常。
- 最终修订为“没有明显异常改变”,医生会进一步检查脑回大小、形状等来做后续诊断。
-
Diagnostic Specialist:
- 结合修订推理,给出最终回答:“No”。
- 体现了跟进专家纠正后的效果:从不确定或错误推理转为正确结论。
再次强调“初始专家→跟进专家”环节在纠错与补充信息上的重要性,并展示了对大脑 MRI 场景下的具体应用效果。
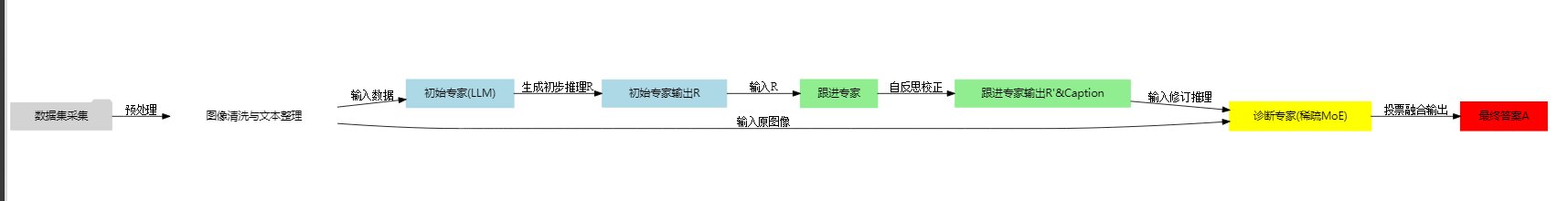
示例: “给定一张胸部 X 光片和问题:是否存在肺炎病灶?”
-
输入:
- 图像:Chest X-ray
- 问题:“请问 X 光片是否显示肺炎病灶?”
-
初始专家(LLM)
- 先生成一个“推理链 R”,例如:
“我看到了肺部有斑片状阴影,可能是炎症迹象……”
- 可能并不完全准确,但可提供逻辑思路。
- 先生成一个“推理链 R”,例如:
-
跟进专家
- 对 R 进行检查与修正,若初始推理有遗漏或错误,补充为:
“结合片状分布与边缘特征,可以进一步支持肺炎病灶的判断……”
- 同时可自动生成一个 Caption:
“该胸片显示双肺纹理增多,右下肺可见斑片影。”
- 对 R 进行检查与修正,若初始推理有遗漏或错误,补充为:
-
诊断专家(稀疏MoE)
- 将修改后的 R’ + Caption + 原图像整合到多模态 T5 结构中,MoE 判断本问题属于“肺部专科专家”领域 → 激活对应子专家进行推理,最终投票输出结论:
- 输出: “是,发现肺炎病灶。”
这一过程正体现了多题可共用此框架(若换成脑部扫描,仍是这套流程),而同一个题目也可能有简单回答或多专家深入回答的区别。
一、拆解【解法】
在该论文中,MedCoT的整体解法可以被视为一个“多层专家 + 可解释推理链(Chain-of-Thought)+ 稀疏混合专家(Sparse MoE)”的综合设计。
与同类算法相比,其最大区别在于以下几点:
-
层级化结构:
- 不是只用一个“单一”大模型回答问题,而是分为“初始专家 → 跟进专家 → 诊断专家”三个子阶段。
- 这种层级设计,模拟临床中“多位医生会诊”流程,有效降低了单点失误的风险。
-
自反思/自检修正:
- 在第二阶段(跟进专家),模型会对初始推理进行自反思,自动修正其中的错误或不够准确的推理链。
- 同类算法大多没有专门的“自反思”环节,或需要人工标注推理路径,而MedCoT能自动生成、自动校正。
-
稀疏混合专家(Sparse MoE)结构:
- 最终阶段的诊断专家使用Sparse MoE,通过“Top-k gating”只激活一小部分擅长特定器官或问题类型的子专家。
- 与常规的“Attention”或“简单特征融合”不同,这种稀疏激活能充分利用专门化子模型,提高准确率与可扩展性。
公式层面简要拆解
-
阶段划分:
- ( R = f ( I , Q ) ) ( R = f(I, Q) ) (R=f(I,Q))
- ( R ′ = SelfReflection ( R , I , Q ) ) ( R' = \text{SelfReflection}(R, I, Q) ) (R′=SelfReflection(R,I,Q))
- ( A = g ( R ′ , I , Q ) ) ( A = g(R', I, Q) ) (A=g(R′,I,Q))
其中,( f ) 表示初始专家生成推理链,SelfReflection 表示跟进专家对推理链的校正,( g ) 表示诊断专家根据最终推理链(( R’ ))输出答案 ( A )。
-
稀疏MoE:
Router ( H ) → Top- k gating → ∑ i ∈ selected w i ⋅ Expert i ( H ) \text{Router}(H) \to \text{Top-}k \text{ gating} \to \sum_{i \in \text{selected}} w_i \cdot \text{Expert}_i(H) Router(H)→Top-k gating→∑i∈selectedwi⋅Experti(H)
不同器官/疾病类型在多模态特征 ( H )(由图像与文本交互得到)下,激活不同专家组合,以求优化性能。
二、将整个解法拆解为更加具体的子解法,直到不可拆解
按照您的说明,将MedCoT的解法进行细分,形成若干子解法,并标明它们与“特征”的对应关系。
解法结构
MedCoT 解法 = 初始专家 + 跟进专家 + 诊断专家
-
子解法1:初始专家(Initial Specialist)
- 特征:医学图像问答需要初步推理链(rationale),但大模型存在幻觉可能。
- 之所以用初始专家子解法,是因为:
- 需要利用大型语言模型的通用推理能力先产出一个(可能不完美)的推理路径。
- 这一步让下一个阶段有可审查的“草稿”,引入了“可解释”的雏形。
-
子解法2:跟进专家(Follow-up Specialist)
- 特征:首次产生的推理往往不够精准,需要自动审视并纠正错误;同时在医学影像问答中,需要进一步描述或挖掘图像信息。
- 之所以用跟进专家子解法,是因为:
- 需要引入自反思策略,对初始推理进行修订。
- 可以额外生成图像Caption,帮助减少图文模态差距,从而得到更准确的中间推理。
-
子解法3:诊断专家(Diagnostic Specialist)
- 特征:医学场景下,图像种类多、病症多,需要同时保证高准确度与可解释性;而不同问题类型可能需要不同专长。
- 之所以用诊断专家子解法,是因为:
- 稀疏MoE可以把不同器官/任务类型映射到对应的专家子网络,提升专业化水平;
- 最终以投票/加权方式输出答案,确保整个“分层多专家”流程在此合流。
若继续拆解:
-
子解法1(初始专家)
- 1.1 使用LLM + Prompt产生初步推理链
- 1.2 暂存输出给下一步
- (因子过程几乎不可再拆解到更小,但可以指出用的是什么LLM、什么提示语)
-
子解法2(跟进专家)
- 2.1 对初始推理做Self-Reflection
- 2.2 若发现错误,基于同一LLM进行修订
- 2.3 生成图像Caption(减少视觉-文本Gap)
- (同理,可视为三大微步骤)
-
子解法3(诊断专家)
- 3.1 读取修订后的推理链 + 图像Caption + 原始图像和问题
- 3.2 输入到多模态T5(或类似结构)进行Cross-Attention
- 3.3 稀疏MoE(Top-k gating)选择最适子专家
- 3.4 最终投票或加权输出答案
三、这些子解法的逻辑链形式(决策树)
从顶层来看,MedCoT在流程上更像是一个串行链条(从初始→跟进→诊断),但在内部使用了“稀疏MoE”这种网络式选择。
MedCoT[整体方法]
└── (1) 子解法1: 初始专家
├── a. LLM产生R(初步推理)
└── b. 输出给下阶段
└── (2) 子解法2: 跟进专家
├── a. 自反思校正R
└── b. 生成图像caption并输出R'
└── (3) 子解法3: 诊断专家
├── a. 多模态融合(Cross-Attention)
├── b. 稀疏MoE选择top-k子专家
└── c. 输出最终诊断答案A
- 子解法1 和 子解法2 依序执行,呈“串行链”。
- 子解法3 中内部有稀疏激活,多条子路径(对应不同子专家),最后汇聚成一个答案输出,可以视为在树的末端“多分支再合流”。
四、是否存在隐性方法?(分析关键步骤的逐行对比)
1. 潜在的隐性方法
-
在“跟进专家”阶段的自反思:论文并未严格定义“自反思”时的具体内部算法步骤(比如是否基于LLM的chain-of-thought再检测?或通过额外评分机制?),但这个修正过程实则是个关键方法。
- 它并不简单是“把结果再扔进去推一下”,而是一个隐含的流程:模型需要判断哪些推理段落有效,哪些无效,然后针对无效部分进行重新推理。这往往由Prompt工程或若干Heuristics来实现。
- 若要将其定义为一个关键方法,可称之为“自反思修正法(Self-Reflection Correction)”,隐含特征是基于内部链式推理检测与局部再生成。
-
在“诊断专家”阶段的稀疏MoE细节:论文提到通过top-k gating选择专家,但在不同输入特征时,如何完成门控分配也可能是个隐性步骤:
- 有些实现可能基于输出分布来选定专家,也可能基于器官标签(若有)来进行专家选择,论文并未详解。
- 可以把这个过程称为“专家门控策略(Expert Gating Strategy)”,视为对多模态特征的隐含运算。
2. 潜在的隐性特征
- 隐性特征 1:自反思中的“有效性判断”标准
- 并未在论文中细化列出,但这是个让模型知道“该如何去判定推理有效/无效”的连续判断过程。可能使用LLM内部 logits 分布或对医疗关键词的匹配度来判断。
- 隐性特征 2:诊断专家如何学习到“器官对应专家”?
- 论文仅说明MoE可动态选择子专家,但尚未明确每位子专家与器官类型的绑定方式是如何学习或初始化的。这是一个潜在特征,也许在训练数据分布中隐含了器官分类信息。
因此,若要把这些隐性方法定义并提炼出来,可列为:
- 自反思修正法:利用LLM对自身推理链进行段落级/要素级审查并做二次生成。
- 专家门控策略:在稀疏MoE内部根据输入特征激活对应子专家的具体规则或机制。
五、方法的潜在局限性
-
多阶段推理导致推理耗时加长:
- 初始专家、跟进专家、最终专家,多重处理需要更多计算资源,对实时性要求高的临床场景或许有压力。
-
模型依赖大型语言模型,可能出现幻觉:
- 尽管有自反思和多专家纠错环节,但LLM本身在医学领域也可能产生不准确内容,尚无法彻底杜绝幻觉。
-
对特征分割与稀疏激活的依赖:
- 如果训练数据在某些器官或病症上不足,MoE对应子专家可能没能得到充分学习,效果受限;模型需要较大的高质量训练集做支撑。
-
隐性方法难以标准化:
- 自反思修正和专家门控策略的具体实现存在不透明度或依赖Prompt经验,难以在论文中被完全量化描述。
提问
以下 20 个问题均基于论文“MedCoT: Medical Chain-of-Thought via Hierarchical Expert”所涉及的概念、实验设置及潜在争议点,力图从不同角度进行“刁难”,并给出简要解答。问题和答案并非逐字摘自原文,而是根据论文内容和背景推断出的可能挑战性问答,旨在加深对论文的理解。
1. 关于多专家模式
Q: 如果在真实临床环境中,一次诊断需要多个专家同时在线参与,那么 MedCoT 模型引入的多层专家会不会耗时过长,降低实用性?
A: 论文确实承认多阶段推理相较于单模型会增加推理时间,但对于医学诊断场景来说,“准确且可解释”优先级通常高于“响应速度”。此外,作者通过稀疏激活的 MoE 方式,尽量减少额外计算负担;只在需要时才启用跟进专家,并在诊断专家中只激活最相关的子专家,以缩短整体耗时。
2. 自反思流程的细节
Q: 论文提到“跟进专家”可以对初始推理进行自反思和修正,但并未详细说明这一过程的内部算法逻辑。若没有明确机制,如何保证修正的质量?
A: 在文中,作者主要通过 Prompt 设计与模型内部的 Chain-of-Thought 机制来实现自反思。尽管并未详细拆解内部代码或算法,但他们在实验中展示了“无跟进专家”和“有跟进专家”在准确率上的差异,间接证明了其有效性。具体实现可因平台不同、Prompt 不同而变化,但核心思路是让 LLM 针对初始推理进行段落级审查并再生成。
3. 有无对比其他多专家方法
Q: 目前同样注重多专家协作的研究也有,比如不同“专家网络”或 Mixture-of-Experts(MoE)模型,为何作者没有与其它类似多专家模型做大规模对比?
A: 论文中将 LLaVA-Med 等主流模型作为基线进行对比,这些模型虽未明确标榜“多专家”,但属于常见医学问答强基线。作者更看重与这些已公开、成熟方法对比,证明多专家 + 自反思在准确率和可解释性上的优势。对于其它多专家架构的研究或许篇幅所限,无法全部收录对比。
4. 连续复合问题处理
Q: 医学图像问答往往不是一句就能结束的问题,可能是多轮对话或合并多个问题,如“这个胸片有没有肺炎?如果没有,可能还有什么病变?”。MedCoT 在多轮、多复合问答时怎样保持一致的推理链?
A: 论文主要聚焦于单轮单问题场景,并未完整展开多轮对话。
作者暗示在跟进专家阶段可以额外生成图像描述,留作上下文;若要支持多轮对话,需要在初始专家与跟进专家之间引入上下文追踪或记忆机制。
该部分暂时属于后续扩展方向。
5. 输入不完整或噪音过多怎么办
Q: 如果提供的医学图像不清晰、标签信息缺失,或者文本问题不完整,那么 MedCoT 的多专家还能保证推理质量吗?
A: 作者并未声称在严重缺失或严重噪音环境下依旧能完美推理。
多专家结构在一定程度上能缓解单专家倾向于“幻觉”的问题,但仍需要至少满足基本画质与文本描述准确。
对于极端噪声或缺失场景,作者只提到或可加强数据清洗和自反思纠错,却没给出明确解决方案。
6. 跟进专家是否冗余
Q: 对有些问题而言,初始专家可能就能回答得很好,跟进专家会不会显得多此一举,导致不必要的重复计算?
A: 从实验看,针对简单问题或非常明显的病变,初始专家准确率可能足够高。
但作者强调实际临床场景“宁可多做一道核查也不要误诊”,因此跟进专家的自反思机制价值高于计算代价。
若在实时性极端要求下,可根据置信度筛选是否调用跟进专家,这也在论文中被简要提到。
7. 稀疏激活如何选择专家
Q: 作者使用稀疏 MoE,但没明确写出“专家门控”策略。例如,是按照器官类型来选,还是模型自动学习器官类别?如果在复杂多病症场景下,如何保证选对专家?
A: 论文中确实没有公开详细门控公式或训练细节,只说明在特征层面通过 top-k gating 自适应地选择子专家。
理论上,若训练数据里器官类别有明显差异,MoE 会学习到相应特征表征。
从实验结果来看,不同专家倾向于专注不同器官,也暗示这种自适应能力存在。
8. 与纯 GPT-4 诊断对比
Q: GPT-4 近来在医疗问答领域表现不错,如果直接用 GPT-4 进行多轮自问自答,是否就能替代 MedCoT?
A: GPT-4 的通用性确实强,但作者指出了两个问题:
- GPT-4 在没有特定医疗数据微调或专业 Prompt 支持时,会产生幻觉或临床错误;
- MedCoT 的多专家投票与分层设计在医学场景更可控,且可部署本地,便于保护患者隐私。
因此二者并非简单替换关系,MedCoT 更关注专业化和本地化部署。
9. 训练成本是否过高
Q: 稀疏 MoE 往往在超大规模训练时才具有明显优势,这篇论文中的数据是否足以支撑如此复杂的模型架构?
A: 从论文看,VQA-RAD、SLAKE-EN 等数据规模确实不算很大。
作者的策略是先使用通用预训练(如 T5、CLIP 等底层特征),然后在特定医学数据上仅做部分调优。
稀疏 MoE 模型主要的好处是推理时只激活部分专家,不会线性增大训练开销。
对于更大规模医疗数据,MoE 的好处会更明显。
10. 如何确保推理链具备医学合规性
Q: 自反思生成的推理链若包含不合规或非医学证据的描述,该如何把关?
A: 论文暂未从医疗法规层面进行讨论。
作者定位该系统为“智能辅助”,而非独立诊断,最终临床结论仍需医生审核。
要实现合规,需要在医疗机构内部部署时增加审批和审核流程,并在训练数据或 Prompt 中加强对错误信息的过滤。
11. 如果需要病理级别判断
Q: 对于病理图像(如显微镜下细胞形态)而非简单 X 光,特征差异更大时,是否需要单独的子专家还是继续使用同样稀疏 MoE?
A: 如果病理影像确实与常规 X 光或 CT 差别极大,一般会添加专门的病理专家模块。
论文里在 PathVQA 数据集上也做了实验,说明只要数据充分,MoE 能学到相应特征。
但若病理类型过于小众或数据缺乏,效果或许有限,需要额外细化子专家或收集更多病理数据。
12. 评估可解释性的方法
Q: 论文强调可解释性,但他们如何客观评估?是否有标准化指标还是仅做了定性案例分析?
A: 作者大多通过“展示生成的推理链是否符合医学逻辑”来做定性分析,并在多位从业者(医生)处做主观评价。
尚无统一量化指标(如“可解释性分数”)可广泛适用,但从问答准确率和推理合理度结合也能一定程度证明效果。
13. 改写初始推理时的信息遗失
Q: 如果跟进专家发现初始推理有错,重新生成后可能覆盖掉某些对的细节,导致信息遗失。有没有办法保留初始推理中的正确信息?
A: 论文对这个问题给的方案是“先判断有效与无效段落”,有效则保留,只有在无效段落才重新生成。
但具体实现依赖提示工程和模型自身能力。
存在一定风险,一旦判断环节不佳,会出现良性内容被覆盖的情况。
14. 与传统影像分析算法对比
Q: 大部分医学影像诊断能用传统计算机视觉(CV)算法,比如分割、检测,然后再做问答,为什么作者坚持多模态语言模型方案?
A: 传统 CV 对特定任务(如检测肿瘤)有效,但在开放式问答中灵活度不足。
作者希望不仅知道有没有病灶,还能回答更广泛的问题。
例如“病灶形态如何?”“有什么并发症风险?” 这需要结合语言、上下文信息,而多模态语言模型更能胜任开放型问答任务。
15. 如果初始问题本身模糊
Q: 读者可能提出一个模糊问题,如“怎么看起来怪怪的?”这并不是医学上的正规问句,模型如何处理?
A: 论文还是假设问题格式相对标准化,至少包含某些可匹配的医学关键词(如疾病名称、症状等)。
如果遇到极度模糊的问题,需要通过语义解析或问句澄清,这属于额外的自然语言处理环节。作者未将其纳入主要研究范围。
16. 扩展到多语种
Q: 如果在非英文或多语种环境(如中文、法语)下应用,会不会出现推理链无法生成或生成乱码?
A: 从论文看,作者并未专门讨论多语言支持,主要依赖 T5、LLMs 等基础模型的多语言能力。
理论上,只要底层模型做了相应多语种训练,并为医学词汇做强化,对其他语言也可行;但现阶段大多数公开数据集仍以英文为主。
17. 多模态与结构化病历数据
Q: 临床诊断通常不只有图像,还有病历、化验结果等结构化数据,论文仅使用图像+自然语言问答,是否太过片面?
A: 确实如此。
作者在论文中聚焦在“医学图像问答”这一子任务,后续可以把该框架拓展到包含更多结构化数据的场景。
多专家思路也有可能整合病历表格、检验报告等,但需要在“诊断专家”阶段为结构化数据编写相应的子专家模块。
18. 使用 MoE 的可扩展性
Q: 当增加更多器官专家时,稀疏 MoE 的规模会不断扩张,门控管理是否会变得复杂,导致训练与推理难度上升?
A: 稀疏 MoE 的初衷就是要在可扩展规模和计算效率间做折衷,只激活 top-k 专家就能让大规模模型的计算量保持相对可控。
不过专家数量极度增长时,门控模块本身也会很复杂,作者承认这是后续扩展的挑战之一,可能需要分层门控或层级专家管理机制。
19. 如何避免不恰当的“平票”
Q: 如果在诊断专家阶段,MoE 选了两三位子专家,但其中一位结论截然不同,另外两位专家相似,最终结果会被简单“多数表决”压制吗?
A: 论文使用了特征加权或概率加权并非绝对多数表决,但没有明文指出是否能避免极少数专家的正确意见被否决。
作者主要在消融实验里证明了多数投票总体准确率更高。
若要避免个别先验更“专业”的专家被忽视,需要引入专家可信度评分或层级加权。
20. 当前方案是否能直接投入临床使用?
Q: 论文中展示了在公开数据集上的优异表现,但在真实医院环境下的落地会否面临伦理、安全及隐私等问题?
A: 作者明确表明这是一种研究型模型,不是直接的临床级产品。
落地需要满足隐私保护、法规审批,并与医院信息系统对接。
论文讨论更多在算法层面可行性与可解释性,并没有提供临床大规模部署的具体流程,也未对法律合规进行详尽说明。
























 393
393

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








