
来源:专知
本文约1000字,建议阅读5分钟
我们提出了一种E(3)-等变Wasserstein自编码器,并将生成模型的潜在空间分解为两个解耦的方面。
摘要
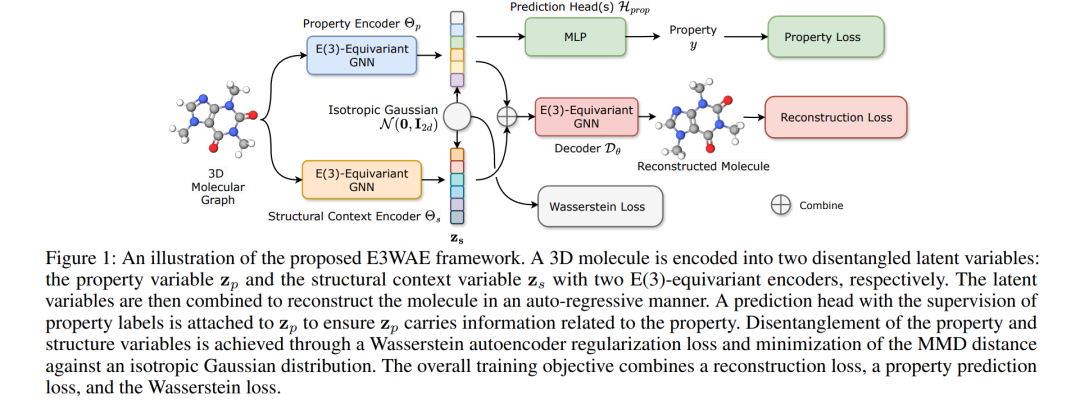
我们考虑条件生成具有显式控制分子属性(如药物相似性(例如药物相似度的定量估计或合成可及性评分)和与特定蛋白质位点有效结合)的三维药物分子。为了解决这个问题,我们提出了一种E(3)-等变Wasserstein自编码器,并将生成模型的潜在空间分解为两个解耦的方面:分子属性和三维分子的其余结构上下文。我们的模型确保对这些分子属性进行显式控制,同时保持坐标表示的等变性和数据似然的不可变性。此外,我们引入了一种新颖的基于对齐的坐标损失,以适应等变网络用于自回归从零开始生成三维分子。大量实验验证了我们模型在基于属性引导和基于上下文引导的分子生成中的有效性,包括从零开始的三维分子设计和针对蛋白质靶标的基于结构的药物发现。
关于我们
数据派THU作为数据科学类公众号,背靠清华大学大数据研究中心,分享前沿数据科学与大数据技术创新研究动态、持续传播数据科学知识,努力建设数据人才聚集平台、打造中国大数据最强集团军。

新浪微博:@数据派THU
微信视频号:数据派THU
今日头条:数据派THU























 393
393

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








