Introduction
在宏基因组学研究中,准确地将组装后的基因组片段(contigs)归属到各自的微生物基因组中,是解析微生物群落功能和生态关系的关键步骤。然而,很多分箱(binning)方法在面对复杂的微生物群落时,常常难以重建出高质量的基因组,且不同工具在不同样本和生态环境中的表现差异显著。
为了解决这一问题,研究人员开发了DAS Tool(Dereplication, Aggregation and Scoring Tool),这是一种自动化的方法,能够整合多个已有的分箱算法的结果,生成优化的、非冗余的高质量基因组集合。在多个复杂环境样本中,DAS Tool展示了比任何单一分箱工具更强的能力,能够恢复更多接近完整的基因组,包括一些之前未被发现的谱系。本文将介绍使用DAS Tool优化宏基因组分箱结果,提升基因组重建的质量和数量。

DAS Tool的文章于2018年发表于Nature Microbiology,软件主页:https://github.com/cmks/DAS_Tool,logo也很有意思。
工作流程
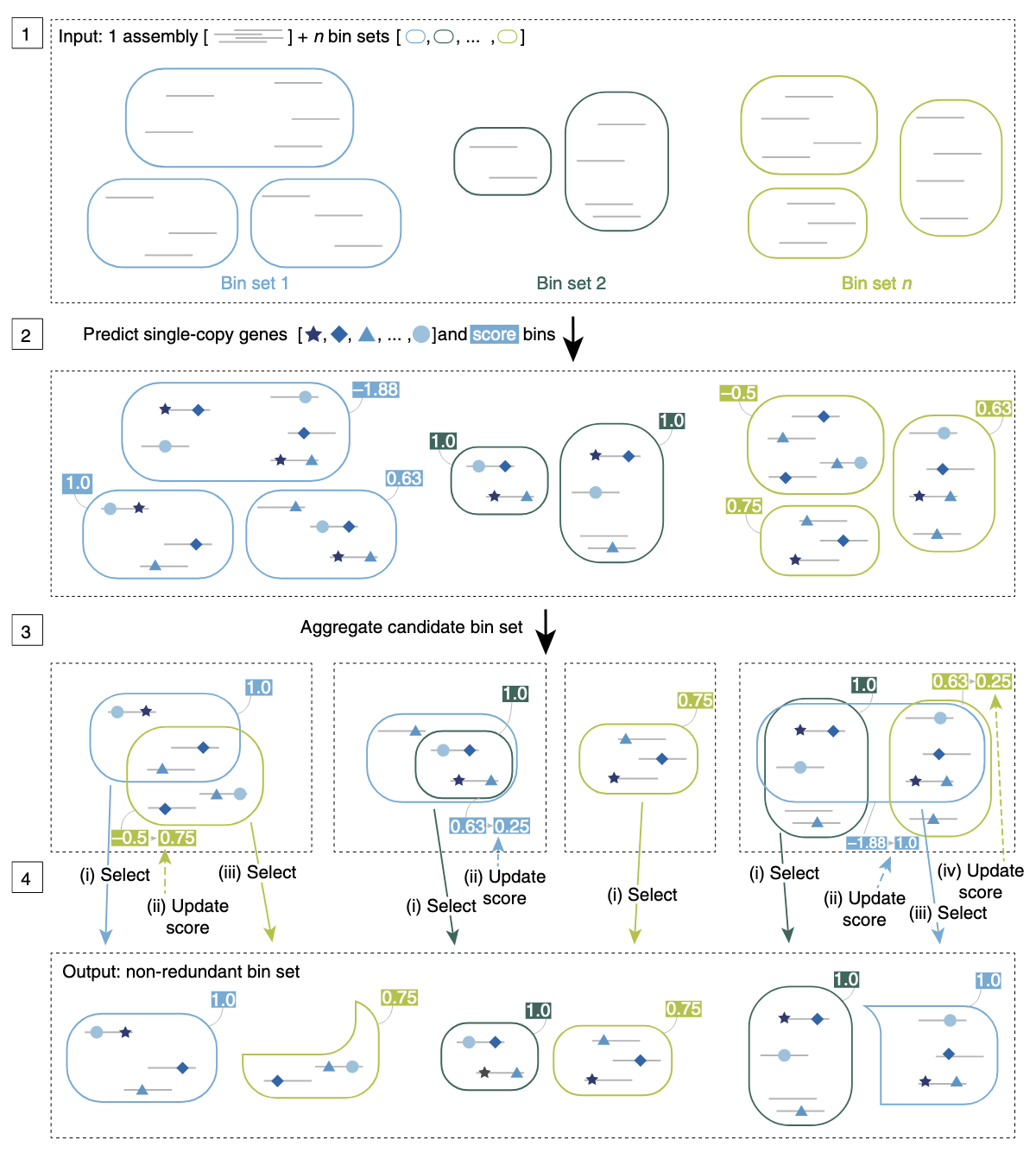
Step 1|整合多种分箱结果
DAS Tool 的输入包括:一个宏基因组组装(scaffolds)和来自不同 binning 工具的多个 bin 结果(每种颜色表示一个工具的输出)。这些分箱工具可能依据不同特征(如 GC 含量、k-mer 频率或丰度信息)进行聚类。
Step 2|识别单拷贝基因并打分
DAS Tool 会在 scaffolds 上预测单拷贝标志基因(single-copy marker genes),并以此对每个 bin 进行质量打分(例如完整度和污染度),用于后续筛选。
Step 3|合并候选 bin 并去除冗余
来自不同工具的 bin 可能存在重叠。DAS Tool 会将这些候选 bin 进行去冗余整合,构建一个统一的候选 bin 集合。
Step 4|迭代优化与筛选
DAS Tool 通过迭代方式从所有候选 bin 中优先选择得分最高的,并在每轮迭代中更新剩余 bin 的得分(考虑重复和覆盖情况),最终输出一个非冗余、高质量的 bin 集合。
这个流程的关键在于:充分融合多个 binning 工具的优点,利用标志基因和打分机制,自动筛选出最优的 bin 组合,有效提升基因组重建的质量和覆盖范围。
效果评估
DAS Tool在模拟微生物群落中的表现验证
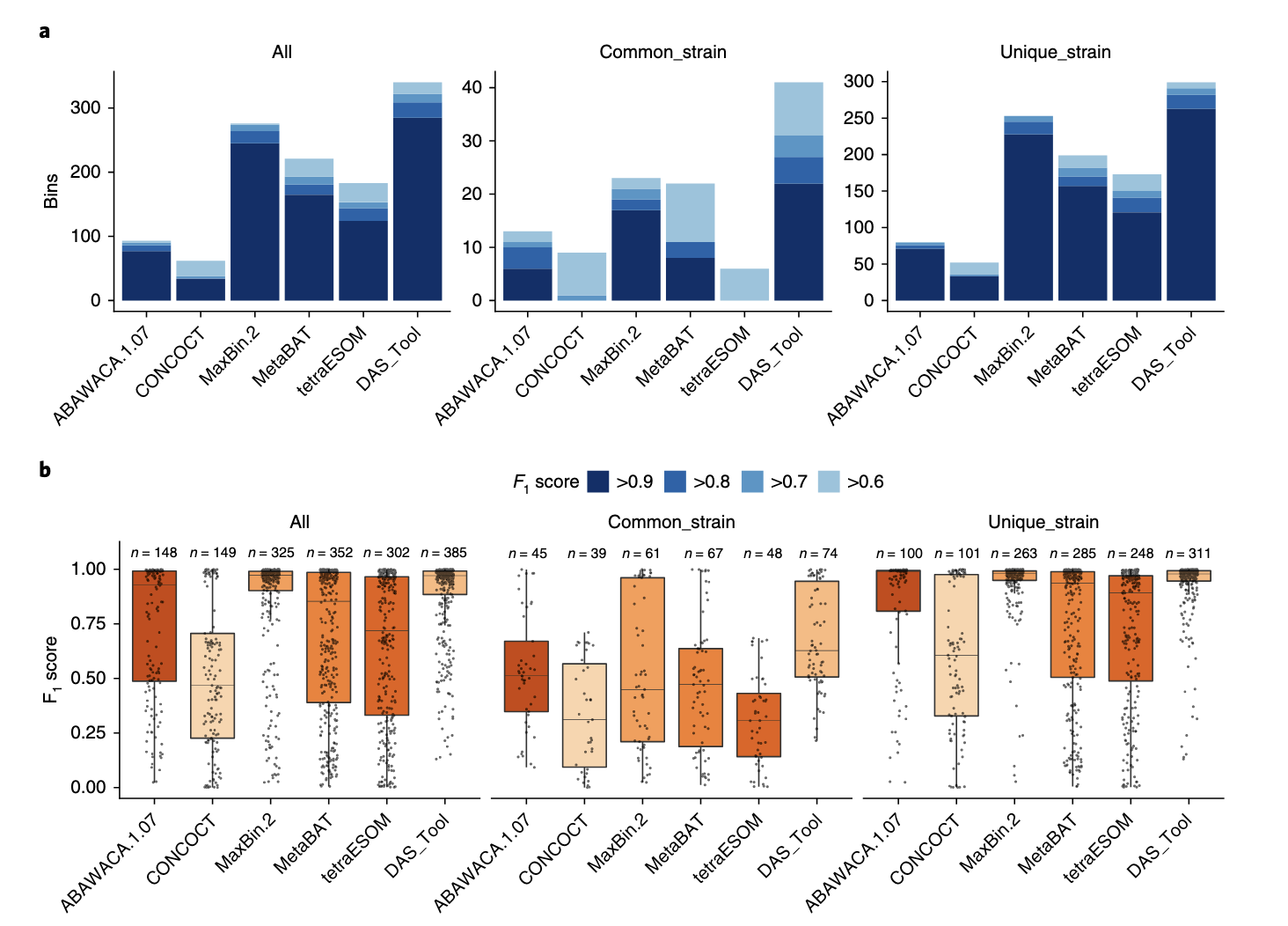
为了验证 DAS Tool 的效果,研究者将其应用于 CAMI challenge 提供的三种复杂度不同的模拟微生物群落数据集(包含 40、132 和 596 个基因组)。使用五种主流 binning 工具(ABAWACA、CONCOCT、MaxBin 2、MetaBAT、ESOM)分别预测分箱,并用 DAS Tool 进行整合优化。
在高复杂度(596 个基因组)数据集中,DAS Tool 重建的高质量基因组数量(F1 分数 > 0.6)显著高于任何单一工具:
- DAS Tool: 共识菌株 41 个、唯一菌株 299 个
- 次优 MaxBin 2: 共识菌株 23 个、唯一菌株 253 个
- ESOM: 虽对唯一菌株效果尚可(173 个),但对存在菌株变异的基因组恢复能力较差(仅 6 个)
此外,DAS Tool 重建的基因组 F1 分数中位数也优于其它工具,尤其在处理菌株变异时展现出更强的能力。不仅在高复杂度样本中表现优越,在中低复杂度数据集上也优于单一方法。
DAS Tool在真实环境样本中的应用
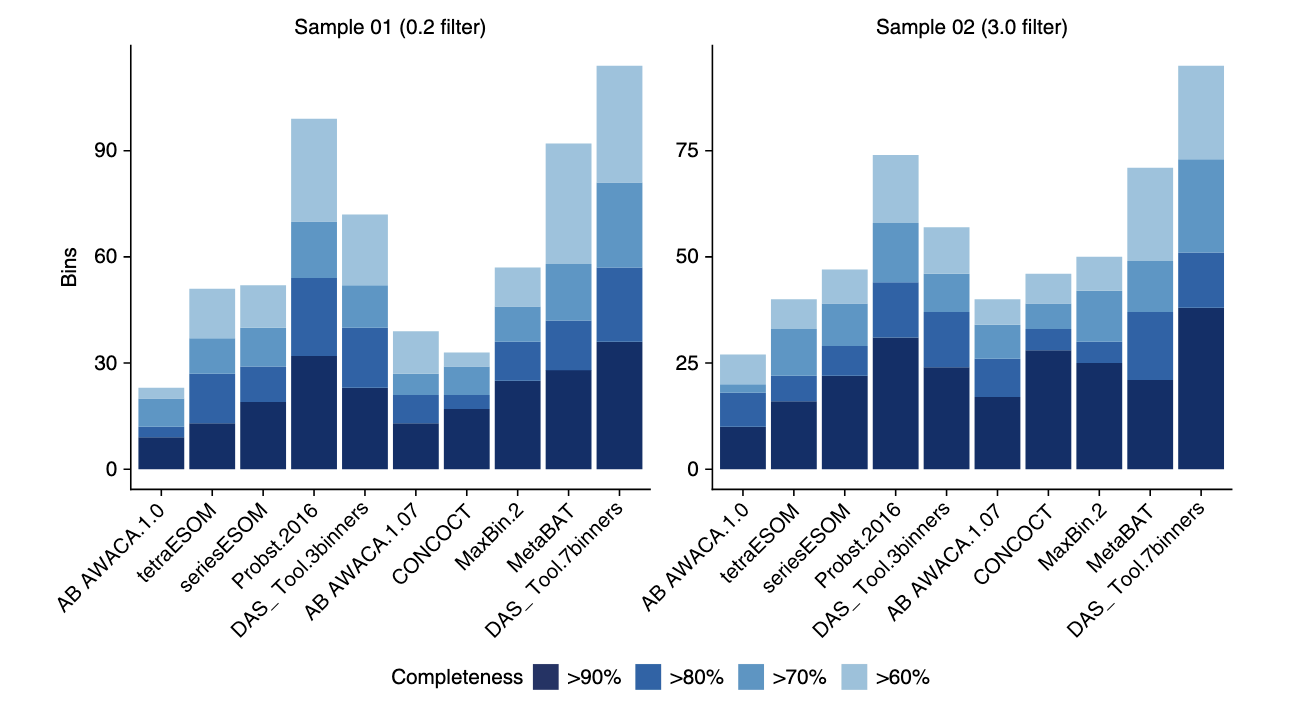
Probst 等人曾从高 CO₂ 冷泉系统中构建了一个经过精细人工筛选的基因组分箱集,成为评估 DAS Tool 表现的理想样本。这些数据来自对不同滤膜(3.0 μm 与 0.2 μm)过滤后的样品进行组装,并采用三种 binning 方法 + 人工校正获得结果。
研究者对原始发表的 bins 及不同 binning 工具(ABAWACA 1.0/1.07、ESOM、CONCOCT、MetaBAT、MaxBin 2)与 DAS Tool 的整合结果进行了对比评估。质量评估采用 CheckM,高质量定义为 >90% 完整度且污染率 <5%。
主要发现如下:
- 使用3种工具整合的 DAS Tool 已超过任一单一方法的效果,但略低于人工精修结果。
- 使用7种工具整合的 DAS Tool 成果优于原始发表结果:
- 0.2 μm 样本: DAS Tool 重建 36 个近全基因组,高于原始的 32 个;
- 3.0 μm 样本: DAS Tool 重建 38 个,高于原始的 31 个;
- 草稿级基因组数量也全面提升。
- 当适度放宽污染率阈值时,草稿基因组数量进一步增加。
在真实环境样本中,DAS Tool 同样展现出强大整合能力,尤其当结合更多 binning 工具时,不仅能提高高质量基因组的数量,也能有效替代部分人工精修过程。
使用方法
安装
1. 最简单的安装方式:使用 conda
conda config --add channels defaults
conda config --add channels bioconda
conda config --add channels conda-forge
conda install -c bioconda das_tool
但我发现conda安装好了之后也需要下载github主页的db.zip文件并解压,后续运行需指定db目录,不然默认用当前目录下的db:
# 下载并解压缩DASTool.zip存档:
unzip DAS_Tool-1.x.x.zip
cd ./DAS_Tool-1.x.x
# Unzip SCG database:
unzip ./db.zip -d db
2. 手动安装(需满足以下依赖项)
- R (>= 3.2.3):https://www.r-project.org
- R 包:
data.table(>= 1.9.6)magrittr(>= 2.0.1)docopt(>= 0.7.1)
- ruby (>= 2.3.1):https://www.ruby-lang.org
- Pullseq (>= 1.0.2):https://github.com/bcthomas/pullseq
- Prodigal (>= 2.6.3):https://github.com/hyattpd/Prodigal
- coreutils(仅 macOS 需要):https://www.gnu.org/software/coreutils
- 以下三种搜索引擎之一:
- DIAMOND (>= 0.9.14):推荐,用于大数据集:https://ab.inf.uni-tuebingen.de/software/diamond
- BLAST+ (>= 2.5.0):https://blast.ncbi.nlm.nih.gov/Blast.cgi
- USEARCH (>= 8.1):http://www.drive5.com/usearch/download.html
注意:USEARCH 免费版仅支持最多 4GB 内存,因此推荐使用 DIAMOND 或 BLAST+。
# 下载并解压缩DASTool.zip存档:
unzip DAS_Tool-1.x.x.zip
cd ./DAS_Tool-1.x.x
# Unzip SCG database:
unzip ./db.zip -d db
# Run DAS Tool:
./DAS_Tool -h
$ R
> repo='http://cran.us.r-project.org' #select a repository
> install.packages('data.table', repos=repo, dependencies = T)
> install.packages('magrittr', repos=repo, dependencies = T)
> install.packages('docopt', repos=repo, dependencies = T)
> q() #quit R-session
3. 使用 Docker
cd ./DAS_Tool-1.x.x
docker build -t cmks/das_tool .
参数说明
安装完成后,可以通过 DAS_Tool -h 查看可用参数:
DAS_Tool [选项] -i <contig2bin> -c <contigs_fasta> -o <输出前缀>
主要参数:
-i, --bins=<contig2bin> 多个 contig-to-bin 表格文件(以逗号分隔)
-c, --contigs=<contigs> 组装后的 contig(FASTA 格式)
-o, --outputbasename=<前缀> 输出文件名前缀
-l, --labels=<标签> 每个 binning 工具的名称(以逗号分隔)
--search_engine=<搜索工具> 用于识别单拷贝基因的搜索工具(diamond/blastp/usearch)[默认:diamond]
-p, --proteins=<蛋白文件> 预测蛋白(可选),跳过基因预测步骤(FASTA 格式)
--write_bin_evals 输出原始 bin 评估结果
--write_bins 输出最终整合的 bin(FASTA)
--write_unbinned 输出未归类的 contigs
-t, --threads=<线程数> 并行线程数 [默认:1]
--score_threshold=<阈值> bin 筛选的得分阈值(0~1)[默认:0.5]
--duplicate_penalty=<重复惩罚> 单拷贝基因重复的惩罚因子(0~3)[默认:0.6]
--megabin_penalty=<megabin惩罚> 超大 bin 的惩罚因子(0~3)[默认:0.5]
--dbDirectory=<数据库路径> 单拷贝基因数据库路径 [默认:db]
--resume 使用之前预测过的单拷贝基因结果
--debug 输出调试信息
-v, --version 查看版本
-h, --help 查看帮助
输入文件准备
1. 多个 binning 工具的输出 [--bins, -i]
每个 binning 工具生成的 contig-to-bin 表格,TSV 格式:
Contig_1 bin.01
Contig_8 bin.01
Contig_42 bin.02
Contig_49 bin.03
不是所有 binning 工具都直接生成此格式。可使用官方提供的脚本
Fasta_to_Contigs2Bin.sh进行转换,在github主页上:
# 示例:将 MaxBin 输出 fasta 文件转为 contigs2bin 表格
~/biosoft/DAS_Tool/src/Fasta_to_Contig2Bin.sh -i /maxbin/output/folder -e fa > maxbin.contigs2bin.tsv
某些工具如 CONCOCT 输出为 CSV,可用 perl 一行命令转为 TSV:
perl -pe "s/,/\tconcoct./g;" concoct_clustering_gt1000.csv > concoct.contigs2bin.tsv
2. 组装后的 contig 文件 [--contigs, -c]
FASTA 格式,如:
>Contig_1
ATCATCGTCCGCATCGACGAATTCGGCGAACGAGTACCCCTGACCATCTCCGATTA...
>Contig_2
GATCGTCACGCAGGCTATCGGAGCCTCGACCCGCAAGCTCTGCGCCTTGGAGCAGG...
3. 可选:预测蛋白序列 [--proteins]
若已有 prodigal 预测结果(.faa 格式),可跳过基因预测步骤。
运行 DAS Tool
基本命令格式如下:
DAS_Tool -i <binning_results.tsv> -l <binning_labels> -c <scaffolds.fasta> -o <输出前缀>
参数说明:
-i:多个 binning 工具的 contigs-to-bin TSV 文件(用逗号连接),注意逗号之间绝对不能有空格,不然会引发Docopt报错-l:与-i对应的 binning 工具名称(用逗号连接)-c:组装后 contigs 的 FASTA 文件-o:输出文件名前缀
示例:
DAS_Tool -i bins.tsv -l metabat,maxbin,concoct -c assembly.fasta -o DAS_Tool_output
输出结果
运行后将生成以下输出文件:
*_DASTool_summary.tsv:输出 bin 的质量与完整性评估汇总*_DASTool_contigs2bin.tsv:最终 contigs-to-bin 映射表*_allBins.eval:若启用--write_bin_evals,输出输入 bin 的评估结果DASTool_bins/:若启用--write_bins,输出整合后的 bin(FASTA 格式)
示例数据与测试
使用 GitHub 提供的 sample_data:
示例 1:使用 4 个 bin 工具结果运行 DAS Tool
DAS_Tool -t 4 -i sample_data/sample.human.gut_concoct_contigs2bin.tsv,\
sample_data/sample.human.gut_maxbin2_contigs2bin.tsv,\
sample_data/sample.human.gut_metabat_contigs2bin.tsv,\
sample_data/sample.human.gut_tetraESOM_contigs2bin.tsv \
--dbDirectory ~/db/DAS_Tool_db \
-l concoct,maxbin,metabat,tetraESOM \
-c sample_data/sample.human.gut_contigs.fa \
-o sample_output2/DASToolRun1
用了4核,对于一个32M的contig文件,用时1min,内存占用200MB。
示例 2:设置更多参数,跳过基因预测,输出评估结果,输出最终的bins,使用多线程
DAS_Tool -t 4 -i sample_data/sample.human.gut_concoct_contigs2bin.tsv,\
sample_data/sample.human.gut_maxbin2_contigs2bin.tsv,\
sample_data/sample.human.gut_metabat_contigs2bin.tsv,\
sample_data/sample.human.gut_tetraESOM_contigs2bin.tsv \
--dbDirectory ~/db/DAS_Tool_db \
-l concoct,maxbin,metabat,tetraESOM \
-c sample_data/sample.human.gut_contigs.fa \
-o sample_output2/DASToolRun2 \
--proteins sample_output2/DASToolRun1_proteins.faa \
--write_bin_evals \
--write_bins \
--score_threshold 0.6
承接MetaWRAP输出结果
MetaWRAP是我们之前介绍过的一个binning流程工具,假如我们一开始已经用MetaWRAP进行了3种工具的binning,现在我们想用DAS_Tool来进行进一步的优化,那么可以用如下命令:
i=KY01867_1_T006D
metawrap binning -o l -t 2 -m 4 -a contigs/contigs_${i}.fasta \
--metabat2 --maxbin2 --concoct reads/${i}*.fastq
那么在INITIAL_BINNING_${i}文件夹下会有如下文件夹:
INITIAL_BINNING_KY01867_1_T006D/
├── concoct_bins
├── maxbin2_bins
├── metabat2_bins
└── work_files
我们使用DAS_Tool进行整合:
mkdir DAS_Tool_${i}
#整理list
mkdir tmp/
rm tmp/*
find INITIAL_BINNING_${i}/metabat2_bins/ -type f -name "bin.[0-9].fa" -exec cp {} tmp/ \;
~/biosoft/DAS_Tool/src/Fasta_to_Contig2Bin.sh -i tmp/ -e fa > DAS_Tool_${i}/metabat_contigs2bin.tsv
~/biosoft/DAS_Tool/src/Fasta_to_Contig2Bin.sh -i INITIAL_BINNING_${i}/maxbin2_bins/ -e fa > DAS_Tool_${i}/maxbin_contigs2bin.tsv
rm tmp/*
cp INITIAL_BINNING_${i}/concoct_bins/bin.*.fa tmp/
~/biosoft/DAS_Tool/src/Fasta_to_Contig2Bin.sh -i tmp/ -e fa > DAS_Tool_${i}/concoct_contigs2bin.tsv
#运行DAS_Tool
DAS_Tool -t 4 -i DAS_Tool_${i}/concoct_contigs2bin.tsv,\
DAS_Tool_${i}/maxbin_contigs2bin.tsv,\
DAS_Tool_${i}/metabat_contigs2bin.tsv \
--dbDirectory ~/db/DAS_Tool_db \
-l concoct,maxbin,metabat \
-c INITIAL_BINNING_${i}/work_files/assembly.fa \
-o DAS_Tool_${i}/DASToolRun2 \
--write_bin_evals \
--write_bins
References
- Sieber, C.M.K., Probst, A.J., Sharrar, A. et al. Recovery of genomes from metagenomes via a dereplication, aggregation and scoring strategy. Nat Microbiol 3, 836–843 (2018). https://doi.org/10.1038/s41564-018-0171-1

关注公众号 ‘bio llbug’,获取最新推送。
























 1027
1027

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








