最初,GAN在被提出时,是一个无监督(无条件)的生成框架:例如在图像合成中,将随机噪声映射到逼真的目标图像。
后来CGAN即条件GAN,输入加入了标签(或者图像特征)等先验信息而不是仅靠噪声来生成,GAN此时可视为有监督(条件)的生成框架。
两种框架已经以各种方式、用于合成某些类型的医学图像。
无条件GAN的图像生成
最近在使用GAN的无监督医学图像生成领域中出现了大量工作,这可以解决诸如数据稀缺和类不平衡之类的问题(Frid-Adar,2018),并有助于了解数据分布的性质及其潜在结构。
现有的工作表明,DCGAN可用于合成逼真的前列腺病变斑块(Kitchen和Seah,2017年),视网膜图像(Schlegl,2017)或肺癌结节(Chuquicusma,2018)。合成的肺癌结节和真实的相比,甚至对放射科医生而言,都难以区分。

Frid-Adar(2018)也使用DCGAN合成肝脏CT不同类别的病变斑块:对于每个类别,即囊肿,转移灶和血管瘤,训练独立的生成模型。出于训练数据集太小,他们使用大量增强的数据来训练GAN。作者证明了除了数据增强外,GAN的合成样本还能改善CNN分类器。
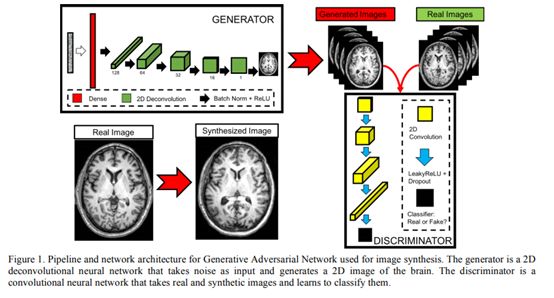
Bermudez(2018)也显示DCGAN也能够生成相当高分辨率的MR数据,甚至只需要少量样品即可。在训练了1500个epoch之后,作者的实验获得了很棒的生成效果(人眼无法判断真假图像)。
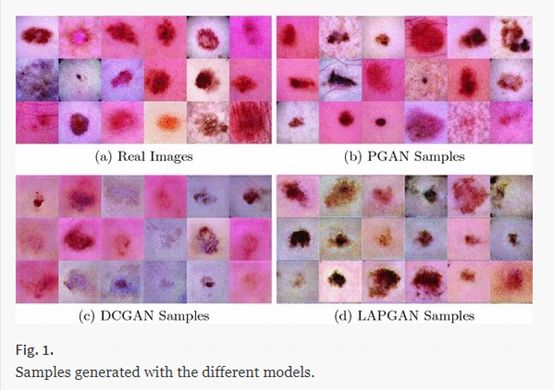
Baur (2018b)比较了DCGAN,LAPGAN对皮肤病变图像合成的影响。由于训练数据方差很大,因此样本数量很少不足以训练出可靠的DCGAN。但是,级联式的LAPGAN和它的变体变现很好,合成样品有也成功地用于训练皮肤病变分类器。Baur(2018a)采用渐进式PGAN(Karras 2017)合成皮肤病变的高分辨率图像,效果极佳,连专业的皮肤科医生都无法地分辨是不是合成的。
条件GAN的图像生成
1. 由MR图像生成CT
许多临床环境中要获取CT图像,但CT成像使患者处于细胞损伤和癌症的放射线风险中。这促使我们尝试通过MR合成CT图像。Nie(2017)利用级联的3D全卷积网络从相应的MR图像合成CT图像。为提高合成CT图像的真实性,除对抗性训练外,他们还通过逐像素重建损失和图像梯度损失训练模型。Nie(2017)要求使用CT和MR图像一一对应的数据集进行训练。
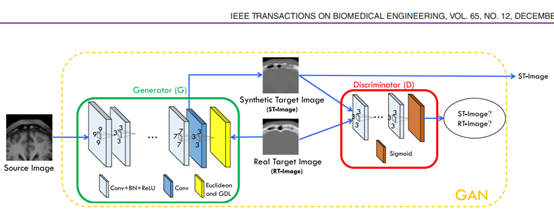
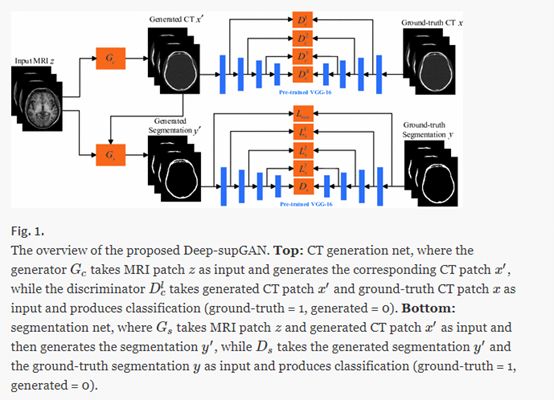
Wolterink(2017a)用cycleGAN将2D MR图像转换为CT图像,而无需匹配的图像对训练。而且由于成对训练数据集并不是完美的匹配的,他们的训练不受此影响,甚至带来了更好的结果。Zhao(2018a)的Deep-supGAN将头部的3D MR数据映射到其CT图像,以促进颅颌面骨结构的分割。为获得更好的转换结果,他们提出了“deep-supervision discriminator(深度监督鉴别器)”,类似于“perceptual loss”,利用预训练的VGG16模型提取的特征表示来区分真实和合成的CT图像和提供梯度更新给生成器。
2. 由CT图像生成MR
与(Wolterink,2017a)类似,Chartsias(2017)将cycleGANs用于未配对的图像到图像转换,从“心脏CT切片和分割图像”生成“心脏MR图像和分割mask”。作者表明,当使用合成数据对模型进行额外训练时,分割模型的性能可提高16%;使用合成数据训练的模型,与用真实数据训练的模型相比,仅差5%。
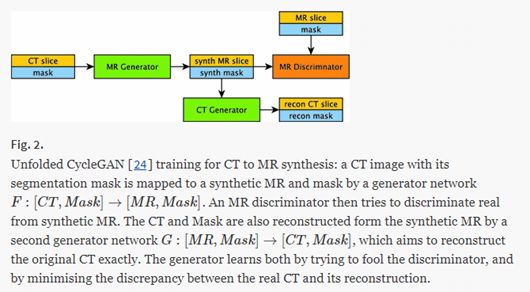
Cohen(2018)指出,在图像到图像转换时难以保留肿瘤/病变部分的特征。为此,Jiang(2018)提出了一种针对cycleGAN的“肿瘤感知”损失函数,以更好地从CT图像合成MR图像。
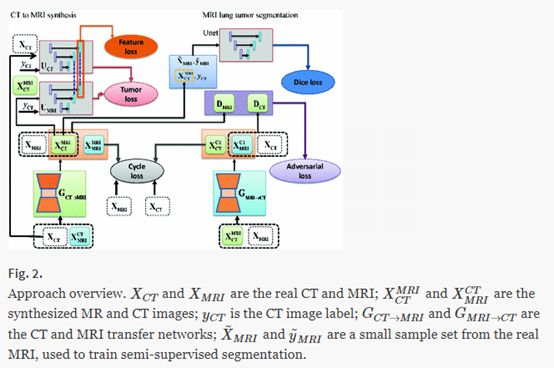
3. 生成Retinal Image 视网膜图像
Costa(2017a)基于Pix2Pix稍加修改,从vessel tree二值图像生成高分辨率eye fundus图像。
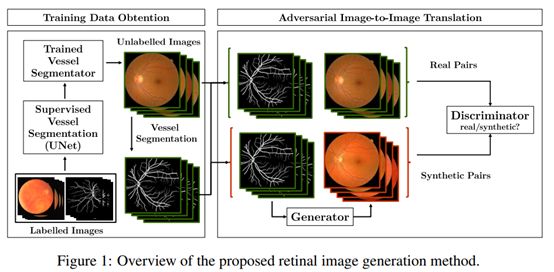
在后续工作中,Costa (2017b)进一步介绍了一种对抗性自动编码器(AAE),它经过训练可将血管树vessel tree图像压缩为多元正态分布,并可以连续重建它们。所得模型通过从多元正态分布中采样来合成任意高分辨率vessel tree图像。合成的vessel tree图像又可以输入到图像到图像的转换模型中,从而形成用于高分辨率视网膜图像合成的端到端框架。
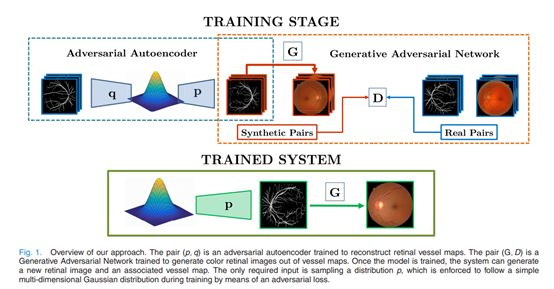
类似地,Guibas (2017)提出了一种两阶段方法,包括经过训练可从噪声中合成vessel tree图像的GAN和Pix2Pix网络,以生成现实的高分辨率血管分割图像和相应的eye fundus图。作者发现使用实际图像训练的U-Net进行分割,和仅用合成样本相比,后者稍差而已。
4. 从CT图像合成PET图像
PET图像经常用于肿瘤学的诊断和分期,PET和解剖CT图像的组合采集是临床常规操作中的标准程序。但是PET设备昂贵并且涉及放射性。因此,医学影像分析界一直致力于直接从CT数据合成PET图像。
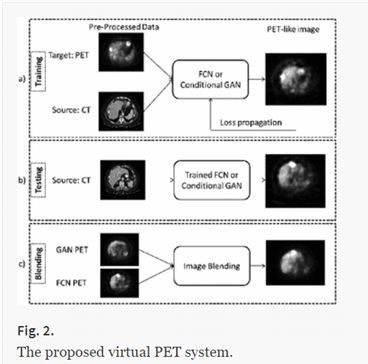
Ben-Cohen(2017)用条件GAN从CT数据合成肝脏PET图像,但其性能在“underrepresented”的肿瘤区域中表现较差。相比之下,FCN网络能够合成肿瘤,但通常会产生模糊的图像。通过混合来自条件GAN和FCN的相应合成PET图像,它们可以实现很高的肿瘤检测性能。
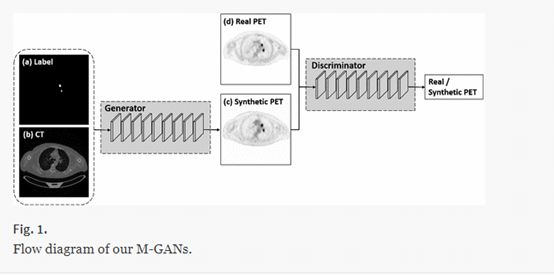
同样,Bi(2017)从成对的CT图像和二进制标签图合成高分辨率的PET图像。作者强调添加标签label图会带来全局更真实的合成效果,并在合成数据上训练的肿瘤检测模型验证了他们的合成PET图像,获得了与在真实数据上训练的模型媲美的结果。他们认为当标记数据稀缺时,合成数据是有益的。
5. 从 MRI图像合成PET图像
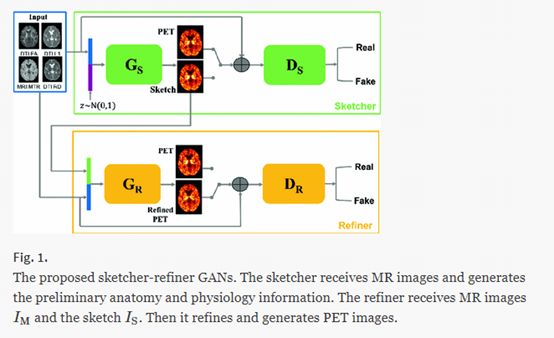
测量人脑PET图像中的髓磷脂含量对于监测疾病进展、了解生理病理学和评估多发性硬化症(MS)的治疗非常重要。但是用于MS的PET成像既昂贵又需要注射放射性示踪剂。Wei(2018)用两个条件GAN的级联,基于3D U-Net的生成器和3D CNN的鉴别器,从MR合成PET图像。作者认为,单cGAN会产生模糊的图像。将综合任务分解为更小更稳定的子问题可以改善结果。
6. 生成超声图像
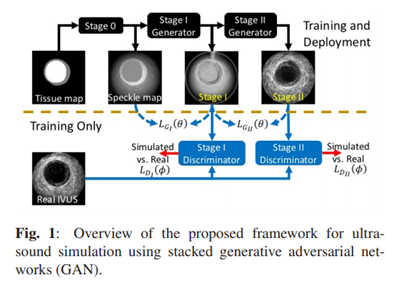
超声图像合成模拟。如论文《Freehand Ultrasound Image Simulation with Spatially-Conditioned Generative Adversarial Networks》、《SIMULATING PATHO-REALISTIC ULTRASOUND IMAGES USING DEEP GENERATIVE NETWORKS WITH ADVERSARIAL LEARNING》
7. 生成X射线图像
Mahapatra(2018)训练cGAN结合扰动的分割图进行胸部X射线合成,结合贝叶斯神经网络进行主动学习。
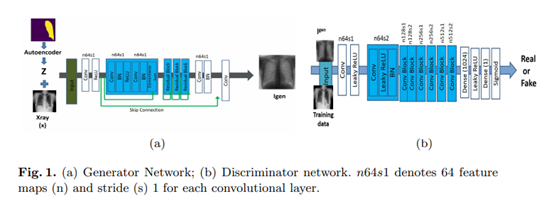
8. 染色归一化
由于制片染色流程以及病理扫描仪的不同,数字病理图像的色彩存在非常显著的差异,这会影响CAD系统。Cho (2017)指出,肿瘤分类器不仅在具有不同染色的数据之间泛化不佳,而且现有的染色归一化方法无法保留重要的图像特征。为此,他们提出了一种“feature-preserving”的cGAN用于染色风格转移:先将组织病理学图像映射到规范的灰度表示,再用cGAN将这些灰度图像转换为具有所需染色的RGB图像。
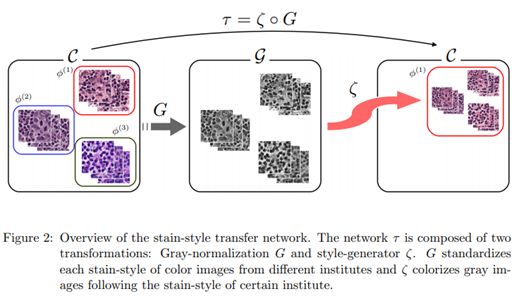
Bentaieb和Hamarneh(2018)尝试通过同时训练条件GAN和特定任务网络(分割或分类模型)来解决染色问题。生成器,鉴别器和特定任务网络的联合优化,可以驱动生成器生成具有为特定任务模型保留相关特征的图像。
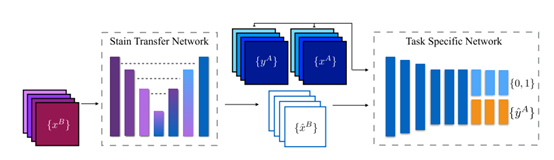
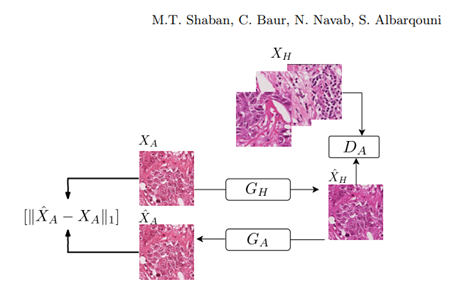
前面提到的方法依赖于成对的训练数据(从源到目标染色),这样的数据集通常很难获得,并且需要诸如配准之类的预处理。Shaban (2018)通过使用cycleGANs进行这个问题。
9. 生成Microscopy图像
Han和Yin(2017)提出了一种类似于Pix2Pix的框架,用于将显微镜图像中的DIC类型和PC类型转换。

10. 生成Blood Vessels 血管图像
对于检测冠状动脉CT血管造影术(CCTA)中的动脉粥样硬化斑块或狭窄,机器学习驱动的方法通常需要大量数据。为解决缺少标记数据的问题,Wolterink(2018)基于WGAN生成合理的3D血管形状图像。Olut(2018)提出steerable GAN合成MRA(磁共振血管成像)图像。
结语
针对无条件和有条件的图像生成,已有许多基于GAN的方法。但这些方法的有效性如何?目前仍然缺乏一种有意义的、通用的量化手段来判断合成图像的真实性。尽管如此,上述工作表明,GAN似乎可成功地用于分类和分割任务中的数据模拟和扩充。








 文章概述了GAN在医学图像生成中的发展,从最初的无条件生成到条件GAN的引入,以及在解决数据稀缺和提高模型性能方面的应用。特别关注了DCGAN在前列腺病变、视网膜图像和肺癌结节生成中的效果。同时,文章指出了评估GAN生成图像真实性的挑战。
文章概述了GAN在医学图像生成中的发展,从最初的无条件生成到条件GAN的引入,以及在解决数据稀缺和提高模型性能方面的应用。特别关注了DCGAN在前列腺病变、视网膜图像和肺癌结节生成中的效果。同时,文章指出了评估GAN生成图像真实性的挑战。
















 1140
1140

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








