1. 烯烃和卤化氢加成
-
两步基元反应
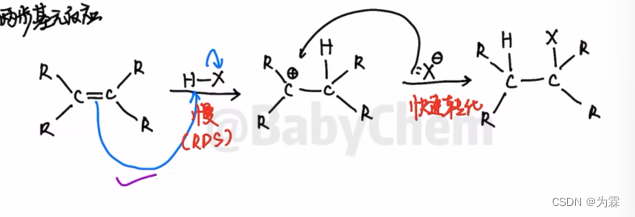
-
烯烃是亲核试剂
2. 烷烃与自由基反应
- 烷烃的分类
- 链烷烃 CnH2n+2
- 物性规律
- 熔点:Mr越大,排列越整齐,作用力越大;单少双多;
- 沸点:Mr越大,bp越大
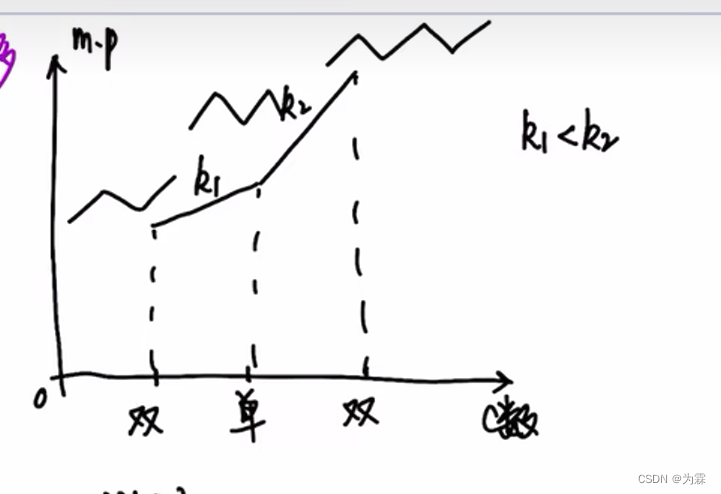
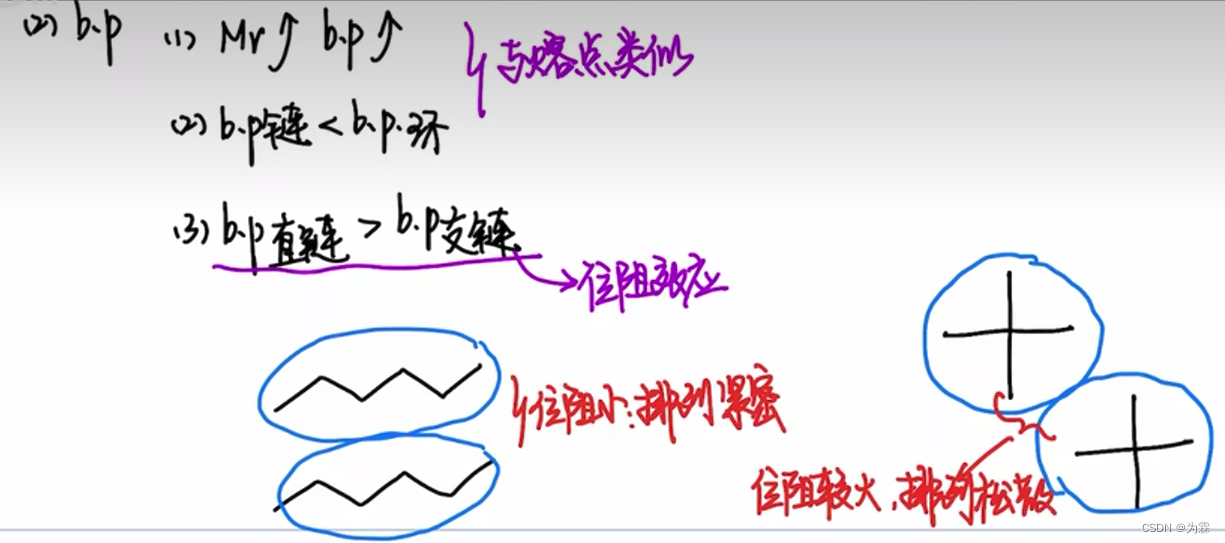
3. 热动力学
反应热力学:恒温恒压下,反应的自发过程会朝着G减小的方向过程
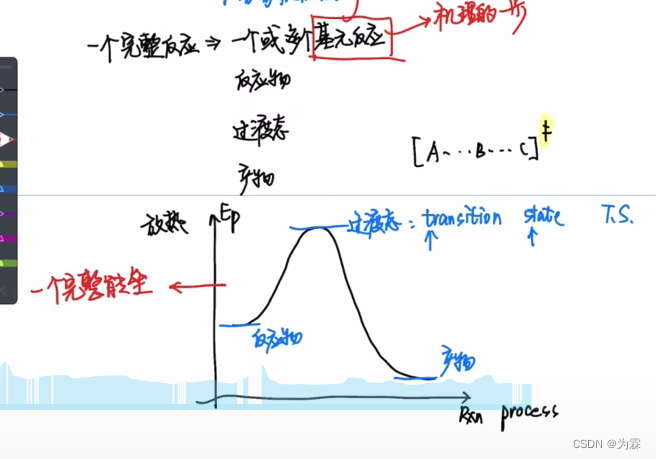
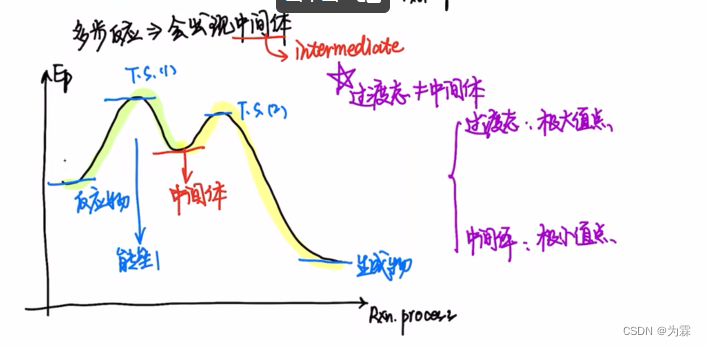

多步反应区去研究哪一步?
多个基元反应,最慢的一步往往决定整个反应的进行程度,也就是决速步
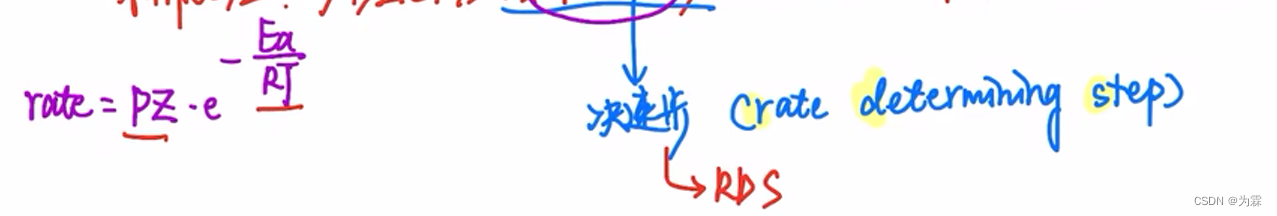
- 哈蒙德假说→判断TS结构 与TS能量接近的一方则过渡态更像哪一方
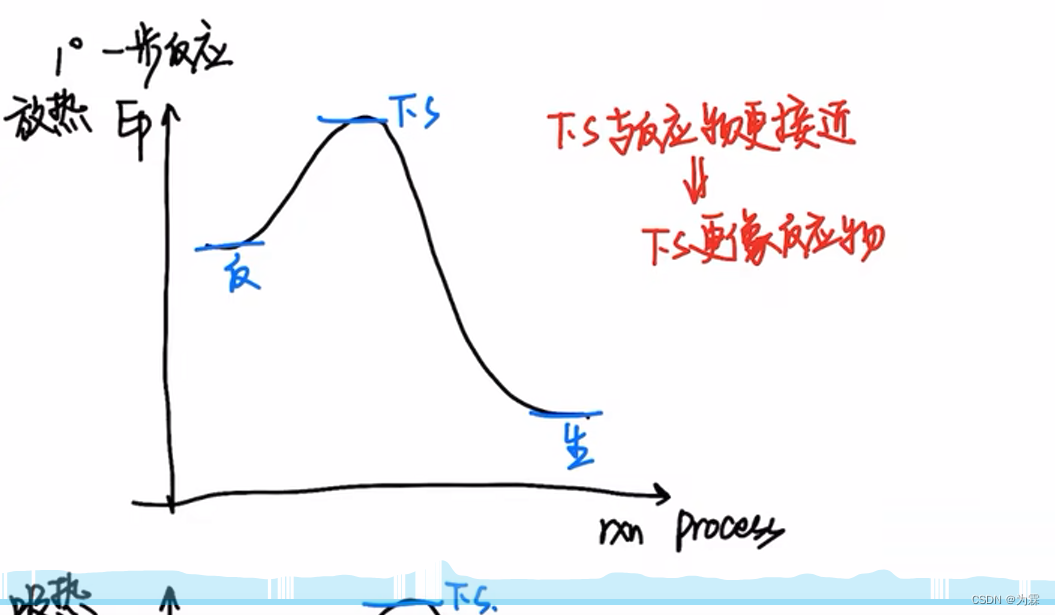
一步反应TS结构和热效应有关;多步反应,过渡态会像中间体
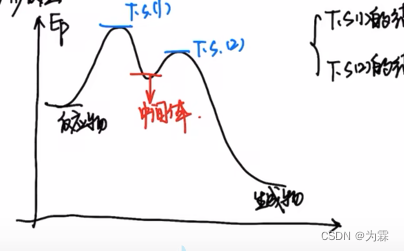
- 自由基反应
- 均裂和异裂




5. 自由基反应机理
-
如何判断自由基中间体稳定性?
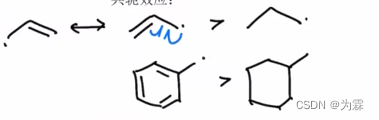
- 超共轭效应(3°C>2°C>1°C):取代基越多的自由基越稳定;
- 共轭效应:烯丙基会更稳定,π电子会形成离域;
苄基自由基>纯环的自由基;- 芳香性:苯环自由基非常不稳定
-
自由基反应机理:
- 链引发:氯气会解离变成氯自由基
- 链转移(决速步骤):氯自由基和甲烷反应生成甲基自由基;不断撞击形成新的自由基
- 链终止:自由基和自由基反应
-
热力学产物和动力学产物分析
- 分清几类物质:反应物;过渡态;中间体;产物
- 如上一个反应中,甲基自由基是中间体
-
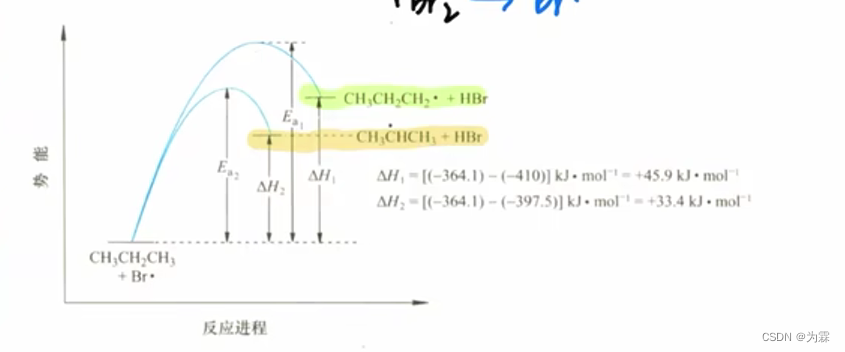
高级烷烃的溴化:只考虑一步链转移
-
看热力学:焓变驱动反应(自由基里假设熵变不变),根据反应物和产物的焓变,判断反应的平衡常数,也就是反应的程度
-
看动力学:速率 阿伦你死公式:根据过渡态和反应物的能垒,判断反应速率

-
两种路径抉择
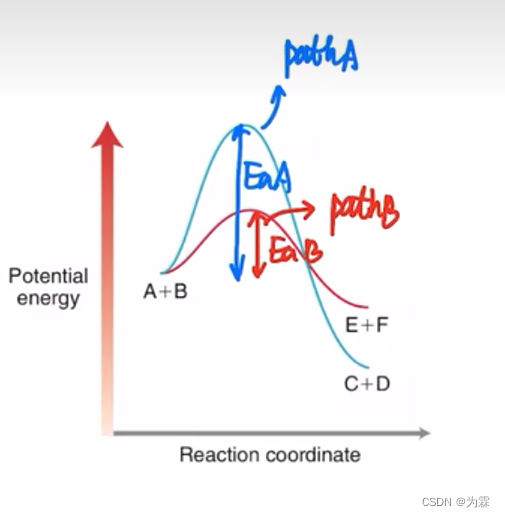
path A: 优势在于C+D的能量低,焓变小(热力学产物)
path B: 优势在于Ea小,(动力学产物 -
不同反应条件要选择不同路径:如果要达到热力学产物,将反应进行到底:时间长;热力学产物生成往往有较高能垒,需要能量高,需要高温;
-
动力学产物:能垒低,速度快,反应时间短,需要低温
高温趋向生成热力学,低温趋向生成动力学问题
























 2473
2473

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








