小罗碎碎念
癌症免疫治疗领域正面临重大挑战,虽免疫疗法革新了部分癌症患者的生存状况,但缺乏有效生物标志物来区分治疗响应者与非响应者、预测毒性和指导治疗选择。
现有研究存在诸多局限,像传统单生物标志物方法受肿瘤微环境和宿主因素影响难以预测疗效,临床数据集缺乏标准化,多组学数据与临床、组织学和影像学数据整合不足等,这严重阻碍了免疫治疗的精准化发展。
在此背景下,名为MANIFEST的多组学平台应运而生。

该平台采用新颖且可扩展的方法,结合AI和机器学习技术,对接受免疫治疗的患者进行深度剖析。通过整合肿瘤分子分析、循环生物标志物检测、原位分析等多模态数据,挖掘潜在生物标志物,探索免疫治疗的响应和耐药机制。
例如,利用代表性测序(RepSeq)解决肿瘤采样偏差问题,借助患者来源的肿瘤片段(PDTFs)构建临床前模型评估治疗效果。
MANIFEST平台的成果对医学AI研究意义重大。其多组学数据和分析结果能为AI模型训练提供丰富素材,助力开发更精准的免疫治疗预测模型。而且,平台在数据整合、模型构建和解释性方面的创新实践,为医学AI研究提供了新思路,有望推动医学AI在癌症免疫治疗领域的广泛应用,促进个性化医疗发展。
交流群
欢迎大家加入【医学AI】交流群,本群设立的初衷是提供交流平台,方便大家后续课题合作。
目前小罗全平台关注量67,000+,交流群总成员1500+,大部分来自国内外顶尖院校/医院,期待您的加入!!
由于近期入群推销人员较多,已开启入群验证,扫码添加我的联系方式,备注姓名-单位-科室/专业,即可邀您入群。
知识星球
对推文中的内容感兴趣,想深入探讨?在处理项目时遇到了问题,无人商量?加入小罗的知识星球,寻找科研道路上的伙伴吧!
一、文献概述
《MANIFEST: Multiomic Platform for Cancer Immunotherapy》由Kok Haw Jonathan Lim等人撰写。
文章介绍了MANIFEST这一用于癌症免疫治疗的多组学平台,旨在解决免疫治疗中缺乏有效生物标志物的问题,通过多组学分析和人工智能技术,实现对患者的深度剖析,为个性化免疫治疗提供支持。
研究背景
免疫治疗改善了许多癌症患者的生存结局,但缺乏能有效区分治疗应答者与无应答者、预测毒性或指导治疗选择的生物标志物。
现有研究存在诸多局限,如传统单生物标志物方法难以预测疗效,数据集缺乏标准化,多组学数据与临床数据整合不足等。
MANIFEST平台介绍
设计
MANIFEST是一项由英国生命科学办公室和医学研究委员会资助的观察性、非干预性临床研究。
由公立医院、学术机构和企业合作组成,通过示范项目,对黑色素瘤、肾癌等四种癌症进行研究,利用现有纵向样本进行平台测试,并前瞻性收集样本。
方法
采用新型可扩展方法,结合人工智能和机器学习,整合多模态数据。
通过不同层级的参与方式,实现从常规诊断到深入肿瘤特征分析,包括高维外周免疫分析、液体活检、空间成像分析等。
项目工作流程及关键技术
肿瘤分子分析
提供标准化免疫基因组数据集,探索多种生物标志物,测试复合生物标志物的预测准确性,利用新兴分子检测方法推动治疗开发。
代表性肿瘤采样
运用RepSeq和fixed - FACS技术,克服肿瘤内异质性带来的采样偏差问题,识别新抗原,评估免疫逃逸机制。
循环生物标志物
利用高分辨率光谱 cytometry等技术,开发外周免疫反应特征,探索非免疫治疗对免疫谱的影响,评估循环肿瘤DNA监测疾病和免疫谱的作用。
原位分析
使用低通量和高通量MxIF技术,结合空间转录组学和计算病理学,探索肿瘤微环境,开发计算病理学生物标志物。
PDTFs
扩大PDTF生物样本库规模,评估免疫治疗反应,探索其作为预测辅助治疗效果和非干预性生物标志物的潜力。
肠道微生物组
评估微生物组特征在不同肿瘤类型和免疫治疗中的适用性,整合微生物组数据与其他数据,推导预测性特征。
分析和深度学习
在可信研究环境中对数据进行集中管理和分析,开发单模态和多模态模型预测免疫治疗反应和毒性,利用数学模型模拟肿瘤 - 免疫相互作用。
二、引言
免疫疗法利用免疫系统治疗癌症,显著改善了许多患者的生存状况。
近十年来,免疫检查点抑制剂已成为多种癌症亚型的标准治疗方案 。
新一代免疫疗法也在不断推进,双特异性抗体和过继细胞疗法获得美国FDA批准,mRNA疫苗试验成果可观,多种细胞因子和溶瘤病毒正处于临床试验阶段。
在临床试验中,联合使用多种免疫治疗药物,或免疫治疗与化疗、靶向治疗、放疗等其他癌症疗法相结合成为趋势,数千种联合方案正在进行临床前评估 。
随着癌症治疗选择日益丰富,追求更优质的个性化医疗成为必然。
研究治疗的原发性和继发性耐药机制对明确新靶点、优化治疗组合至关重要。目前,基础、转化和临床研究都在探索这些机制,以提高患者的治疗反应率和生存率。
然而,免疫治疗仍存在诸多问题。只有少数患者能从免疫治疗中获益,且所有患者都面临严重毒性风险,全球范围内的经济毒性负担也日益加重。
更合理地使用当前和未来的高成本治疗手段迫在眉睫,开发疾病和患者特异性的生物标志物以指导治疗选择和临床决策十分必要。
现有的生物标志物几乎无法有效区分治疗应答者和无应答者、预测毒性或指导治疗选择。
传统的单一生物标志物方法因肿瘤微环境复杂和多种宿主因素影响,难以预测疗效和指导下一代免疫疗法的开发。虽然大型临床注释数据集提供了有用信息 ,但操作人员之间缺乏标准化,限制了数据的通用性。
现有数据集主要关注肿瘤DNA和RNA的批量分析,缺乏肿瘤微环境的空间数据,以及需要新鲜样本和及时处理的检测读数。
纵向数据的缺失阻碍了对治疗耐药机制和患者间及患者内固有异质性的理解,成为一大障碍。此外,组学数据与常规临床、组织学和影像学数据的整合有限,通过可穿戴技术进行的患者报告结局和监测也较为缺乏。
深度学习虽在单模态数据中应用渐广,但尚未扩展到多模态数据以开发可靠的预测特征。个性化免疫治疗的临床需求未得到满足,对卫生资源和经济产生了深远影响。
近年来,公私合作或联盟模式不断涌现,如欧洲、美国乃至全球范围内的网络,旨在解决免疫肿瘤学领域的生物学和临床未满足需求(补充表S1)。
例如,大规模适应性癌症患者队列的综合免疫分析(参考文献3)是一个由欧洲癌症研究与治疗组织和欧盟支持的大型联盟,联合学术和产业合作伙伴,对接受标准免疫治疗的结直肠癌、肺癌、头颈癌、乳腺癌和肾癌患者进行分子和空间分析,是一个潜在的生物标志物发现的丰富数据存储库。
在本研究中,我们介绍了英国范围内的联盟和平台——免疫治疗特征多组学分析以证明疗效和毒性(MANIFEST,www.manifest-io.org.uk)。该平台汇聚了癌症免疫治疗、生物标志物发现与开发以及临床试验方面的学术和产业专家。
MANIFEST利用现有和新颖的可扩展方法,对每位接受免疫治疗的患者进行深度分析,致力于实现多模态数据的整合和建模。
三、项目设计
MANIFEST被设计为一项观察性、非干预性的临床研究,由英国生命科学办公室和医学研究委员会提供资金支持。该联盟由主要的公立医院/综合癌症中心(英国国家医疗服务体系)、学术机构和大学组成,并且得到了多个行业合作伙伴在非竞争性合作模式下的前期追加投资。
为了展示MANIFEST平台的实用性,研究团队开展示范项目,最初聚焦于黑色素瘤、肾细胞癌、膀胱癌和三阴性乳腺癌这四种癌症类型。
在这些癌症的治疗中,无论是对标准免疫疗法还是新兴免疫疗法,治疗结果和毒性的预测仍是尚未满足的重大需求。具体而言,研究人员可获取3000多名患者的已有纵向样本,这些样本来自多项已报道的免疫检查点抑制剂研究,且获得了现有研究伦理委员会的批准。这些回顾性队列将对平台进行压力测试,确保检测的质量控制、一致性和性能验证。
此阶段的成果将为多模态数据整合方法设定基准,并生成第一代多模态生物标志物特征,以便在前瞻性队列中进行评估。
与此同时,研究团队将利用合作的英国国家医疗服务体系站点现有的管理和生物样本库能力,进行前瞻性的样本(血液、粪便和组织)采集与处理。采用分层方法,计划在3年内对约3000名早期和晚期疾病患者的患者及肿瘤样本进行分析。
四、方法
MANIFEST作为一个不依赖于癌症亚型的平台,运用新颖且可扩展的方法,结合人工智能(AI)和机器学习(ML)技术,对适应临床场景的多模态数据进行整合。
MANIFEST的目标是找到用于预测免疫治疗反应、耐药性以及免疫相关不良事件(irAE)的生物标志物,发现新的治疗靶点,并建立一个临床前模型生物样本库。
该平台的创新点包括新型先进的数据生成和分析方法、可扩展且快速的临床前建模平台、集中且统一的临床和多模态生物标志物数据,以及在考虑知识产权的情况下确保安全的工作流程,并且能够与其他可信研究环境实现互操作,以最大程度地获取研究成果。
借助现有的基础设施以及学术界和产业界的合作关系,MANIFEST将利用新兴技术,在整个联盟中形成交叉协作、培训和技能提升的良好氛围。
对于高通量生物标志物的发现,MANIFEST会采用标准的诊断工作流程(适用于一级参与者)。
通过二级和三级参与者的深入分析,能够进一步对肿瘤进行特征描述,其中涉及以探索为目的的技术,例如高维外周免疫分析、液体活检(对游离DNA(cfDNA)进行甲基化分析,并对细胞类型、肿瘤细胞和免疫细胞进行反卷积),以及将空间图像分析方法与分子分析(全外显子测序、批量和长读长RNA测序(RNA-seq),以及T细胞受体(TCR)和B细胞受体(BCR)测序)相结合。
对于部分选定的患者,研究人员将拓展代表性测序(RepSeq;参考文献4)的应用。RepSeq是一种新型肿瘤采样方法,能够克服实体瘤中普遍存在的采样不足偏差。同时,还会利用患者来源的肿瘤片段(PDTF;参考文献5、6)进行临床前建模,以开展药物敏感性筛选。
最后,MANIFEST会组建一支由AI和ML专家组成的团队,负责多模态数据的采集和整合工作。
五、工作流程
MANIFEST包含七个分析工作流程(见图1),可对新鲜和固定的肿瘤组织,以及纵向采集的血液和粪便样本进行全面分析。
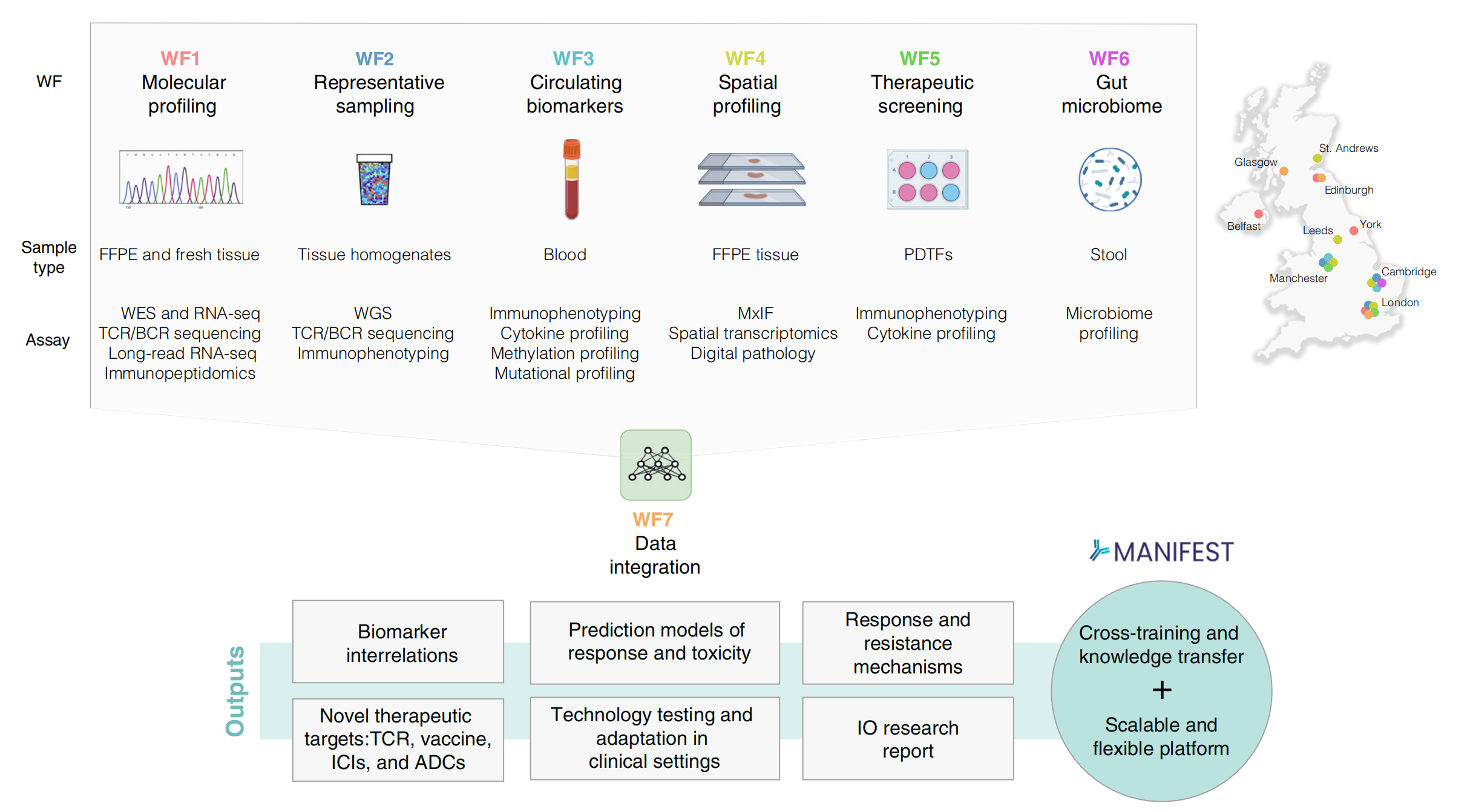
- 分子分析(WF1 - Molecular profiling)
- 样本类型:福尔马林固定石蜡包埋(FFPE)组织和新鲜组织
- 检测方法:全外显子测序(WES)、RNA测序(RNA - seq) 、T细胞受体/ B细胞受体测序(TCR/BCR sequencing) 、长读长RNA测序、免疫肽组学
- 旨在获取肿瘤分子层面信息,探索免疫治疗相关生物标志物。
- 代表性采样(WF2 - Representative sampling)
- 样本类型:组织匀浆
- 检测方法:全基因组测序(WGS) 、TCR/BCR测序、免疫表型分析
- 克服实体瘤采样偏差问题,全面捕捉肿瘤分子特征。
- 循环生物标志物(WF3 - Circulating biomarkers)
- 样本类型:血液
- 检测方法:免疫表型分析、细胞因子分析、甲基化分析、突变分析
- 用于动态监测疾病负担、治疗反应等情况。
- 空间分析(WF4 - Spatial profiling)
- 样本类型:FFPE组织
- 检测方法:多重免疫荧光(MxIF) 、空间转录组学、数字病理学
- 研究肿瘤微环境空间分布,助力治疗策略制定。
- 治疗筛选(WF5 - Therapeutic screening)
- 样本类型:患者来源的肿瘤片段(PDTFs)
- 检测方法:免疫表型分析、细胞因子分析
- 评估肿瘤浸润免疫细胞对治疗的反应,筛选治疗方案。
- 肠道微生物组(WF6 - Gut microbiome)
- 样本类型:粪便
- 检测方法:微生物组分析
- 探索肠道微生物组与免疫治疗反应和免疫相关不良事件的关联。
- 数据整合(WF7 - Data integration)
整合上述工作流程产生的数据,输出包括生物标志物关联、治疗反应和毒性预测模型、反应与耐药机制、新型治疗靶点(如TCR相关、疫苗、免疫检查点抑制剂(ICIs) 、抗体药物偶联物(ADCs) ) 、临床环境中的技术测试与适配以及免疫肿瘤学(IO)研究报告等。
此外,MANIFEST项目具备交叉培训和知识转移功能,是一个可扩展且灵活的平台 ,图中还标注了项目涉及的英国相关地点。
在支持可扩展的生物标志物发现的同时,该平台旨在整合新兴技术,推动生物学研究的发展。
这些工作流程的模块化特性使其在平台的整个生命周期中,都能融入新的检测方法和技术。
在肿瘤分子分析方面,源于肿瘤批量分析的免疫治疗生物标志物,常因肿瘤内部普遍存在的异质性,以及测序方式和分析方法的差异而失效。虽然肿瘤突变负荷(TMB)、PD-L1蛋白状态和DNA错配修复缺陷已获得FDA批准,但它们的预测性能仍依赖于具体情境。
新兴的复合生物标志物(如TMB和IFN-γ特征;参考文献7)虽有前景,但需要进行严格的标准化和验证。MANIFEST将从接受一线免疫检查点抑制剂治疗的初治患者样本中,获取标准化的免疫基因组数据集。利用临床级检测方法,对福尔马林固定石蜡包埋的样本进行全外显子测序和批量RNA测序。
同时,还会探索已确定和潜在的生物标志物,如克隆性TMB、新抗原负荷和质量、HLA单倍型以及基因表达谱等。对复合的、空间稳定的免疫基因组生物标志物的预测准确性进行测试。
此外,新兴的分子检测方法将对TCR/BCR指标进行量化,包括克隆大小、扩增、克隆性和多样性,以便为基于细胞和抗体的治疗开发筛选出优先的抗原特异性克隆。长读长RNA测序和免疫肽组学等探索性方法,将专注于检测高质量的新抗原,优化抗原预测,并为疫苗开发提供支持。
在代表性肿瘤采样方面,实体瘤的肿瘤内异质性给准确的生物标志物发现带来了巨大挑战,这是由于不同肿瘤区域的独特亚克隆导致的采样偏差造成的。
多区域采样虽能缓解这一问题,但受到成本、人力以及标准治疗实施难度的限制。为此,MANIFEST采用了RepSeq这一新颖方法,它能将多余的手术肿瘤组织均质化,以获取全面的分子特征(参考文献4,8)。
RepSeq将与fixed-FACS技术联合使用,fixed-FACS可从匀浆中富集目标亚群,克服肿瘤纯度低的问题,并实现对肿瘤微环境(TME)的详细分析(参考文献4)。MANIFEST将对200个肿瘤应用RepSeq结合分子分析检测,以识别克隆性和持续性新抗原,评估免疫逃逸机制,并探究它们与免疫治疗反应的关系。
同时,该平台还将评估代表性TCR和BCR库作为免疫治疗反应和治疗发现生物标志物的效用,对代表性匀浆应用新兴的TCR检测方法。
此外,利用fixed-FACS技术,将肿瘤分子特征与TME特征相结合,对肿瘤浸润淋巴细胞、PD-L1表达和免疫细胞亚群比例进行量化。
在循环生物标志物方面,循环生物标志物能为疾病负担、治疗反应、肿瘤特征和免疫相关不良事件(irAEs)提供动态信息。
外周免疫生物标志物、细胞因子和cfDNA相关方法在预测免疫治疗结果方面展现出一定潜力,但仍需进行严格的标准化和验证。
MANIFEST将使用高分辨率光谱细胞术对外周血单个核细胞亚群进行表征,以开发外周免疫反应特征,这些特征是免疫治疗反应和irAEs发生的基础。
考虑到跨模态治疗的趋势,MANIFEST将利用观察性队列中的纵向样本,探索非免疫肿瘤学(IO)疗法对免疫谱的影响。细胞因子分析将作为补充,首先建立一个发现面板,并在后续前瞻性研究中不断优化。
此外,还会采用cfDNA相关方法评估微小残留病,监测治疗反应,并描绘免疫谱。MANIFEST将与商业合作伙伴合作,利用肿瘤信息检测方法,以及包括新兴反卷积技术在内的全基因组DNA甲基化分析方法,对循环免疫细胞中的cfDNA进行分析(参考文献9)。
在原位分析方面,空间分析和机器学习的进展为在免疫治疗背景下探索TME提供了机会。
了解TME成分的空间分布对制定治疗策略至关重要,但由于成本高昂、需要专业知识,以及缺乏标准化的数据收集和图像分析方法,空间生物学工具的应用仍不充分。
虽然多重免疫荧光(MxIF)和免疫组织化学(IHC)主要用于探索性研究,但MANIFEST联盟之前开发的方案表明,它们在接近临床应用的定量验证方面具有潜力(参考文献10)。
MANIFEST将部署多个低通量MxIF面板,用于高通量、可重复的组织分析。在有条件的情况下,代表多个肿瘤区域的组织微阵列和纵向样本,将有助于进行经济高效且可扩展的分析。与专家共识声明一致的标准化协议,将促进检测方法的应用和临床使用的监管验证。
对于有特殊反应的部分患者,高通量MxIF(>40种标记物)和空间转录组学将作为补充,整合蛋白质和RNA数据,并对趋化因子等关键靶点进行量化,以推动研究发现。通过高通量计算病理学流程,MANIFEST旨在从诊断用的苏木精和伊红染色数字全切片图像中,识别与免疫治疗反应相关的形态学和拓扑学特征。
在有匹配分子数据的情况下,将进一步研究这些形态学关联,以开发计算病理学生物标志物,这是一种经济高效且可扩展的方法。此外,利用匹配的全切片图像和MxIF数据,还将采用虚拟染色技术,为数千个样本提供可扩展的分析视角。
患者来源的肿瘤片段(PDTFs)方面,临床前模型对于从观察数据中获得功能性见解至关重要,但在免疫治疗研究中,其可重复性和可扩展性仍是重大挑战。
PDTFs是新鲜手术切除的肿瘤组织,切成1至2毫米直径后冷冻保存,它保留了肿瘤的原始结构和免疫微环境(参考文献5,6)。
值得注意的是,PDTFs能准确预测供体患者对各种免疫治疗药物的临床反应,提供了一种快速(<48小时)、通用且准确的模型,可用于评估肿瘤浸润免疫细胞对治疗(包括新疗法和联合策略)的反应(参考文献6)。
PDTFs还有望发现对标准免疫疗法反应和耐药的生物标志物,特别是在评估辅助治疗的益处方面。MANIFEST将扩大PDTF生物样本库规模,系统评估对免疫检查点抑制剂和其他治疗方法的免疫反应。该平台将通过深度分析,包括高维细胞术、多重免疫荧光(MxIF)、细胞因子/趋化因子分析以及T细胞受体(TCR)和B细胞受体(BCR)测序,为合理的联合治疗和新化合物测试提供便利。
借助前瞻性队列中的实时临床数据,MANIFEST将探索PDTFs作为包含天然肿瘤免疫细胞浸润的体外模型,用于预测辅助治疗益处的潜力,并评估其作为非干预性生物标志物融入临床试验的可行性。
肠道微生物组方面,肠道微生物组与免疫治疗反应和免疫相关不良事件(irAEs)有关,但在不同患者群体和免疫疗法中识别一致的基于微生物组的生物标志物仍具有挑战性(参考文献11)。
这部分是由于参考基因组数据库不完整,以及过度依赖物种和属水平的分类,而细菌功能具有菌株特异性。微生物组生物标志物可用于指导口服活生物治疗产品(特定细菌组合)的开发,以刺激免疫反应,增强免疫检查点抑制剂的疗效。
MANIFEST平台将与商业合作伙伴合作,评估已验证的微生物组特征在典型肿瘤类型和免疫肿瘤学(IO)药物中的适用性。
前瞻性队列研究将整合微生物组数据与临床和多组学数据集,以推导免疫治疗反应、耐药性和irAEs的预测特征。
分析和深度学习方面,传统的免疫治疗生物标志物开发侧重于单一数据类型,无法捕捉抗肿瘤免疫的复杂性。
免疫治疗反应和irAEs的多模态预测指标在理解耐药机制和识别新治疗靶点方面具有更大潜力。然而,多模态数据整合的进展因缺乏正交数据集而受阻,限制了方法的基准测试。
MANIFEST上述工作流程产生的数据将在可信研究环境中进行集中管理和分析,高性能计算基础设施以及商业合作伙伴提供的云服务和管理解决方案为此提供支持。利用标准化、大规模、高质量的数据集,该平台将系统探索数据模态之间的互补性和相互作用。
首先将开发单模态模型来预测免疫治疗反应和irAEs,然后使用后期融合技术将其整合到可扩展的模块化多模态模型中(参考文献12)。这些模型将结合多种来源的数据,同时处理数据缺失和变异性问题。人工智能的安全性、可解释性和稳健性至关重要,将通过知识蒸馏、不确定性量化和事后分析等技术增强对模型预测的信心。
MANIFEST致力于提供用于免疫治疗反应和irAE预测的单模态和多模态模型,并配备可解释性工具来识别生物标志物,增强临床可解释性。
此外,数学模型将模拟肿瘤 - 免疫相互作用,预测空间肿瘤微环境(TME)结构对免疫治疗反应的影响,并实现免疫治疗策略的虚拟试验。
六、未来展望
MANIFEST为当前免疫治疗面临的挑战提供了全面的精准医学解决方案,有助于生物标志物的发现,辅助预测标准治疗及新兴干预措施的治疗效果和毒性。该平台针对多种癌症类型采用标准化方法,保证了广泛的适用性,利于反向转化研究和技术转移。
研究团队期望MANIFEST能构建丰富复杂的数据存储库,通过简化数据访问流程,推动进一步的探索和转化研究。临床和样本层面的数据将进行匿名化处理,多模态数据集会集中存储在可信研究环境中,并利用强大的防火墙进行数据分区管理。
元数据标记可确保多组学数据集的无缝整合,既支持针对患者个体的分析,也有助于在队列层面发现新的生物标志物,为免疫治疗策略提供依据。
平台产生的数据还有望成为评估新兴生物标志物和靶点异质性的参考数据集。其最终目标是为研究人员和临床医生提供推动科研进展的工具,就像癌症基因组图谱等联盟在癌症研究领域产生的深远影响一样。
在扩展阶段,MANIFEST将继续借助卫星项目对平台进行压力测试,并为核心数据库提供数据,扩充资源。此外,平台还致力于拓展其作为伴随诊断工具的功能,为学术和商业合作伙伴提供有价值的转化研究见解。
通过建立大型数据和检测生态系统,借助临床网络支持研究人员主导的研究,以及开展与私营部门的合作,实现平台的长期可持续发展。这一模式基于良性循环,即使用平台的各方承诺将数据用于迭代学习。
结束语
本期推文的内容就到这里啦,如果需要获取医学AI领域的最新发展动态,请关注小罗的推送!如需进一步深入研究,获取相关资料,欢迎加入我的知识星球!

























 1884
1884

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








