点评 |孙育杰(北京大学)、钟桂生(上海科技大学)
责编 | 兮
显微镜是人类最伟大的发明之一,自17世纪列文虎克把显微镜应用于微生物研究以来,人们就一直孜孜不倦的追求显微镜分辨率的提高,以期待看到更微小的细胞结构,了解生命活动的本质。但由于光学显微镜分辨率受衍射现象限制,在进入本世纪前一直没有取得突破。
进入21世纪以来多种超高分辨率荧光成像技术被提出,新型超高分辨率显微镜产品也如雨后春笋般出现,打破了光学分辨率的极限, 将光学分辨率提高到几十纳米的尺度, 可以用来观察精细的亚细胞结构和生物分子定位信息,被广泛地应用于生物学研究中,相关工作也因此获得了2014年的诺贝尔化学奖。但把光学显微镜分辨率进一步提高到分子水平,以观察纳米尺度的亚细胞结构乃至单个生物大分子内的结构仍是巨大的挑战。
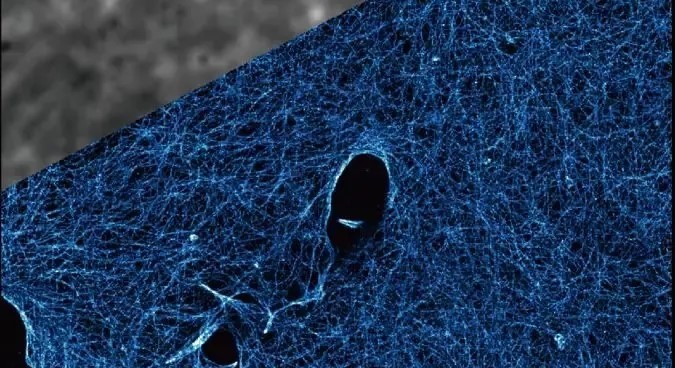
2019年9月9日,中国科学院生物物理研究所徐涛院士领衔的生命科学仪器研制中心团队(共同一作为谷陆生、李媛媛和张淑文)在Nature Methods杂志发表了题为“Molecular resolution imaging by repetitive opticalselective exposure”的论文,提出了一种基于干涉定位成像的新技术,并据此研制出新型的ROSE单分子干涉定位显微镜(Repetitive Optical Selective Exposure),可以分辨点距为5 nm的DNA origami结构,把显微镜的分辨率提升到3 nm以内的分子尺度,单分子定位精度接近1 nm。

ROSE采用6个不同方向和相位的干涉条纹去激发荧光分子,荧光分子的发光强度与其所处条纹的相位相关,因此可以通过荧光分子强度与干涉条纹的相位关系来判断荧光分子的精确位置信息。该方法可类比于GPS定位,GPS定位即是通过几颗卫星到GPS信号源的距离来判断信号








 最低0.47元/天 解锁文章
最低0.47元/天 解锁文章















 2163
2163











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








