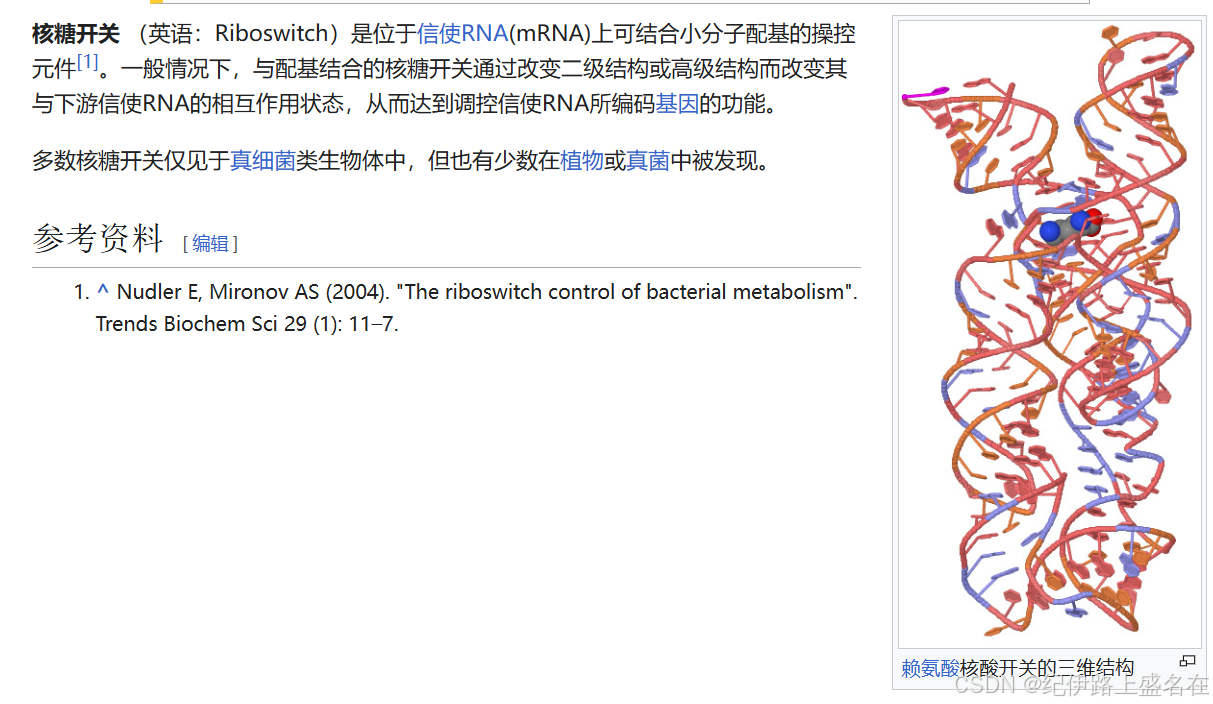
核糖开关 (英语:Riboswitch)是位于信使RNA(mRNA)上可结合小分子配基的操控元件。一般情况下,与配体结合的核糖开关通过改变二级结构或高级结构而改变其与下游信使RNA的相互作用状态,从而达到调控信使RNA所编码基因的功能。
多数核糖开关仅见于真细菌类生物体中,但也有少数在植物或真菌中被发现。
在分子生物学中,核糖开关是信使 RNA 分子上的一个调控片段,它能结合小分子,导致mRNA 翻译的蛋白质生产发生变化。因此,含有核糖开关的 mRNA 直接参与调节其自身的活性,以响应其效应分子浓度。现代生物使用 RNA 结合小分子,并区分密切相关的类似物,这一发现扩展了 RNA 已知自然能力,使其不仅限于编码蛋白质、催化反应或结合其他 RNA 或蛋白质大分子。
——》我们可以简单将核糖开关理解为mRNA上的一个“domain”,这个domain是通过与配体结合来改变/影响mRNA的翻译过程,可以认为是mRNA自调节自催化的一个机制一个结构。
该术语“核糖开关”的原始定义是指它们直接感知小分子代谢物浓度。尽管这个定义仍然被广泛使用,但一些生物学家已经使用了更广泛的概念,包括其他顺式调控 RNA。
所以广义定义上,核糖开关不仅仅局限于mRNA上的一个功能domain元件,也可以拓展至其他的顺式调控RNA,那非编码的又是调控RNA的元件就很多了。
——》更广义的报道,可以依据狭义以及广义交叉结合起来理解:
核糖开关(Riboswitches)是一类非编码RNA元件,主要存在于细菌mRNA的5′非编码区(5′UTR),通常由适配体(aptamer)和表达平台(expression platform)两个功能域组成。当特定分子(ligand,配体)结合适配体域时,会引起表达平台域的局部构象发生变化,从而打开或关闭下游基因的表达。核糖开关广泛存在于细菌中,它们在细菌的硫代谢、辅酶合成、氨基酸合成等基础代谢中发挥着非常重要的调控作用,迄今为止,已有20余类感应不同分子的核糖开关在细菌中被确认。
核糖开关(riboswitch)最早是由Winkler等人于2002年在大肠杆菌中发现并命名的,这是一类非编码RNA元件,主要在细菌mRNA的5'非编码区( UTR) 被发现,但在真核生物mRNA的3'UTR及初始转录产物的内含子区段也有发现。由于一直以来非编码区均是分子生物学研究的热点之一,因此作为该领域的重要组成部分,核糖开关也成为了近几年基因表达调控研究的一个热点。
RNA结构开关(RNA structural switches)是基因表达的重要调控因素,广泛存在于细菌中。然而,在真核生物中,RNA结构开关的研究和鉴定却相对有限。在细菌中,一些RNA开关被称为核糖开关(riboswitches),它们通过结合小分子配体诱导RNA构象变化,从而控制基因表达。尽管植物和真菌中已鉴定出一些硫胺素焦磷酸感应核糖开关,但在人类中已知的RNA开关仅有两个:一个是依赖于蛋白质的血管内皮生长因子A(VEGFA)RNA开关,另一个是基于m6A修饰的RNA开关。因此,RNA开关在高等真核生物基因表达中的总体影响仍不清楚。
在细菌中,核糖开关(riboswitches)通过结合小分子配体(ligands),诱导RNA构象变化,从而控制基因表达。例如,核糖开关可以感知环境中的代谢物浓度,并通过改变其二级结构(secondary structure)调控相关基因的转录或翻译。然而,在真核生物中,尽管植物和真菌中已鉴定出一些硫胺素焦磷酸(thiamine pyrophosphate)感应核糖开关,但在人类中已知的RNA开关仅有两个:一个是依赖于蛋白质的血管内皮生长因子A(VEGFA)RNA开关,另一个是基于m6A修饰的RNA开关。因此,RNA开关在高等真核生物基因表达中的总体影响仍不清楚。



参考:
https://zh.wikipedia.org/wiki/%E6%A0%B8%E7%B3%96%E5%BC%80%E5%85%B3
























 1328
1328

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








