 AbMole是ChemBridge在中国唯一官方指定合作伙伴。
AbMole是ChemBridge在中国唯一官方指定合作伙伴。
由美国莫菲特肿瘤研究中心的Sevil Ozcan、Saïd M. Sebti发表的名为“Oxadiazole-isopropylamides as Potent and Noncovalent Proteasome Inhibitors”的论文中,研究人员通过高通量筛选ChemBridge化合物库发现了能改善乳腺癌的全新CT-L非共价抑制剂。AbMole(奥默生物)是ChemBridge在中国的唯一官方指定合作伙伴。

ATP依赖的泛素−蛋白酶体途径负责调控真核细胞中蛋白质的降解。其中,26S蛋白酶体是一个由19S调节复合物(RP)和20S核心颗粒(CP)组成的多功能复合物。该蛋白酶体介导的三种主要催化反应,分别是:肽酰谷氨酰肽水解(PGPHL)、胰蛋白酶样水解(T-L)和糜蛋白酶样水解(CT-L)。其中,CT-L在凋亡和抑癌蛋白的降解中发挥重要作用。因此,研究人员想开发具有良好抑瘤效果的新型CT-L抑制剂。研究人员从ChemBridge化合物库中筛选出新型CT-L抑制剂,并进行了进一步的活性和结构优化。
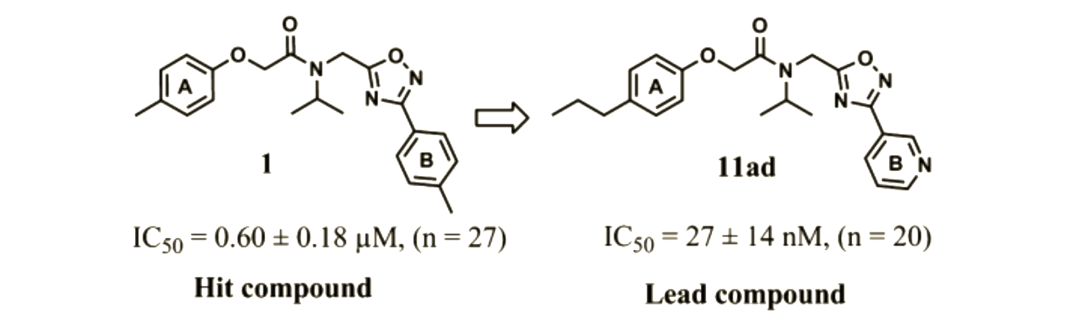
图1.A:苗头化合1和先导化合物11ad的结构和IC50。
现有的蛋白酶体抑制剂是通过醛基、硼酸酯、乙烯砜和环氧酮通过共价修饰与CT-L发挥作用的,但对癌症细胞和正常细胞没有选择性。本文研究人员以各种化合物对癌症细胞中CT-L的活性抑制为评判标准进行筛选,最后从ChemBridge化合物库中筛选出新型CT-L抑制剂,并在美国癌症研究协会会议中公布。

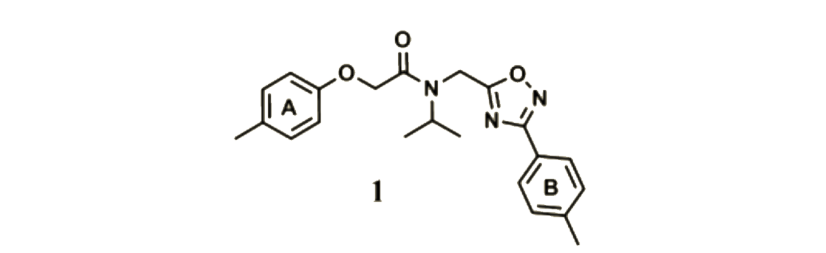
图2.研究人员首次在美国癌症研究协会会议中公布了新型CT-L抑制剂及其结构。
为了验证化合物1与CT-L的结合方式,研究人员将化合物1和CT-L共价结合抑制剂Lactacystin与20S蛋白酶体孵育,并通过测定CT-L的透析结合,判断化合物1与CT-L结合的可逆性。结果显示,经过一段时间后,化合物1处理的CT-L开始恢复活性,说明化合物1和CT-L是非共价结合的。
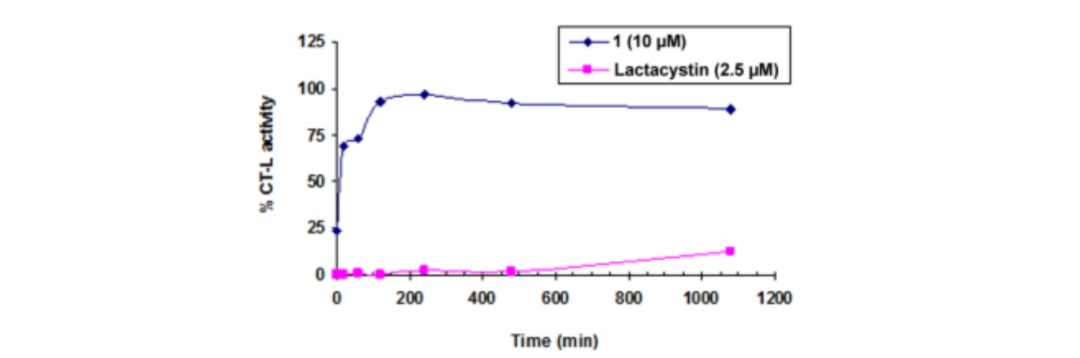
图3.透析实验揭示化合物1与CT-L发生非共价结合。
随后,研究人员对化合物1进行了结构的优化。发现在A环上增加对位的碳原子数,比如把甲基替换为乙基有更好的活性,而使用芳杂环替代B苯环也能够提高活性。于是,研究人员优化得到化合物11ad。
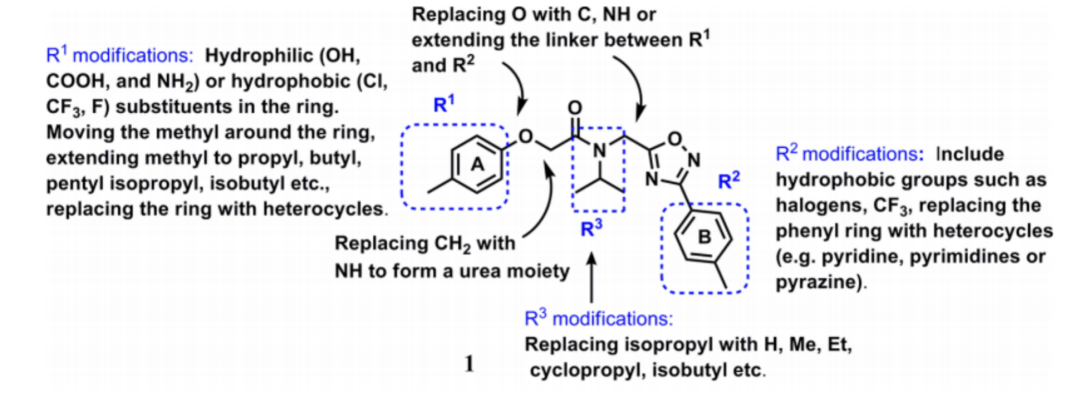
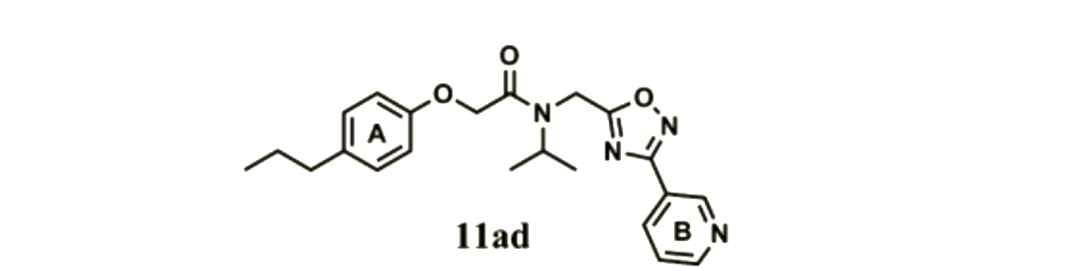
图4.化合物1的结构优化思路及优化得到的化合物11ad结构
最后,研究人员对优化得到的化合物11ad的CT-L抑制活性在乳腺癌细胞上进行测评。研究人员分别用不同浓度化合物1和化合物11ad处理乳腺癌细胞系MDA-MB-231,并检测其对CT-L和细胞活力的影响。结果显示,化合物11ad对乳腺癌细胞的CT-L活性和细胞活力有很好的抑制作用,能够显著抑CT-L,并改善乳腺癌。
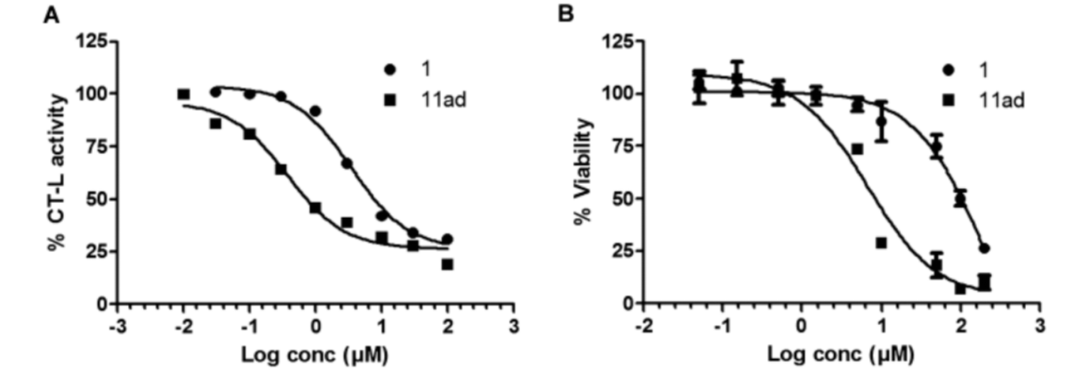
图5.化合物1和化合物11ad对CT-L和乳腺癌抑制活性的对比
更多内容请访问:www.abmole.cn






















 289
289

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








