简要思维导图
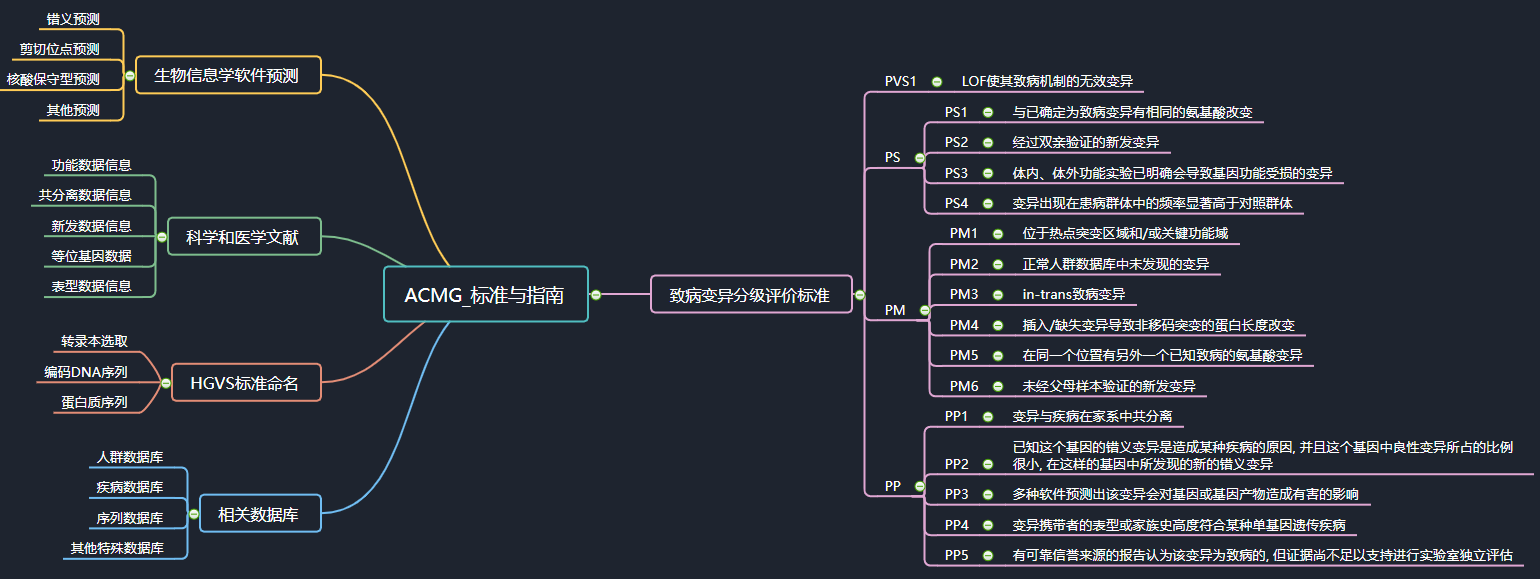
ACMG位点评级图解

PVS1
已知的疾病机制是LoF的基因中存在无效变异 (无义、移码、±1/2经典剪接位点、起始密码子、单个或多外显子缺失或重复);以及RNA验证证实存在异常转录的非经典剪接变异。
使用PVS1证据前,应首先确认基因与疾病的临床有效性和致病机制,根据基因与疾病的临床有效性评分等级调整PVS1的应用。此外LoF是已知的疾病机制。目前超过1750基因有“基因-疾病有效性评分等级”。(https://search.clinicalgenome.org/kb/gene-validity)。
将LoF确定为一种疾病的机制可能会有主观因素,但判断LoF是否为疾病的致病机制可以参考ClinGen单倍剂量不足评分(haploinsufficiency score, HI)、LoF不耐受概率评分(probablity of LoF intolerance, pLI)、LoF变异观察值/期望值上限分数(loss-of-function observed/expected upper bound fraction, LOEUF)。
PS1
待评估变异与先前已确定的致病变异具有相同的氨基酸变异。
PS2
先证者无家族史,经双亲验证,待评估变异为新发变异。
PS3
在体外或体内已建立的功能研究表明待评估变异对基因或基因产物具有破坏性影响。
PS3和PP3可以一起用于错义变异。功能分析是评估蛋白质的功能/活性;计算机模拟预测可以评估进化保守性,两者是相互独立的。
PS4
与对照组相比,待评估变异在受累个体中的发生频率显著增加。
PM1
待评估变异位于无良性变异的突变热点区域和/或关键且确定的功能域(例如酶的活性位点)。PM1仅适用于错义变异(PM2_Supporting证据的错义变异)。
PM2
待评估变异在基因组聚集数据库(Genome Aggregation Database, gnomAD)中不存在(如果是隐性基因,存在极低的频率)。
携带罕见变异是非常普遍的现象,并不能达到中等程度的致病性证据。因此参考ClinGen SVIWG(ClinGen序列变异解释工作组, Sequence Variant Interpretation Working Group, SVIWG)推荐,在参考群体中未见或罕见变异的证据PM2从中等证据降级为支持性证据(PM2_Supporting)。
PM3
在隐性遗传病中,待评估变异的反式位置(in trans) 上检测到致病变异。
PM4
非重复区域的框内缺失/插入或终止密码子丧失引起的蛋白质长度变化。不适用于移码突变、无义变异和剪接位点变异。
对于单个氨基酸的框内缺失或插入,谨慎使用该证据,除非有基因特异性证据保证能在中等水平使用,否则该证据降至支持性水平(supporting)。
PM5
待评估变异(须为新的错义变异)与一个已确定(不能假定为致病的)为致病的错义变异同处于一个氨基酸位点(如Trp38Ser和Trp38Leu)。
PS1/PM5均适用于错义变异。PS1用于不同的碱基突变引起同一个氨基酸改变的错义变异;PM5用于同一个氨基酸位置的新的错义变异。
PM6
待评估变异假定为新发变异,未经过父母验证。
PP1
在一个明确已知导致疾病的基因中,多个受影响的家庭成员中的疾病共分离。
PP2
一种基因中的错义变异,具有低的良性错义变异率,其中错义变异是疾病的常见机制。
PP3
多行计算证据支持对基因或基因产物的有害影响(保守,进化,剪接影响等)。
PP4
患者的表型或家族史对于具有单一遗传病因的疾病具有高度特异性。
PP5
最近有可靠来源报告变异为致病性,但实验室无法获得证据进行独立评价。
BP1
基因中的错义变体,已知其主要截短变体会导致疾病。
BP2
在完全外显显性基因/疾病的致病性变体中观察到反式,或在任何遗传模式的致病性变体中观察到顺式。
BP3
在没有已知功能的重复区域中的框内缺失/插入。
BP4
多行计算证据表明对基因或基因产物没有影响(保守、进化、剪接影响等)。
BP5
在具有疾病的替代分子基础的病例中发现的变异。
BP6
最近有可靠来源报告称变异为良性,但实验室无法获得证据进行独立评价。
BP7
一种同义(沉默)变体,其剪接预测算法预测对剪接共有序列无影响,也不会产生新的剪接位点,并且核苷酸不高度保守。
BS1
等位基因频率高于疾病的预期。
BS2
在健康成人个体中观察到隐性(纯合子)、显性(杂合子)或X连锁(半合子)疾病,预期在早期出现完全隐性遗传。
BS3
成熟的体外或体内功能研究表明,对蛋白质功能或剪接没有损害作用。
BS4
受影响的家庭成员之间缺乏隔离。
BA1
等位基因频率在外显子组测序计划(ExAC)、1000基因组计划(1000G)或外显子组聚集联盟(genomAD)中为5%。
参考文献:
Richards, S. et al. (2015). “Standards and guidelines for the interpretation of sequence variants: a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology”. Genetics in Medicine 17, 405–423. DOI: 10.1038/gim.2015.30


























 2355
2355

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?










