目录
- PDeepPP 融合 ESM-2 蛋白语言模型与 Transformer-CNN 架构,显著提升肽段识别准确率和效率。
- 新型语言模型 Ab-Affinity 结合遗传算法和模拟退火,提高抗体与 SARS-CoV-2 刺突蛋白结合亲和力。
- APM 模型实现了原子级蛋白质复合物设计,并在抗体和多肽设计中取得了领先性能。
- 评估 AlphaFold2/3 复合物预测的评分指标,发现基于界面的指标更可靠,并开发了新的组合评分 C2Qscore 提升准确性。
- AlphaFold3 模型难以捕捉磷酸化引起的蛋白质结构变化,深度学习模型在预测蛋白质动态构象方面存在局限。
- BRAGE 基准评估检索增强大型语言模型在生物制药领域的查询和参考文献理解能力,揭示了当前模型的局限性和领域适应的潜力。
- BRIDGE 模型利用粗粒化图神经网络准确预测蛋白质相互作用,赋能药物研发。
- CellFlow 利用流匹配技术,精准预测细胞对多种扰动的反应,加速药物研发和功能基因组学研究。
- 基于可解释人工智能,研究对 17 种肽段-HLA-I 结合预测工具进行了迄今为止最全面的基准测试,揭示了 STMHCpan 和 BigMHC 等自注意力模型的优越性能,并强调了高质量数据和混合方法的重要性。
- DTMol 利用扩散变换器实现精准的口袋分子对接,显著提升对接精度并发现新的活性化合物。
1. PDeepPP:肽段识别深度学习框架
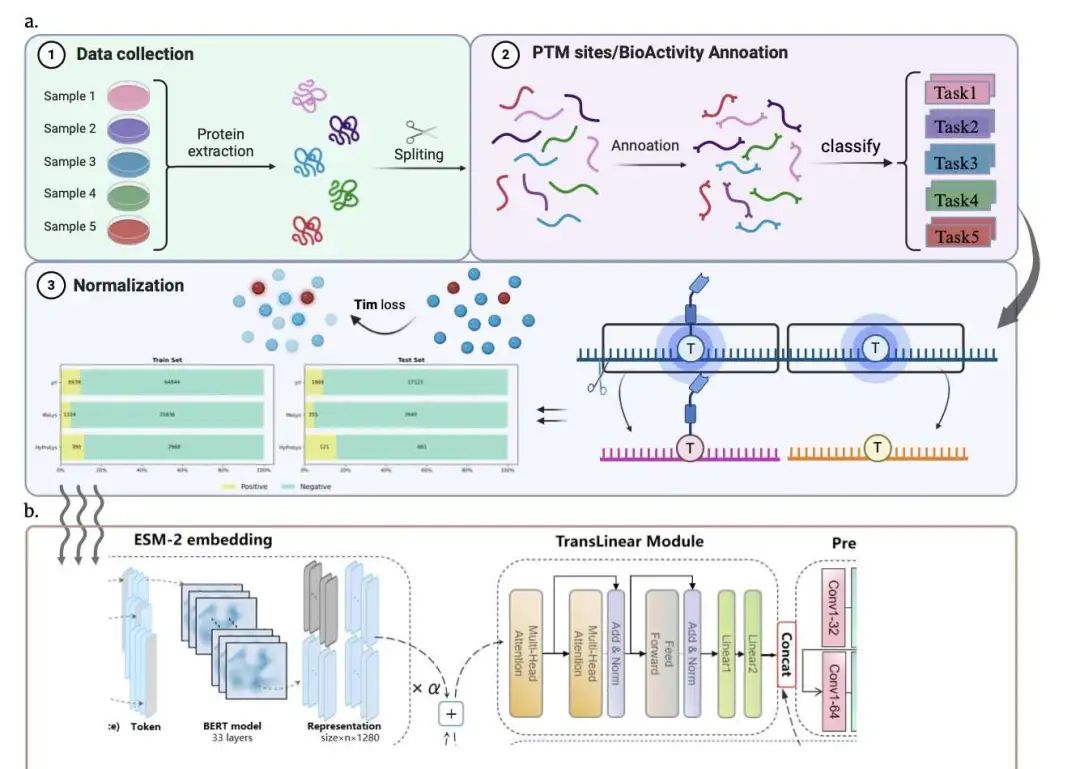
PDeepPP 引入了一种统一的深度学习框架,通过融合 ESM-2 蛋白语言模型嵌入和混合 Transformer-CNN 架构进行肽段识别。该设计在各种生物信息学任务中实现了高精度和可扩展性。研究者在 33 项基准生物任务(包括抗菌肽、抗癌肽和糖基化位点识别)中对 PDeepPP 进行了评估,其性能显著优于现有方法。例如,在抗菌肽检测中,PDeepPP 实现了 97.26% 的准确率和 0.9977 的 PR AUC,并将抗疟疾检测中的假阴性减少了 37.5%。
PDeepPP 通过并行的 PosCNN 和 Transformer 分支捕获局部和全局特征。这种双路径架构在 UMAP 空间中实现了 29% 的类别分离改进,表明其在复杂序列数据中具有更高的可解释性和鲁棒性。此外,利用 ESM-2,PDeepPP 将蛋白质序列知识有效地迁移到下游任务。其混合嵌入(90% ESM-2 + 10% 特定任务)在低数据场景 (n < 500) 下实现了 92.4% 的平均召回率,比传统方法高出 34.7%。
为了解决数据集不平衡的问题,PDeepPP 采用了 TIM(Transductive Information Maximization)损失函数。与标准交叉熵不同,TIM 增加了特征和标签之间的互信息,减少了过拟合,并提高了少数类的精度。与基于比对的方法相比,PDeepPP 实现了 218 倍的加速,每分钟可处理 15,000 个序列,同时在糖基化位点预测中保持 99.5% 的特异性。它以最小的资源成本提供了可扩展的高通量注释。
与 UniDL4BioPep 和 MusiteDeep 等最先进的工具相比,PDeepPP 在多个数据集上展现出更优越的 AUC、精确率 - 召回率和错误率降低。在某些设置下,它将误报减少了 21,000 多个,同时保持了较高的真阳性率。消融研究表明,移除 CNN 或 Transformer 分支都会显著降低模型性能。移除 CNN 会使误报增加 2.1 倍,而移除 Transformer 会使假阴性增加 37.5%,证明了这两个模块都是必不可少的。来自消融测试的 UMAP 可视化清楚地表明,完整的 PDeepPP 模型形成了更紧密、更易分离的簇。移除模块会模糊这些边界,证实了完整的混合结构对于特征区分的必要性。
PDeepPP 的开源代码、数据和预训练模型可在 GitHub 和 Hugging Face 上获取,为肽生物活性和翻译后修饰预测提供了一个可复现和可扩展的平台。
2. 语言模型助力抗体亲和力成熟优化
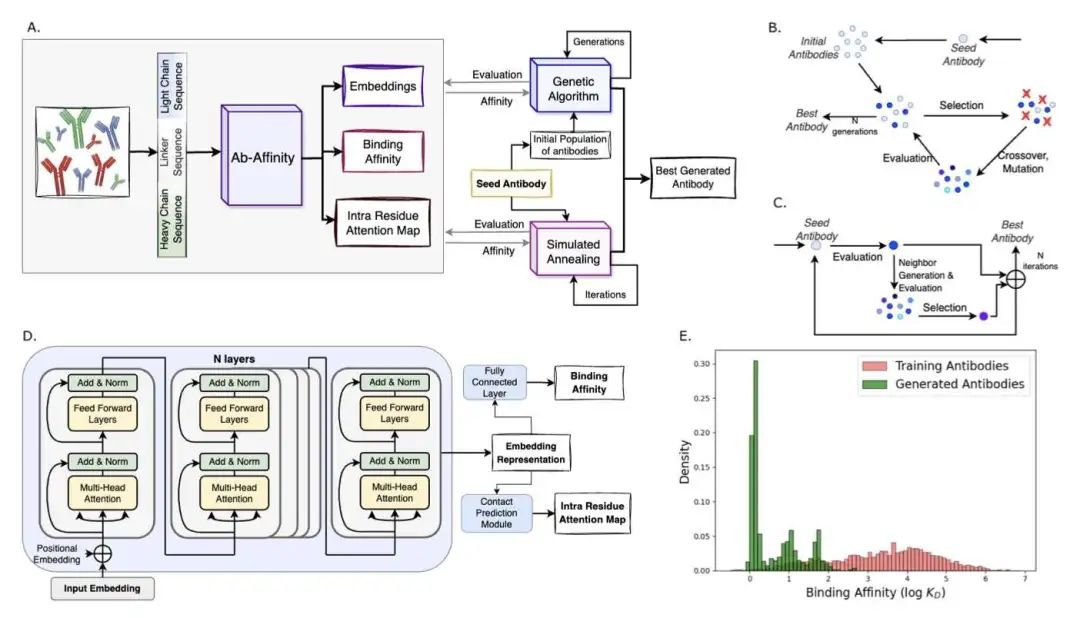
研究者引入了一种名为 Ab-Affinity 的新型大型语言模型,用于预测抗体与 SARS-CoV-2 刺突蛋白的结合亲和力。通过将 Ab-Affinity 与遗传算法和模拟退火相结合,研究者能够显著增强抗体亲和力,预测结合强度相比实验结果提高了 160 多倍。该模型不仅能够高精度预测亲和力,还有助于生成性能优于现有方法的新型抗体。这对于像 SARS-CoV-2 这样快速进化的病毒尤为重要,因为新变种不断对治疗构成挑战。
研究结合了计算技术和实验验证,表明使用 Ab-Affinity 设计的抗体展现出增强的分子相互作用和与靶肽的稳定性。分子动力学模拟证实了这些改进,为下一代抗体开发提供了切实可行的途径。Ab-Affinity 的成功在于它能够通过模拟退火和遗传算法等方法探索适应性景观。这些方法确保了生成的抗体既新颖又具有生物学上的合理性,避免了随机突变的缺陷,并为抗体成熟提供了可控的方法。
Ab-Affinity 的性能优于 DG-Affinity 和 ESM-2 等其他现有计算模型,为亲和力成熟提供了更有针对性的解决方案。其在生成具有优异生物物理特性的合成抗体方面的成功,为抗体工程的未来树立了新的标杆。
3. APM:原子级蛋白质复合物生成模型
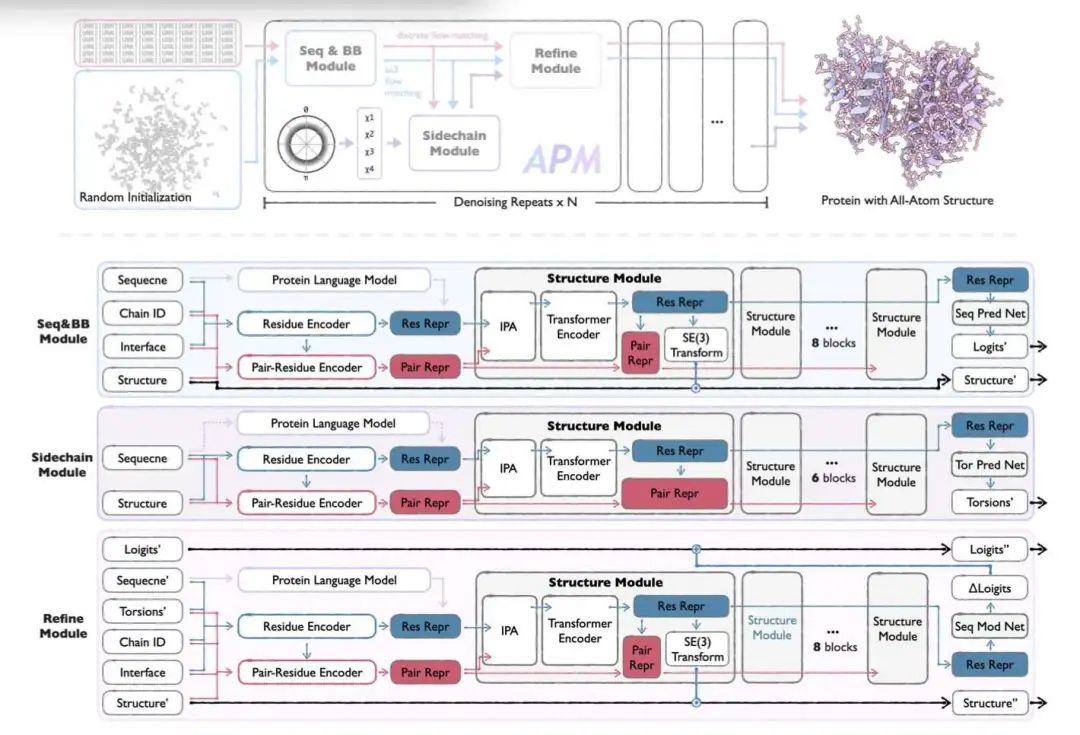
APM (All-Atom Protein Generative Model) 是一种新型生成框架,旨在以全原子分辨率对多链蛋白质复合物进行建模、折叠和生成,弥补了传统单链模型的不足。与依赖伪序列链接进行多链建模的方法不同,APM 通过架构和数据层面的创新来处理天然的多链结构,从而能够精确建模链间相互作用。APM 集成了一个三模块流程:(1)Seq&BB 模块,通过流匹配共同生成主链和序列;(2)Sidechain 模块,生成全原子侧链构象;(3)Refine 模块,以全原子意识优化结构。为了在生成过程中保持序列 - 结构一致性,APM 采用了一种新颖的解耦噪声和两阶段训练策略,从而在两种模式下都能实现高保真重建。
在单链任务的基准测试中,APM 的性能与 ESM3 和 ESMFold 等领先模型相当,并且在各种蛋白质长度的反向折叠和结构生成方面优于 MultiFlow 和 ProteinGenerator。APM 是首批在没有 MSA 的情况下对多链蛋白质进行可靠折叠和反向折叠的生成模型之一,其性能优于 Boltz-1 (noMSA),并实现了高氨基酸恢复率和 scTM 分数。在从头复合物生成中,APM 实现了比 Chroma 更强的结合能和更低的 RMSD,验证了其使用全原子特征设计紧密堆积界面的能力。APM 的逐链条件生成提供了可控的复合物形成,支持链独立折叠和协同结合的灵活设计策略。
在下游应用中,APM 在抗体 CDR-H3 共同设计(RAbD 基准)和靶向肽设计(LNR 数据集)中取得了最先进的性能,在结合亲和力和结构质量方面超过了 dyMEAN、DiffAb 和 PepGLAD 等专用模型。通过显式建模所有原子细节、原生处理多链系统以及支持零样本和微调设计任务,APM 为下一代蛋白质复合物设计铺平了道路,并在治疗开发中具有广泛的应用前景。
4. AlphaFold 蛋白质复合物预测评估
本研究评估了常用评分指标在评估 AlphaFold2 (通过 ColabFold) 和 AlphaFold3 预测的蛋白质复合物模型质量方面的能力,揭示了它们在准确评估异二聚体界面方面的关键差异。研究使用 325 个高分辨率异二聚体结构作为基准,发现使用模板的 ColabFold 和 AlphaFold3 产生的正确模型比例相似且较高,两者均优于不使用模板的 ColabFold,尤其是在生成高 DockQ 分数模型方面。研究表明,特定于界面的分数(尤其是 ipTM 和模型置信度)是评估蛋白质复合物模型最可靠的指标,在所有数据集中始终与 DockQ 表现出最高的相关性。全局分数(如 pLDDT 和 PAE)的效果不如基于界面的指标(如 ipLDDT 和 iPAE)。值得注意的是,pDockQ2 与实际模型质量的相关性较差,经常错误分类高质量模型。为了解决这些不一致性,作者开发了 C2Qscore,这是一种使用多个特定于界面的指标进行线性回归的组合评分。C2Qscore 的性能优于单个指标和未加权平均值,尤其是在 X 射线验证的数据集中。研究得出了关键指标(如 ipTM)的特定方法阈值,以便更好地将模型分类为正确或错误,包括 AlphaFold 定义的“灰色区域”(ipTM = 0.6-0.8)。这些阈值提高了评估精度并减少了假阳性。虽然 AF3 在不同重复中产生更一致的结果,但 CF-T(使用模板的 ColabFold)生成了略多的高质量预测。然而,在更广泛的质量范围内评估时,AF3 模型更可靠。在复杂的冷冻电镜衍生组件中,研究强调了所有评估方法的局限性:当存在多个二聚体构型时,由于参考不匹配,DockQ 经常错误分类好的模型,但 C2Qscore 保持相对稳健。作者将 C2Qscore 集成到 ChimeraX 插件 PICKLUSTER v2.0 中,使研究人员能够使用详细的、可定制的指标(包括对 AlphaFold3 模型的支持)可视化和评估预测的界面。这项工作为解释和比较 AF2/ColabFold 和 AF3 的蛋白质复合物预测结果提供了实用指南,提供了评分阈值、基准测试见解和提高计算结构生物学置信度的工具。
5. AlphaFold3 难以预测磷酸化诱导的构象变化
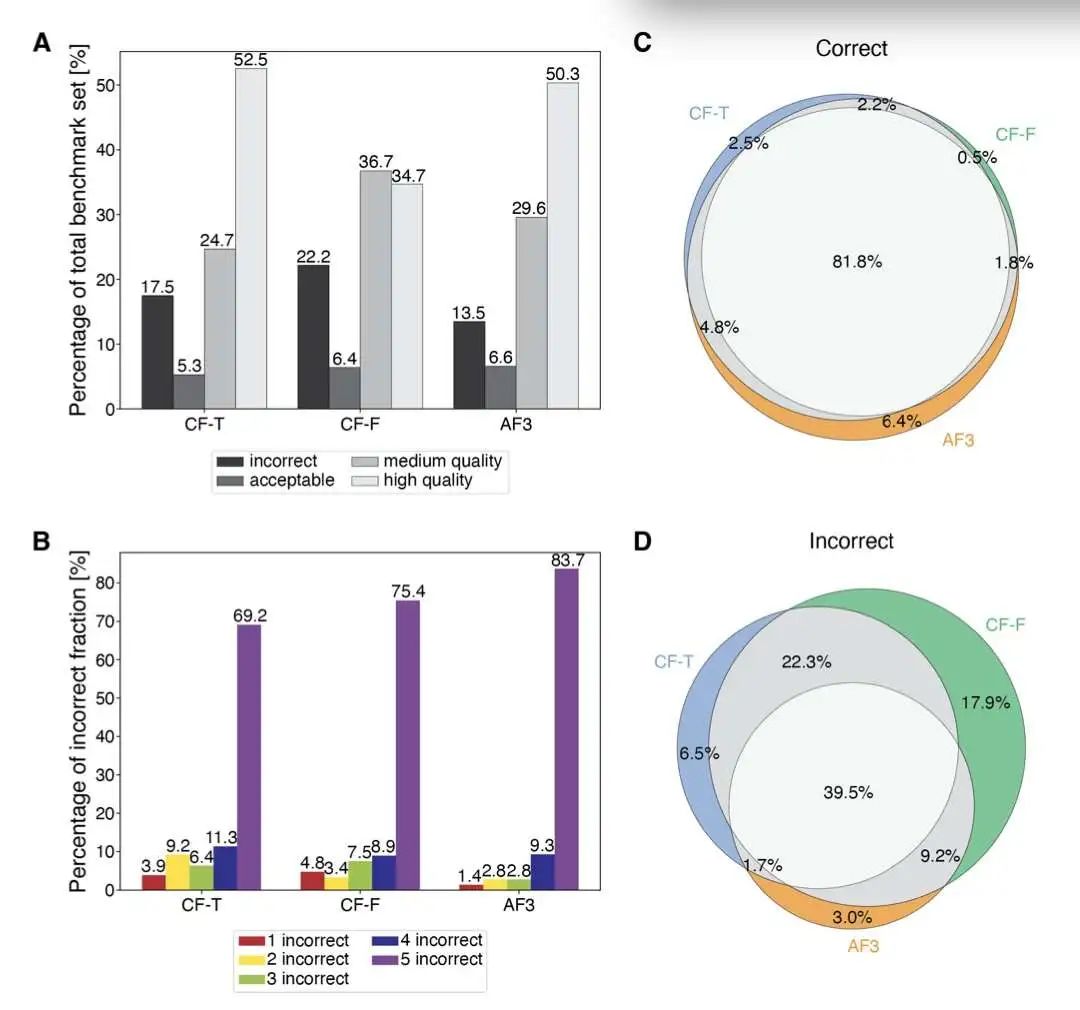
本研究系统评估了 AlphaFold 模型捕捉磷酸化诱导结构变化的能力,使用了 109 个蛋白质的磷酸化 § 和非磷酸化 (NP) 构象数据。研究发现,尽管 AlphaFold3 有所进步,但包括 AF2、AF3 和 AF3-p 在内的所有模型都主要预测主要的构象状态,对磷酸化驱动的结构多样性表现出有限的敏感性。研究引入了构象多样性评分 (CDS 和 pCDS) 来量化结构变异性,发现仅 23% 的蛋白质在磷酸化后表现出明显的结构变化,大多数磷酸化作用只是微妙地稳定了已有的构象。
进一步分析表明,磷酸化更多地是微调而不是从根本上改变蛋白质结构,65% 的聚类同时包含 P 和 NP 构象。这表明许多磷酸化效应是调节性的,而不是结构性转变。不同磷酸化位点类型的影响也不同,单点磷酸化事件,尤其是涉及磷酸酪氨酸 (PTR) 的事件,会引起最明显的局部和全局构象变化,而磷酸丝氨酸 (SEP) 的影响最小,与其稳定作用一致。即使是磷酸化感知模型 AlphaFold3-p,与 AF2 和 AF3 相比也仅显示出适度的改进,与磷酸化状态对齐的比例分别为 73%、70% 和 64%,差异无统计学意义。
所有模型都倾向于预测主要的结构簇,这可能是由于 PDB 训练数据中的偏差和共同进化限制,限制了它们探索罕见或功能相关的替代状态的能力。在超过 80% 的蛋白质中,AlphaFold 模型的结构预测聚集在一起,并且所有模型都与 98% 的蛋白质中最主要的结构集合对齐,无论磷酸化状态如何。残基水平分析表明,磷酸化诱导的变化更可能发生在结构域和具有更高溶剂可及性的柔性卷曲区域,尤其是在多结构域蛋白质中。
本研究强调了当前深度学习模型的一个关键局限性:虽然它们擅长预测稳定的构象,但在模拟磷酸化诱导的灵活性方面却存在不足,而这种灵活性通常对生物功能至关重要。作者提倡使用包含更多不同 PTM 结构的更丰富的训练数据集,并建议改进类似 AlphaFold 的模型,以更好地捕捉局部结构调整和罕见的磷酸化驱动构象。
6. BRAGE:首个生物制药领域检索增强生成基准
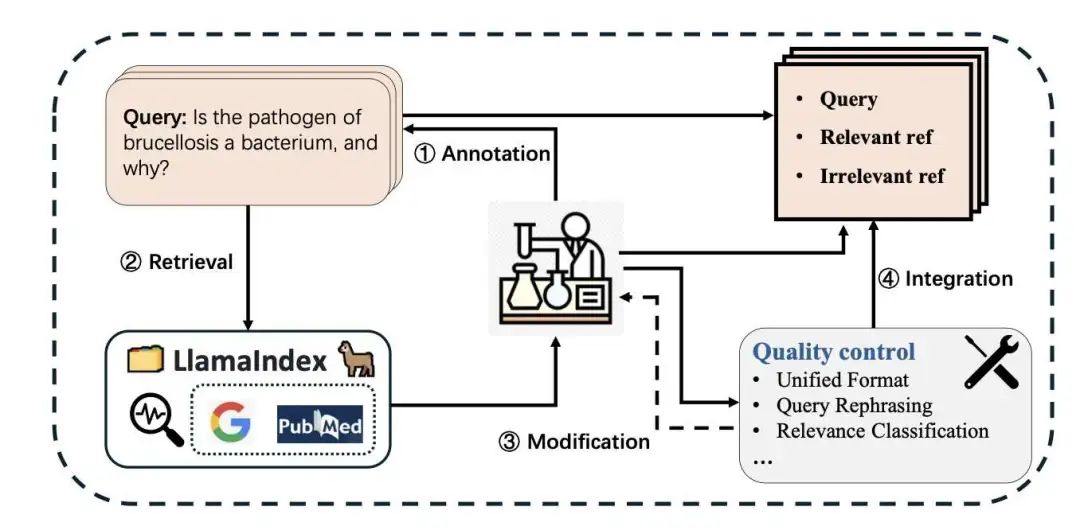
BRAGE 基准旨在评估检索增强大型语言模型 (LLM) 在生物制药领域的查询和参考文献理解能力 (QRUC)。与以往侧重于封闭式问答的基准不同,BRAGE 使用涵盖英语、法语、德语和中文四种语言的开放式专家策划生物制药查询和参考文献,更准确地反映了现实世界的科学任务。BRAGE 评估了 LLM 的两项互补能力:识别相关参考文献和排除不相关参考文献,这对于避免在药物开发和公共卫生等高风险领域出现幻觉至关重要。作者提出了一种新颖的基于引用的分类指标,将评估框架为查询 - 参考文献对的二元分类。这能够对 RAG 设置下的 LLM 性能进行细粒度、可扩展且与人类一致的评估。该基准包括 400 个专家策划的查询,超过 2,400 个相关参考文献和 1,800 个不相关参考文献,涵盖五个核心生物制药主题:基础生物学、药物设计、临床转化、伦理/法规和传染病。
结果表明,主流 LLM(GPT-4o、Claude 3、Gemini、LLaMA3、Qwen)在特定于生物制药的 QRUC 中仍然存在显著的性能差距。即使是顶级模型也常常难以过滤掉嘈杂的参考文献并正确利用复杂的生物医学证据。使用生物制药知识(通过 CPT+SFT)对 LLaMA3 进行微调可将宏观 F1 值从 69.5% 提高到 75.1%,这既突出了生物医学 RAG 应用领域适应的挑战,也突出了其潜力。Gemini-1.5-pro、GPT-4o 和 o3-mini 表现最佳,尽管不同语言的召回率与精确度之间存在权衡。诸如 DeepSeek-R1 之类的推理型 LLM 在过度思考时往往会接受所有引用,即使是不相关的引用。
人工评估证实了所提出指标的可靠性,与基于分类的得分偏差小于 1%,验证了其在未来多语言生物医学 RAG 评估中的适用性。BRAGE 代表了评估 LLM 在科学和生物医学应用方面向前迈出的重要一步,它为提高检索增强生成中的事实性和相关性提供了一个稳健、多语言和细粒度的基准。
7. BRIDGE 模型:高效预测蛋白质相互作用
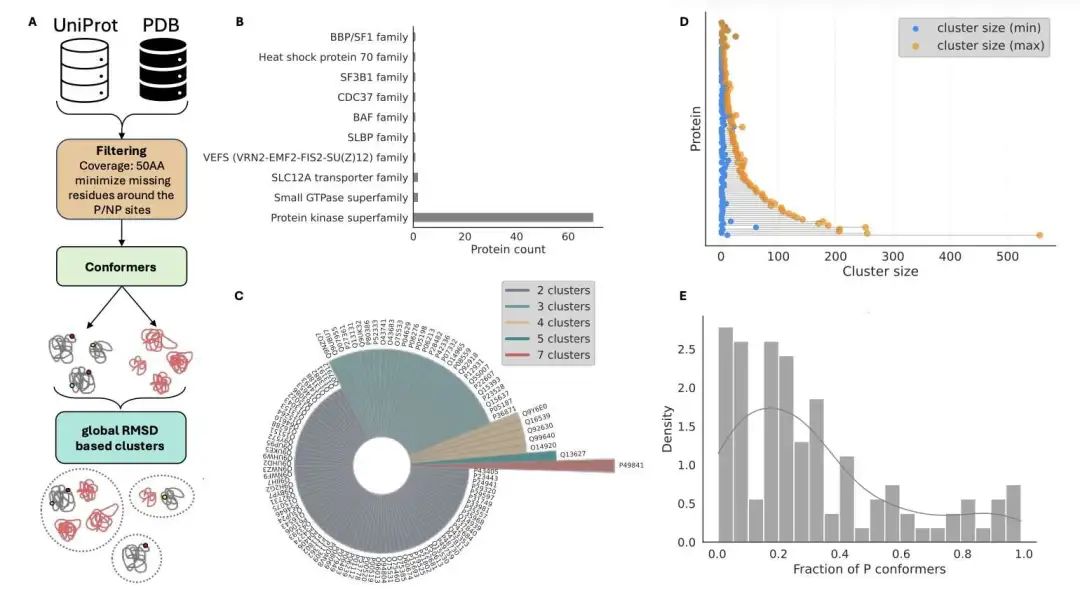
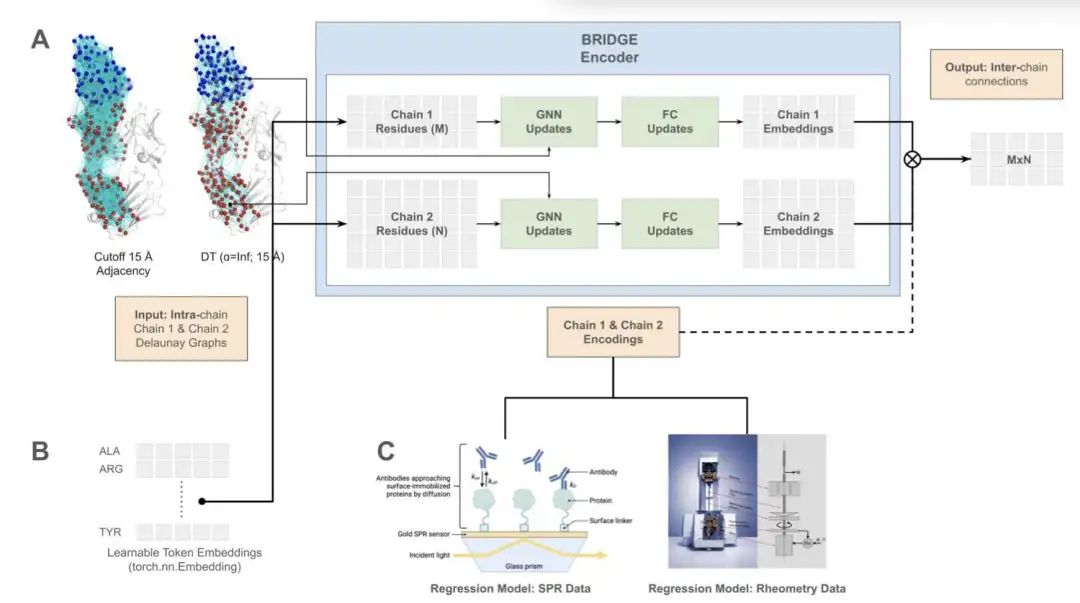
BRIDGE 模型是一种基于 Delaunay 镶嵌的粗粒化图神经网络,用于预测蛋白质链间的残基相互作用,并生成紧凑且具有生物物理意义的蛋白质界面嵌入向量。研究表明,该模型在实验数据上的链间接触预测准确率高达 0.84 (F1),超越了 SpatialPPI 2.0 等现有方法。这种基于 Delaunay 镶嵌的边缘预测方法有效捕捉了关键的生物物理特性,同时避免了结构噪声的干扰。
BRIDGE 嵌入向量可直接用于治疗性下游任务。在抗体 - 抗原亲和力预测中,即使训练数据较少,BRIDGE-Affinity 的性能也优于几乎所有现有方法,甚至与 DG-Affinity 相当,且无需依赖专有数据集。与许多复杂的基于对接的方法不同,BRIDGE 仅需分离链的结构即可进行预测,使其非常适用于尚未解析完整抗体 - 抗原复合物的早期治疗工作流程。
此外,BRIDGE-Viscosity 利用相同的嵌入向量预测抗体溶液粘度,其留一交叉验证 Spearman 相关系数高达 0.978,优于 PfAbNet、Sharma 和 SCM 等领先模型,且无需进行对接或数据增强。BRIDGE 的泛化能力核心在于使用 Delaunay 镶嵌定义残基间的物理连接,过滤无关接触,并实现高效的图构建,边缘数量减少了 70%。
与拥有数十亿参数的大型蛋白质语言模型(例如 980 亿参数的 ESM-3)相比,BRIDGE 模型的参数少于一百万,证明了特定领域先验知识可以在不牺牲性能的前提下显著降低计算需求。BRIDGE 嵌入向量的降维(UMAP)结果显示,其可根据生物物理特性(如粘度和亲和力)进行聚类,提供了一个可解释的潜在空间,反映了有意义的相互作用模式。
BRIDGE 模型具有模块化和可扩展性,可以整合核酸、小分子或其他蛋白质拓扑结构,为结构生物学和药物发现领域的更广泛应用打开了大门。通过仅使用实验数据集进行训练,并避免对 AlphaFold 模型的依赖,BRIDGE 建立了一个稳健、可解释且多功能的平台,用于在各种治疗环境中模拟蛋白质界面。
8. CellFlow:单细胞表型建模新利器
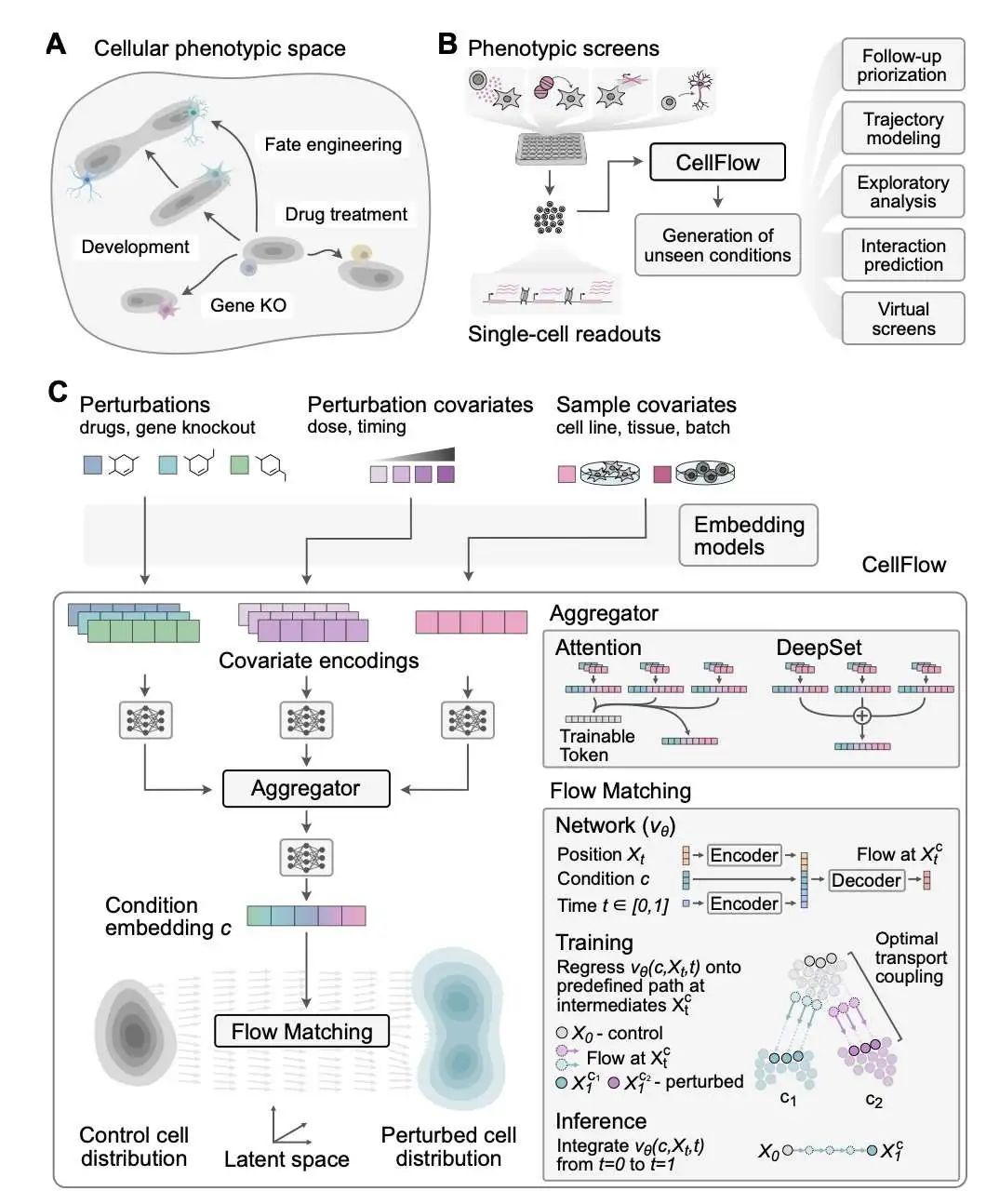
CellFlow 是一款基于流匹配的生成式单细胞表型建模框架。该模型利用最优传输和流匹配技术,从源分布生成受扰细胞群,能够模拟药物剂量反应关系和基因修饰等复杂扰动效应。研究表明,CellFlow 在预测多个供体细胞因子反应方面表现出色,尤其在仅测量一个供体细胞因子效应的情况下,其性能显著优于基线模型。
此外,CellFlow 还成功应用于斑马鱼胚胎扰动研究,准确预测了未观察发育阶段的基因敲除效应,证明了其在复杂多细胞系统中推断表型变化的能力。在类器官工程领域,CellFlow 能够精准预测组合形态发生素处理后的异质细胞群,有助于设计更优的细胞命运编程实验策略。
该模型具有良好的可扩展性,可应用于近千万个外周血单个核细胞 (PBMCs),即使在训练数据有限的情况下,也能准确预测不同处理条件下供体特异性细胞因子反应。CellFlow 在药物组合筛选方面也展现出显著优势,能够改进差异基因表达预测,并在包含未见条件的药物组合中超越传统模型。CellFlow 的一个关键特性是能够预测未见条件下的细胞反应,为未经测试的治疗效果提供新见解,这对药物开发和功能基因组学至关重要。凭借整合多种扰动并在不同实验设置中预测表型结果的能力,CellFlow 有望通过减少对穷举实验探索的需求,加速表型筛选的发现进程。
9. AI 驱动肽段-HLA 结合预测工具大比拼
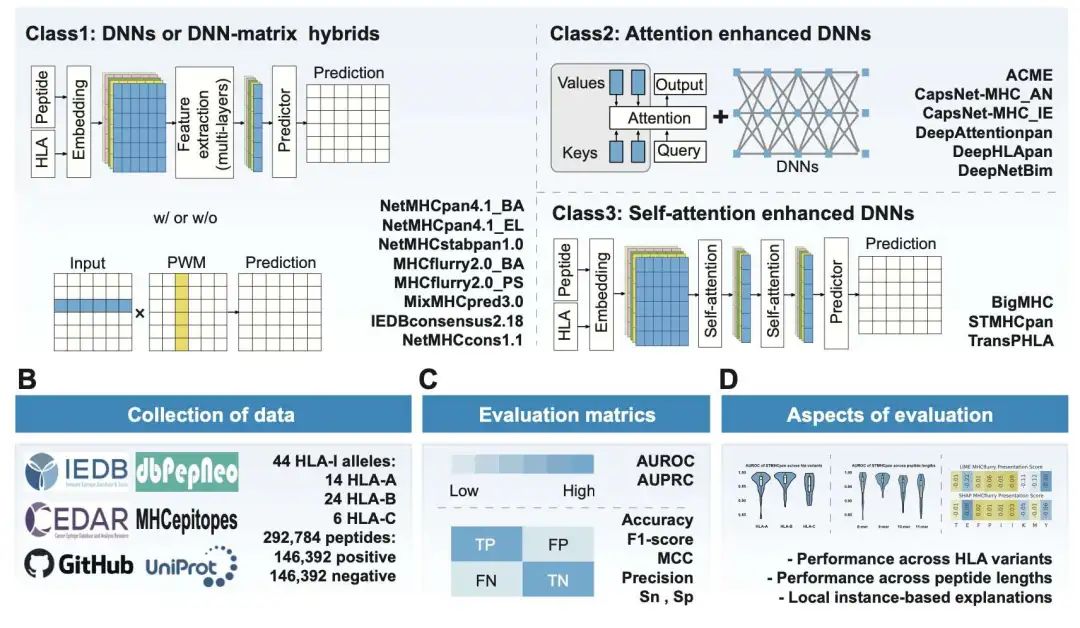
本研究对 17 种肽段-HLA-I 结合预测工具进行了迄今为止最广泛的基准测试,使用了超过 290,000 个肽段和 44 个 HLA-I 等位基因,并采用严格筛选的独立数据集。结果显示,基于自注意力的模型 STMHCpan 和 BigMHC 表现最佳,STMHCpan 的 AUROC 达到 0.961,AUPRC 达到 0.965,在几乎所有肽段长度和 HLA 变体中都优于其他方法。
研究进一步发现,使用洗脱配体 (EL) 数据训练的模型性能优于使用结合亲和力 (BA) 数据训练的模型。例如,NetMHCpan4.1_EL 和 MHCflurry2.0_PS 都超过了它们各自基于 BA 数据训练的版本,这表明高质量的质谱衍生数据集的重要性。此外,胶囊网络模型 CapsNet-MHC_AN 也表现出强大的性能和较低的计算成本,表明空间特征层次结构为基于 Transformer 的架构提供了一种可行的替代方案。
利用 SHAP 和 LIME 进行的可解释性分析揭示了跨等位基因的关键结合位点,特别是 P2 和 P9。SHAP 提供了更稳定且与生物学更一致的解释,尤其对于 HLA-C*05:01 等稀有等位基因。计算丙氨酸扫描通过比较归因分数与预测的 ΔΔG 值验证了模型解释,证实了 SHAP 突出显示对结合能贡献最大的残基的能力。STMHCpan、BigMHC 和 MHCflurry2.0_PS 在测试肽段中一致地识别出关键结合残基,其预测与基于能量的结构模型吻合良好,而归因值低的工具则表现出更高的假阴性率。
研究表明,9 聚体肽段在所有工具中的预测效果最佳。HLA-A 和 HLA-B 等位基因的预测准确性高于 HLA-C,这主要是因为可用的训练数据更多,这突显了扩展代表性不足等位基因训练集的必要性。此外,结合多个预测器的集成模型,例如 MHCflurry2.0 对 AP 和 BA 模块的逻辑集成,比单独的组件提供了更好的性能,这表明了混合方法的强大功能。
这项研究不仅对当前的肽段-HLA-I 预测工具进行了排名,还引入了一个集成了可解释人工智能的开放基准测试平台,为下一代免疫信息学工具的开发提供了路线图。
10. DTMol:基于结合口袋的分子对接
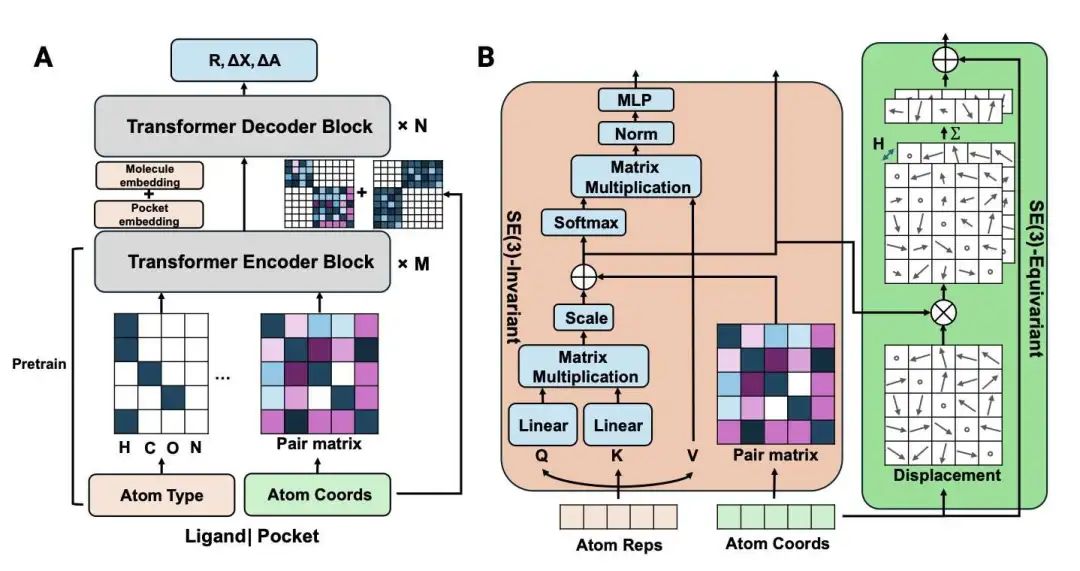
DTMol 是一种基于扩散变换器的全新分子对接模型,专注于结合口袋而非整个蛋白质,从而显著提高了对接精度。研究者利用预训练的分子和口袋编码器以及 SE(3) 等变变换器解码器,捕捉配体和蛋白质口袋之间精细的几何和化学相互作用。与 DiffDock 等盲对接方法不同,DTMol 通过分离结合口袋来减少构象搜索空间和计算复杂度,从而实现更具表达力和效率的基于变换器的建模。
DTMol 在 PoseBuster (77.65% top-1 RMSD < 2Å) 和 PDBBind 基准测试 (45.05% top-1 RMSD < 2Å) 上均实现了最先进的性能,超越了 Smina、Gnina 等传统工具以及最近的基于机器学习的方法。该模型在旋转 (SO(3))、平移 (T(3)) 和原子扰动空间上使用扩散,避免了基于扭转建模的缺点,并在坐标空间中实现了稳定且方差保持的采样。
该模型的关键创新在于变换器中结合了 SE(3) 不变和 SE(3) 等变分支的混合注意力机制,能够同时模拟原子特性和空间构型。在针对 JAK2 (PDB ID: 6BBV) 的实际虚拟筛选任务中,DTMol 是唯一在预测和实验测量的抑制剂活性之间实现正秩相关的方法,并识别出 2 种新的活性化合物。此外,DTMol 避免了在推理过程中依赖 RDKit 生成的种子构象,增强了鲁棒性,使其更适合在实际药物发现工作流程中部署。精心设计的训练方案,包括分阶段微调、预热学习率计划和使用具有时间分割验证的大规模精选数据集以避免数据泄漏,进一步支持了该模型的成功。
DTMol 通过将生成模型与特定口袋上下文相结合,为基于结构的虚拟筛选设定了新标准,在药物发现中提供了强大的性能、可解释性和实际影响。

如何学习大模型 AI ?
由于新岗位的生产效率,要优于被取代岗位的生产效率,所以实际上整个社会的生产效率是提升的。
但是具体到个人,只能说是:
“最先掌握AI的人,将会比较晚掌握AI的人有竞争优势”。
这句话,放在计算机、互联网、移动互联网的开局时期,都是一样的道理。
我在一线互联网企业工作十余年里,指导过不少同行后辈。帮助很多人得到了学习和成长。
我意识到有很多经验和知识值得分享给大家,也可以通过我们的能力和经验解答大家在人工智能学习中的很多困惑,所以在工作繁忙的情况下还是坚持各种整理和分享。但苦于知识传播途径有限,很多互联网行业朋友无法获得正确的资料得到学习提升,故此将并将重要的AI大模型资料包括AI大模型入门学习思维导图、精品AI大模型学习书籍手册、视频教程、实战学习等录播视频免费分享出来。

第一阶段(10天):初阶应用
该阶段让大家对大模型 AI有一个最前沿的认识,对大模型 AI 的理解超过 95% 的人,可以在相关讨论时发表高级、不跟风、又接地气的见解,别人只会和 AI 聊天,而你能调教 AI,并能用代码将大模型和业务衔接。
- 大模型 AI 能干什么?
- 大模型是怎样获得「智能」的?
- 用好 AI 的核心心法
- 大模型应用业务架构
- 大模型应用技术架构
- 代码示例:向 GPT-3.5 灌入新知识
- 提示工程的意义和核心思想
- Prompt 典型构成
- 指令调优方法论
- 思维链和思维树
- Prompt 攻击和防范
- …
第二阶段(30天):高阶应用
该阶段我们正式进入大模型 AI 进阶实战学习,学会构造私有知识库,扩展 AI 的能力。快速开发一个完整的基于 agent 对话机器人。掌握功能最强的大模型开发框架,抓住最新的技术进展,适合 Python 和 JavaScript 程序员。
- 为什么要做 RAG
- 搭建一个简单的 ChatPDF
- 检索的基础概念
- 什么是向量表示(Embeddings)
- 向量数据库与向量检索
- 基于向量检索的 RAG
- 搭建 RAG 系统的扩展知识
- 混合检索与 RAG-Fusion 简介
- 向量模型本地部署
- …
第三阶段(30天):模型训练
恭喜你,如果学到这里,你基本可以找到一份大模型 AI相关的工作,自己也能训练 GPT 了!通过微调,训练自己的垂直大模型,能独立训练开源多模态大模型,掌握更多技术方案。
到此为止,大概2个月的时间。你已经成为了一名“AI小子”。那么你还想往下探索吗?
- 为什么要做 RAG
- 什么是模型
- 什么是模型训练
- 求解器 & 损失函数简介
- 小实验2:手写一个简单的神经网络并训练它
- 什么是训练/预训练/微调/轻量化微调
- Transformer结构简介
- 轻量化微调
- 实验数据集的构建
- …
第四阶段(20天):商业闭环
对全球大模型从性能、吞吐量、成本等方面有一定的认知,可以在云端和本地等多种环境下部署大模型,找到适合自己的项目/创业方向,做一名被 AI 武装的产品经理。
- 硬件选型
- 带你了解全球大模型
- 使用国产大模型服务
- 搭建 OpenAI 代理
- 热身:基于阿里云 PAI 部署 Stable Diffusion
- 在本地计算机运行大模型
- 大模型的私有化部署
- 基于 vLLM 部署大模型
- 案例:如何优雅地在阿里云私有部署开源大模型
- 部署一套开源 LLM 项目
- 内容安全
- 互联网信息服务算法备案
- …
学习是一个过程,只要学习就会有挑战。天道酬勤,你越努力,就会成为越优秀的自己。
如果你能在15天内完成所有的任务,那你堪称天才。然而,如果你能完成 60-70% 的内容,你就已经开始具备成为一名大模型 AI 的正确特征了。
这份完整版的大模型 AI 学习资料已经上传CSDN,朋友们如果需要可以微信扫描下方CSDN官方认证二维码免费领取【保证100%免费】
























 8509
8509

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








