 AbMole是ChemBridge在中国唯一官方指定合作伙伴。
AbMole是ChemBridge在中国唯一官方指定合作伙伴。
由Zingg D, Bhin J等人在Nature上发表的名为”Truncated FGFR2 is a clinically actionable oncogene in multiple cancers “的文章。在该文章中,使用了购自AbMole 的Y-27632(M1817)。文章揭示了FGFR2(成纤维细胞生长因子受体2)基因中E18外显子截断变异(FGFR2ΔE18)在多种癌症中的致癌作用。本文将详细介绍这项研究的实验过程与实验结果,带您深入了解FGFR2ΔE18如何成为癌症研究的新焦点。
研究团队首先利用Sleeping Beauty转座子系统,在小鼠乳腺肿瘤模型中进行了大规模的转座子插入诱变筛选。转座子是一种能在生物体内移动的DNA片段,能够随机插入到基因组中,从而破坏或激活附近的基因。研究团队通过在小鼠乳腺组织中引入转座子,筛选出了能够驱动肿瘤形成的转座子插入位点。结果发现,FGFR2内含子17(I17)是转座子插入的热点区域,这些插入导致FGFR2的E17-E18转录本缺失,形成了FGFR2ΔE18变异体。
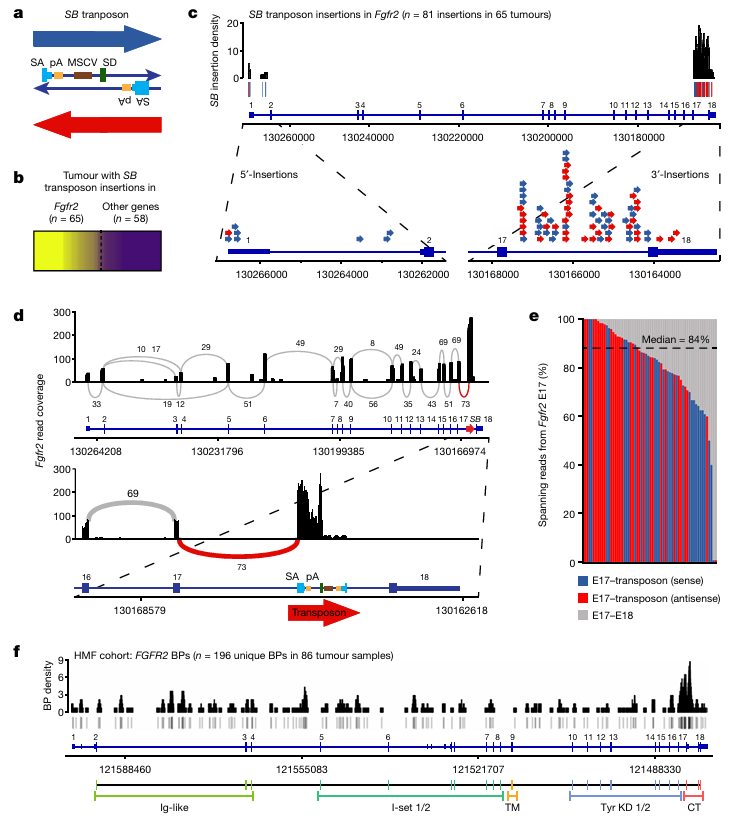
图1SB转座子筛选和WGS分析鉴定出复发性FGFR2 E18截断。
之后为了进一步验证FGFR2ΔE18的致癌性,研究团队构建了多种表达FGFR2不同变异体的小鼠模型。这些模型包括表达全长FGFR2(FGFR2FL)、FGFR2ΔE18以及多种FGFR2融合变异体的小鼠。通过体内实验,研究团队观察到FGFR2ΔE18变异体在小鼠乳腺组织中显著促进了肿瘤的形成,且肿瘤生长速度明显快于表达全长FGFR2的小鼠。同时,他们还发现,FGFR2ΔE18的致癌性不依赖于特定的融合伴侣基因,显示出更强的独立致癌能力。
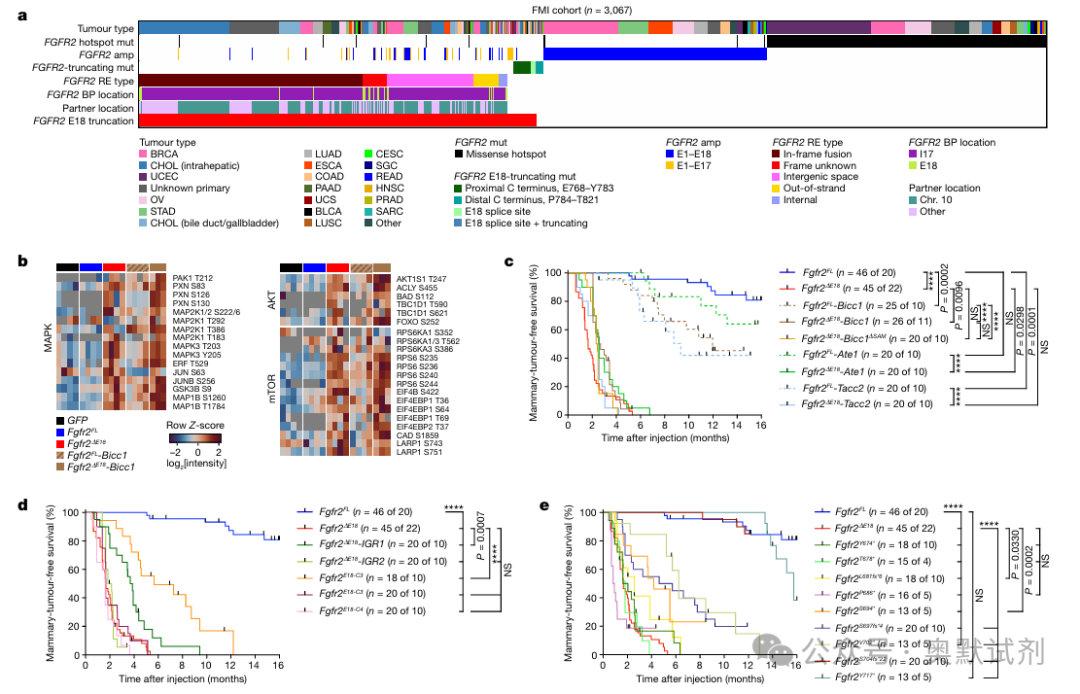
图2:人FGFR2 E18截短改变是小鼠的致癌驱动因素。
然后研究团队利用Hartwig Medical Foundation(HMF)和Foundation Medicine(FMI)的人类癌症全基因组测序数据进行了深入分析。他们发现,FGFR2 E18截断变异在人类多种癌症类型中广泛存在,尤其是在胆管癌中最为常见。这些变异包括无义突变、移码突变以及复杂的重排事件,它们共同导致了FGFR2ΔE18的表达。
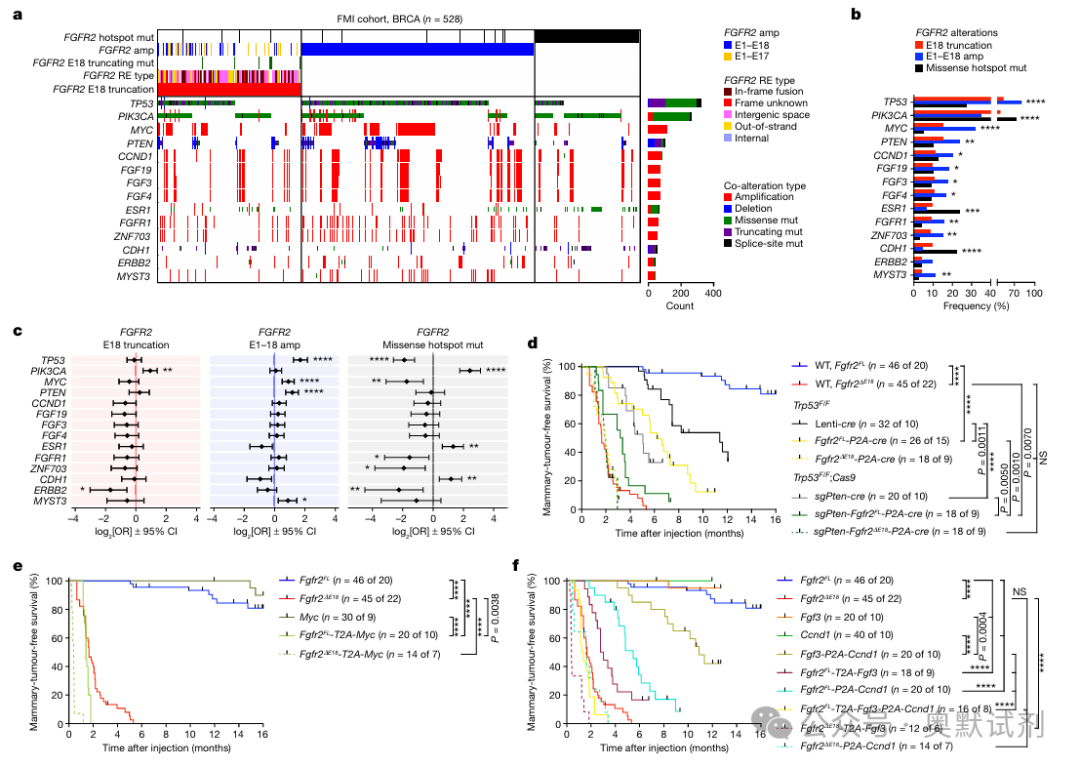
图3:FGFR2改变的致癌能力取决于共同发生的驱动因素
最后为了揭示FGFR2ΔE18的致癌机制,研究团队又进行了一系列功能性实验。他们利用细胞培养系统、软琼脂克隆形成实验以及磷酸化蛋白质组学分析等方法,深入探讨了FGFR2ΔE18在细胞增殖、信号通路激活以及肿瘤形成中的作用。实验结果表明,FGFR2ΔE18变异体通过激活MAPK和PI3K-AKT-mTOR信号通路,显著促进了细胞的增殖和存活。此外,他们还发现,FGFR2ΔE18对FGFR抑制剂表现出高度的敏感性,这为未来的靶向治疗提供了重要依据。

图4人类和小鼠FGFR2改变癌症模型对FGFRi敏感。
实验结果显示,FGFR2ΔE18变异体在多种小鼠模型中均表现出显著的致癌性。与全长FGFR2相比,FGFR2ΔE18的致癌性更强且更加独立。全长FGFR2的致癌性往往需要依赖其他共驱动基因(如TP53、MYC等)的协同作用,而FGFR2ΔE18则能够在没有这些共驱动基因的情况下独立驱动肿瘤的形成。
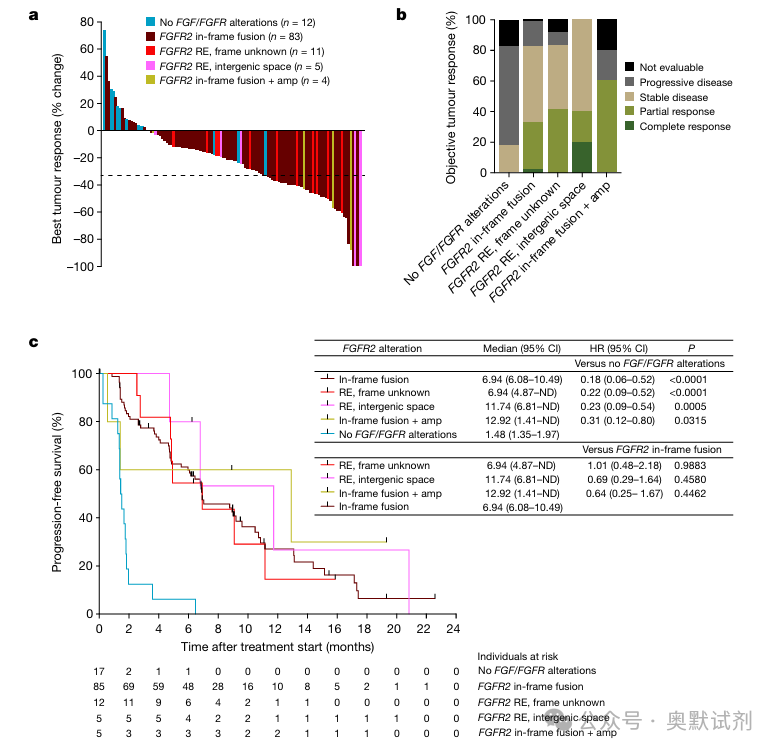
图5胆管癌患者对fgfr靶向治疗的反应与FGFR2 RE类型无关。
通过对人类癌症全基因组测序数据的分析,研究团队发现FGFR2 E18截断变异在多种癌症类型中均有存在。这些变异不仅存在于胆管癌等常见肿瘤中,还广泛分布于乳腺癌、肺癌、胃癌等多种癌症中。这一发现进一步证明了FGFR2ΔE18作为致癌驱动因素的普遍性和重要性。
功能性实验结果表明,FGFR2ΔE18变异体通过激活MAPK和PI3K-AKT-mTOR信号通路促进了细胞的增殖和存活。这些信号通路在肿瘤发生和发展过程中起着至关重要的作用。FGFR2ΔE18通过激活这些通路为肿瘤细胞的生长提供了必要的生存信号和环境支持。
实验还发现,FGFR2ΔE18变异体对FGFR抑制剂表现出高度的敏感性。这一发现为未来基于FGFR2ΔE18的靶向治疗提供了重要依据。研究团队认为通过针对FGFR2ΔE18的靶向治疗可以有效地抑制肿瘤的生长和扩散,提高患者的生存率和生活质量。
FGFR2ΔE18变异体的发现为我们理解癌症发生和发展提供了新的视角和思路。这一变异体作为独立的致癌驱动因素在多种癌症中广泛存在且对FGFR抑制剂高度敏感,为未来的精准医疗和靶向治疗提供了重要靶点和策略。随着研究的深入和技术的进步,我们有理由相信FGFR2ΔE18将成为癌症诊断和治疗领域的重要突破点之一。未来我们需要进一步探索FGFR2ΔE18变异体的具体作用机制和调控网络以便开发出更加有效和安全的靶向治疗方法造福广大癌症患者。
更多内容请访问:www.abmole.cn






















 523
523

 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








