听了好久10X 10X的,一直都没弄明白到底是怎么回事,这次系统学习一下,因此想粗略总结一番。
前言
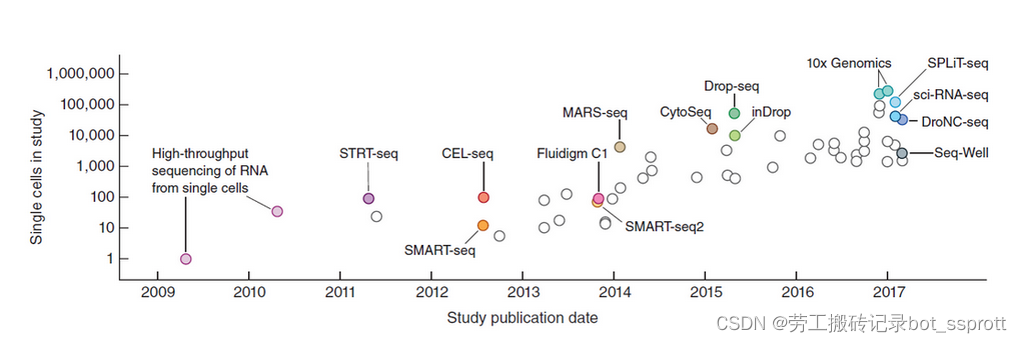
首先,明确单细胞测序技术发展迅速,出现很多类型的平台进行辅助,但10X因为测序上下限大,处理灵活,被广泛使用。
(10X Genomics 一次测序可以捕捉100-80,000个细胞,具有极高的细胞通量。单细胞的测序通量平均也在50,000 reads/per cell 左右,而如果使用细胞核进行测序则平均通量为25,000 reads/per nuclei。)
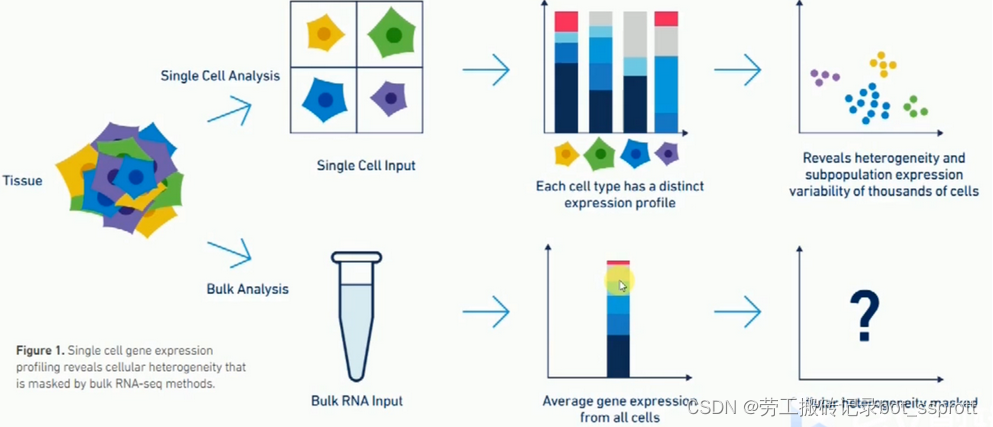
单细胞测序技术能够解决①常规测序中因样本量太少无法进行测序的问题;②PCR扩增的偏好性问题;③细胞间的异质性。
比如,bulk RNA-seq将样本中所有细胞混在一块,测的是细胞内基因表达的平均值。而单细胞测序将每个细胞分开进行扩增,测的是每个细胞中基因表达的值,能够解决细胞间异质性的问题。
单细胞测序避免PCR扩增偏好性:在扩增的时候不同核酸序列在同样的条件下扩增程度不一样。有些核酸序列容易被扩增,有些核酸序列不容易被扩增,导致在同样时间同样条件下可能获得不一样的扩增倍数,所以扩增后的核酸序列丰度与扩增前是有一定的差异的。
单细胞测序能够避免PCR扩增偏好性,并不是在扩增本身有了技术变革,而是因为它所计算的不是扩增后的核酸序列的相对丰度,而是计算了扩增前核酸序列的实际数值。。。
原理阐述
细胞分选
微流控交叉(十字)系统
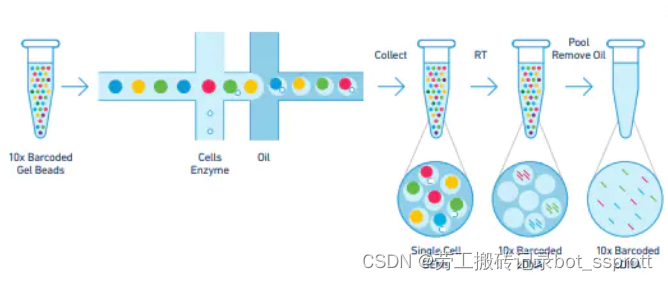
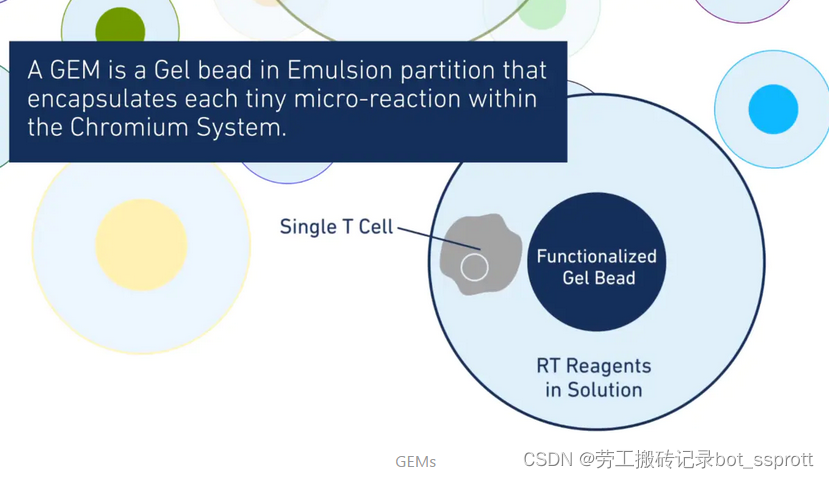
凝胶微珠(带有Barcode的Gel Beads)进入交叉系统中,在第一个十字中与细胞悬液、酶相结合,在第二个十字中与油相结合,形成凝胶微珠-细胞-油的包裹结构(GEMs【Gel Bead in emulsion】)。
凝胶微珠是如何识别细胞的呢?
凝胶微珠表面结构如下:
Read1+10x Barcode+UMI+Poly(dT)+sequence
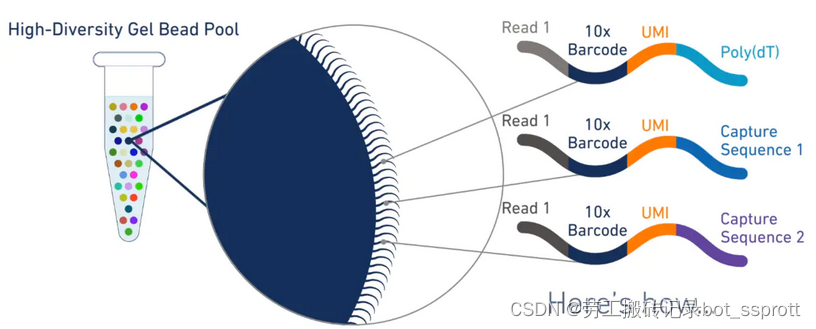
Read1:上游引物。(确定Barcode与UMI来源)
10x Barcode:与细胞融合,标记细胞。每个细胞有不同的Barcode。
UMI:用于标记mRNA。每条mRNA有不同的UMI。
Poly(dT):用于识别RNA的3'末端有一个polyA的尾巴,捕获mRNA。
构建文库
PCR扩增
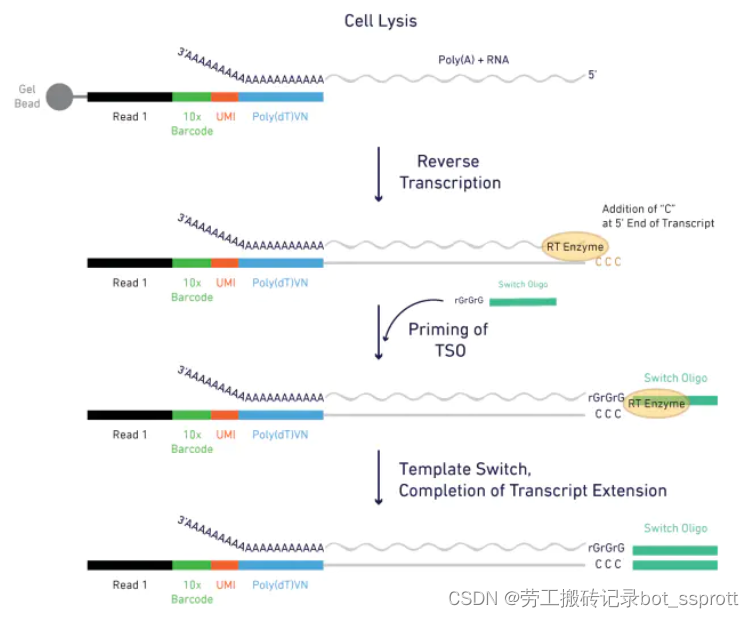
反转录(RT)成cDNA
10x Genomic中V2与V3文库有所区别
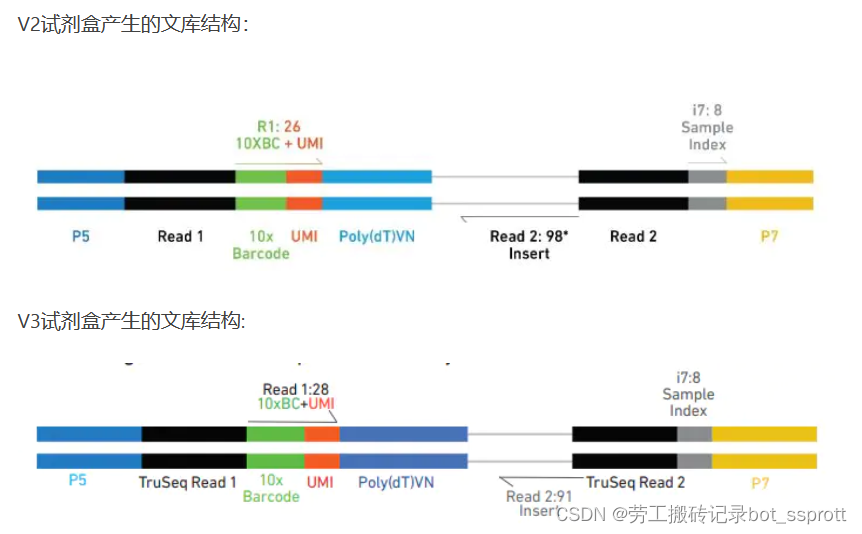























 3067
3067











 被折叠的 条评论
为什么被折叠?
被折叠的 条评论
为什么被折叠?








